反相高效液相色谱法测定金嗓口服液中绿原酸含量
余晟岚,徐 果
(1.重庆医科大学附属第二医院,重庆 400010; 2.中国人民解放军第三军医大学大坪医院野战外科研究所,重庆 400042)
金嗓口服液是医院生产的中成药口服液,具有外透风热、内散肺郁、清热解毒及利咽宣声的作用,适用于风热犯肺结于咽喉所致的声音嘶哑及急慢性咽喉炎、急慢性扁桃体炎。其主要成分为金银花、板蓝根、黄芩、薄荷、玄参等中药,在相关标准中只对金银花中的绿原酸有定性鉴别,而无有效成分的含量测定,且金银花为主要成分。为更有效地控制质量及提高标准,笔者采用高效液相色谱法测定该复方制剂中绿原酸的含量,现报道如下。
1 仪器与试药
VARIN型双泵高效液相色谱仪,Prostar 210UV型检测器。绿原酸对照品(中国药品生物制品检定所,批号为10753-200413);金嗓口服液(第三军医大学大坪医院自制,批号分别为130113,130227,130308);甲醇(批号为 1001743)为色谱纯,磷酸(AR,批号为 110214),水为纯化水。
2 方法与结果
2.1 色谱条件及系统适用性试验
色谱柱:Ultimate ODS C18柱(250 mm ×4.6 mm,5 μm);流动相:乙腈 -0.5% 磷酸溶液(26 ∶74);流速:1.0 mL /min;检测波长:328 nm[1-5];灵敏度:1.0 AUFS;柱温:室温;进样量:10 μL。理论板数按绿原酸峰计算应不低于3 500,色谱图见图1。
2.2 对照品贮备液制备
称取真空干燥的对照品绿原酸约10.50 mg,精密称定,用50%甲醇溶解,定容至50 mL容量瓶,摇匀,作为对照品贮备液。
2.3 方法学考察
线性关系考察:精密量取 2.2项下对照品贮备液 0.5,1.0,2.0,3.0,4.0,5.0,6.0 mL,分别置 10 mL 容量瓶中,用 50% 甲醇定容后摇匀,各进样10 μL,以峰面积(Y)为纵坐标、质量浓度(X)为横坐标进行线性回归,得回归方程 Y=14 324 219.73 X+974 813.5,r=0.999 8(n=7)。结果表明,绿原酸质量浓度在0.010 5~0.126 0 g/L范围内与峰面积线性关系良好。
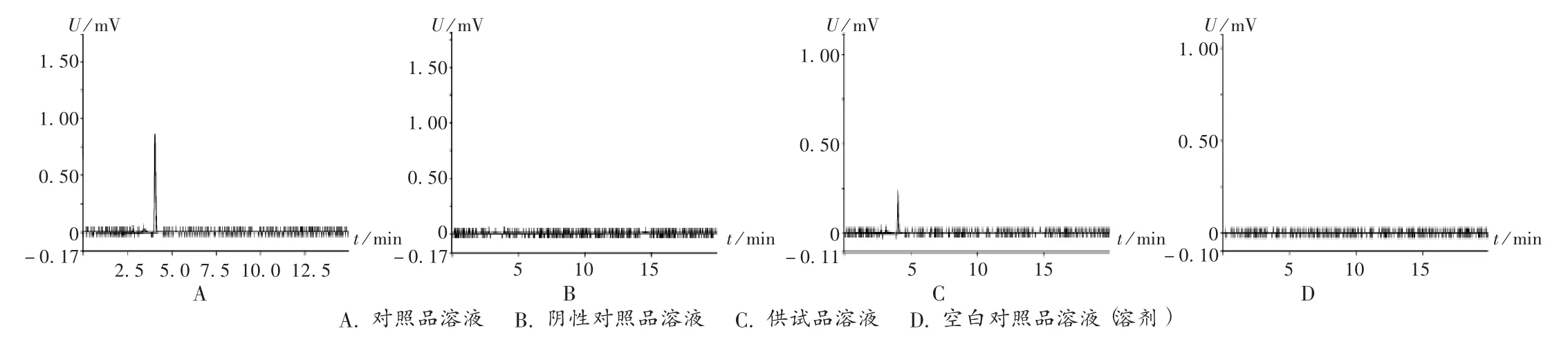
图1 高效液相色谱图
精密度试验:精密吸取质量浓度为0.0105g/L的同一绿原酸对照品溶液10 μL,重复进样7次,测定峰面积。结果的 RSD=1.04%(n=7),表明仪器精密度良好。
稳定性试验:将同一供试品溶液放置 0,2,4,12,18,24,36 h后,分别依法各进样10 μL,测定峰面积并计算样品含量。结果峰面 积 的 RSD 分 别 为 2.0% ,1.9% ,2.1% ,含 量 的 RSD 为2.31%,2.25%,2.30% (n =7)。表明供试品溶液在 36 h 内稳定。
重复性试验:取同一批(批号为130117)样品5份,制备供试品溶液,照拟订方法进样测定峰面积。结果的 RSD=1.6%(n=5),表明方法重复性良好。
加样回收试验:精密吸取样品(批号分别为120815,121015,121206,130117,130227,130308)6 份各 1 mL,置 10 mL 容量瓶中,另精密加入绿原酸对照品 0.5,1.0,2.0 mL,按样品含量测定项下方法分别测定含量,计算回收率。结果见表1。
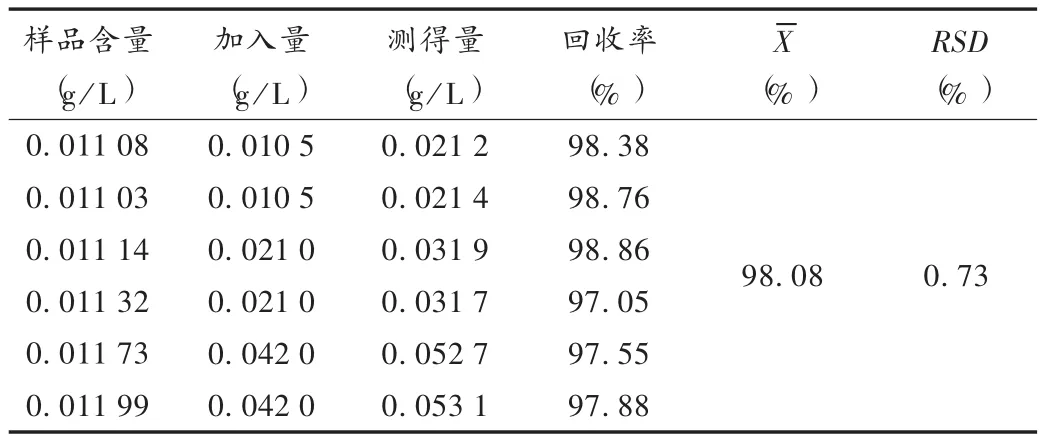
表1 绿原酸加样回收试验结果(n=6)
2.4 样品含量测定
精密吸取样品(先用低温离心机以3 000 r/min的速率离心15 min)6 mL,置50 mL棕色容量瓶中,超声处理20 min,加入50%甲醇溶液至刻度,用0.45 μm微孔滤膜过滤,精密吸取滤液4.0 mL到50 mL棕色瓶中,加50%甲醇至刻度,作为供试品溶液。依法测定5批样品,用外标法计算含量,结果见表2。
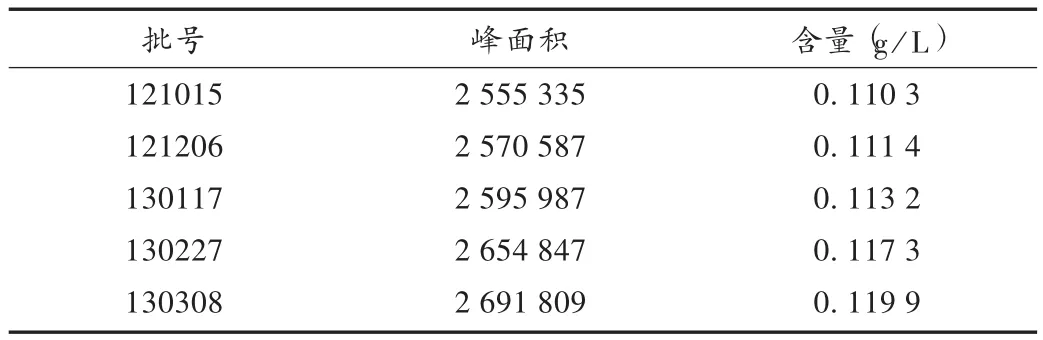
表2 样品含量测定结果(n=5)
3 讨论
采用RP-HPLC测定金嗓口服液中绿原酸的含量,方法简便、快速、重复性好。在色谱条件的选择试验中,分别比较了0.02 mol/L的磷酸二氢钠 -甲醇(75∶25,调 pH =3.2)与乙腈 -0.5% 磷酸溶液(26∶74)2种流动相,分别采用同1种ODS C18柱测定。结果以后者为流动相时获得良好分离[6-7]。
取对照品溶液,在200~800 nm波长范围扫描,结果绿原酸在328 nm波长处有最大吸收,故选择328 nm为检测波长。
供试品溶液的制备过程中采用了2种方法。方法一:取样品20 mL,置水浴上蒸干,加入50%甲醇热溶,过滤,取滤液6 mL(低温离心机以3 000 r/min离心15 min),置50 mL棕色容量瓶中,加50%甲醇定容至刻度,用0.45 μm的微孔滤膜过滤,精密吸取4 mL置50 mL棕色瓶中,加50%甲醇至刻度。方法二:精密吸取样品(先用低温离心机以3 000 r/min离心15 min)6 mL置50 mL棕色容量瓶中,超声处理20 min,加入50%甲醇溶液至刻度,用0.45μm的微孔滤膜过滤,精密吸取滤液4.0 mL至50 mL棕色瓶中,加50%甲醇至刻度。测定结果显示,方法一杂质峰很多,相邻峰不容易分开;而方法二相邻峰对主峰无干扰,杂峰明显减少,并且峰形对称。故选择方法二作为供试品溶液的制备方法[8-10]。
供试品溶液稳定性试验表明,24 h内测定时峰面积一致,但随着放置的天数增加,绿原酸峰面积有所减少。
作为院内自制制剂,为更好地保证每一批次样品的含量一致并提高质量控制标准,更好地为临床用药服务,笔者认为,对绿原酸含量测定结果应控制在2.0 g/L以上。
参考文献:
[1]国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2010:205-206.
[2]俞 秀.RP-HPLC法测定利鼻片中绿原酸的含量[J].海峡药学,2011,23(2):46.
[3]徐 冬,汪 涛,张杰.RP-HPLC法测定利鼻片中黄芩苷的含量[J].中国药师,2010,13(2):256.
[4]聂翠翠,彭家钢,杨瑞芬.高效液相色谱法测定复方芩兰口服液中绿原酸和黄芩苷的含量[J].湖北中医药大学学报,2011,13(5):30-32.
[5]桑旭峰,吴海雯,徐奇超.HPLC同时测定银黄口服液中绿原酸和黄芩苷含量[J].中成药,2005,27(1):96-98.
[6]钟小群,蔡庆顺,寒勋衔.HPLC法测定石韦药材中绿原酸的含量[J].江西中医学院学报,2002,14(2):16-17.
[7]陈桂云,王进洪,丁以华.HPLC测定爽阴药液中绿原酸的含量[J].中成药,2001(9):26-27.
[8]国家医药管理局中草药情报中心站.植物药有效成分手册[M].北京:人民卫生出版社,1986:739.
[9]蒋俊春.高效液相色谱法测定蒲金散结胶囊中绿原酸含量[J].中国药业,2012,24(21):62-63.
[10]梁聂彦,陈学松.高效液相色谱法测定路边菊中绿原酸含量[J].中国药业,2012,23(21):21-22.

