高岭石对金属置换吸附机理的理论分析
方志杰,鄢翠,莫曼,杨惠君,张艺耀,张敏
(1.广西科技大学土木建筑工程学院,广西柳州545006;2.深部岩土与地下工程国家重点实验室,北京100083;3.桂林理工大学土木与建筑工程学院,广西桂林541004)
0 引言
随着我国经济的飞速发展,冶金、矿产、化工、电镀等行业排放了大量的废弃物,这些废弃物中含有众多重金属污染物,通过各种途径进入土壤和水源,对人们的健康生活构成了严重的威胁。对于环境污染的治理方法大体上可划分为生物、物理、化学及矿物处理法,而利用高岭石、蒙脱石等粘土矿物作为新型除污材料成为目前研究的热点,应用高岭石治理金属污染[1-2]也已经取得了一定的进展:众多实验表明高岭石有较强的吸附能力[3-6];文献[7]发现高岭石对稀土离子具有较强的吸附作用;文献[8-10]等通过实验发现钴、铁、镍等金属离子易于被高岭石和蒙脱石吸附。虽然这些实验研究结果在利用高岭石治理金属污染方面取得了一定的进展,但是目前人们对高岭石吸附金属离子的机理认识还有待深化,特别是有关高岭石阳离子置换吸附重金属离子机理等一系列重要的基本问题还没有得到系统解决,因此相关的理论研究尤其显得重要。
为了更好地理解高岭石的吸附性能,本文采用量子力学的第一性原理计算方法来分析高岭石对金属的置换吸附性能,在原子层面上对高岭石中阳离子与外部金属离子之间置换吸附的机理进行解释,并进一步分析被吸附铁金属在高岭石中的微观作用。
1 计算方法及模型构建
本计算方法采用密度泛函理论,所用的赝势为PAW势,理论计算软件为VASP。计算中所有的原子位置均根据Hellmann-Feynman静电力进行驰豫,平面波函数的截断能设置为400 eV,布里渊区的K点设置为2×2×2。所选择的吸附金属元素为Be、Mg、Ca、Cr、Mn、Fe、Sr、Cu和Zn,这些掺杂元素将分别替代高岭石中阳离子Al和Si的位置。收敛精度为每个原子能量至1.0×10-4eV,作用在每个原子的力不超过0.1 eV/nm。
高岭石晶体属于点群P1,基本的化学分子式为Al2Si2O9H4,其1∶1层状结构是由一个SiO4四面体层和一个AlO6八面体层构成。根据基本化学分子式并采用实验的晶体常数[11]:a=0.515 5 nm,b=0.515 5 nm,c=0.740 5 nm,α=75.14°,β=84.12°,γ=60.18°所建立高岭石的原胞为17个原子(图1),1个原胞包括2个铝原子、2个硅原子、4个氢原子和9个氧原子,计算在1个2×2×1的超晶胞(4个原胞共68个原子)中进行。计算模拟当中,单金属掺杂为1个外在金属完全替代高岭石超晶胞当中1个阳离子(掺杂比为1.47%),双金属掺杂为2种比例为1∶1的外在金属完全替代高岭石超晶胞当中2个阳离子(掺杂比为2.94%)。
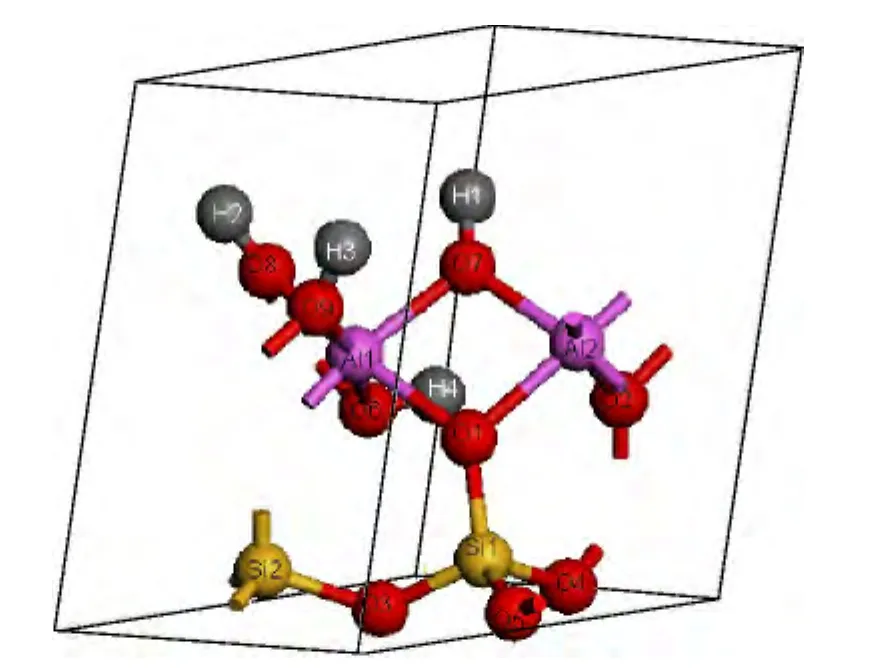
图1 高岭石的晶体结构Fig.1 Crystal structure of kaolinite
根据文献[12-13]中的形成能公式,缺陷形成能Hf(a,q)由几个变量决定,对于高岭石杂质的计算系统,缺陷形成能的公式为

式中:E(a,q)表示含有显示电性q、缺陷a的超晶胞总能;E(kaolinite)表示68个原子的超晶胞总能;EF(费米能级)是以价带顶能量值(EVBM)为基准,不考虑高岭石的化学势范围;nAl、nSi、nA、nO、nH分别表示超晶胞里面铝原子、硅原子、杂质原子、氧原子、氢原子的数量;u0Al和u0Si分别表示铝原子和硅原子的化学势。这些化学势可以简单地视为单质铝和单质硅的基态能量,即

同理,把杂质原子的化学势视为单质原子的基态能量,即

对于H和O原子,把它们的化学势视为氢气和氧气的基态能量,即
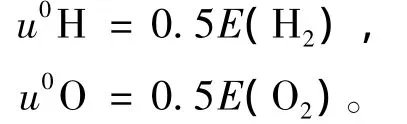
另外,缺陷的跃迁能级εa(q/q0)定义为带电量为q和带电量为q0相同的费米能级值,即

2 计算结果
2.1 金属替代Al和Si位置的高岭石形成能分析
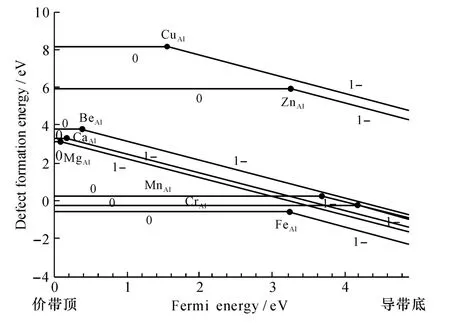
图2 高岭石的形成能(代替铝原子)Fig.2 Formation energies of kaolinite(substitute for Al)

图3 高岭石的形成能(代替硅原子)Fig.3 Formation energies of kaolinite(substitute for Si)
图2、图3分别为金属替代高岭石阳离子Al和Si位置时形成能随费米能级变化示意图,图中大字体元素为外来的金属原子,小字体元素符号为被替代阳离子原子,实心圆点为中性阶段(标示为0)与负电性阶段(标示为1-)的转换点。
由图2可知,费米能级从EVBM到ECBM(导带底能量值)移动的时候,杂质的形成能也发生变化。以MgAl为例,当费米能级位于价带顶时,形成能为3.16 eV,此时镁原子不容易进入高岭石内部;当费米能级向导带底移动时,MgAl的形成能降低;当费米能级位于3.23 eV时,MgAl的形成能开始为负,表明此时镁原子可以进入高岭石晶体内部。当Ca、Mn和Be原子在费米能级向导带底移动到一定程度时,出现了形成能降低为零的情况,表明这些原子也易于进入高岭石晶体内部;Fe和Cr原子的缺陷形成能一直处于零以下,表明Fe和Cr原子更易于进入高岭石内部;而Zn原子和Cu原子的形成能太高,很难进入高岭石晶体内部。计算结果符合自然界中高岭石吸附金属的实际情况。
从形成能结果上看,在2价金属Be、Ca和Mg这三种原子中,Mg原子进入高岭石的形成能最低。过渡元素Fe、Cr和Mn在q=0的情况下,这些元素替代铝原子时形成能都很低,特别是Fe和Cr,具有负的形成能。从跃迁能级考虑,它们的跃迁能级都是属于深能级,表明这些元素进入高岭石之后很难产生负电性。而Cu原子和Zn原子都具有相对来说很高的形成能和较深的跃迁能级,分别位于价带顶以上1.57和3.25 eV。因此,从计算结果来看,认定Cu原子、Zn原子很难在高岭石晶体中存在,也很难在高岭石中产生负电性。
高岭石的形成能随费米能级的变化(替代硅位置)如图3所示。在替代Si原子过程中,除了Al原子在费米能级接近到导带底的时候可以出现负的形成能,其他的掺杂金属均很难替代高岭石的Si位置。从内部缺陷来看,Al原子替代Si原子属于一种反位缺陷,这种缺陷在费米能级大的时候,有可能出现,但是数量极少。从缺陷跃迁能级来看,除了Ga和Al,其他的跃迁能级都属于深能级,Ga很难进入硅位置,因此,不会出现负电性,而Al虽然可以进入硅位置,但数量极少,不可能给高岭石带来较多的负电性。从图2和图3可知,掺杂的金属更容易替代高岭石中的Al原子而不是Si原子。
2.2 双金属进入Al位置的高岭石形成能分析
图4为两种金属离子(双掺杂时两种金属的比例为1∶1)替代铝原子的形成能变化图。两种金属进入铝原子位置时,Sc+Sr的组合最适合进入铝位置,Mg、Be、Ca与Sc的组合也比较容易一起替代铝原子。由图2可知,Mg、Be、Ca和Sc都很容易进入铝位置,而Fe与Mg、Be、Ca组合则很难进入铝位置。出现这种情况的原因是:被替代的2个Al原子共6价,而替代金属因为Mg、Be、Ca是2价态金属,Fe为3价态金属,而Sc为4价态金属,一个2价态金属和另外一个4价态金属很容易共同进入高岭石中两个3价态铝原子位置,而一个2价态金属和另外一个3价态金属则很难共同进入高岭石中两个3价铝原子的位置。

图4 高岭石在双金属掺杂下的形成能(替代Al位置)Fig.4 Formation energies of kaolinite under the dual-metal doping condition(substitute for Al)
从形成能结果上看,Fe原子很容易置换进入高岭石。为更好地了解金属铁在高岭石内部的作用情况,从VASP计算结果中提取态密度图(图5、图6),其中图5为高岭石的铁原子替代铝原子的总态密度图,杂质能级一般出现在禁带宽度的中间,靠近价带顶的位置。图6为铁原子在高岭石的分波态密度图,铁的d电子有2个主峰分别位于价带顶和禁带宽度中间,这表明铁金属的进入将会极大影响高岭石的能带结构。
图7、图8分别为铝原子和铁原子在高岭石中的电荷密度图。由图8可知,铁原子在高岭石内部主要是与O原子形成共价键。而从图7知,被替代的Al原子在高岭石内部并没有和O原子形成共价键,这表明Fe原子进入高岭石内部替代Al原子之后会与O原子形成更强的共价键。这也从一个侧面解释了Fe原子杂质比较容易在高岭石成分中出现并更为稳定。

图5 高岭石的杂质总态密度Fig.5 Total DOS of Fe doping in Kaolinite

图6 Fe原子在高岭石分波态密度Fig.6 Partial DOS of Fe doping in kaolinite

图7 Al元素在高岭石中的电荷密度Fig.7 Electron density cap of Al doping in kaolinite

图8 Fe元素在高岭石中的电荷密度Fig.8 Electron density cap of Fe doping in kaolinite
3 结论
本文利用VASP计算软件建立高岭石模型,分析了不同金属杂质代替高岭石中硅酸盐组分铝和硅的位置后的形成能、跃迁能级、态密度、电荷密度,得到以下结论:
(1)金属替代硅位置时,金属离子很难进入硅位置并产生负电性,当替代铝位置时,所有的二价金属元素都有比较低的跃迁能级。而过渡金属中Fe、Cr和Mn有比较低的形成能,这些元素会比较容易进入高岭石晶体;都有较深的跃迁能级,导致它们无法带来负电性。Cu和Zn的形成能和跃迁能级都比较高,导致在自然界中很难进入高岭石晶体。
(2)多种金属掺杂进入铝位置时,一个2价态的金属和一个4价态的金属组合是很容易共同进入铝元素位置的,而一个2价态和一个3价态金属则很难共同进入。
(3)在电荷密度的分析中,铁元素的进入容易影响高岭石的能带结构,而铁原子进入高岭石铝位置之后,会产生比Al—O键更强的Fe—O共价键。
[1]杭小帅,周健民,王火焰,等.粘土矿物修复重金属污染土壤[J].环境工程学报,2007,1(9):113-120.
[2]袁东海,张孟群,高士祥,等.几种粘土矿物和粘粒土壤吸附净化磷素的性能和机理[J].环境化学,2005,24(1):7-11.
[3]Wang X L,Li Y.Measurement of Cu and Zn adsorption onto surficial sediment components:New evidence for less importance of clay minerals[J].Jounral of Hazardous Materials,2011,189(3):719-723.
[4]Veli S,Alyüz B.Adsorption of copper and zinc from aqueous solutions by using natural clay[J].Journal of Hazardous Materials,2007,149(1):226-233.
[5]Wang Y,Tang X W,Chen Y M,et al.Adsorption behavior and mechanism of Cd(Ⅱ)on loess soil from China[J].Journal of Hazardous Materials,2009,172(1):30-37.
[6]简家成,刘峥,赖丽燕,等.偏高岭土地聚物制备条件及其水化过程[J].桂林理工大学学报,2014,34(3):544-548.
[7]Wan Y X,Liu C Q.Study on adsorption of rare earth elements by kaolinite[J].Journal of Rare Earths,2005,23(3):377-381.
[8]Bhattacharyya K G,Gupta S S.Calcined tetrabutylammonium kaolinite and montmorillonite and adsorption of Fe(Ⅱ),Co(Ⅱ)and Ni(Ⅱ)from solution[J].Applied Clay Science,2009,46(2):216-221.
[9]Eren E.Removal of lead ions by Unye(Turkey)bentonite in iron and magnesium oxide-coated forms[J].Journal of Hazardous Materials,2009,165(1):63-70.
[10]徐玉芬.粘土矿物对废水中Cu2+、Cd2+、Cr3+的吸附实验研究[J].矿产综合利用,2008(3):28-31.
[11]Bish D L,Von Dreele R B.Rietveld refinement of non-hydrogen atomic positions in kaolinite[J].Clays and Clay Minerals,1989,37(4):289-296.
[12]Wei S-H.Overcoming the doping bottleneck in semiconductors[J].Computional Materials Science,2004,30(3):337-348.
[13]Wei S-H,Zhang S B.Defect properties of CuInSe2and Cu-GaSe2[J].Journal of Physics and Chemistry of Solids,2005,66(11):1994-1999.

