Tin-mZrmO2n (n=2-7, 0≤m≤n)团簇结构和稳定性研究
石小峰, 李秀燕, 高燕林, 杨 致, 刘瑞萍
(太原理工大学物理与光电工程学院, 太原 030024)
Tin-mZrmO2n(n=2-7, 0≤m≤n)团簇结构和稳定性研究
石小峰, 李秀燕, 高燕林, 杨 致, 刘瑞萍
(太原理工大学物理与光电工程学院, 太原 030024)
应用密度泛函理论中的B3LYP方法对Tin-mZrmO2n(n=2-7,0≤m≤n) 团簇的基态几何结构、相对稳定性和电子结构进行了理论研究. 结果表明,与桥氧链接的Ti原子被Zr原子取代后形成的混合团簇较为稳定;在团簇尺寸一定的条件下(即n相同),随着Zr原子数m的增加,团簇的结合能基本呈线性增大,团簇的稳定性增强;Ti、Zr、O原子之间发生了电荷转移现象,形成了稳定的Ti-O-Zr键.
Tin-mZrmO2n团簇; 密度泛函理论; 几何结构; 稳定性; 电子结构
1 引 言
过渡金属氧化物 TiO2是一种宽禁带半导体材料,具有强的氧化还原性和良好的化学稳定性,同时还具有无毒且成本低等特点[1-3]. 1972年,Fujishima和Honda发现TiO2单晶电极能够光催化分解水[4]. 1976年,Cary报道了TiO2水浊液在近紫外光的照射下可使多氯联笨脱氯,并且可以非选择性地氧化 (降解) 各类有机物,生成CO2和H2O. 此后,对TiO2光催化性质的研究引起了研究人员的广泛关注. 然而TiO2用作光催化材料受到下面的限制: (1) 带隙较宽,只能吸收波长小于387 nm的紫外光,而紫外光仅占太阳光谱的4%左右,使得TiO2对太阳光的利用率较低;(2) 光生电子-空穴对寿命短,光催化的量子效率低. 人们对TiO2进行了大量的研究,致力于其光响应范围的拓宽和量子效率的提高[5-10].
研究表明,与ZrO2、SiO2、Al2O3等稳定结构氧化物的复合可以显著影响TiO2的结构和光催化性能,其中TiO2/ZrO2复合材料尤其值得关注[11-13]. Zr与Ti同属IVB族元素,具有相似的原子半径(Ti:2 Å;Zr:2.16 Å)和相同的价态(+4). TiO2和ZrO2都是n型半导体,具有相似的物理和化学性质. Zr和Ti能以任意的比例形成固溶体,Zr在TiO2中也能在很宽的浓度范围内进行替位掺杂. ZrO2不仅可以作为TiO2的载体,而且能与其形成双金属氧化物催化剂,因为ZrO2本身也具备光催化性能[14,15]. ZrO2/TiO2复合氧化物不仅具有ZrO2和TiO2各自的优点,它们之间的强相互作用还会导致新的催化活性位的产生.
Chen等[13]制备了多孔TiO2/ZrO2纳米复合材料,研究显示第二相的加入有助于提高500℃以上高温处理时TiO2多孔结构的稳定性,且能起到细化晶粒和阻碍TiO2由锐钛矿相向金红石相转变的作用. 在光催化降解乙烯的实验中, TiO2/ZrO2表现出优于TiO2的光催化活性. 研究表明,把TiO2/ZrO2复合氧化物用作电极,可以显著提高太阳能电池的效率. 通过调节ZrO2的加入量(Ti/Zr的摩尔比例在5~50%范围内变化),可以调整TiO2的带隙和比表面积,从而影响其光电性质[16].对TiO2/ZrO2复合薄膜的气敏特性的研究结果显示,TiO2/ZrO2在150℃低温下对低浓度的CO和NO2气体有显著的响应[17].
研究还表明,TiO2与ZrO2的复合会使二者之间发生电荷转移,形成Zr-O-Ti键,增强材料的表面酸性,从而有益于光催化性能的提高. Wu等[11]发现650℃高温煅烧形成的TiO2/ZrO2复合材料用于乙苯脱氢的产率最大,分析表明TiO2与ZrO2之间形成了稳定的Ti-O-Zr键,对其催化性能的提高产生了重要的影响. Neppolian等人[12]采用溶胶凝胶法制备了不同质量比的TiO2/ZrO2复合纳米晶材料,用于降解4-氯苯酚. 结果发现TiO2/ZrO2复合材料的光催化性能比纯的TiO2和ZrO2都明显提高,研究同样证实了Ti-O-Zr键的形成与TiO2/ZrO2的催化性能之间存在密切联系.
团簇的性质既不同于块体材料,也不同于其组成单体,具有明显的尺寸依赖性. 团簇结构与性质的研究对于理解物质从微观到宏观的过渡具有重要作用[18]. 对TiO2相关团簇的理论研究是揭示TiO2微观结构和光催化机理的重要手段. Wang等[19]对 (TiO2)n(n=1-4) 及TiOy(y=1-3) 的电子结构进行了实验研究和理论计算,得到了团簇的几何构型和阴离子光电子谱. Qu and Kroes等[20]采用密度泛函理论 (DFT) 在B3LYP水平上研究了 (TiO2)n(n=1-9) 团簇的电子结构和稳定性,并预测了每类团簇的基态结构. 其他研究者也对TiO2团簇的结构及性能进行了系统的理论研究[21-23]. 与较多的TiO2/ZrO2复合材料的实验研究形成鲜明对照的是,理论研究开展得很少,相关混合团簇的理论研究还鲜有报道. 本文利用密度泛函理论对Tin-mZrmO2n(n=2-7,0≤m≤n) 团簇的几何结构、稳定性和电子结构进行研究,为揭示TiO2/ZrO2复合材料的微观结构和光催化作用机理提供参考.
2 计算方法
为了找到Tin-mZrmO2n(n=2-7,0≤m≤n) 团簇的基态结构,对每一尺寸团簇我们考虑了大量可能初始构型.在具体选取团簇初始构型时,采取了两步走的方法,第一步是找出 (TiO2)n团簇的基态构型,在这一过程中不仅考虑了文献[20]中的团簇结构而且还参考了Foltin等人[24]有关 (ZrO2)n团簇的构型;第二步是在以上所得每一 (TiO2)n基态结构中用Zr原子逐次取代Ti原子,考虑多种取代位置,而后又就各种不同的异构体构型进行结构优化,并在同一水平上进行了频率计算. 所有优化好的构型都做了频率分析,发现都没有虚频,说明得到的优化构型都是势能面上局域最小点,而不是过渡态或高阶鞍点.
本文所有计算基于Gaussian09软件包[25]. 计算采用DFT[26]中的杂化密度泛函B3LYP方法,在6-31G*水平上进行了结构优化和频率计算. 所有初始构型的自旋多重度均考虑了1、3、5,结果发现自旋多重度为1时体系能量较低,所以本文初始构型的自旋多重度均为1. 对于体系中的O原子采用6-3IG*基组进行了全电子计算,而Ti、Zr原子的核电子采用了LANL2DZ有效核电势 (Effective Core Potential,ECP),其价电子采用LANL2DZ基组计算. 为了验证本文所用方法的可靠性,我们首先计算了TiO2和ZrO2,这两种结构都具有C2v对称性,Ti-O、Zr-O键长分别为1.649 Å和1.802 Å,O-Ti-O和O-Zr-O的键角分别为111.2°和106.9°,这与文献[27]和[24]的计算结果相吻合,这说明本文所选用的方法和基组是合适的.
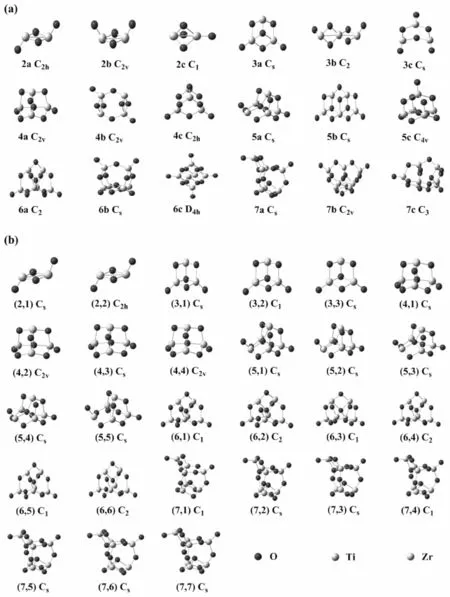
图1 (a) (TiO2)n (n=2-7) 团簇的几何结构;(b) Tin-mZrmO2n (n = 2-7,1≤m≤n) 团簇的基态结构Fig.1 (a) Geometrical structures of (TiO2)n(n=2-7) clusters ;(b) Ground-state structures of Tin-mZrmO2n (n=2-7,1≤m≤n) clusters
3 结果与讨论
3.1 团簇的基态构型
3.1.1 (TiO2)n(n=2-7) 团簇的几何结构
首先我们对 (TiO2)n团簇进行了优化,图1(a) 给出了 (TiO2)n团簇的基态及亚稳态构型,图中团簇按照总能量的高低进行排列. 其中na表示最低能量结构,nb和nc表示能量稍高的亚稳态. 表1给出了每个团簇的点群、相对能和最低频率.
Ti2O4团簇基态结构2a具有C2h对称性且拥有两个反式对称的端氧,其端位、桥位的Ti-O键和Ti-Ti键长分别为1.632、1.843和2.721 Å,这一结果与文献[13,23]相符;亚稳态结构2b拥有两个順式对称的端氧,其能量比2a结构高出0.2767 eV. 对于Ti3O6团簇,3a结构具有Cs对称性,有两个键长为1.627 Å的端位Ti-O键和一个3配位的氧原子;具有C2对称性的3b结构呈线形,由两个相互垂直的Ti-O-Ti-O组成的菱形和两个端位Ti-O键组成,其能量比3a高出0.3788 eV;3c具有Cs对称性,其能量比3a结构高0.8848 eV. 4a为Ti4O8的基态结构,此类结构由4个彼此相连的六元环和 2个自由氧原子构成,具有C2v对称性,其亚稳态结构4b、4c的能量分别比4a结构高出0.2669、0.4049 eV. Ti5O10团簇的基态结构5a具有Cs对称性,拥有2个端氧和7个桥氧,且在结构中心有一4配位的氧原子,其亚稳态结构5b同样具有Cs对称性,其能量比5a结构高0.0985 eV. 对于Ti6O12团簇,基态结构6a具有C2对称性,其亚稳态结构6b、6c的能量比6a分别高出0.8508、1.9685 eV. 7a为Ti7O14团簇的基态结构,具有Cs对称性且拥有两个端氧原子和一个3配位的氧原子,其余均为桥氧,7b、7c为亚稳态结构,其能量分别比基态结构高0.4548、0.8635 eV.
3.1.2 Tin-mZrmO2n(n= 2-7,1≤m≤n) 团簇的基态结构
在已优化好的 (TiO2)n(n=2-7) 团簇基础上用Zr原子逐次取代Ti原子得到多种几何构型,经过几何参数全优化后得到了混合团簇的基态结构. 图1(b) 给出了Tin-mZrmO2n(n=2-7,1≤m≤n) 团簇的基态结构和相应的对称性,将团簇简单表示为 (n,m),其中n为Ti、Zr总的原子数,m为Zr原子数.
n=2:结构 (2,1) 为 (TiO2)2基态结构中一个Ti原子被Zr取代的基态构型,具有Cs对称性,其端位Ti-O键长与2a的相比略有增大 (1.635 Å),端位Zr-O和Ti-Zr键长分别为1.780 Å、2.866 Å;结构 (2,2) 为 (ZrO2)2,具有C2h对称性,其端位Zr-O、Zr-Zr键长分别为1.784 Å、3.016 Å.n=3:结构 (3,1)具有Cs对称性,其端位Ti-O键长为1.629 Å;(3,2) 结构具有C1对称性,其端位Ti-O、Zr-O键长分别为1.631、1.783 Å;结构 (3,3) 为 (ZrO2)3,具有Cs对称性,其端位Zr-O键长为1.786 Å,与结构 (3,2) 相比Zr-O键变长.n=4:该类结构中心有一个4配位的氧原子,表现出了明显的离子性,因为在含氧的共价化合物中,氧原子一般不大于3配位[13], 随着Ti原子被Zr逐次取代,端位Ti-O键长由1.621 Å (4,1) 增大到1.624 Å (4,2)、1.625 Å (4,3),而端位Zr-O键长由1.778 Å (4,3) 增大到1.779 Å (4,4).n=5:结构 (5,1) 为一个Ti原子被Zr取代的基态结构,其端位平均Ti-O键长为1.616 Å,随着更多的Ti原子被Zr逐次取代,端位平均Ti-O键长逐渐增大,由1.616 Å依次变为1.623 Å (5,2)、1.628 Å (5,3)、1.630 Å (5,4).n=6:该类结构具有两个端氧和一个 4 配位的O原子,其余O原子均为桥氧,随着Zr原子数的增多端位平均Ti-O键长呈增大趋势,分别为1.619 Å (6,1)、1.621 Å (6,2)、1.624 Å (6,3)、1.626 Å (6,4) 和1.627 Å (6,5).n=7:结构 (7,1) 为 (TiO2)7团簇中一个与桥氧链接的Ti原子被Zr取代后的基态结构,其端位平均Ti-O键长为1.619 Å;结构 (7,2)、(7,3) 亦为与桥氧链接的Ti原子被Zr取代后的基态结构,其端位平均Ti-O键长分别为1.621、1.623 Å. 结构 (7,4)、(7,5)、(7,6)平均Ti-O键长分别为1.624、1.626、1.627 Å.
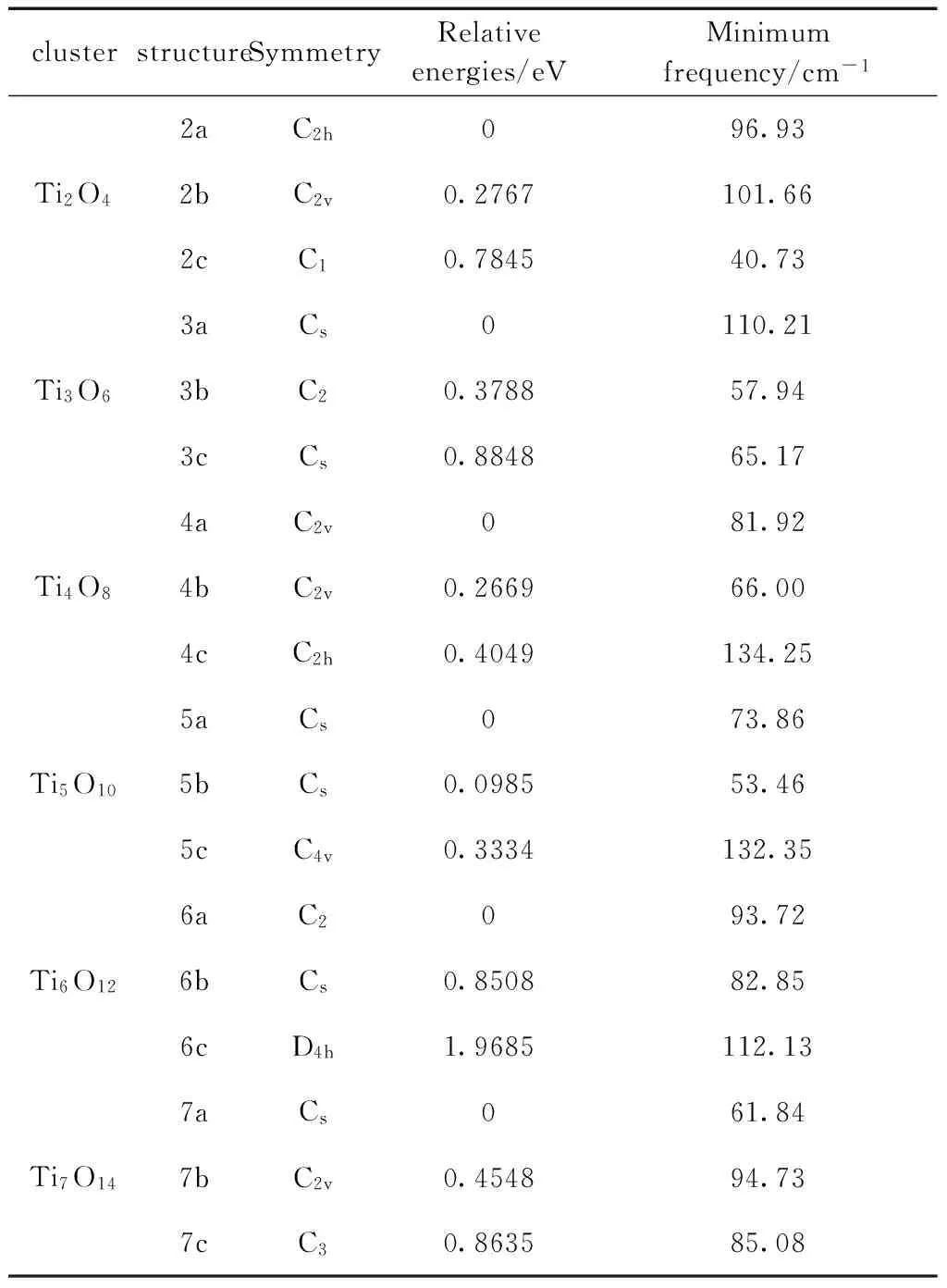
表1 (TiO2)n (n = 2-7) 团簇的几何参数
3.2 团簇的相对稳定性
通过分析团簇的平均结合能可以了解团簇的相对稳定性,具体到混合团簇,很重要的一点就是看它的稳定性是否相对于相应纯团簇的稳定性有所提高. 团簇Tin-mZrmO2n的平均结合能Eb(n,m)的计算公式如下:
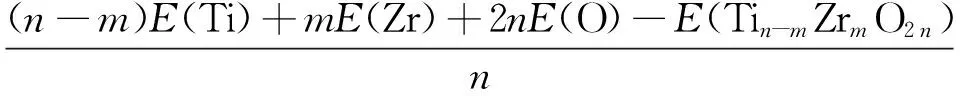
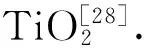
3.3 团簇的电子结构
为了进一步研究Tin-mZrmO2n团簇的轨道成键方式,我们以Tin-mZrmO2n(n=4,m=0、1、2、3、4)系列团簇为例,对优化后的团簇基态结构采用NBO方法分析了团簇的电荷布居特性和部分成键性质. 其中自由Ti原子的最外层电子排布为4s23d2,自由Zr原子最外层电子排布为5s24d2. 由于成键后电子重新分布问题,我们分别考虑了Ti的4s、3d、4p、5s、4d、5p轨道和Zr的5s、4d、5p、5d、6s、6p轨道. 表2给出了Tin-mZrmO2n(n=4,m=0、1、2、3、4) 基态结构各轨道上的NBO电荷 (外层电子) 分布.
在自由团簇中,由于处在不等价空间位置的原子感受到不同的势场,一部分原子将失去电荷,另一部分原子将得到电荷,从而出现电荷转移现象[29]. 从表2可以看出,O原子的2s轨道的NBO电荷数分布在1.70~1.87之间,O原子的NBO电荷主要分布在2p轨道,2p轨道的NBO电荷数在4.73~5.31之间. 从以上数据可以看出O原子的2s轨道失去电荷,2p轨道得到电荷,说明O原子内部发生了轨道杂化现象. 对于Ti原子,只有Ti3ZrO8团簇中的10号Ti原子的4s轨道有NBO电荷,其NBO电荷数为0.16,其余4s轨道NBO电荷数为0;Ti原子的电荷分布主要集中在3d轨道,3d轨道的NBO电荷数在2.08~2.15之间,从表中我们可以看到只有Ti2Zr2O8团簇的Ti原子4p轨道NBO电荷数不为零 (0.08),除Ti3ZrO8团簇中的10号Ti原子的5s轨道NBO电荷数为零,其余Ti原子的5s轨道有少量NBO电荷 (0.14、0.15),Ti原子的4d、5p轨道也有少量电荷 (0.06~0.29). 以上数据说明Ti原子的4s轨道失去了电荷,而3d轨道得到了电荷,发生了轨道杂化现象. Zr原子的5s轨道有少量的NBO电荷 (0.11、0.13),大部分NBO电荷分布在4d轨道,电荷在1.55~1.64之间,5p、5d、6p轨道上存在少量NBO电荷,NBO电荷在0.04~0.19之间. 从数据不难看出Zr原子的5s、4d轨道失去电荷,5p、5d、6p轨道得到少量电荷,说明Zr原子内部发生了轨道杂化现象.
进一步分析数据不难发现,Ti原子和Zr原子向O原子转移了部分电荷. Ti原子4s轨道,Zr原子5s、4d轨道的电荷转移到了O原子的2p轨道上,而且Zr原子向O原子转移的电荷数大于Ti原子向O原子转移的电荷数. 众所周知,元素的电负性与键能和反应热之间存在着内在的联系,如果成键原子的电负性差值越大,键能就越大,反应热效应就越大,反应就越容易进行,形成的化合物就越稳定. O、Ti、Zr的电负性值分别为3.44、1.54和1.33,很明显O与Zr的电负性差值大于O与Ti的电负性差值,所以随着Zr原子数的增加团簇的稳定性增强. 我们还发现,随着Zr原子数的增加Ti原子的平均NBO电荷数在增加,而Zr原子的平均NBO电荷数在减少,这说明Ti与Zr之间发生了电荷转移现象,形成了稳定的Ti-O-Zr键,Ti-O-Zr键的形成有利于Tin-mZrmO2n团簇光催化性能的提高,这与文献[11]、[12]中的结论一致.

图2 Tin-mZrmO2n(n=2-7,0≤m≤n) 基态结构的平均结合能随Zr原子数m的变化关系Fig.2 The curves of Eb(n, m) of the ground-state structures of Tin-mZrmO2n (n = 2-7,1≤m≤n) clusters vs. the number of Zr atoms

图3 Tin-mZrmO2n (n=4,m=0、1、2、3、4) 团簇基态结构HOMO、LUMO和几个占据轨道Fig.3 The HOMO, LUMO and several occupied molecular orbital pictures of the ground-state structures of Tin-mZrmO2n (n=4,m=0、1、2、3、4) clusters
团簇的前线轨道可以在一定程度上反映体系电子结构的特点,通过对HOMO和LUMO等一些轨道的分析,可以得到团簇的成键信息[30]. 图3给出Tin-mZrmO2n(n=4,m=0、1、2、3、4) 团簇基态结构的HOMO、LUMO和其它的一些占据轨道. 从图3可以看出,Ti4O8、Ti3ZrO8、Ti2Zr2O8、TiZr3O8、Zr4O8团簇的HOMO、HOMO-1、HOMO-2和HOMO-3轨道都是离域π成键轨道.
在此以Ti2Zr2O8为例给出其轨道成分分析. Ti2Zr2O8团簇的HOMO轨道主要由O (1,2) 原子的2pz(67.00%)、3pz(33.00%) 轨道和O (3,4,5,6) 原子中2pz(56.20%)、3pz(43.80%) 轨道构成;HOMO-1轨道主要由O (1,2) 原子的2pz(67.30%)、3pz(32.70%) 轨道,O (3,6) 原子中2px(24.00%)、2py(23.80%)、2pz(30.70%)、3pz(21.50%) 轨道和O (4,5) 原子中2px(36.30%)、2pz(24.30%)、3px(22.30%)、3pz(17.10%) 轨道构成;HOMO-2轨道主要由O (1,2) 原子的2px(49.90%)、2py(18.50%)、3px(21.90%)、3py(9.70%) 轨道,O (3,6) 原子中2px(31.20%)、2py(28.80%)、2pz(40.00%) 轨道和O (4,5) 原子中2px(25.80%)、2pz(38.40%)、3px(20.00%)、3pz(15.80%) 轨道和O8原子的2py(55.10%)、3py(44.90%) 轨道构成;HOMO-3轨道主要由O (1,2) 原子的2px(48.60%)、2py(21.12%)、3px(19.78%)、3py(10.50%) 轨道和O (3,4,5,6) 原子中2pz(62.32%)、3pz(37.68%) 轨道构成.
4 结 论
采用密度泛函理论(DFT)中的B3LYP方法,在6-31G*基组水平上对Tin-mZrmO2n(n=2-7,0≤m≤n) 团簇基态几何结构、相对稳定性和电子结构进行了研究,得到的主要结论如下:
(1) 用Zr原子逐次替换TinO2n团簇中的Ti原子,发现与桥氧链接的Ti原子被Zr取代后形成的混合团簇稳定性较高.
(2) Tin-mZrmO2n混合团簇的稳定性高于TinO2n团簇,且随着Zr含量的增加,混合团簇的稳定性增强.
(3) 从团簇的NBO电荷分布可以清楚的看到,Tin-mZrmO2n混合团簇中Ti、Zr、O原子之间发生了电荷转移现象,形成了稳定的Ti-O-Zr键,将有助于TiO2光催化性能的提高.
[1] Pascual J, Camassel J, Mathieu H. Resolved quadrupolar transition in TiO2[J].Phys.Rev.Lett., 1977, 39: 1490.
[2] Linsebigler A, Lu G, Yates J T. Photocatalysis on TiOnsurfaces: principles,mechanisms,and selected results[J].Chem.Rev., 1995, 95: 735.
[3] Hoffman M R, Martin S T, Choi W,etal. Environmental applications of semiconductor photocatalysis[J].Chem.Rev., 1995, 95: 69.
[4] Fujishima A, Honda K. Electrochemical photolysis of water at a semiconductor electrode[J].Nature, 1972, 238: 37.
[5] Xia X H, Lu L, Walton A S,etal. Origin of significant visible-light absorption properties of Mn-doped TiO2thin films[J].ActaMater., 2012, 60: 1974.
[6] Deng Q R, Xia X H, Guo M I,etal. Mn-doped TiO2nanopowders with remarkable visible light photocatalytic activity[J].Mater.Lett., 2011, 65: 2051.
[7] Dvoranová D, Brezová V, Mazúr M,etal. Investigations of metal-doped titanium dioxide photocatalysts[J].Appl.Catal. B, 2002, 37: 91.
[8] Tada H, Kiyonaga T, Naya S I. Rational design and applications of highly efficient reaction systems photocatalyzed by noble metal nanoparticle-loaded titanium(IV) dioxide[J].Chem.Soc.Rev., 2009, 38: 1849.
[9] Zhang H J, Chen G H, Bahnemann D W. Photoelectrocatalytic materials for environmental applications[J].J.Mater.Chem., 2009, 19: 5089.
[10] Liu G, Wang L, Yang H G,etal. Titania-based photocatalysts-crystal growth,doping and heterostructuring[J].J.Mater.Chem., 2010, 20: 831.
[11] Wu J C, Chung C S, Ay C L,etal. Nonoxidative dehydrogenation of ethylbenzene over TiO2ZrO2catalysts: II. The effect of pretreatment on surface properties and catalytic activities[J].J.Catal., 1984, 87: 98.
[12] Neppolian B, Wang Q, Yamashita H,etal. Synthesis and characterization of ZrO2-TiO2binary oxide semiconductor nanoparticles: Application and interparticle electron transfer process[J].Appl.Catal. A, 2007, 333: 264.
[13] Chen X, Wang X, Fu X. Hierarchical macro/mesoporous TiO2/SiO2and TiO2/ZrO2nanocomposites for environmental photocatalysis[J].EnergyEnviron.Sci., 2009, 2: 872.
[14] Eseribano V S, Amores J M G, López E F,etal. Surface and structural characterization of ZrO2-CeO2-supported molybdenum oxide catalysts[J].Mater.Chem.Phys., 2009, 114: 848.
[15] Eseribano V S, López E F, Panizza M,etal. Charaeterization of cubic ceria- zirconia powders by X-ray diffraction and vibrational and electronic spectroscopy[J].SolidStateSci., 2003, 5: 1369.
[16] Kitiyanan A, Ngamsinlapasathian S, Pavasupree S,etal. The preparation and characterization of nanostructured TiO2-ZrO2mixed oxide electrode for efficient dye-sensitized solar cells[J].J.SolidStateChem., 2005, 178: 1044.
[17] Mohammadi R M, Fray D J. Synthesis and characterisation of nanosized TiO2-ZrO2binary system prepared by an aqueous sol-gel process: Physical and sensing properties[J].Sens.ActuatorsB, 2011, 155: 568.
[18] Wang G H. Recent progress on cluster physics[J].ProgressinPhysics, 1994, 14: 121(in Chinese) [王广厚. 团簇物理的新进展[J]. 物理学进展, 1994, 14: 121]
[19] Wu H, Wang L S. Electronic structure of titanium oxide clusters: TiOy(y=1-3) and (TiO2)n(n=1-4)[J].J.Chem.Phys., 1997, 107: 8221.
[20] Qu Z W, Kroes G. Theoretical study of the electronic structure and stability of titanium dioxide clusters (TiO2)nwith n=1-9[J].J.Phys.Chem. B, 2006, 110: 8998.
[21] Hamad S, Catlow C R A, Woodley S M. Structure and stability of small TiO2nanoparticles[J].J.Phys.Chem. B, 2005, 109: 15741.
[22] Li S, Dixon D A. Molecular structures and energetics of the (TiO2)n(n = 1-4) clusters and their anions[J].J.Phys.Chem. A, 2008, 112: 6646.
[23] Bandyopadhyay I, Aikens C M. Structure and stability of (TiO2)n,(SiO2)n,and mixed TimSin-mO2n[n=2-5, m = 1 to (n-1)] clusters[J].J.Phys.Chem. A, 2011, 115: 868.
[24] Foltin M, Stueber G J, Bemstein E R. Investigation of the structure, stability, and ionization dynamics of zirconium oxide clusters[J].J.Chem.Phys., 2001, 114: 8971.
[25] Frish M J, Truck G W, Schlegel H B,etal.Gaussian09user'sreference[M]. Revision A. l, Gaussian Inc., Wallingford CT, 2009.
[26] Parr R G, Yang W.Density-functionaltheoryofatomsandmolecules[M]. New York: Oxford University Press, 1989.
[27] Walsh M B, King R A, Sehaefer H F. The structures,electron affinities,and energetic stabilities of TiOnand TiOn(n = 1-3)[J].J.Chem.Phys., 1999, 110: 5224.
[28] Kitiyanan A, Sakulkhaemaruethai S, Suzuki Y,etal. Structural and photovoltaic properties of binary TiO2-ZrO2oxides system prepared by sol-gel method[J].Compos.Sci.Technol., 2006, 66: 1259.
[29] Zhang X R, Cui Y N, Hong L L. Aromatic character studies on Mn0,±(M = Ir,Pt; n = 3,4) clusters via nucleus-independent chemical shifts (NICS) calculation and geometric structure[J].J.Comput.Theor.Nanosci., 2009, 06: 640.
[30] Sun J, Lu W C, Zhao L Z,etal. Structures and electronic properties of Al7X0,-and Al13X1,2,12-clusters with X=F, Cl, and Br [J].J.Phys.Chem. A, 2007, 111: 4378.
Structure and stability of Tin-mZrmO2n(n=2-7, 0≤m≤n) clusters
SHI Xiao-Feng, LI Xiu-Yan, GAO Yan-Lin, YANG Zhi, LIU Rui-Ping
(College of Physics and Optoelectronics, Taiyuan University of Technology, Taiyuan 030024, China)
The geometrical configurations, stability and electronic structures of the Tin-mZrmO2n(n=2-7, 0≤m≤n) clusters have been investigated by using B3LYP method of density functional theory (DFT). The calculated results show that the most stable structures for Tin-mZrmO2nclusters can be obtained by substituting Ti atoms connected to bridging oxygen atoms with Zr atoms. The mixed Tin-mZrmO2nclusters are more stable than TinO2nclusters. For the same size Tin-mZrmO2nclusters (nis the same), the binding energies increase approximately linearly with the increase of the number of Zr atoms, which means the Tin-mZrmO2ncluster with more Zr atoms is relatively more stable. The charge transfer occurs among Ti, Zr and O atoms, indicating the formation of Ti-O-Zr bond in the mixed Tin-mZrmO2nclusters.
Tin-mZrmO2nclusters; Density functional theory; Geometrical configuration; Stability; Electronic structure
103969/j.issn.1000-0364.2015.12.012
2014-01-10
教育部科学技术研究重大项目基金(212104); 国家自然科学基金(11104199);山西省自然科学基金(2012011021-3)
石小峰(1985—),女, 山西人, 硕士研究生, 主要从事团簇结构和性质研究.E-mail: shixiaofeng5510@163.com
O561
A
1000-0364(2015)06-0983-10

