板蓝根颗粒质量标准研究
戴耀清,薛非凡
(1.湖北省襄阳市食品药品检验所,湖北 襄阳 441021; 2.湖北省襄阳市食品药品监督管理局,湖北 襄阳 441021)
板蓝根颗粒质量标准研究
戴耀清1,薛非凡2
(1.湖北省襄阳市食品药品检验所,湖北 襄阳 441021; 2.湖北省襄阳市食品药品监督管理局,湖北 襄阳 441021)
目的 建立板蓝根颗粒的质量标准。方法 使用薄层色谱法对板蓝根进行薄层鉴别。采用高效液相色谱法,使用Inertsil ODS-3柱(250 mm×4.6 mm,5 χm)为色谱柱,甲醇-水(14∶86)为流动相,流速1 mL/min,柱温为室温(27℃),检测波长为260 nm。结果 薄层色谱法得到的薄层色谱中,供试品在与对照药材和对照品色谱相应的位置上,显相同颜色的斑点。当腺苷进样量在0~0.848 χg范围内与峰面积线性关系良好(r=0.999 9,n=6),加样回收试验的回收率为98.91%,RSD=0.61%(n=9)。结论 该法简便、准确、可靠、专属性强、重复性好,可作为板蓝根颗粒的质量标准。
板蓝根颗粒;质量标准;薄层色谱;高效液相色谱法;腺苷
板蓝根颗粒由板蓝根组方,具有清热解毒、凉血利咽功效,用于肺胃热盛所致咽喉肿痛、口咽干燥、腮部肿胀,急性扁桃腺炎、腮腺炎见上述证候者[1]800。原标准仅有 1项薄层鉴别,无含量测定项。在原标准的基础上,参考板蓝根药材标准,增加1个薄层鉴别,以对照药材和表告依春对照品为对照对其所含表告依春进行鉴别[2-3],提高了鉴别的专属性;含量测定指标有测腺苷[4-6]、靛玉红[7]、表告依春[8]、蔗糖[9]、靛蓝与靛玉红[10]、氨基酸[11]。本研究中以其水溶性成分腺苷(抗炎成分)作为控制指标进行含量测定,结果表明质量标准专属性强、可控性好,可更好地控制板蓝根颗粒的内在质量。现报道如下。
1 仪器与试药
岛津LC-10A型高效液相色谱仪(检测器为SPD-10AVP型紫外检测器,CBM-102工作站);CP-225D型电子天平(北京赛多利斯仪器系统有限公司);KQ-100B型超声波清洗仪(昆山市超声仪器有限公司)。板蓝根对照药材(批号为 121177-200302),精氨酸对照品(批号为0872-9802);腺苷对照品(供含量测定用,批号为110879-200202),均由中国药品生物制品检定所提供;板蓝根颗粒(珠海正太制药有限公司,批号为20110501,20110502,20110503,20110504,20110505,20110506,20110507,20110508,20110509,20110510);硅胶 G(青岛海洋化工厂);732型强酸性阳离子树脂、无水乙醇、浓氨水、乙醇均为分析纯,甲醇为色谱纯。
2 方法与结果
2.1 精氨酸与板蓝根[4]薄层色谱鉴别
取本品1.0 g,加水50 mL使溶解,滤过,滤液通过处理好的732型强酸性阳离子树脂(柱长10 cm,内径1.5 cm),用水洗至洗脱液呈中性,再用2 mol/L的氨水150 mL洗脱,弃去前50 mL洗脱液,收集后100 mL洗脱液,水浴蒸干,残渣加稀乙醇1 mL使溶解,作为供试品溶液。按处方比例取缺板蓝根的药材,按照制备工艺制得板蓝根阴性样品,按供试品溶液的制备方法制成阴性对照品溶液。另取板蓝根对照药材0.5 g,加稀乙醇20 mL,超声处理20 min,滤过,滤液蒸干,残渣加稀乙醇1 mL使溶解,作为对照药材溶液;再取精氨酸对照品适量,加稀乙醇制成每1 mL中含0.2 mg的溶液,作为对照品溶液。照2010年版《中国药典(一部)》附录ⅥB薄层色谱法试验,吸取上述4种溶液各5 μL,分别点于同一硅胶G薄层板上,以无水乙醇-浓氨水(3∶2)为展开剂,展开,取出,热风吹尽薄层板上的氨,喷以茚三酮试液,加热至斑点显色清晰。供试品溶液色谱中,在与对照药材溶液和对照品溶液色谱相应位置上显相同颜色的斑点,阴性对照品溶液色谱中则无此班点(见图1)。
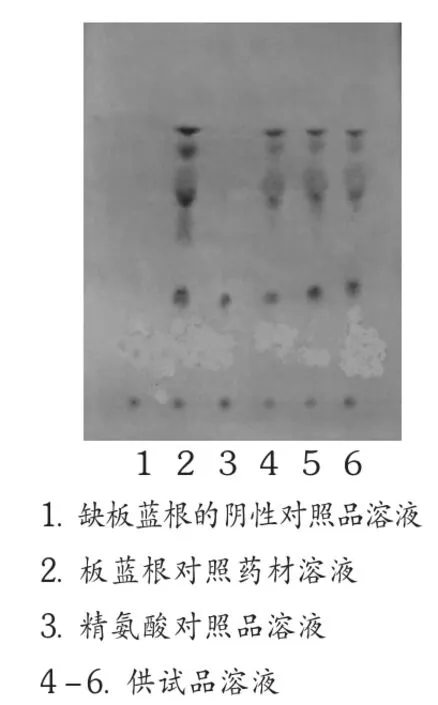
图1 薄层色谱图
2.2 腺苷含量测定
2.2.1 色谱条件
色谱柱:Inertsil ODS-3柱(250 mm×4.6 mm,5 μm),柱温:室温,27℃,流动相:甲醇-水(14∶86),检测波长:260 nm,流速:1 mL/min,进样量:10 μL。
2.2.2 溶液制备
精密称取腺苷对照品适量,加甲醇制成每1 mL含6 μg的溶液,即得对照品溶液。取本品装量差异项下内容物1.5 g,精密称定,置25 mL容量瓶中,加 30%甲醇约 20 mL,超声处理30 min (120 W,40 kHz),取出,放冷,加30%甲醇稀释至刻度,摇匀,滤过,取续滤液,即得供试品溶液。取不含板蓝根的阴性样品约1.5 g,精密称定,照供试品溶液制备方法制成阴性对照品溶液。
2.2.3 方法学考察
阴性干扰试验:吸取阴性对照品溶液10 μL,注入液相色谱仪。结果在腺苷峰相应位置上未见色谱峰(见图2),表明阴性样品对测定无干扰,该方法可用于本品腺苷含量的测定。
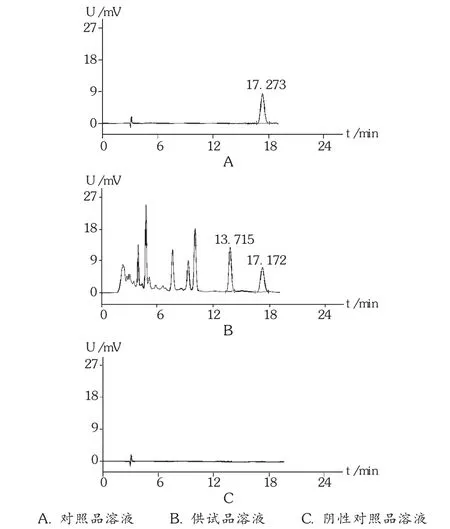
图2 高效液相色谱图
线性关系考察:精密称取腺苷对照品10.6 mg,置25 mL容量瓶中,加甲醇稀释至刻度,摇匀,精密吸取此对照品溶液1,2,2,2,2 mL,分别置 100,100,50,25,10 mL容量瓶中,加 30%甲醇稀释至刻度,摇匀,分别制成 0,4.24,8.40,16.96,33.92,84.80 μg/mL质量浓度的对照品溶液,吸取上述溶液各10 μL,注入色谱仪测定,以腺苷进样量为横坐标、峰面积(Y)为纵坐标进行线性回归,得回归方程 Y=141 144.6 X+1 183.7,r=0.999 9 (n=6)。结果表明,腺苷进样量在0~0.848 μg范围内与峰面积呈良好的线性关系。
精密度试验:取一定质量浓度(8.48 μg/mL)的对照品溶液,连续进样6次,测定峰面积。结果的 RSD为1.52%(n=6),表明仪器精密度良好。
稳定性试验:取同一供试品溶液在不同时间点(0~10 h)进样测定峰面积。结果的 RSD为1.31%(n=6),表明供试品溶液在10 h内保持稳定。
重复性试验:取同一批样品6份,按拟订方法测定结果含量0.116,0.114,0.115,0.117,0.117,0.114 mg/g,RSD为 1.14% (n=6),表明方法的重复性良好。
加样回收试验:取已知含量的样品(批号为20110501,含量为0.116 mg/g)9份,分别精密加入84.58 μg/mL的腺苷对照品溶液1.00 mL,按拟订方法测定含量,计算回收率。结果见表1。

表1 腺苷加样回收试验结果(n=9)
2.2.4 样品含量测定
取样品 10批(批号为 20110501,20110502,20110503,20110504,20110505,20110506,20110507,20110508,20110509,20110510),照拟订方法测定含量。结果 10批含量平均值为0.108 mg/g。
3 讨论
3.1 板蓝根薄层鉴别
板蓝根含精氨酸、亮氨酸、脯氨酸、缬氨酸等多种氨基酸,其氨基酸类成分含量很高。参照2010年版《中国药典(一部)》板蓝根药材鉴别项下方法[1]191并结合本品特点,将样品水溶后通过强酸性阳离子树脂柱,使氨基酸类成分得以富集,并去除了糖等黏稠物质的干扰,使样品溶液澄清,易于点样。同时本法展开时间较短,精氨酸对照品斑点 Rf值适中,考虑到本制剂仅板蓝根1味药材,且薄层板上样品与对照药材所有斑点均能对应,故将本法收载为本品的薄层鉴别;另参照药典中板蓝根药材鉴别表告依春[1]191项下方法鉴别表告依春。
3.2 腺苷含量测定
指标成分:含量测定的指标成分是板蓝根药材测表告依春(抗病毒成分),板蓝根颗粒以其水溶性成分腺苷(抗炎成分)作为控制指标进行含量测定,标准互补,双相控制,可形成完整的质量控制链。
流动相选择:以甲醇-水(8∶92)进行初试验,结果保留时间较长。调整为甲醇-水(14∶86)后,保留时间适中,腺苷峰与相邻色谱峰完全分离,分离度大于2.0,柱效较高,有效地节省了检验
时间,故选用甲醇-水(14∶86)为流动相。
测定波长选择:取腺苷对照品适量,加甲醇制成适宜质量浓度的供试品溶液,于紫外分光光度计上扫描测定,结果在259.6 nm波长处有最大吸收,参考2010年版《中国药典(一部)》冬虫夏草[1]106含量测定项下腺苷的测定波长,选用260 nm作为测定波长。
3.3 样品处理
提取溶剂:取本品3份(1.501 4,1.503 6,1.505 4 g),每份约1.5 g,精密称定,分别置25 mL容量瓶中,分别加甲醇、60%甲醇、30%甲醇各20 mL,超声处理30 min,取出,放冷,定容,摇匀,滤过,进样,测定各份样品的含量,以确定提取溶剂。结果表明甲醇提取效率最低(0.022 mg/g),峰形也较差;60%甲醇(0.106 mg/g)提取峰形虽然较好,但所得含量低于 30%甲醇(0.113 mg/g);30%甲醇提取峰形好,所得含量高。故选用30%甲醇作为提取溶剂。
提取时间:取本品3份(1.494 5,1.501 3,1.492 2 g),每份约1.5 g,精密称定,分别置25 mL容量瓶中,加30%甲醇约20 mL,分别超声处理20,30,40 min,取出,放冷,定容,摇匀,滤过,进样,测定各份样品的含量(0.095,0.113,0.113 mg/g),以确定提取时间。结果表明,超声处理30 min即提取完全。
[1]国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医
药科技出版社,2010.
[2]迟芳振,苏微国,车洪勇.板蓝根颗粒薄层色谱鉴别[J].药物分析杂志,1999,19(1):61-62.
[3]王小龙,邢海英.板蓝根颗粒鉴别方法改进[J].现代中药研究与实践,2004,18(1):47-48.
[4]许润春,杨 明,苏艳挑.HPLC测定板蓝根中腺苷含量[J].中成药,2005,27(6):742-753.
[5]郭 立,梁恒兴,赵 斌,等.板蓝根和大青叶类药材腺苷含量的测定[J].中成药,2006,28(7):1 064-1 066.
[6]张敏如,洪 亮,郭 群.高效液相法测定发酵虫草药粉和金水宝胶囊中腺苷的含量[J].中草药,1994,25(2):77-78.
[7]闵志良,况 英,冷文金.板蓝根颗粒质量标准的研究[J].药物分析杂志,2007,27(2):289-291.
[8]颜艺周,邹品文.HPLC法测定板蓝根颗粒中靛玉红的含量[J].中国药房,2008,9(3):211-212.
[9]安益强,贾晓斌,陈 彦,等.RP-HPLC测定不同厂家板蓝根颗粒中表告依春的含量[J].中华中医杂志,2009,24(4):529-531.
[10]粱奇峰,温欣荣,彭梦侠,等.板蓝根颗粒中蔗糖含量红外光谱法测定[J].化学研究与应用,2009,21(7):1 073-1 075.
[11]崔 熙,李松林,王建新,等.南、北板蓝根的鉴别和氨基酸含量比较分析[J].中药材,1992,15(5):17-18.
Study on Quality Standard of Banlangen Granules
Dai Yaoqing1,Xue Feifan2
(1.Xiangyang Municipal Drug and Food Administration,Xiangyang,Hubei,China 441021; 2.Xiangyang Food and Drug Administration,Xiangyang,Hubei,China 441021)
Objective To establish the quality standard of Banlangen Granules.M ethods The identification of Isatidis radix was used by TLC.The high performance liquid chromatography(HPLC)was used with the Inertsil ODS-3 column(250 mm×4.6 mm,5 μm)as the chromatographic column,methanol-water(14∶86)as the mobile phase,the flow rate of 1.0 mL/min and column temperature at 27℃.The wavelength of detector was 260 nm.Results The test sample and the reference medicinal material demonstrated the same color chromatographic spots at the corresponding position.The linear range of adenosine was 0-0.848 μg/mL(r=0.999 9,n=6),and the average recovery rate was 98.91%,RSD=0.61%(n=9).Conclusion This method is simple,accurate,reliable with good specificity and good reproducibility,and can be used for the quality standard of Banlangen Granules.
Banlangen Granules;quality standard;TLC;HPLC;adenosine
2013-08-14;
2014-08-12)
R284.1;R286.0
A
1006-4931(2015)03-0021-03

