载阿托伐他汀钙的普朗尼克/mPEG-b-PLGA混合胶束
刘 蕾, 徐慧萍, 卜永强, 宋仕永
(河南大学 药物研究所,河南 开封 475004)
载阿托伐他汀钙的普朗尼克/mPEG-b-PLGA混合胶束
刘蕾, 徐慧萍, 卜永强, 宋仕永*
(河南大学 药物研究所,河南 开封 475004)
摘要:目的研究普朗尼克/mPEG-b-PLGA混合胶束中两载体配比对载阿托伐他汀钙聚合物胶束性能的影响。方法制备不同配比的mPEG-b-PLGA、F127载阿托伐他汀钙聚合物混合胶束,用激光粒度分析仪(DLS),稳态荧光光谱仪,紫外分光光度计(UV)等对其粒径、临界胶束浓度、载药量以及体外释放的性质进行了考察。结果混合胶束在载药量、稳定性等方面都由于单一普朗尼克胶束,通过药物体外释放试验比较,在24h时,混合胶束的释放量明显提高,药物更完全的释放。结论在普朗尼克载阿托伐他汀钙胶束的制备中加入一定比例的mPEG-b-PLGA可不同程度的提高其性能,具有一定的应用前景。
关键词:阿托伐他汀钙;普朗尼克F127;mPEG-b-PLGA;混合胶束
动脉粥样硬化是动脉硬化血管病中最常见也是最重要的一种疾病,其发病原因主要为动脉壁上沉积一层像小米粥样的含胆固醇、类脂等黄色物质,从而造成动脉管壁增厚变硬、失去弹性和管腔缩小,若管径狭窄达75%以上时,则可能发生心肌梗死、心绞痛、心律失常、甚至猝死。大量临床实验证明他汀类药物作为调脂药物可有效防治该病的发生和发展,其中阿托伐他汀钙(ATV)是目前临床上使用最广泛的他汀类药物之一。阿托伐他汀钙因其口服吸收相对较好,多以片剂、胶囊剂进行使用,但口服该药物后,患者常出现胃肠道不适,甚至产生头痛、头晕、皮疹、视觉模糊和味觉障碍等副作用。而且因其经肝内广泛代谢,绝对生物利用度较低。
近年来,纳米技术在药物传输系统中的应用在生物医药界受到了广泛关注,不同的有机材料和无机材料已经用于药物传输系统的研制,其中某些已经应用于临床(如脂质体、微粒、纳米粒、胶束等)。这些药物传输载体能够将药物包裹或吸附于纳米粒子之中且可以特异性地进入病变细胞和组织,达到高效靶向的药物治疗。聚合物胶束因其粒径小、毒性小、可控释易降解等生物特性,尤其受到国内外生物医学及药学领域的高度关注[1-3],目前,已有一大批抗癌药聚合物胶束新剂型被研制出来,如载顺铂的NC-6004[4]、载紫杉醇的NK105[5]、载阿霉素的SP1049C[6]和NK911[7]等已经进入临床前应用阶段。聚合物胶束可以由一种表面活性剂组成,也可以由两种或两种以上的表面活性剂按照一定比例混合而得,后一种即为混合胶束,其通过利用不同嵌段共聚物协调链段数量,使多个功能聚集到1个药物传递系统中,可以克服单一聚合物形成的胶束稳定性差从而导致载药量低[8-9],生物利用度低等一系列问题[10-11]。普朗尼克(Pluronic)是一种多功能材料,由聚氧乙烯-聚氧丙烯-聚氧乙烯( PEO-PPO-PEO) 三嵌段组成,具有低毒性、实用性、生物相容性及逆转肿瘤多药耐药性(MDR)等优点。近年来,有很多关于Pluronic F127混合胶束的报道,如P123/F127载紫杉醇混合胶束[12],P105/F127载多西他赛的混合胶束[13],又如F127-b-poly (ε-caprolactone)载阿霉素混合胶束[14]等。PLGA是指聚乳酸( lactic acid, PLA)与聚乙醇酸( glycolic acid, PGA)的共聚物,是目前较为常用的生物可降解材料之一,其降解速率可通过调节其分子量PLA与PGA的配比得以控制[15];又有研究[16]证明,包含亲水层(如PEG)的PLGA的纳米粒子具有长循环性。
我们在使用F127制备载阿托伐他汀钙聚合物胶束的基础上,添加入不同比例的mPEG5000-b-PLGA,制备得到混合胶束,并考察了混合胶束的粒径、临界胶束浓度、载药量以及体外释放等性质。为制备高效、毒副作用小的阿托伐他汀钙新剂型提供理论支持。进一步的药理研究还在进行中。
1材料与仪器
1.1 药品、试剂
阿托伐他汀钙原料药物(ATV,纯度98.9%,河南大学药物研究所);Pluronic@ F127(美国sigma-aldrich公司);mPEG5000-b-PLGA 75/25 M=50000(济南岱罡生物科技有限公司);芘(Py,北京百灵威科技有限公司);甲醇为色谱纯、丙酮为分析纯(天津市富宇精细化工有限公司);去离子水(杭州娃哈哈集团有限公司)。
1.2 实验仪器
紫外-可见分光光度计(UV-2000, UNICO公司);荧光光谱仪(FluoroSENS Gilden公司);zeta电位及激光粒度分析仪(nano-ZS90 Malvern公司);冷冻干燥机 (LL1500,赛默飞世尔科技有限公司);恒温培养振动器(ZWY-2102C,上海智城分析仪器制造有限公司);电子天平(CP214,奥豪斯仪器(上海)有限公司);超声波清洗器(KQ116,昆山市超声仪有限公司);恒温磁力搅拌器(85-2,巩义市予华仪器有限责任公司)。
2实验方法
2.1 F127聚合物胶束与载ATV的F127聚合物胶束的制备
将0.2 g的F127加入到20 mL的去离子水中,室温搅拌5 h至6 h,即为F127聚合物胶束;另将0.2 g F127与25 mg阿托伐他汀钙溶入适量的甲醇溶液中,完全溶解后,逐滴加入到20 mL去离子水中,室温搅拌,至甲醇溶液完全挥发,将溶液8 000 r/min离心5 min,5 mL注射器取上清液,0.22 μm水系滤膜过滤,即得载阿托伐他汀钙的F127聚合物胶束。
2.2 mPEG5000-b-PLGA、F127 (PF)混合胶束与载ATV PF混合聚合物胶束的制备
采用溶剂挥发法分别制备mPEG5000-b-PLGA、F127 摩尔质量比为1∶1、1∶5、1∶10的混合胶束。首先,固定mPEG5000-b-PLGA为20 mg,用PE管分别称取不同质量的F127后,加入适量的丙酮溶液至完全溶解,然后将上述溶液分别逐滴加入到20 mL去离子水中,待丙酮完全挥发后,将该液8 000 r/min离心5 min,0.22 μm水系滤膜过滤,即得空白PF混合胶束。另将1 mL的20 mg/mL mPEG5000-b-PLGA丙酮溶液逐滴加入到盛有20 mL去离子水的烧杯中,约15 min 后,将3 mL的3 mg/mL的ATV甲醇溶液缓缓加入到上述溶液中,室温搅拌,待丙酮甲醇完全挥发后,将该溶液8 000 r/min离心5 min,0.22 μm水系滤膜过滤,即得载ATV的PF混合胶束。
2.3 胶束粒径的测定
采用zeta电位及激光粒度分析仪(DLS)测定胶束粒径分布,测定角度90°,温度25 ℃。
2.4 临界胶束浓度(CMC)的测定
利用芘探针荧光法测定[17-18]F127、不同摩尔配比的PF混合胶束临界胶束浓度的CMC, 首先准确称取芘0.6 mg,溶于适量的丙酮中,完全溶解后转移到500 mL容量瓶中,用丙酮定容,得到浓度为6×10-6mol/L的芘-丙酮储备液。然后将一定体积的芘-丙酮储备液加入到不同的容量瓶内,放置阴暗处使丙酮自然挥发,将配制好的F127、PF聚合物混合胶束溶液(浓度范围在1×100—1×10-5mg/mL)加入到容量瓶内,使芘的浓度为1×10-7mol/L。然后再将溶液在室温下超声20 min,放置于恒温培养震荡器40 ℃孵育48 h,使芘与胶束之间充分平衡,然后采用稳态荧光光谱仪测试芘的荧光强度,荧光条件:激发波长335 nm,波长范围为350~500 nm,激发和发射狭缝宽度均为5 cm。以芘在第一峰373 nm和第三峰384 nm的荧光强度比值为Y轴,胶束浓度的对数为X轴作图,由数据点的水平切线与突变曲线的切线的交点处为CMC值。
2.5 阿托伐他汀钙体外分析方法的建立
阿托伐他汀钙标准曲线的建立:准确称取阿托伐他汀钙6.1 mg,溶于25 mL甲醇中,所得溶液作为储备液,然后分别精密量取该溶液0.08、0.20、0.25、0.30、0.40、0.45 mL置于5 mL的容量瓶中,加去离子水稀释定容,阿托伐他汀钙最终浓度分别为0.020、0.049、0.061、0.073、0.098、0.110 mg/mL。采用紫外分光度法分别测定样品在最大吸收波长(λmax241 nm)处的吸光度,然后根据测得数据,以阿托伐他汀钙(ATV)标准溶液浓度C(μg/mL)对吸光度进行线性回归分析,得到ATV的标准曲线方程。
2.6 F127、PF混合胶束载药量的测定
采用紫外分光光度法测定胶束中ATV 的含量,分别精密称取一定量的F127、PF混合胶束胶束冻干品置于10 mL容量瓶内,加甲醇溶液超声破坏胶束结构,然后取定量的该溶液,精确稀释使该系列浓度涵盖在UV标准曲线的有效浓度范围内。在最大吸收波长241 nm下用紫外分光光度计测量它们的吸光度值A,根据测量结果绘制标准曲线计算药物的浓度,再根据:载药量(DL%)=(胶束中的药物量/胶束的总质量)×100%,计算得到F127、PF混合胶束的载药量。
2.7 载ATV的F127、PF混合胶束药物体外释放
采用透析法进行体外载药胶束药物释放实验:将5 mL新鲜制备的胶束溶液装入透析袋(截留分子量为8 000~14 000) 中,然后将上述透析袋置于50 mL PH为7.4PBS释放介质中,37 ℃ 120 r/min搅拌,于特定时间取样3 mL,分别于0.5、1、2、4、6、9、12、24 h取样2 mL,同时补充等量相应的新鲜释放介质。释放样品阿托伐他汀钙(ATV)的浓度采用UV法测定,并按照下列公式计算阿托伐他汀钙(ATV)的累积释放量。
式中Er:阿托伐他汀钙累积释放量(%);Ve:取样体积(mL);V0:释放介质体积(mL);Ci:第i次取样时阿托伐他汀钙的浓度(μg/mL);mdrug:载药胶束中阿托伐他汀钙的含量(μg);n:取样次数。
3结果与讨论
3.1 聚合物胶束粒径测定
不同摩尔比的PF混合胶束粒径测定结果如表1,我们可以看出F127的空白胶束平均粒径为23 nm,当将阿托伐他汀钙加入到F127胶束中后,阿托伐他汀钙分子进入到胶束的疏水核,形成的载药粒径为114 nm,这与文献报道[19]基本一致。当F127胶束中引入mPEG5000-b-PLGA胶束形成PF摩尔比为1∶1、1∶5、1∶10混合胶束后,粒径均一,平均粒径为110 nm;载入阿托伐他汀钙的混合胶束的平均粒径为123 nm,略大于并接近于空白的混合胶束,可以认定阿托伐他汀钙的载入对混合胶束的粒径影响不大。实验结果表明,载药混合胶束粒径呈单峰分布,均小于200 nm(PDI<0.2)。聚合物胶束的粒径小于200 nm,可大大降低胶束被RES识别和摄取的机会通过EPR效应,从而聚集于病变部位,实现被动靶向作用[20];疏水内核使其具有较高的载药能力,从而提高药物疗效。

表1 不同摩尔比的PF混合胶束粒径和载药量统计表

图1 F127、mPEG5000-b-PLGA、PF混合胶束粒径分布图
3.2 紫外分光光度(UV)分析方法的建立
将阿托伐他汀钙标准溶液浓度C(mg/mL)与吸光度进行线性拟合得到阿托伐他汀钙的标准曲线如图2,曲线方程为:A=40.38011C-0.00325 (R2=0.997),线性范围:0.164~98.4 μg/mL,由相关系数(R2)可知,在测定的浓度范围内,线性良好。
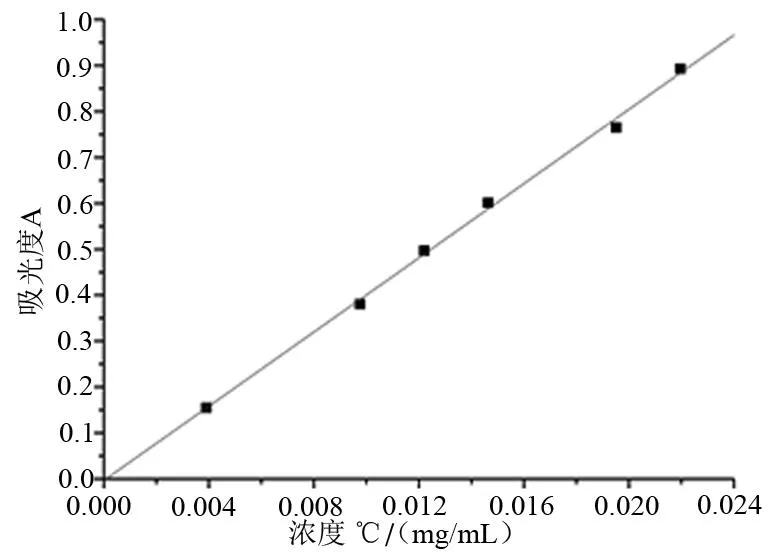
图2 阿托伐他汀钙标准曲线
3.3 PF混合胶束载药量考察
不同摩尔比的PF混合胶束载药量测定结果如表1所示,F127的载药量约为10%,引入mPEG5000-b-PLGA形成混合胶束后载药量发生显著的变化。当PF摩尔比为1:10时混合胶束载药量较低约为8.3%;但当PF摩尔比为1∶5时,混合胶束的载药量为10.5%,大于F127的载药量;继续加大mPEG5000-b-PLGA的量(PF的摩尔比为1∶1时),混合胶束的载药量明显增高,达到22%,远远高于F127的载药量。实验结果表明:适当的引入mPEG5000-b-PLGA(PF摩尔比为高于1∶5时)可以提高胶束的载药量,增强药效。
3.4 临界胶束浓度(CMC)的测定
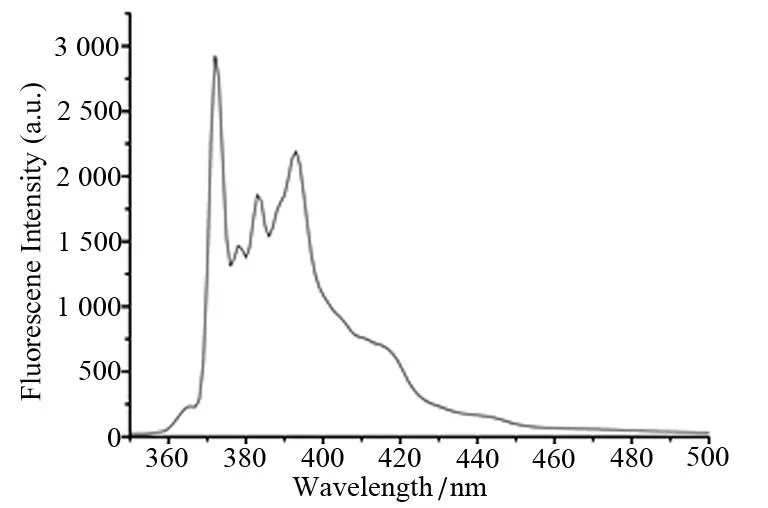
图3 芘的荧光光谱图
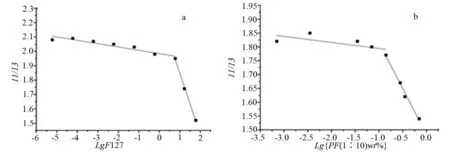
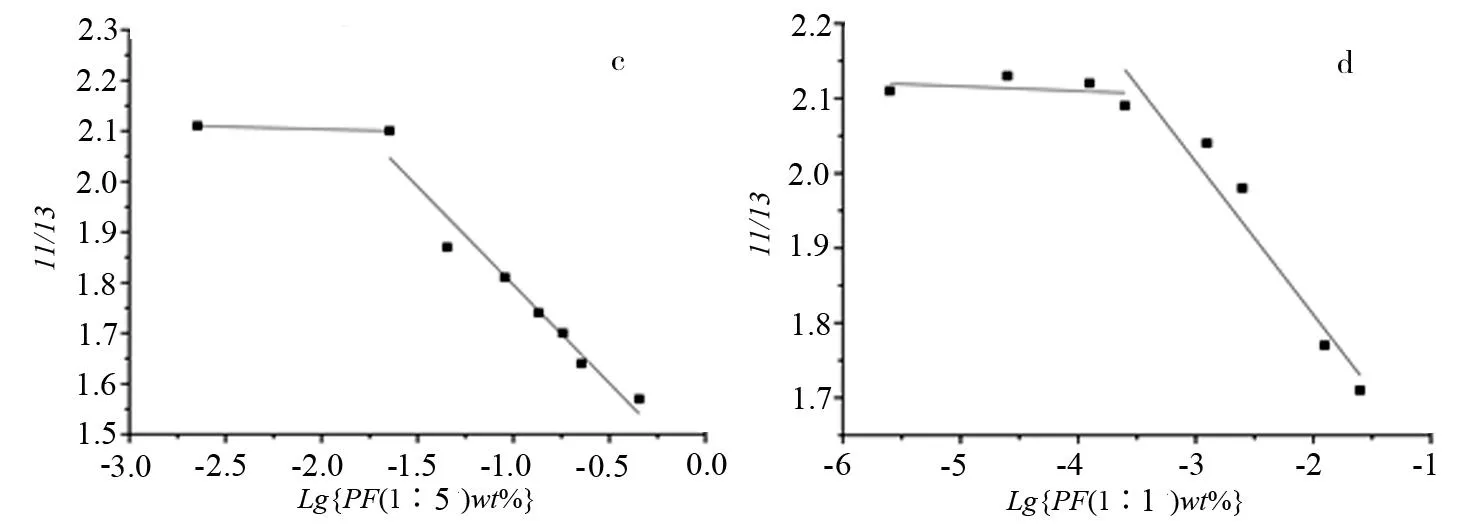
图4 芘荧光光谱中I1/I3的值与PF混合胶束、F127胶束浓度对数(LgC)的关系曲线图
经拟合计算我们可以得出F127的CMC值(图4a)为24.3mg/mL与文献报道基本一致;当少量引入PLGA时(PF摩尔比为1∶10如图4b),CMC值降低(约为1.2×10-1mg/mL);继续增加PLGA的摩尔比(PF 1∶5时如图4c)CMC值继续降低(约为1.6×10-2mg/mL),当PF摩尔比为1∶1时(如图4d),CMC值最低约为3.6×10-4mg/mL。CMC是胶束稳定性的重要参数,CMC值越低,说明胶束的热力学稳定性越高[21]。实验结果表明:PF混合胶束的CMC值远远低于F127空白胶束,说明mPEG5000-b-PLGA的引入可以增加胶束热力学稳定性,随着PLGA摩尔分数的增加,混合胶束的稀释稳定性增加。
3.5 载ATV的F127、PF混合胶束体外释放
如图5所示,F127胶束、PF混合胶束在2 h内没有突释现象,累计释放量均不超过40%,说明聚合物胶束具有缓释作用;在24 h时,F127的积累释放量为45%,混合胶束的释放量明显增高,说明mPEG5000-b-PLGA的引入可以增加药物的释放量,使药物更完全的释放;但混合胶束的释放速率大于F127的释放速率,原因尚不明确,相关研究表明可能与普朗尼克F127疏水嵌段插入疏水核心形成了较多亲水孔道有关[22-23]。
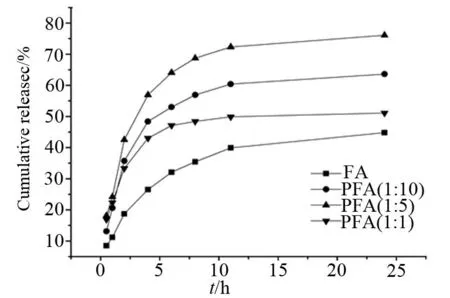
图5 载ATV的F127胶束与不同摩尔PF混合胶束体外释放曲线
4结论
研究结果显示,不同摩尔配比的mPEG5000-b-PLGA、F127混合胶束,载药后粒径与F127单一胶束接近,但稳定性和载药量均随mPEG5000-b-PLGA摩尔质量的增加而增加,而且mPEG5000-b-PLGA的引入可以明显增加胶束的释放量,使释放更加完全。相比于单一F127制备的聚合物胶束,PF混合胶束更适合于载阿托伐他汀钙新剂型的研制。
参考文献:
[1] Kwon G S, Kataoka K, et al. Block copolymer micelles as long-circulating drug vehicles [J]. Advanced Drug Delivery Reviews, 1995(16):295-309.
[2] Kwon G S , Okano T, et al. Polymeric micelles as new drug carriers [J]. Advanced Drug Delivery Reviews, 1996(21):107-116.
[3] Kwon G S, et al. Diblock copolymer nanoparticles for drug delivery [J]. Critical Reviews in Therapeutic Drug Carrier Systems, 1998,15(5):481-512.
[4] Plummer R, Wilson RH, et al. A Phase I clinical study of cisplatin-incorporated polymeric micelles (NC-6004) in patients with solid tumours [J]. British Journal of Cancer, 2011(104):593-598.
[5] Hamaguchi T, Matsumura Y, et al. NK105,a paclitaxel-incorporating micellar nanoparticle formulation, can extend in vivo antitumour activity and reduce the neurotoxicity of paclitaxel [J]. British Journal of Cancer, 2005(92):1 240-1 246.
[6] Danson S, Ferry D, et al. Phase I dose escalation and pharmacokinetic study of pluronic polymer-bound doxorubicin (SP1049C) in patients with advanced cancer [J]. British Journal of Cancer, 2004(90):2 085-2 091.
[7] Matsumura Y,Hamaguchi T,et al.Phase I clinical trial and pharmacokinetic evaluation of NK911, a micelle-encapsulated doxorubicin [J]. British Journal of Cancer,2004,91:1 775-1 781.
[8] Alexandridis P, Holzwarth J F, et al. Micellization of Poly(ethy1ene oxide)-Poly(propy1ene oxide)-Poly(ethy1ene oxide)Triblock Copolymers in Aqueous Solutions: Thermodynamics of Copolymer Association [J]. Macromolecules, 1994(27):2 414-2 425.
[9] Bose S, Roy M, et al. Recent advances in bone tissue engineering scaffolds [J]. Trends Biotechnology, 2012(30):546-554.
[10] Wei Zhang, Yuan Shi, et al. Ultifunctional PluronicP123/F127 mixed polymeric micelles loaded with paclitaxel for the treatment of multidrug resistant tumor [J]. Biomaterials, 2011(32):2 894-2 906.
[11] Saxena, Vipin, Hussain, et al. Polymeric Mixed Micelles for Delivery of Curcumin to Multidrug Resistant Ovarian Cancer [J]. Journal of Biomedical Nanotechnology, 2013(9):1 146-1 154.
[12] Wei Zhang, Yuan Shi, Yanzuo Chen, et al. Multifunctional Pluronic P123/F127 mixed polymeric micelles loaded with paclitaxel for the treatment of multidrug resistant tumors [J]. Biomaterials, 2011(32):2 894-2 906.
[13] Liangcen Chen, Xianyi Sha, Xinyi Jiang, et al. Pluronic P105/F127 mixed micelles for the delivery of docetaxel against Taxol-resistant non-small cell lung cancer: optimization and in vitro, in vivo evaluation [J]. International Journal of Nanomedicine, 2013(8):73-84.
[14] Qi Zhou, Zhao Zhang, Tao Chen, et al. Preparation and characterization of thermosensitive pluronic F127-b-poly(ε-caprolactone) mixed micelles [J]. Colloids and Surfaces B: Biointerfaces, 2011(86):45-57.
[15] Bose S,Roy M,Bandyopadhyay A.Recent advances in bone tissue engineering scaffolds [J]. Trends Biotechnol,2012(30):546-554.
[16] Acgoustakis K,Beletsi A. Effect of copolymer composition on the physicochemical characteristics,in vitro stability and biodistribution Of PLGA-mPEG nanoparticles [J]. International Journal of Pharmaceutics, 2003(259):115-127.
[17] JAguiar P, Carpena. On the determination of the critical micelle concentration by the pyrene 1:3 ratio method Journal of Colloid and Interface [J]. Journal of Colloid and Interface Science, 2003(258):116-122.
[18] Louisa Ould-Ouali, et al. Biodegradable Self-Assembling PEG-Copolymer as Vehicle for Poorly Water-Soluble Drugs [J]. Pharmaceutical Research, 2004(21):1 581-1 590.
[19] Rajib Basak, Ranjini Bandyopadhyay. Encapsulation of Hydrophobic Drugs in Pluronic F127 Micelles: Effects of Drug Hydrophobicity, Solution Temperature, and pH [J]. Langmuir, 2013(29):4 350-4 356.
[20] Rajib Basak, Ranjini Bandyopadhyay. Encapsulation of Hydrophobic Drugs in Pluronic F127 Micelles: Effects of Drug Hydrophobicity, Solution Temperature,and pH [J]. Langmuir, 2013(29):4 350-4 356.
[21] Qisheng Huo, Jun Liu, Li-Qiong Wang. A New Class of Silica Cross-Linked Micellar Core-Shell Nanoparticles [J]. Journal of Am Chem Soc, 2006,128:6 447-6 453.
[22] Kovzlov M Y, Melik-Nubarov N S . Relationship between Pluronic block copolymer structure, critical micellization concentration and partitioning coefficients of low molecular mass solutes [J]. Macromolecules, 2000(33):3 305-3 313.
[23] Hu Y, Jiang X Q, et al. Preparation and drug release behaviors of nimodipine-loaded poly(caprolactone) -polyethylene oxide)-polylactide amphiphilic copolymer nanoparticles [J]. Biomaterials, 2003(24):2 395-2 404.
[责任编辑李武营]
Atorvastatin calcium-loaded pluronic/mPEG-b-PLGA mixed micelles
LIU Lei,XU Huiping,BU Yongqiang, SONG Shiyong*
(InstituteofPharmaceuticsofHenanUniversity,Henan,Kaifeng475004,China)
Abstract:ObjectiveResearch of effect of two carrier Pluronic and mPEG-b-PLGA molar ratio on the atorvastatin calcium(ATV)-loaded polymer micelles.MethodsPreparation of different ratio of mPEG-b-PLGA, F127 load of ATV polymer mixed micelles, the particle size, critical micelle concentration, drug loading content and release properties in vitro were studied by laser particle size analyzer (DLS), steady state fluorescence spectrometer, UV spectrophotometer (UV). ResultsATV-PF micelles had superiorities over ATV-F micelles in drug loading content, stability and so on. From the drug release experiment in vitro, at 24h, contents of the mixed micelles drug release were significantly higher than Pluronic micelles and more completely. Conclusion Adding certain proportion of mPEG-b-PLGA in preparation of ATV-loaded Pluronic micelles can improve the properity of micelles to some extent, and has a potential application in the further.
Key words:torvastatin calcium(ATV); Pluronic F127; mPEG-b-PLGA; mixed micelles
*通讯作者:宋仕永(1979-),男,河南临颍县人,副教授,从事纳米药剂学的教学与科研工作。
作者简介:刘蕾(1977-),女,河南南阳市人,副教授,从事药用材料的开发与应用工作。
基金项目:河南省教育厅科学技术研究重点项目(13A350054)。
收稿日期:2015-05-12
文章编号:1672-7606(2015)03-0166-05
中图分类号:R944.1
文献标识码:A

