非诺贝特-羟丙基-β-环糊精固体分散体的制备及体外表征
谷福根,徐丽艳,高源源,吴春芝
非诺贝特-羟丙基-β-环糊精固体分散体的制备及体外表征
谷福根1*,徐丽艳2,高源源2,吴春芝1
目的 制备水难溶性药物非诺贝特(Fenofibrate,FNB)的固体分散体并进行体外表征。方法 以羟丙-β-环糊精(HP-β-CD)为载体材料,制备FNB的固体分散体,测定药物的包合率并进行物相鉴定及其体外溶出度考察。结果 FNB与HP-β-CD确已形成了固体分散体,且药物主要以无定型形式存在。固体分散体中FNB的体外溶出速率较原药显著提高。结论 HP-β-CD可用作FNB固体分散体制备的良好载体材料。
非诺贝特;HP-β-CD;固体分散体;物相鉴定;溶出度
0 引言
非诺贝特(Fenofibrate,FNB)为第3代氯贝丁酯类降血脂药,临床上可用于治疗高三酰甘油血症、高胆固醇血症及混合型高脂蛋白血症,具有疗效确切、毒副作用小、耐受性良好等特点[1]。但该药几乎不溶于水,其口服制剂体内吸收差,生物利用度低,严重影响其疗效[2-3]。由于水难溶性药物的体外溶出通常是其体内吸收的限速步骤[4],故改善此类药物的溶出度是提高其体内生物利用度及临床疗效的非常有效手段。固体分散体技术是制剂学中解决水难溶性药物溶出度差的常用手段之一[5-6]。在药物固体分散体的制备中,常采用水溶性PEG、PVP、糖、有机酸等材料作为载体,而以β-CD或其衍生物作为固体分散体载体的研究迄今国内未见报道,国外鲜有研究报道[7]。羟丙-β-环糊精(HP-β-CD)是一种非常重要的β-CD的水溶性衍生物,具有水溶性好、安全性高等优点[8]。笔者在前期研究中发现,HP-β-CD在水溶液中可明显增加FNB的溶解度[9],但由于该药物的分子体积较大,与HP-β-CD所形成超分子结构包合物的稳定性较差,从而导致药物的包合率较低,对药物溶出改善效果也不够理想。鉴于上述分析,本文首次尝试以HP-β-CD作为载体材料,采用常用固体分散体制备方法,制备FNB的固体分散体并考察其体外溶出行为,旨在为今后研究开发该药物的高生物利用度制剂提供重要理论依据。
1 仪器与试药
1.1 仪器 UV-2401PC紫外分光光度计(日本岛津);AB265-S型电子天平(瑞士梅特勒-托利多公司);SHZ-88A型往复水浴恒温振荡器(太仓市实验设备厂);HJ-5多功能恒温搅拌器(江苏省金坛市荣华仪器制造有限公司);KQ2200B型超声波清洗器(昆山市超声仪器有限公司);DFⅡ型集热式磁力加热搅拌器(江苏省金坛市荣华仪器制造有限公司);DHG-9140A型电热恒温鼓风干燥箱(上海精宏实验设备有限公司);ZRS-8智能溶出试验仪(天津大学无线电厂);Advance D8型X-射线粉末衍射仪(德国Bruker公司);NETZSCH STA 409 PC/PG热分析仪(德国耐驰仪器制造有限公司)。
1.2 试药 非诺贝特(批号:20091208,纯度100.3%,武汉银河化工有限公司);羟丙-β环糊精(批号:20091208,纯度99%,山东新大精细化工有限公司);十二烷基硫酸钠(AR,批号:20040520,天津市凯通化学试剂有限公司),其他试剂均为分析纯。
2 方法与结果
2.1 FNB分析方法的建立[10]
2.1.1 测定波长的选择 精密称取FNB 2.0 mg于100 mL量瓶中,分别加入乙腈和50%乙腈溶液适量,超声使溶解,放冷至室温,以对应溶剂稀释至刻度,摇匀,即得2种溶剂配制的FNB对照品溶液。将上述对照品溶液分别以相应溶剂为空白,于紫外分光光度计在200~400 nm波长范围内扫描,测定最大吸收波长。结果测得FNB在乙腈中的最大吸收波长为280 nm,在50%乙腈中的最大吸收波长为288 nm。
2.1.2 HP-β-CD紫外光谱的测定 称取HP-β-CD 5 mg,置于10 mL量瓶中,分别加入乙腈或50%的乙腈5 mL,超声处理5 min,放冷至室温,加对应溶剂至刻度,摇匀,以0.45 μm微孔滤膜过滤后,取续滤液,以对应溶剂为空白,于紫外分光光度计在200~400 nm波长范围内扫描。结果可见,HP-β-CD在上述波长范围内几乎无吸收,不干扰FNB的测定。
2.1.3 标准曲线的制备 精密量取上述以乙腈配制的FNB对照品溶液1.0、2.0、3.0、4.0、5.0、6.0、7.0 mL于10 mL量瓶中,用乙腈为溶剂定容,摇匀,即得浓度分别为2.3、4.6、7.0、9.3、11.6、13.9、16.2 μg/mL的药物标准溶液,以乙腈为空白,在280 nm波长处测定其吸光度。以吸光度(Y)为纵坐标、药物浓度(X)为横坐标作线性回归,结果求得标准曲线为:Y=0.047 7 X+0.013 3(r=0.999 9,n=7),表明在上述浓度范围内FNB的吸光度与其浓度呈良好线性关系;同法,精密量取上述以50%乙腈为溶剂的FNB对照品溶液,以50%乙腈为溶剂依法配制系列FNB标准溶液,以50%乙腈为空白,在288 nm波长处测定吸光度并绘制标准曲线。结果求得标准曲线方程为:Y=0.046 2 X+0.010 2(r=0.999 3,n=7),表明在上述浓度范围内FNB的吸光度与其浓度呈良好线性关系。
2.1.4 方法回收率的测定 按1∶1克分子比分别精密称取FNB与HP-β-CD,二者混合后,以乙腈为溶剂,依次配制FNB浓度分别为4.7、9.4、14.1 μg/mL的混合溶液。以0.45 μm微孔滤膜过滤后,取续滤液,以乙腈为空白,在280 nm波长处测定吸光度,并根据上述对应的标准曲线方程,计算FNB的浓度并计算方法的回收率,测定结果见表1。同法,以50%乙腈为溶剂,依次配制低、中、高不同浓度的1∶1克分子比FNB与HP-β-CD混合液,以50%乙腈为空白,在288 nm波长处测定吸光度,再根据对应标准曲线方程,计算药物浓度及方法的回收率,测定结果见表2。可见,采用乙腈或50%的乙腈,FNB测定方法的回收率符合要求。
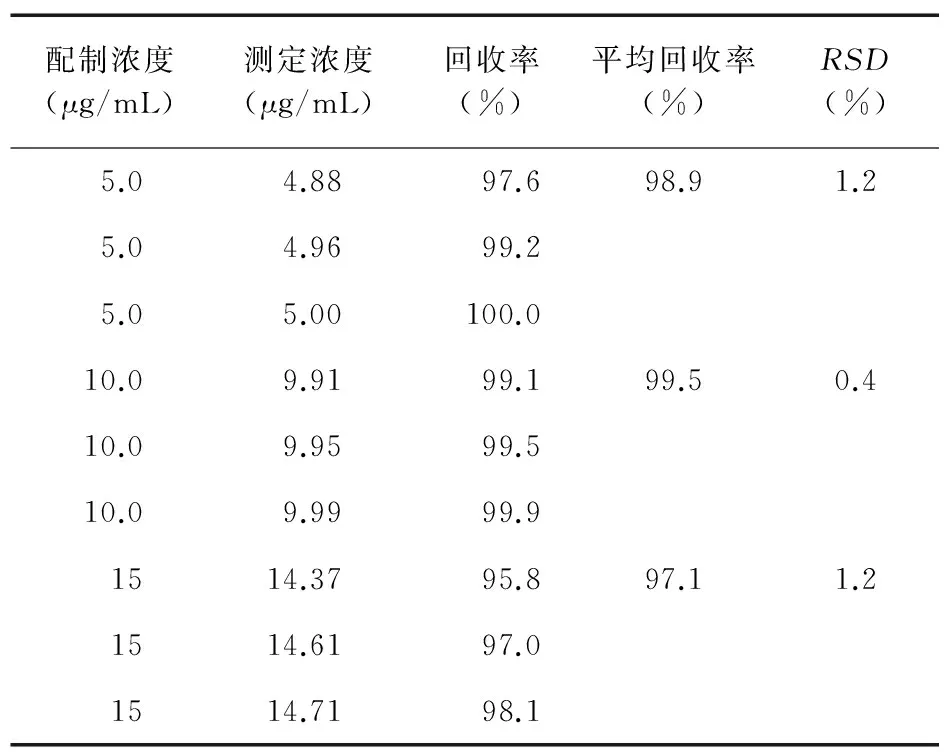
表1 以乙腈为溶剂FNB测定方法的回收率

表2 以50%乙腈为溶剂FNB测定方法的回收率
2.2 固体分散体的制备 按药物与HP-β-CD的克分子比为1∶1,称取FNB 0.4 g,以2 mL丙酮溶解后,在不断研磨下,将药液缓缓滴加到盛有1.6 g的HP-β-CD固体粉末的乳钵中,待滴加完毕后,继续研磨至均匀后,将所得产物置于真空干燥器中,于60 ℃,真空度为-0.09 kPa的条件下,减压干燥2 h,放冷至室温,取出固体产物,过80目筛后,即得。
2.3 包合率的测定 精密称取上述FNB固体分散体5.0 mg,置于25 mL量瓶中,一份用50%乙腈溶解并稀释至刻度,摇匀。精密量取上述溶液3 mL于10 mL量瓶中,以50%乙腈稀释至刻度,摇匀,以50%乙腈为空白,于紫外分光光度计在288 nm波长测定吸光度,代入对应的标准曲线方程,计算固体分散体中FNB的总浓度(Ct)。另一份FNB固体分散体,以乙腈为溶剂,同法处理后,以乙腈为空白,在280 nm波长测定吸光度,并代入对应的标准曲线方程,计算固体分散体中游离的FNB的浓度(Cf)。最后根据公式:包合率(K,%)=(1-Cf/Ct)*100,计算药物的包合率。结果测得所制备3批FNB固体分散体中药物的平均包合率为3.23%±0.38%(n=3)。可见,在FNB固体分散体中药物的包合率很低。
2.4 固体分散体的物相鉴定
2.4.1 差示热量扫描法(DSC) 分别测定FNB原药、HP-β-CD、克分子比1∶1的物理混合物及FNB-HP-β-CD固体分散体的DSC图谱,测定条件:以α-Al2O3为参比,在氮气保护下,升温速率为:10 ℃/min,温度从30 ℃升至250 ℃,测定结果见图1。可见,FNB在80~90 ℃内有一明显的吸热峰存在,HP-β-CD在此温度范围内无明显吸热峰,而物理混合物存在一小的吸热峰,且其位置与FNB的吸热峰较接近;固体分散体也存在吸热峰,但出峰早于物理混合物,说明有新物相形成。
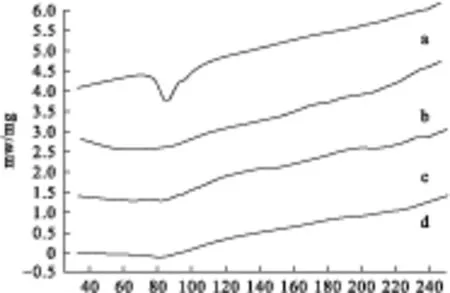
图1 样品DSC图谱
2.4.2 X-射线粉末衍射分析(XRD) 分别测定FNB原药、HP-β-CD、克分子比1∶1的物理混合物及FNB-HP-β-CD固体分散体的XRD图谱,测试条件:Cu-Ka辐射,管电压为40 kV,电流40 mV,扫描步长0.05 °,扫描速度5 °/min,扫描角度范围5~70 °。测定结果见图2。可见,FNB原药有非常强的多个晶体衍射峰存在,而HP-β-CD并无衍射峰存在,物理混合物有多个衍射峰存在,固体分散体与物理混合物相比,衍射峰数量明显减小且强度较小,说明在FNB固体分散体中,药物的存在形式与物理混合物有明显差异。
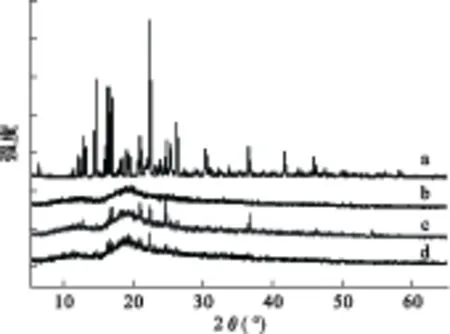
图2 样品的X-射线衍射图谱
2.5 溶出度的考察[11-12]
2.5.1 标准曲线的制备 精密称量FNB 10 mg,置于50 mL量瓶中,加无水乙醇5 mL使溶解,用1%的十二烷基硫酸钠(SDS)溶液稀释至刻度,摇匀。精密量取上述溶液5 mL置于50 mL量瓶中,用1%的SDS溶液稀释至刻度,摇匀,即得浓度为20 μg/mL的FNB标准溶液。精密吸取上述标准溶液2.5、3.75、5.0、6.25、7.5、8.25 mL于10 mL量瓶中,配制浓度为5.0、7.5、10.0、12.5、15.0、16.5 μg/mL的FNB系列溶液,以1% SDS溶液为空白,在290 nm处测定吸光度(Y),以FNB浓度(C)为横坐标、吸光度(A)为纵坐标,作线性回归,结果求得标准曲线方程为:A=0.444 C+0.014 2(r=0.999 8,n=6)。表明在上述浓度范围内FNB的吸光度与其浓度呈良好线性关系。
2.5.2 溶出度的测定 按照2010年版《中国药典》(二部)附录中溶出度测定法第二法(浆法),依法测定。分别称取FNB原药25 mg及相当量的药物固体分散体,以900 mL的1% SDS溶液为溶出介质,在测定温度为(37±0.5)℃、转速为100 r/min的条件下,分别于投入溶出杯后5、10、15、20、40、60、90 min取样5 mL,同时补加同温同体积的溶出介质,样品以0.45 μm微孔滤膜过滤,取续滤液以溶出介质适量倍数后,以溶出介质为空白,在290 nm处测FNB吸光度,根据上述标准曲线方程计算药物的浓度并求得累积溶出度。测定结果见图3。可见,固体分散体FNB在60 min接近完全溶出,而原药在相同时间内仅溶出约40%。

图3 FNB固体分散体及原药溶出曲线(n=3)
3 讨论
在FNB固体分散体的制备过程中,采用了沸点低、毒性较小且对药物溶解性能良好的丙酮作为溶剂,由于载体材料HP-β-CD在丙酮中不溶,故采用研磨法所制固体产物在减压干燥条件下,除去丙酮后,理论上应得到的是药物的固体分散体而非药物的环糊精包合物。为了证实这一推测,在本研究中对所制固体产物中药物的包封率进行了精确测定。在参考文献[10]的基础上,笔者在预实验中发现,HP-β-CD在乙腈中完全不溶,而在50%的乙腈可溶,FNB在上述2种乙腈中均可溶解,因此,本文通过采用50%的乙腈为溶剂,测定所制固体产物中FNB的总含量(包括被包封的药物部分与游离的药物部分),再通过采用纯乙腈为溶剂,测定所制备产物中游离部分FNB的含量,从而准确地计算出药物的包封率。本研究结果发现,所制备3批次产物中药物的包封率仅为3%,表明固体产物中绝大部分药物以游离形式而非以包合物的形式存在。DSC与XRD法物相鉴定结果表明,固体产物中药物与HP-β-CD已形成一全新物相,药物主要以无定型的形式存在。综合以上研究结果,FNB与HP-β-CD确已形成了固体分散体。
溶出度结果表明,FNB与HP-β-CD形成固体分散体后,药物的溶出速度显著提高,其原因主要是由于形成固体分散体后,绝大部分FNB以无定型形式分布在水溶性良好的HP-β-CD表面上,导致药物的表面积显著增大,进而加快溶出速度[13]。另一次要原因是,有少量药物与HP-β-CD形成了包合物,也会导致药物溶出的改善。鉴于FNB形成固体分散体后,其溶出速度明显提高,而溶出步骤通常又是难溶性药物体内吸收的限速步骤,因此推测该药物在体内的吸收以及生物利用度会有显著改善。
由于在现代制药工业中,β-环糊精(β-CD)或其衍生物通常用作包合材料,通过制备药物的环糊精包合物来改善一些难溶性药物的溶解度、溶出度、体内生物利用度等固有缺点,而本文首次尝试采用HP-β-CD作为固体分散体的载体,来制备难溶性药物的固体分散体,以期改善药物的溶出特性。本研究结果充分证实,β-环糊精(β-CD)或其衍生物是制备药物固体分散体的良好载体,这为今后在制药工业中更好地开发利用该类药用辅料提供了崭新的思路。
[1]李学明,顾立,王永禄,等.熔融乳化法制备非诺贝特纳米混悬剂[J].中国医药工业杂志,2009,40(5):349-354.
[2]Chen YP,Lu Y,Chen JM,et al.Enhanced bioavailability of the poorly water-soluble drug fenofibrate by using liposomes containing a bile salt [J].Int J Pharm,2009,376(1):153-160.
[3]Huang QP,Wang JX,Zhang ZB,et al.Preparation of ultrafine fenofibrate power by solidification process from emulsion[J].Int J Pharm,2009,368(1):160-164.
[4]Hanafy A,Spahn-Langguth H,Vergnault G,et al.Pharmacokinetic evaluation of oral fenofibrate nanosuspensions and SLN in comparison to conventional suspensions of micronized drug[J].Adv Drug Del Rev,2007,59(2):419-426.
[5]Lian X,Dong J,Zhang J,et al.Soluplus® based 9-nitrocamptothecin solid dispersion for peroral administration:Preparation,characterization,in vitro and in vivo evaluation[J].Int J Pharm,2014,477(1-2):399-407.
[6]Siahi-Shadbad MR,Ghanbarzadeh S,Barzegar-Jalali M,et al.Development and characterization of solid dispersion for dissolution improvement of furosemide by cogrinding method[J].Adv Pharm Bull,2014,4(4):391-399.
[7]Rahman Z,Zidan AS,Khan MA.Risperidone solid dispersion for orally disintegrating tablet:its formulation design and non-destructive methods of evaluation[J].Int J Pharm,2010,400(1-2):49-58.
[8]Liu M,Cao W,Sun Y,et al.Preparation,characterization and in vivo evaluation of formulation of repaglinide with hydroxypropyl-β-cyclodextrin[J].Int J Pharm,2014,477(1-2):159-166.
[9]谷福根,高源源,吴春芝,等.非诺贝特与2种β-环糊精水溶性衍生物在水溶液中包合作用研究[J].中南药学,2013,11(4):258-261.
[10]Van HT,Piel G,De Hassonville SH,et al.Determination of the free/included piroxicam ratio in cyclodextrin complexes:comparison between UV spectrophotometry and differential scanning calorimetry[J].Eur J Pharm Sci,2002,15(4):347-353.
[11]王悦,王永禄,李学明,等.非诺贝特纳米混悬剂溶出度测定与体内吸收的相关性评价[J].中国现代应用药学,2010,27(11):1013-1018
[12]翁腾飞,戚建平,卢懿,等.非诺贝特纳米悬液的制备及在Beagle犬体内的生物利用度[J].中国医药工业杂志,2014,45(3):234-239
[13]Sanganwar GP,Gupta RB.Dissolution-rate enhancement of fenofibrate by adsorption onto silica using supercritical carbon dioxide[J].Int J Pharm,2008,360(1):213-218.
Preparation and characterization of fenofibrate-hydroxypropyl-β-cyclodextrin solid dispersion
GU Fu-gen1*,XU Li-yan2,GAO Yuan-yuan2,WU Chun-zhi1
(1.Affiliated Hospital,Inner Mongolia Medical University,Hohhot 010050,China;2.School of Pharmacy,Inner Mongolia Medical University,Hohhot 010110,China)
Objective To prepare a water-insoluble drug fenofibrate (FNB) solid dispersion and investigate its related characteristics.Methods The FNB solid dispersion was prepared by using HP-β-CD as carrier material.The drug encapsulation efficiency,physical phase identification andinvitrodissolution test of the FNB solid dispersion were also accomplished.Results The FNB solid dispersion formed with HP-β-CD existed in an amorphous form.Theinvitrodissolution of FNB from the solid dispersion was more rapid than that from the intact drug.Conclusion HP-β-CD may use as a good carrier in the preparation of FNB solid dispersion.
Fenofibrate; HP-β-CD; Solid dispersion; Physical phase identification; Dissolution
2014-11-24
1.内蒙古医科大学附属医院,呼和浩特 010050;2.内蒙古医科大学药学院,呼和浩特 010110
内蒙古医科大学附属医院博士启动金项目(NYFYBQ2010018)
10.14053/j.cnki.ppcr.201507017
*通信作者

