不同剂量右美托咪定治疗剖宫产患者术中寒战效果观察
王淑伟
(广东省深圳市坪山新区人民医院,广东 深圳 518118)
不同剂量右美托咪定治疗剖宫产患者术中寒战效果观察
王淑伟
(广东省深圳市坪山新区人民医院,广东 深圳 518118)
目的 探讨不同剂量的右美托咪定(DEX)治疗剖宫产患者术中寒战的效果。方法 选取剖宫产手术麻醉后出现寒战的产妇150例,随机分为5组:0.3μg/kg右美托咪定组(A组),0.5μg/kg右美托咪定组(B组),1.0μg/kg右美托咪定组(C组),曲马多组(D组)和生理盐水组(E组),每组30例。胎儿娩出后缓慢静注相应药物,其中A组予右美托咪定0.3μg/kg+20mL生理盐水,B组予右美托咪定0.5μg/kg+20mL生理盐水,C组予右美托咪定1.0μg/kg+20mL生理盐水,D组予曲马多1.0mg/kg+20mL生理盐水静注,E组仅予20mL生理盐水静注,均于10min内泵注完毕。观察各组给药前(t0)及给药后15min(t1)、30min(t2)Ramsay评分、总体寒战控制效果以及不良反应的发生情况。结果A组寒战控制有效率为93%,B、C、D组临床有效率均为90%。4组相比差异无统计学意义(P>0.05)。A、B、C、D组给予DEX后t1、t2时的Ramsay评分相比t0时均明显升高(P<0.05),E组t1、t2时Ramsay评分与t0比较差异无统计学意义(P>0.05)。组间比较,给药后B、C、D组Ramsay评分高于E组(P均<0.05),t2时C组Ramsay评分均明显高于B组(P<0.05)。其余各组间Ramsay评分比较差异无统计学意义(P均>0.05)。D组发生不良反应者较多,使用DEX的患者随剂量增加不良反应发生率升高。结论 右美托咪定和曲马多均对剖宫产手术中寒战有良好的治疗作用,低剂量的右美托咪定在取得良好治疗效果的同时,较少有不良发应发生,值得临床应用。
右美托咪定;剖宫产;寒战
麻醉后寒战(postanestheticshivering,PAS)是临床麻醉的常见并发症,发生率通常在5%~65%[1],其发生可能与低温、致热原因素、患者因素(性别、年龄等)、药物因素、消毒以及缺氧等有关[2-3]。剖宫产麻醉后术中寒战的出现会干扰监护仪的监测和手术者的操作,还会使产妇机体耗氧量成倍增加,容易引起低氧血症、心肌缺血、眼内压颅内压增高、乳酸中毒及术后切口感染等并发症的发生,给胎儿和产妇的身体健康和生命安全带来严重威胁[4-5]。因此,剖宫产患者麻醉后术中寒战的防治十分必要。目前,多以中枢性药物来防治PAS,比如哌替啶和曲马多等,但其不良反应的发生率较高,临床应用受到限制[6]。右美托咪定(dexmedetomidine,DEX)已被国内外研究证实具有很好的抗寒战作用,且不良反应较少,但目前研究尚未获得统一剂量和统一疗效[7]。本研究通过观察不同剂量DEX治疗剖宫产患者术中寒战的效果,以期为临床寻找治疗剖宫产患者术中寒战的最佳药物和DEX的最佳剂量。
1 临床资料
1.1 一般资料 选择2013年1—12月在我院麻醉科接受剖宫产并在行腰-硬联合麻醉后出现术中寒战症状的患者150例。患者年龄20~36(25.8±5.7)岁;体质量58~79(65.3±4.2)kg;ASAⅠ~Ⅱ级;手术方式为腹膜内或腹膜外剖宫产术;患者均为单胎妊娠。肝肾功能无异常,无心血管疾病史,无食物、药物过敏史,无精神、神经疾病,无妊娠合并高血压、子痫等疾病。将患者随机分为5组:0.3μg/kg右美托咪定组(A组)、0.5μg/kg右美托咪定组(B组)、1.0μg/kg右美托咪定组(C组)、曲马多组(D组)和生理盐水组(E组),每组30例。各组患者身高、体质量、年龄等一般资料比较差异无统计学意义(P>0.05),具有可比性。本研究经医院伦理委员会批准,患者签署知情同意书。
1.2 方法
1.2.1 腰-硬麻醉和DEX应用方法 患者术前均禁食8h、禁饮6h,入室后常规监测BP、HR、Sp(O2)、ECG。开放上肢静脉,建立静脉通路。控制室温24~26 ℃,湿度40%~60%。行腰-硬联合麻醉,穿刺间隙为L3—4或L2—3,见脑脊液后缓慢注入0.5%布比卡因1.5~2mL,并向上置管4cm留作术后镇痛用。麻醉满意后开始手术,术中常规监测BP、HR、Sp(O2),当患者出现寒战并持续3min仍不能缓解同时胎儿已娩出,静脉缓慢给药,均于10min内泵注完毕。A组:DEX0.3μg/kg+20mL生理盐水;B组:DEX0.5μg/kg+20mL生理盐水;C组:DEX1.0μg/kg+20mL生理盐水;D组:曲马多1mg/kg+20mL生理盐水;E组仅予20mL生理盐水静注。
1.2.2 监测与观察指标 观察寒战给药前(t0)及给药后15min(t1)、30min(t2)时的HR、平均动脉压(MAP)、Sp(O2)变化;在相应时间点进行Ramsay镇静评分(1分:不安静,烦躁;2分:安静合作;3分:嗜睡,能听从指令;4分:睡眠状态,但可唤醒;5分:呼唤反应迟钝;6分:深睡状态,呼唤不醒。其中2~4分为镇静满意,5~6分为镇静过度)。记录寒战程度,采用Wrench分级:0 级为无寒战,1级为竖毛和/或外周血管收缩和/或外周紫绀但无肌颤,2级为仅一组肌群肌颤,3级为超过一组肌群肌颤,4级为全身肌颤;将t2时的寒战控制效果作为判定疗效的依据(优:无寒战症状;良:寒战减轻;差:无明显效果。有效率为优、良者占本组全部病例数的百分比)。记录术毕恶心/呕吐、眩晕、低血压(收缩压<90mmHg,1mmHg=0.133kPa)、心动过缓(心率<60次/min)和牵拉反应等不良反应发生率。

2 结 果
2.1 各组不同时间点生命体征比较 组内比较:C、D组患者t1、t2的HR与t0时间显著下降(P均<0.05),A组、B组、E组t1、t2时HR与t0时比较差异无统计学意义(P均>0.05)。各组各时点的MAP及Sp(O2)比较差异无统计学意义(P>0.05)。组间比较,C组与D组各时点HR比较差异无统计学意义(P均>0.05)。C组与D组t1、t2时HR与E组比较显著下降(P均<0.05)。其余剂量组各时点的HR与E组比较差异无统计学意义(P均>0.05)。各组同一时点的Sp(O2)及MAP比较差异无统计学意义(P均>0.05)。见表1。

表1 各组不同时点生命体征比较
注:①与t0比较,P<0.05;②与E组比较,P<0.05。
2.2 各组寒战控制效果比较A组寒战控制有效率为93%,B、C、D组有效率均为90%。4组控制寒战均取得明显的效果,且差异无统计学意义(P>0.05)。见表2。
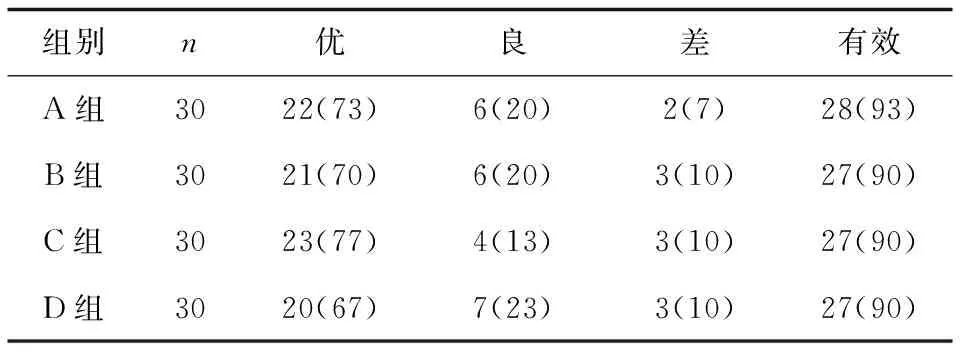
表2 各组寒战控制效果比较 例(%)
2.3 各组Ramsay评分比较 组内比较,A、B、C、D组t1、t2时Ramsay评分与t0比较差异有统计学意义(P均<0.05),E组不同时间点比较差异无统计学意义(P>0.05)。组间比较,B、C、D组t1、t2时Ramsay评分均明显高于E组(P均<0.05),t2时C组Ramsay评分明显高于其他各组(P均<0.05)。其余各组间Ramsay评分差异均无统计学意义(P均>0.05)。见表3。
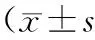
表3 各组Ramsay评分比较,分)
注:①与t0比较,P<0.05;②与E组比较,P<0.05;③与C组比较,P<0.05。
2.4 各组不良反应情况比较 C组、D组不良反应发生率显著高于其他各组(P均<0.05),其中C组心动过缓发生率明显高于其他各组(P均<0.05)。见表4。
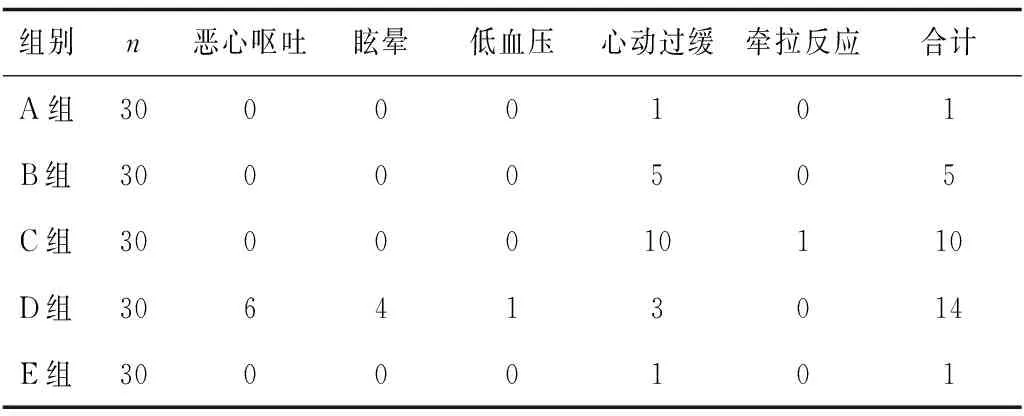
表4 各组不良反应情况比较 例
3 讨 论
PAS是临床麻醉的常见并发症,剖宫产是产科常见的手术类型之一,由于剖宫产患者特殊的生理改变(如妊娠晚期基础代谢率增高、血液循环加快、胎儿剖出后因腹内压骤降使散热增多、羊水和出血带走了大量热量等)以及腰-硬联合麻醉可抑制产妇的体温调节机制,使剖宫产发生PAS的可能大大增加[8-9]。而PAS的出现会影响手术操作,对胎儿和产妇的健康和安全产生不利影响。
本研究中,使用了DEX的患者HR均有下降,但仅C组相比给药前下降有明显差异。这可能是较大剂量的DEX造成的降压作用较为明显造成的。而各组MAP随时间增加虽有所降低,但无显著差异,且不良反应观察结果显示并未增加低血压的发生。这说明DEX可以维持术中MAP的稳定,这对于手术具有重要意义。在术中适当控制性降压,可以在保证器官在满足血供和氧供的同时,减少术中出血的概率,保持术野清晰,减少因血压过高造成的心脑血管意外,提高手术安全性。王志强[10]研究表明,在对全麻手术患者预防寒战时,使用生理盐水和曲马多的2组患者,用药5 min后收缩压、舒张压及心率明显高于使用DEX的患者,也提示了DEX的降压作用。本研究中,使用了不同剂量的DEX患者和使用了曲马多的患者在控制寒战发生中均取得了满意的效果,有效率均达到90%以上。李静等[11]也有类似研究结果。在Ramsay评分比较中,随着DEX应用剂量的增加,患者的镇静效果也有所增加,呈剂量依赖性。此外,在不良反应的观察中,使用了DEX的患者,随着剂量的增加发生心动过缓的概率也逐渐升高。有研究表明,心动过缓是DEX的常见不良反应[12]。本研究结果显示,在剖宫产手术中,低剂量的DEX可以明显降低心动过缓的发生率,提示低剂量的DEX可能具有更高的安全性。这是由于DEX药理机制决定的,其可激活中枢和周围神经系统中的α2受体,产生抗交感神经作用[13],并同时加强迷走神经心脏反射,从而降低心率,表现为心动过缓,低剂量的药物可能会减弱该种作用。有研究表明,恶心、呕吐是DEX等静脉麻醉药的常见不良反应[14]。吴伟华等[15]的研究表明,小剂量(0.5 μg /kg)DEX 缓慢静脉注射对椎管内麻醉后产生寒战的患者具有很好的抗寒战和镇静作用,且呼吸抑制、恶心呕吐等不良反应发生率较曲马多低,这与本研究结果一致。本研究中,A、B、C组患者均未发生明显眩晕、恶心呕吐等不良反应,这可能是由于本研究样本量较小,观察时间也较短造成的,对术后较长时间后的不良反应的发生还需要更多的研究。
综上所述,DEX是一种很好的治疗剖宫产患者术中寒战的药物,在使用0.3 μg/kg的小剂量时即可取得满意的疗效,同时可降低心动过缓等不良反应的发生率,其特有的维持MAP稳定的作用在手术中具有重要意义。该药物在临床具有广大的应用前景,但在其他类型的麻醉手术中的适宜剂量还需进一步探究。
[1] Crowley LJ,Buqqy DJ. Shivering and neuraxial anesthesia[J]. Reg Anesth Pain Med,2008,33(3):241-252
[2] 张红,冯艺. 全身麻醉术后寒战相关危险因素的研究[J]. 临床麻醉学杂志,2010,26(3):203-205
[3] Bajwa SJ,Gupta S,Kaur J,et al. Reduction in the incidence of shivering with perioperative dexmedetomidine:A randomized prospective study[J]. J Anaesthesiol Clin Pharmacol,2012,28(1):86-91
[4] 陆凤妹. 剖宫产术中寒战的原因探讨及护理干预[J]. 护理实践与研究,2011,8(21):146-147
[5] Carpenter L,Baysinger CL. Maintaining perioperative normothermia in the patient undergoing cesarean delivery[J]. Obstet Gynecol Surv,2012,67(7):436-446
[6] 史鸣. 曲马多的临床应用进展[J]. 中国实用医药,2009,4(24):241-243
[7] Kim YS,Kim YI,Seo KH,et al. Optimal dose of prophylactic d-exmedetomidine for preventing postoperative shivering[J]. Int J Med Sci,2013,10(10):1327-1332
[8] 王晓宁,刘丽,汪润,等. 低剂量曲马多预处理对剖宫产术麻醉后寒战的影响[J]. 中国医药,2012,7(12):1578-1580
[9] Ghobadifar MA,Zabetian H,Karami MY. Spinal pethidine and shivering for elective caesarean section[J]. Anaesth Intensive Care,2013,41(6):805
[10] 王志强. 右美托咪定与曲马多在全麻手术中预防寒战作用的比较[J]. 中国医药指南,2013,11(4):581-582
[11] 李静,黄德樱,向强. 右美托咪定与曲马多治疗剖宫产术中寒战的对比研究[J]. 心理医生,2012,21(4):323-324
[12] Piao G,Wu J. Systematic assessment of dexmedetomidine as an anesthetic agent:a meta-analysis of randomized controlled trials[J]. Arch Med Sci,2014,10(1):19-24
[13] 王志,唐显玲. α2-肾上腺素能受体激动剂右美托咪定在围术期的应用进展[J]. 医学综述,2010,16(20):3173-3175
[14] Bajwa S,Kulshrestha A. Dexmedetomidine:an adjuvant making large inroads into clinical practice[J]. Ann Med Health Sci Res,2013,3(4):475-483
[15] 吴伟华,蓝建良,程土荣,等. 右美托咪定和曲马多治疗椎管内麻醉后寒战效果的比较[J]. 浙江创伤外科,2013,18(3):443-444
10.3969/j.issn.1008-8849.2015.23.032
R
B
1008-8849(2015)23-2592-03
2014-04-20

