替加环素对耐碳青霉烯类鲍曼不动杆菌体外抗菌活性分析及联合用药研究
张晓玲 刘鹏 彭宗生 杜学娜
随着临床碳青霉烯类抗生素(如亚胺培南、美罗培南等)广泛应用于鲍曼不动杆菌感染,鲍曼不动杆菌对碳青霉烯类抗生素的耐药率也逐年提高,2012年的CHINET的流行病学调查显示,显示耐碳青霉烯类鲍曼不动杆菌(carbapenem resistant acinetobacter baumannii,CRAB)占临床分离的鲍曼不动杆菌50%以上。替加环素是临床针对CRAB的一个新的选择,同时有建议替加环素与其他抗生素联合使用,以增加疗效。本实验采用CLSI推荐的检测MIC的参考方法琼脂稀释法检测替加环素对CRAB的MIC值。另外根据本院临床用药常规,应用肉汤微量稀释棋盘法测定替加环素分别联合氨苄西林舒巴坦和黏菌素对CRAB的MIC值,并计算部分抑菌浓度指数(fractional inhibitory concentration index,FICI),以了解秦皇岛地区替加环素对CRAB的体外药物敏感性以及和氨苄西林舒巴坦、黏菌素E联用的体外活性,为该药在临床上的使用提供体外药物检测依据。
1 材料与方法
1.1 菌株来源 收集秦皇岛市三家大型医院2012年1月至2014年5月临床分离的CRAB共51株,同一患者只收集一次菌株,以保证菌株的不重复性。对患者的临床病历进行评估,选择有明确感染病例,同时记录患者的科室、病种、年龄,是否接受侵入性操作等基本情况。按照CLSI 2012年M100-S21中折点判定标准厄它培南 MIC≥0.5 mg/L,美罗培南 MIC≥2.0 mg/L或亚胺培南MIC≥2.0 mg/L,判定为耐碳青酶烯类药物菌株。质控菌株为:大肠埃希菌ATCC25922和铜绿假单胞菌ATCC27853。
1.2 抗菌药物 替加环素标准粉(美国辉瑞制药有限公司,批号:L28832-6)储存于≤20℃冰箱内,避免反复冻融。美罗培南(住友制药),亚胺培南(杭州默沙东制药有限公司),厄他培南(杭州默沙东制药有限公司)可立其丁(Sigma公司),氨苄西林(中国药品生物制品检定所),舒巴坦(哈尔滨制药总厂)。
1.3 试剂与仪器 培养基Mueller-Hinton琼脂和肉汤(英国Oxoid公司),VITEK-32细菌鉴定仪(法国生物公司梅里埃)。
1.4 方法
1.4.1 替加环素 MIC值测定:药敏试验严格按照2009年《新型甘氨酰环素类抗菌药物替加环素的体外药敏试验操作规程》〔1〕的要求采用肉汤稀释法测定替加环素对CRAB的MIC值。根据《替加环素体外药敏试验操作规程专家共识》〔2〕,使用的M-H肉汤当天新鲜配制。另外由于替加环素理化性质活泼,试验中配制M-H肉汤稀释的药物原液和稀释的过程要严格避光,减少与空气接触的时间(黑布遮盖,加盖)。稀释好的不同浓度的含替加环素的M-H培养基加橡胶塞密封置于培养箱中24 h观察结果。目前CLSI没有替加环素的药敏结果判定标准,只给出了替加环素药敏试验中质控菌株可接受的质量控制范围。本研究中CRAB应用大肠埃希菌ATCC25922的质控范围0.03~0.25 mg/L。另外,由于 CLSI中尚无替加环素的MIC及折点判定标准,根据《替加环素体外药敏试验操作规程专家共识》,本研究中替加环素的折点采用FDA的折点判定标准:MIC≤2 mg/L为敏感,MIC≥8 mg/L为耐药,MIC=4 mg/L为中介。采用WHONET 5.6软件,建立药敏结果数据库并进行药敏结果数据分析。
1.4.2 体外联合药敏实验:肉汤微量稀释棋盘法:从细菌培养皿上挑取提纯的CRAB菌落2~4个,接种于M-H肉汤中增菌12 h,将增菌后的肉汤稀释成0.5麦氏浊度。将替加环素,氨苄西林舒巴坦(氨苄西林、舒巴坦按2∶1),黏菌素,根据美国临床实验室标准化委员会(CLSI)2012版执行标准分别倍比稀释为1/32-4MIC。使用96孔U型板,按棋盘法设计,将已稀释好的不同浓度的菌液和抗菌药物两两加入孔中,最后留一孔不加抗生素作为阳性对照。37℃ 24 h观察结果。结果判定部分:抑菌浓度(FIC)指数计算公式:FIC=FICA+FICB,其中FICA=MICA药联用/MICA药单用,FICB 相同。协同:FIC≤0.5,相加:0.5 <FIC≤1,无关:1<FIC≤4,拮抗:FIC>4。
2 结果
2.1 51株CRAB来源分类 本研究检测2012年1月至2014年5月秦皇岛三所大型医院112例鲍曼不动杆菌其中共51例CRAB占46%。对菌株来源进行统计,其中来源于ICU的CRAB 21例,都曾伴有侵入性操作,占41.2%。另外肿瘤患者合并感染14例,重度肺炎6例,外伤手术后感染患者3例,尿路感染3例,菌血症2例,腹膜炎1例,重度糖尿病1例。见表1。
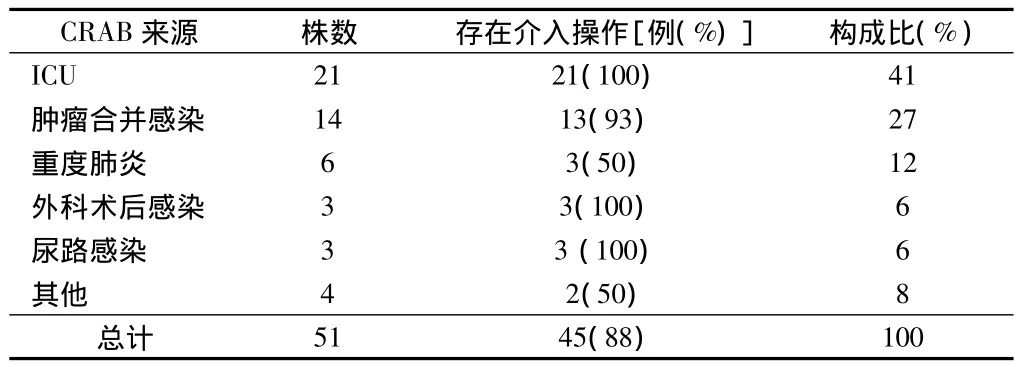
表1 51株CRAB来源分类
2.2 替加环素对51株 CRAB的体外抗菌活性和CRAB对替加环素的体外敏感率分布 51株CRAB中,对替加环素敏感共29株,占56.9%,中介共12株占23.5%,耐药共10株占19.6%。可见替加环素对CRAB具备较好的体外抗菌活性。51株CRAB对替加环素的体外敏感率分布,MIC为2 mg/L时,敏感率达56.9%,MIC 为 4 mg/L,敏感率达 76.5%,MIC 为8 mg/L,敏感率达80.4%,MIC 为16 mg/L,敏感率达91.3%。MIC50 为2 mg/L,MIC90 为16 mg/L,具有较好的体外敏感率。见表2、3。
2.3 替加环素分别与氨苄西林舒巴坦、黏菌素E联用,经棋盘法检测并计算部分抑菌浓度指数(FICI),替加环素+氨苄西林舒巴坦有协同作用4例占8%,相加作用15例占30%,无关32例占62%。而替加环素+黏菌素E的组合有6例相加(11%),其余全部表现为无关。可见在协同率和相关率上替加环素+氨苄西林舒巴坦的组合优于替加环素+黏菌素E的组合。见表4。

表2 替加环素对51株CRAB的体外抗菌活性
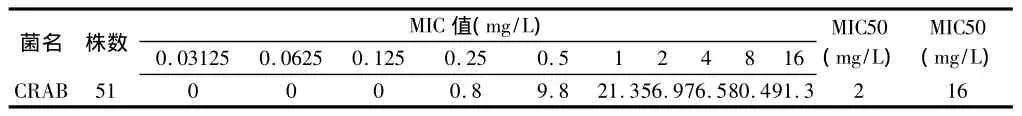
表3 CRAB对替加环素的体外敏感率分布 %

表4 替加环素分别与氨苄西林舒巴坦、可立其丁联用部分抑菌浓度指数(FICI) 例(%)
3 讨论
随着碳青霉烯类抗生素广泛应用于鲍曼不动杆菌感染,鲍曼不动杆菌对碳青霉烯类抗生素的耐药率也逐年提高。近年来,CRAB导致的感染呈全球蔓延趋势,且广泛分布于医院感染患者的体液中,尤其是ICU病房中免疫力低下和有介入性操作的患者[3]。分析原因可能是ICU患者免疫力低下同时都伴有侵入性操作,而且长期应用抗生素,催生了CRAB。另外由于CRAB是院内感染的主要菌种,不可忽视的方面是ICU病房的消毒隔离措施以及医务人员的手消毒是否到位等。秦皇岛三所大型医院112例鲍曼不动杆菌其中共51例CRAB占46%。秦皇岛地区CRAB的流行趋势不容乐观。
针对CRAB,应用新的抗菌药物或抗菌药物组合越发重要。替加环素作为新一代超广谱抗生素,是第一个被批准应用于临床的甘氨酰环素类抗菌药物,它的作用机制主要是通过与核糖体30S亚基结合从而抑制蛋白质的合成[4]。是目前少数对耐碳青霉烯类鲍曼不动杆菌有抗菌活性的抗菌药物之一。但研究表明替加环素的抗菌活性具有时间依赖性[5],由于替加环素血药浓度低,组织浓度较高,需要与其他抗菌药物联用。
鲍曼不动杆菌具有高度的天然固有耐药性和获得性耐药性,治疗鲍曼不动杆菌感染尤其是耐药的鲍曼不动杆菌感染药物选择非常有限,非传统药物如多黏菌素等虽然对肾脏及神经系统有高毒性,但仍然可以作为药物组合在临床应用。研究表明,鲍曼不动杆菌容易对多黏菌素E产生异质性耐药,但异质性耐药菌株能够部分恢复对其他抗菌药物的敏感性,需联合其他抗菌药物如替加环素[6]。另外,对耐碳青霉烯类不动杆菌,其往往对含舒巴坦敏感,因为舒巴坦可以直接作用于细菌的PBP2,从而显示出它对不动杆菌的独特的杀菌作用[7]。
本研究显示,替加环素对CRAB表现出较好的体外抗菌活性,对CRAB的体外敏感率达56.9%,成为仅次于多黏菌素的体外最有效的抗菌药物。另外由于该药在临床用药方便及与其它药物无交叉耐药,且肝肾毒性低等特点,使其在临床抗感染治疗中具有非常乐观的前景。替加环素与氨苄西林舒巴坦联用,协同加相关率可达到38%,优于替加环素与多黏菌素E联用,在替加环素与多黏菌素E的组合中,除6例相关外,其余全部无关。
随着替加环素在临床使用的增加,需要快速、准确的药敏结果指导临床合理使用该类抗菌药物。同时,做好替加环素和替加环素和其他抗生素的体外药敏监测,为临床科学、合理、高效的使用此药提供支持,是临床细菌工作者需要做的一项重要工作。
1 王辉,倪语星,陈民钧,等.新型甘氨酰环素类抗菌药物替加环素的体外药敏试验操作规程.中华检验医学杂志,2009,32:1208-1213.
2 王辉,俞云松,王明贵,等.替加环素体外药敏试验操作规程专家共识.中华检验医学杂志,2013,36:584-587.
3 张冀霞,王占伟,王启,等.替加环素对临床常见多重耐药菌的体外抗菌活性研究.中华检验医学杂志,2013,36:308-312.
4 杜小幸,王海萍,傅鹰,等.不同药敏方法检测替加环素对鲍曼不动杆菌敏感性的比较.中华检验医学杂志,2013,36:598-599.
5 van Ogtrop ML,Andes D,Stamstad TJ,et al.In vivo pharmacodynamic activities of two glycyleyelines(GAR-936 and WAY 152,288)against various gram-positive and gram-negative bacteria.Antimierob Agents Chemother,2000,44:943-949.
6 Moffatt JH,Harper M,Harrison P,et al.Colistin resistance in Acinetobacter baumannii is mediated by complete loss of lipopo-lysaceharide production.Antimicrob Agents Chemother,2010,54:497l-4977.
7 张樱,陈亚岗,杨青.不动杆菌感染及耐药枧制的研究进展.国外医学流行病学传染病学分册,2005,32:109-112.

