醒脑静注射液对脑梗死患者疗效及炎性因子MMP-2MMP-9水平的影响
吕风亚山东菏泽市立医院神经内科 菏泽 274031
醒脑静注射液对脑梗死患者疗效及炎性因子MMP-2MMP-9水平的影响
吕风亚
山东菏泽市立医院神经内科 菏泽 274031
目的 观察醒脑静注射液对急性脑梗死(ACI)患者疗效及炎性因子、MMP-2、MMP-9水平的影响。方法 将124例急性脑梗死患者随机分为2组,对照组(n=62)给予常规西医治疗,观察组(n=62)给予常规西医联合醒脑静注射液治疗;比较2组治疗前后的临床效果及血清肿瘤坏死因子-α(TNF-α)、白细胞介素-6(IL-6)、基质金属蛋白酶-2(MMP-2)、基质金属蛋白酶-9(MMP-9)水平的变化。结果 观察组总有效率优于对照组(P<0.05);2组治疗后的TNF-α、IL-6、MMP-2、MMP-9均较治疗前降低(P<0.05),且观察组上述四指标改善程度较对照组更佳(P<0.05)。结论 醒脑静注射液有利于改善脑梗死患者的神经功能缺损,且能够减轻细胞因子介导的炎性反应,对脑组织具有良好的保护作用。
急性脑梗死(ACI);醒脑静注射液;炎性因子;MMP-2;MMP-9
急性脑梗死(acute cerebral infarction,ACI)是指脑血管因为多种原因导致的血管闭塞,并由此产生的血管供应区脑功能损害和神经症状的临床综合征[1]。研究显示,醒脑静注射液对ACI的脑神经损伤有较好的保护作用,但其具体的作用机制尚不明确[2]。本研究观察了醒脑静注射液治疗ACI患者的临床效果及其对TNF-α、IL-6、MMP-2、MMP-9等重要炎性因子水平的影响,以期为醒脑静注射液治疗ACI提供循证依据。现将有关结果整理报告如下。
1 资料和方法
1.1 一般资料 本研究已经过本院伦理委员会批准,并与患者或患者家属签署知情同意书。采用随机双盲对照研究方法,选择我院2012-01-2014-06收治的124例ACI患者为研究对象,临床诊断参照《各类脑血管疾病诊断要点(1996)》[3]中相关标准,所有患者均于发病72h内入院治疗,均经过头颅MR或CT确诊;同时,排除脑出血,合并肿瘤及心、肝、肾、血液系统等严重疾病,严重意识障碍,近期溶栓治疗者。依照随机数字表法将全部患者分为2组,对照组(n=62)给予常规西医治疗,观察组(n=62)给予常规西医联合醒脑静注射液治疗。对照组男35例,女27例;年龄52~78岁,平均(63.5± 8.8)岁;颈内动脉梗死18例,椎基底动脉梗死17例,基底节区梗死13例,脑叶梗死7例,脑干梗死4例,混合型梗死3例。观察组男37例,女25;年龄51~76岁,平均(64.2±8.3)岁;颈内动脉梗死19例,椎基底动脉梗死15例,基底节区梗死14例,脑叶梗死6例,脑干梗死4例,混合型梗死4例。2组一般资料比较差异无统计学意义(P>0.05),具有可比性。
1.2 治疗方法
1.2.1 对照组:给予调控血压、降糖、吸氧、维持水及电解质平衡、扩张脑动脉、抗血小板聚集、营养脑细胞等常规西医治疗;对于并发脑水肿、颅内高压的ACI患者给予脱水降颅压等治疗;疗程15d。
1.2.2 观察组:在对照组治疗方案基础上给予醒脑静注射液(生产企业:河南天地药业股份有限公司;批准文号:国药准字Z41020664;规格:10mL/支)治疗,20mL醒脑静注射液+250mL 0.9%氯化钠注射液(或5%葡萄糖注射液)静滴,1次/d。疗程15d。
1.3 研究方法 2组患者分别在入院后次日、治疗15d后清晨空腹采集肘静脉血2mL送实验室待检,采用双抗夹心酶联免疫吸附法(WLISA)测定TNF-α、IL-6、MMP-2、MMP-9,操作步骤严格按照说明书进行。对比2组患者治疗前后的TNF-α、IL-6、MMP-2、MMP-9水平。
1.4 疗效评价 疗效评价参照《脑卒中患者临床神经功能缺损程度评分标准及临床疗效评分标准》制定。疗效分为5个等级:(1)基本痊愈:病残0级或神经功能缺损评分(NIHSS评分)减少91%~100%;(2)显著进步:NIHSS评分减少46%~90%;(3)进步:NIHSS评分减少18%~45%;(4)无效:NIHSS评分减少17%或增加<17%;(5)恶化:NIHSS评分增加>18%;(6)死亡。总有效率=(基本痊愈+显著进步+进步)/总病例数×100%。NIHSS评分减少比率=[(治疗后-治疗前)/治疗前]×100%。
1.5 统计学处理 本组数据采用SPSS 15.0软件包进行处理,计量资料以均数±标准差(±s)表示,组间比较采用t检验,计数资料以率(%)表示,比较采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 临床效果 观察组总有效率优于对照组(P<0.05),见表1。

表1 2组效果比较 [n(%)]
2.2 观察指标 2组治疗后的TNF-α、IL-6、MMP-2、MMP-9均较治疗前降低(P<0.05),且观察组上述四指标改善程
度较对照组更佳(P<0.05)。见表2。
表2 2组各项指标比较(±s)
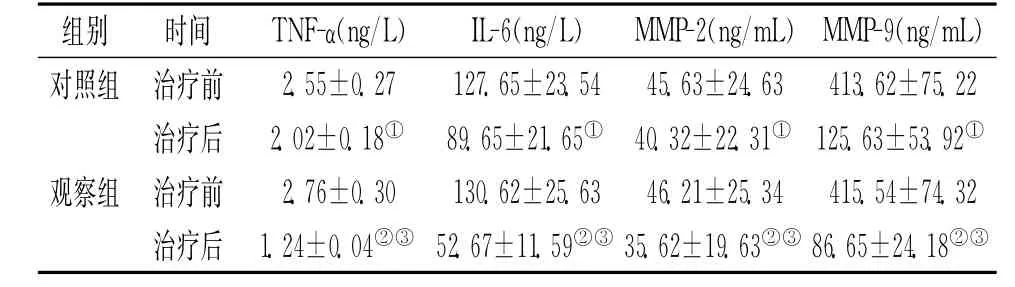
表2 2组各项指标比较(±s)
注:与对照组治疗比较,①P<0.05;与观察组治疗前比较,②P<0.05;与对照组治疗后比较,③P<0.05
组别 时间 TNF-α(ng/L) IL-6(ng/L) MMP-2(ng/mL)MMP-9(ng/mL)对照组 治疗前 2.55±0.27 127.65±23.54 45.63±24.63 413.62±75.22治疗后 2.02±0.18① 89.65±21.65①40.32±22.31①125.63±53.92①观察组 治疗前 2.76±0.30 130.62±25.63 46.21±25.34 415.54±74.32治疗后 1.24±0.04②③52.67±11.59②③35.62±19.63②③86.65±24.18②③
3 讨论
ACI是临床上较为常见的脑血管疾病,但该病对健康危害极大。研究表明[4],ACI的急性期病死率为5%~15%,存活患者致残率为70%左右。ACI病发后若能够迅速恢复血液循环,改善脑代谢,则脑损伤为可逆性,仍能够恢复受损的神经细胞。近几年的研究结果显示,炎性反应在脑缺血继发性损伤中发挥着重要作用。TNF-α、IL-6是常见的炎症细胞因子,在脑缺血-再灌注损伤中作用明显。动物实验[5]结果显示,在白鼠脑缺血后,外周血出现明显的炎性反应,并产生大量TNF-α、IL-6等细胞因子,而该细胞因子进入脑组织后,又会加重对脑神经的损伤。基质金属蛋白酶是一组锌依赖的具有活性的蛋白水解酶,广泛存在于细胞外基质[6]。MMP-2能够造成血管内皮细胞及平滑肌细胞的损伤,这种损伤又会刺激MMP-2表达,在并间质中不断积累沉积,若动脉粥样硬化斑块出现破裂,则溃疡形成会更加刺激MMP-2的表达,且MMP-2的表达水平和脑梗死面积、神经功能缺损程度存在较大相关性。MMP-9是和ACI关系最密切的基质金属蛋白酶,且作为缺血组织产生的炎性细胞因子,不仅能够增加血脑屏障的通透性,诱发脑水肿,还可以将稳定粥样硬化斑块变为不稳斑块,加重脑梗死病情[7]。因此,本研究选择的TNF-α、IL-6、MMP-2、MMP-9均是能够观察脑梗死病情严重程度的参照指标。
醒脑静注射液的主要成分是天然麝香、冰片、栀子、郁金,来源于我国经典古方“安宫牛黄丸”并将其改制为水溶性注射液。纵观该方剂,麝香可开窍辟秽,通络散淤;冰片辅麝香之力,能开窍醒脑;栀子可清泻三焦之邪热,助君药清热解毒;郁金则有化痰、开郁、通窍之功。诸药配伍,共奏开窍醒脑、安神定志、清热解毒、镇惊止痛、凉血行气之效[8]。现代药理学研究结果显示,醒脑静注射液的有效成分能够较为轻松地通过血脑屏障,对神经细胞产生直接的营养作用[9]。动物实验[10]结果显示,醒脑静注射液能够降低家兔的血脑屏障通透性,减轻脑水肿,清除氧自由基,延缓神经细胞凋亡,能够比较有效保护脑缺血再灌注损伤的脑组织和脑神经。本研究中,治疗后的2组患者的TNF-α、IL-6、MMP-2、MMP-9虽然都有一定程度降低,但观察组的上述四指标的降低幅度要大于对照组,表明醒脑静注射液治疗脑梗死患者时在抑制炎症细胞因子、提高脑神经抗缺氧能力方面具有积极价值。
[1]李芳君,谢少玲 .醒脑静注射液对大鼠脑缺血-再灌注损伤的保护作用[J].中药材,2011,34(7):1 111-1 113.
[2]中华神经科学会,中华神经外科学会.各类脑血管疾病诊断要点[J].中华神经科杂志,1996,29(6):379-380.
[3]中华神经科学会,中华神经外科学会.脑卒中患者临床神经功能缺损程度评分标准及临床疗效评分标准[J].中华神经科杂志,1996,29(6):381.
[4]娄益飞.醒脑静注射液对急性脑梗死患者血清IL-1、IL-6水平影响的临床研究[J].中国中医急症,2014,23(5):984-985.
[5]李宏斌.醒脑注射液对脑出血患者白介素-6和肿瘤坏死因子-α浓度的影响[J].中国现代医生,2011,49(4):9-12.
[6]李海滨.醒脑静注射液对急性脑梗死患者血清白细胞介素-6、12的影响及其临床意义苏相[J].首都医药,2012,8(16):39-39.
[7]宋建波,夏媛媛.醒脑注射液治疗脑损伤后意识障碍的疗效评价[J].中国实用医药,2012,7(23):189-190.
[8]王媛安.醒脑静注射液联用依达拉奉注射液治疗急性脑出血疗效分析[J].中国实用神经疾病杂志,2013,16(16):81-83.
[9]潘陈为,潘珍珍,陈永平,等.醒脑静注射液对高血氨大鼠空间学习记忆能力的影响[J].中华中医药学刊,2011,29(3):585-587.
[10]张晓玲,翟丽萍,官俏兵,等 .醒脑静注射液对急性脑梗死患者血清PD-ECGF表达的干预作用[J].中华中医药学刊,2013,31(7):1 579-1 581.
(收稿2014-11-16)
R743.33
A
1673-5110(2015)21-0064-02

