人巨细胞病毒核酸定量检测试剂盒临床应用及初步评价*
武警北京市总队第三医院检验科(北京100141)
王述莲 邓中平△ 呼建民 戴立忠△ 黄基容 王 军△ 艾颖娟△
人类巨细胞病毒(Human cytomegalovirus,HCMV)亦称细胞包涵体病毒,为疱疹病毒科β属的双螺旋DNA病毒,由于感染的细胞肿大,并具有巨大的核内包涵体,所以称为巨细胞病毒。HCMV的感染途径主要为接触、输血、宫内和产道等,感染较常见于胎儿、新生儿、孕妇等,孕妇感染可致新生儿先天畸形[1]。当机体免疫缺陷或免疫系统处于抑制状态下,极易受HCMV感染,如器官移植后接受免疫抑制治疗、恶性肿瘤化疗后、艾滋病患者等,这些患者一旦感染,常致较高的病死率和严重的疾病[2]。
目前国内外已有基于实时荧光定量PCR技术定量检测HCMV-DNA的试剂盒应用于临床检测中,但这些试剂盒多半以煮沸法提取核酸,且其检测灵敏度不高,约在10000copies/ml左右;另外,这些试剂盒大多缺乏完善的质控体系,还需要进一步完善和提高技术水平,使此类产品更加满足临床准确诊断的需要。
最近,新出现了一种人巨细胞病毒核酸定量检测试剂盒(PCR-荧光探针法),它完全免去了核酸提取中煮沸过程。根据其说明,HCMV核酸浓缩后经核酸释放剂裂解,全部释放参与到PCR反应中,整个过程无污染、操作极其简单、迅速。本研究拟通过检测临床样本,将其与市场上的煮沸试剂进行比对,来评估这一新方法准确性及特异性。
材料与方法
1 研究对象 本次研究共检测血清样本192例,其中男性97例(50.5%),女性95(49.5%),年龄0d至37岁,-20℃冰箱保存。
2 主要试剂和仪器 试剂购自湖南圣湘生物科技有限公司,采用浓缩一步法技术处理样本(以下简称“新型试剂”或“浓缩一步法试剂”),具有内标监控假阴性,最低检测限为400copies/ml;同时,选择一种临床使用较多的国产HCMV核酸检测试剂,采用煮沸法提取样本核酸,没有内标监控,作为对照试剂,最低检测限为1000copies/ml。核酸扩增仪采用美国Applied Biosystems公司的ABI7500实时荧光定量PCR仪。
3 方 法 采用两种荧光定量PCR检测试剂对192例临床样本(每例样本一分为三,保留一份样本作为复检)进行检测,方法如下:
煮沸法:取50μl临床样本,加入50μl DNA提取液充分混匀,100℃恒温处理10min,12 000rpm 离心5min备用;取5μl作为PCR反应的模板,加入分装有PCR反应液的反应管中上机检测。
浓缩一步法:取100μl血清样本,加入等体积的浓缩液,12 000rpm离心5min,弃上清,加入50μl核酸释放剂,用枪头挑起沉淀,吸打几次,将沉淀打散混匀静置10min作为待测样本备用。在PCR反应管中加入10μl待检样本,吸打混匀,加入40μl PCR反应液,吸打混匀上机检测即可。
4 统计学方法 数据进行一致性分析,灵敏度、特异度分析和Kappa检验一致性分析。
结 果
1 扩增曲线对比:两种试剂对比检测结果表明:浓缩一步法试剂检测样本扩增效率高,扩增曲线挺拔美观,呈典型的“S”型;体系中含有内标,内标曲线整齐集中,可以很好的判断检测样本中是否具有PCR抑制物,避免假阴性。
2 根据煮沸法试剂检测结果将临床样本分为阳性组和阴性组,统计结果见表1。

表1 煮沸法试剂与浓缩一步法试剂检测结果统计表
3 浓缩一步法试剂与煮沸法试剂检测结果的一致性分析:总一致性百分比符合率=(a+d)/(a+b+c+d)=(101+85)/192×100%=96.88%,用SPSS统计学软件进行一致性检验,Kappa值等于0.973,说明两方法高度一致。
4 浓缩一步法试剂与HCMV-pp65抗原结果的对比统计分析,见表2。

表2 浓缩一步法试剂的准确性评价
灵敏度Se=a/(a+c)×100%=80/(80+8)×100%=90.91%;特异度Sp=d/(b+d)×100%=79/(25+79)×100%=75.96%;灵敏度Se+特异度Sp=90.91%+75.96%=166.87%>100%。
5 煮沸法试剂与HCMV-pp65抗原结果的对比统计分析,见表3。

表3 煮沸法试剂的准确性评价
6 不符样本的复核结果及其分析:根据结果,有6例样本(样本信息见表4)浓缩一步法试剂与煮沸法试剂检测结果不符,其中4例(编号分别为:230814、231061、231128以及231952)煮沸法试剂检测为阴性(检测浓度处于400~1000copies/ml且样本性状相对复杂),而浓缩一步法试剂检测为阳性(检测浓度高于400copies/ml);另2例(编号为230949、231812)煮沸法试剂检测为阳性,而浓缩一步法试剂检测为阴性。在两个试剂盒的靶基因扩增区域外围序列,设计引物对,对这6例样本进行PCR扩增,克隆测序复核,结果4例浓缩一步法试剂检测为阳性的样本测序结果均包含HCMV-DNA序列,可能其灵敏度较之煮沸法试剂更高或抗干扰能力更强;而煮沸法试剂检测阳性的2例样本无PCR扩增片段,怀疑为交叉污染所致。
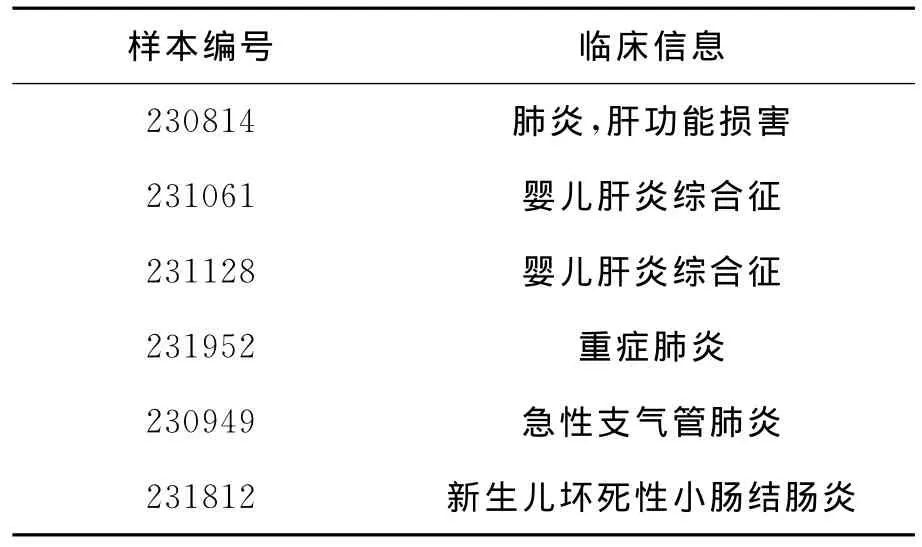
表4 6例不符样本临床信息表
应用Kappa评价方法对浓缩一步法试剂和煮沸法试剂检测结果进行诊断一致性分析,检验水准为α=0.05。对Kappa值的参考评价原则如下:0.75<κ≤1时,诊断一致性好;0.4<κ≤0.75时,诊断一致性一般;0≤κ≤0.4时,诊断一致性差。经SPSS15.0软件Kappa检验的输出结果显示,Kappa值=0.973,P=1.000。α=0.05检验水准下,浓缩一步法试剂与煮沸法试剂检测结果的一致性有统计学意义,诊断一致性好。
讨 论
HCMV感染常用的实验室诊断方法有血清学检查、抗原血症检测及基于PCR技术的检测方法等。血清学方法很多,酶联免疫吸附试验是最常用的方法,有灵敏度高、特异性好和重复性好等长处,方法简单,不需要特殊仪器,但该方法灵敏度明显不如抗原血症检测,且不利于早期诊断。最常用于抗原血症检测的抗原为pp65,它是HCMV活动性感染的早期标志性产物,是目前监测HCMV活动性感染和指导抗病毒治疗的重要方法,但是pp65抗原血症检测仅适合于血标本,且标本要求及时处理。PCR技术由于高灵敏度、高特异性、快速、简便等优点,使其为人巨细胞病毒的检测提供了又一新的途径。定量PCR的出现,打破PCR只能定性的局面,其中荧光定量PCR以其高灵敏度、高特异性、低污染率、实时监测等特点,可为临床提供更加准确、客观的检测结果,并及时地了解病情及预后[4]。目前国内临床上主要采用煮沸法对人巨细胞病毒的核酸进行提取,具体是先将样本高速离心,再加裂解液,煮沸,高速离心,取上清为模板。该方法核酸提取过程较复杂,样本处理耗时长,且在处理样本时,经过煮沸裂解、高速离心富集DNA等多个步骤,样本中的DNA存在损耗,同时由于采用了水浴或金属浴的高温加热步骤,容易造成气溶胶污。
本研究对人巨细胞病毒荧光定量PCR检测方法与常规的煮沸法进行对比研究。整个临床试验过程均在严格控制下进行,由经专门培训的测试人员进行检测分析。用浓缩一步法检测,处理简单,无需加热,可大大减少污染的发生,扩增和荧光检测均由仪器自动进行,通过查看样本的Ct值判断阴阳性。
本次研究共检测样本192例,根据煮沸法试剂检测结果分为两组:其中阳性组103例,阴性组89例。新型人巨细胞病毒核酸检测试剂与煮沸法试剂的阳性一致性百分比98.06%,阴性一致性百分比95.51%,总一致性百分比96.88%;对6例不符样本的复核结果表明:6例样本的测序结果均与新型试剂相符。对复核后的结果进行Kappa检验一致性分析:结果Kappa值=0.973,表明新型试剂与煮沸法试剂及复核检测的结果具有很好的一致性。在与HCMV-pp65抗原检测结果的对比中,两种试剂均表现出较好的准确性。
整个品评过程发现,浓缩一步法的样本处理和检验过程在一个离心管和一个PCR反应管中即可完成,样本中的核酸在浓缩液和核酸释放剂的作用下释放并参与到PCR反应过程中,只需一次离心,无需加热,抗污染能力强,操作过程简单,实验结果的重复性大大提高,对操作人员的技术要求较低。浓缩一步法还可以节省检验时间,可以让临床医生及患者及早得到诊断结果,避免等待试验结果的焦虑。从两种试剂的扩增曲线来看浓缩一步法试剂检测样本扩增效率高,扩增曲线平滑、挺拔美观,呈典型的“S”型;体系中含有内标,内标曲线整齐集中,曲线优美。
通过本次对比品评可以看出,浓缩一步法扩增检测方法操作极其简单,减少污染环节,有内标监控假阴性,结果准确,比已上市的煮沸法试剂具更好的灵敏度和准确性,具有较高的临床应用价值。
[1] Syggelou A,Iacovidou N,Kloudas S,etal.Congenital cytomegalovirus infection[J].Ann N Y Acad Sci,2010,1205(2):144-147.
[2] Tania Crough,Rajiv Khanna.Immunobiology of human cytomegalovirus:From bench to bedside[J].Clinical Microbiology Reviews,2009,22(1):76–98.
[3] 舒焰红,赵 杨.活动性人巨细胞病毒感染的病毒基因表达特点[J].实用医学杂志,2009,25(24):4113-4115
[4] Revello MG,Gorini G,Gerna G.Clinical evaluation of a chemiluminescence immunoassay for determination of immunoglobulin g avidity to human cytomegalovirus[J].Clin Diagn Lab Immunol,2004,11(4):801-805.

