以α-亚硝基-β-萘酚钴渣制备氧化钴的试验研究
刘云派,柳中梅
(江西理工大学 冶金与化学工程学院,江西 赣州 341000)
目前,一些湿法炼锌厂的含钴硫酸锌溶液采用β-萘酚除钴[1],每年产生α-亚硝基-β-萘酚钴渣8 000t左右[2]。对这类钴渣可以采用硫酸焙烧工艺制取氧化钴[3-5],但这种方式对大气环境易造成污染。为了寻找绿色环保方法,利用二价钴的简单化合物比三价钴化合物稳定[6]、而三价钴的螯合物比二价钴的螯合物稳定[7]的性质,以亚硫酸钠为还原剂,将钴渣中的三价钴还原为二价钴,并转化为CoSO3沉淀,然后再用盐酸浸出、草酸铵沉淀法制备氧化钴。
1 试验部分
1.1 试剂与仪器
试剂:工业级混合二甲苯、苯、甲苯、P204、磺化煤油,蒸馏水,分析纯浓硫酸、浓盐酸、浓氨水、亚硫酸钠、草酸铵、双氧水、柠檬酸、甲基橙、α-亚硝基-β-萘酚、盐酸羟胺等。
试验仪器:500mL三颈瓶,球型冷凝管,500 mL蒸馏瓶,直型冷凝管,KDM型调温电热套,SHB-3循环水多用真空泵,FA1004电子天平,电热恒温干燥箱,UV/VIS 2802PCS紫外可见分光光度计,7200可见分光光度计,X荧光光谱仪,原子吸收光谱仪等。
1.2 原料成分及性质
试验所用原料来为湿法炼锌厂的α-亚硝基-β-萘酚钴渣,为深红色湿物料,含水率约40%,其化学组分见表1。可以看出,钴渣中除钴外,还有锌、铁、锰、镍等金属元素,且锌、铁质量分数较高。α-亚硝基-β-萘酚钴渣非常稳定,不溶于水,不易被任何酸、碱分解,在大多数有机溶剂中溶解度较小[8]。

表1 钴渣化学组分的质量分数 %
1.3 试验方法与工艺流程
钴渣先用0.5mol/L硫酸溶液洗涤,然后水洗至中性,过滤,在120℃下干燥。取15.12g干燥后的钴渣于500mL三颈瓶中,加入200mL混合二甲苯,3.27g亚硫酸钠固体,蒸馏水40mL,在回流状态下反应一段时间后过滤,滤渣用25 mL浓度为1.0mol/L盐酸回流浸出1h得到氯化钴溶液。氯化钴溶液经H2O2氧化除铁、P204萃取除杂、草酸铵沉钴、草酸钴煅烧等过程制得纯度较高的氧化钴产品。工艺流程如图1所示。
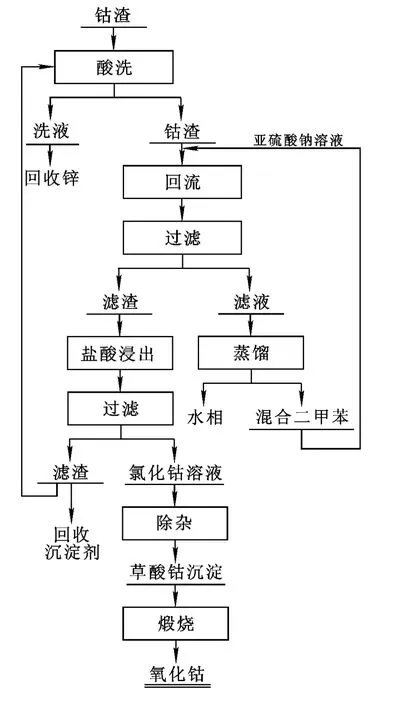
图1 从钴渣中提取钴的工艺流程
2 试验结果与讨论
2.1 酸洗除杂
α-亚硝基-β-萘酚钴是一种化学性质非常稳定的固体螯合物,而锌、铁、锰等金属离子与α-亚硝基-β-萘酚形成的配合物稳定性较差,同时,夹带的部分金属硫酸盐可溶于水,因此,可通过水洗去除大部分锌、铁、锰及水溶性硫酸盐。
以0.5mol/L硫酸溶液为洗涤剂洗涤钴渣,然后水洗至中性,再在120℃条件下干燥。洗涤后钴渣的化学组分见表2。可以看出,铁洗脱率为50%左右,锌、锰、铜、镍等金属离子洗脱率达90%以上。
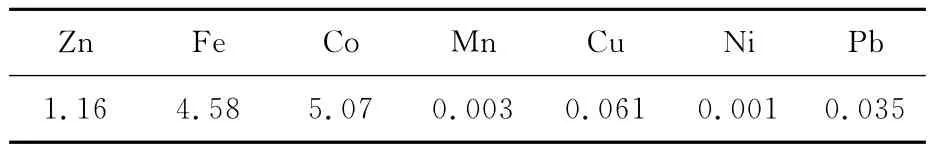
表2 酸洗后钴渣化学组分的质量分数 %
2.2 钴的浸出
2.2.1 有机溶剂的选择
钴与α-亚硝基-β-萘酚的螯合物结构稳定。为了有效分离钴,先用有机溶剂将α-亚硝基-β-萘酚钴螯合物溶解,然后还原钴。
试验条件下,用苯、甲苯、混合二甲苯等有机溶剂进行对比试验,结果见表3。
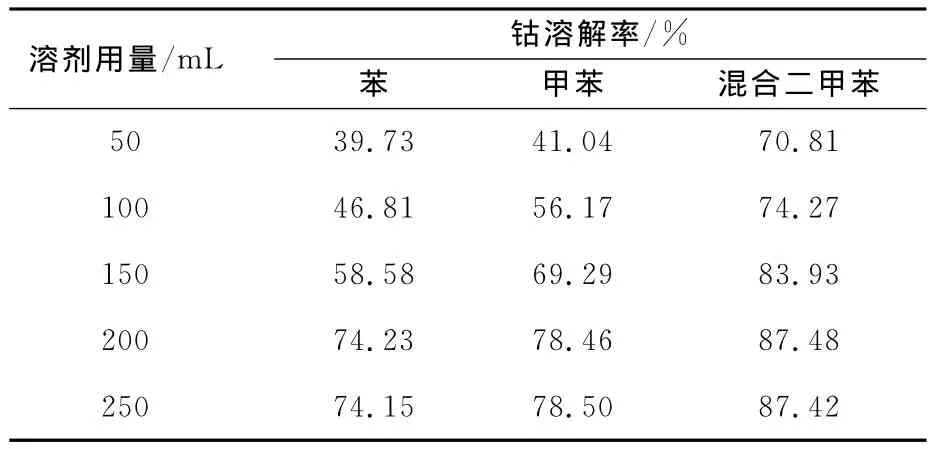
表3 不同溶剂对钴溶解率的影响
从表3看出:随溶剂用量增加,钴溶解率增大;溶剂用量超过200mL时,钴溶解率增大不明显。相同条件下,混合二甲苯对钴的溶解效果最好,其次是甲苯。相对于苯、甲苯而言,混合二甲苯沸点较高,可使反应在较高温度下进行,有利于亚硝基的脱除,因此,试验确定以混合二甲苯作溶剂。
2.2.2 还原剂的选择
钴渣中的钴主要以三价形式存在,为了更好地将钴浸出,必须利用还原剂将其转化为二价钴。用于冶金工业的还原剂种类较多,其中常用的有活泼的金属单质、低价化合物及部分有机物。亚硫酸钠是一种水溶性较好、廉价易得且还原能力较强的物质,其中:
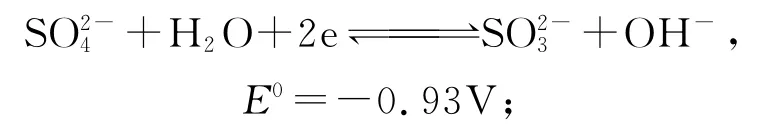
而
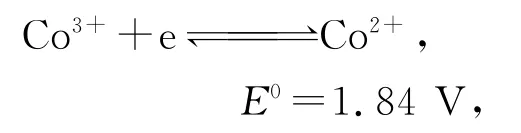
因此,亚硫酸钠完全可以将三价钴还原为二价钴,同时过量的亚硫酸钠可作为沉淀剂将二价钴转化为CoSO3沉淀。本研究中,亚硫酸钠既是还原剂也是沉淀剂。
2.2.3 还原反应温度对钴浸出率的影响
钴渣质量15.12g,混合二甲苯用量200mL,亚硫酸钠质量3.27g,浓度为1.0mol/L盐酸25 mL,回流时间2h。还原温度对钴浸出率的影响试验结果见表4。从表4看出:随反应温度升高,钴浸出率升高;当温度达到130~140℃即回流温度时,钴浸出率最大,为87.48%。反应温度较低时,钴渣在混合二甲苯中的溶解度较小,SO2-3与螯合物中的Co3+发生碰撞的几率较小,即Co3+还原速率偏低;而提高温度,既可增大钴渣在混合二甲苯中的溶解度,也提高了SO2-3随溶剂分子进入螯合物内部与Co3+发生还原反应及沉淀反应的速率。
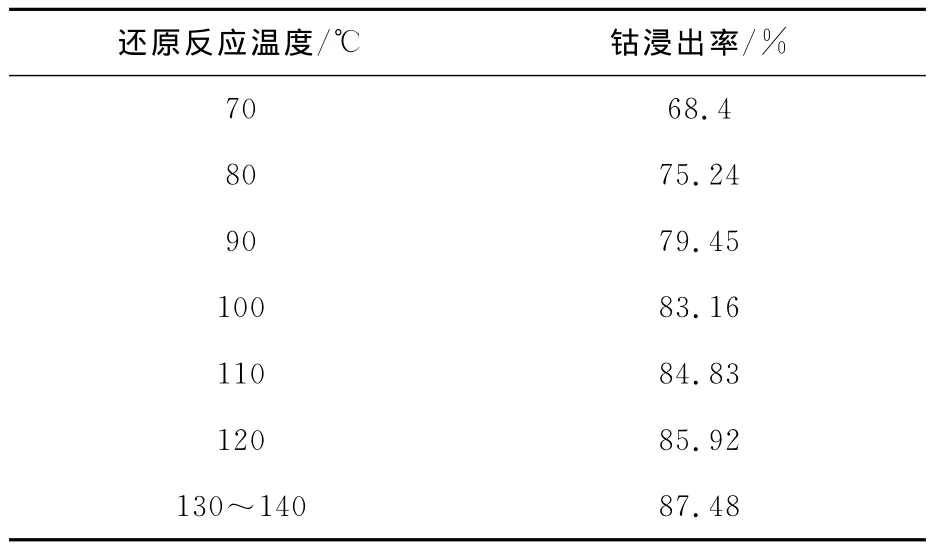
表4 还原温度对钴浸出率的影响
另一值得关注的问题是,酸洗后的钴渣在120~200℃范围内烘干过程中不发生分解;而在有水和有机溶剂存在时,温度高于80℃,钴渣就会发生分解,产生大量黄色气体。这种黄色气体产生的机制可能是:
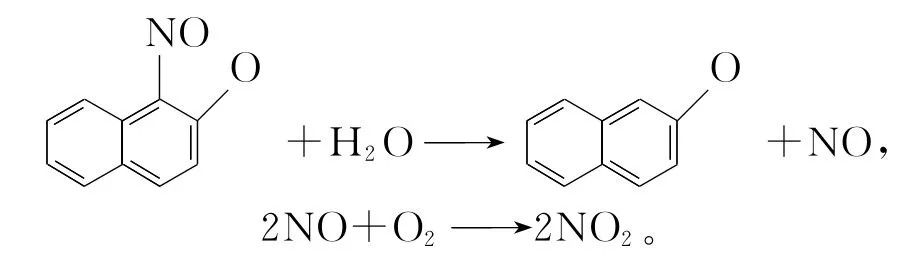
萘环上亚硝基的脱落破坏了钴渣螯合物的结构,使其失去了对Co3+的螯合作用,可见提高温度有利于亚硝基的脱落。由于混合二甲苯的沸点为137~140℃,因此,在混合二甲苯中回流可达到较好的浸出钴效果。
2.2.4 还原反应时间对钴浸出率的影响
钴渣质量15.12g,混合二甲苯体积200mL,亚硫酸钠质量3.27g,浓度为1.0mol/L盐酸25 mL,还原反应回流时间对钴浸出率的影响试验结果见表5。可以看出:回流1h时,钴浸出率仅为58.62%;回流2h时,钴浸出率为87.48%;之后随回流时间延长,钴浸出率稍有下降。这是因为,在回流过程中,有少量类似沥青的聚合物产生,其结构及其产生机制尚不清楚,这种胶状聚合物容易将已沉淀的CoSO3包裹起来,从而影响盐酸对钴的浸出。因此,过长的回流时间反而降低钴浸出率。
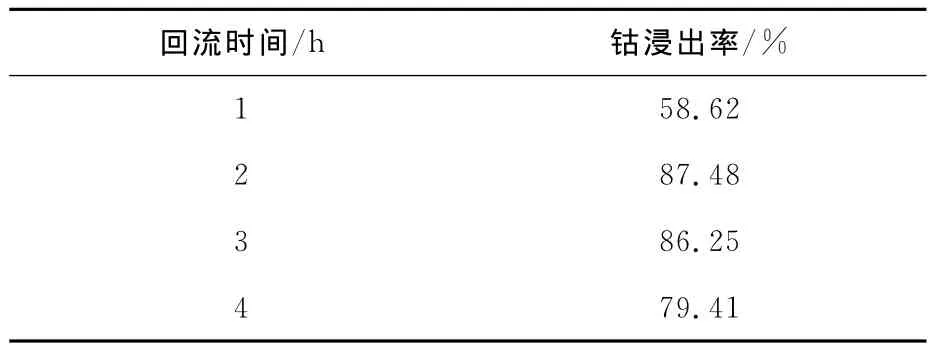
表5 回流时间对钴浸出率的影响
2.3 浸出液净化
氯化钴浸出液是在还原条件下得到的,溶液中残存的铁主要以二价铁形式存在。为了更好地去除杂质铁,先用 H2O2将Fe2+氧化为Fe3+,然后用氨水调节pH为5.0~5.2,使Fe3+水解沉淀去除铁[9],铁去除率可达90%以上,基本满足工艺要求。
除铁后的氯化钴溶液中还含有锌、锰等金属杂质,采用P204溶剂萃取法除杂[10],锌、锰等杂质金属的去除率均达95%以上。
2.4 氧化钴产品的制备
用草酸铵将钴离子沉淀为不溶于水的草酸钴,然后经过滤、煅烧制得氧化钴产品。产品化学成分分析结果见表6。可以看出,该产品已达到有色金属行业YS/T256—2000Tl的技术要求。
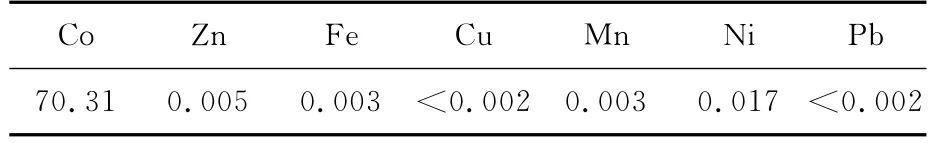
表6 产品氧化钴化学成分质量分数 %
3 结论
根据溶剂扩散原理,用混合二甲苯溶解α-亚硝基-β-萘酚钴渣,用亚硫酸钠作还原剂,具有很好的提钴效果。钴渣在有机溶剂中受热会发生脱亚硝基反应,提高反应温度有利于钴渣螯合物的分解。最佳条件下,钴浸出率为87.48%。如何抑制聚合物生成值得进一步研究。
[1]吴健辉.用β-萘酚从硫酸锌电解液中去除钴的研究[J].湿法冶金,2008,27(1):38-40.
[2]孙明生.从α-亚硝基-β-萘酚钴渣中制取氯化钴的工艺研究[J].中国有色冶金,2009(5):50-54.
[3]蒋伟,王海北,刘三平,等.β-萘酚钴盐渣的综合利用[J].有色金属,2009,61(4):87-89.
[4]姜洪波,都兴红.用湿法炼锌除钴渣生产氧化钴的可行性研究[D].沈阳:东北大学,2009.
[5]曹秀红.电解锌钴渣净化综合回收工艺研究[J].资源再生,2011(1):50-51.
[6]天津大学无机化学教研室.无机化学[M].北京:高等教育出版社,2007:421-424.
[7]黄可龙.重有色金属精细化工产品生产技术[M].湖南:中南工业大学出版社,1996.
[8]张永奇.从α-亚硝基-β-萘酚除钴渣中制取氧化钴[D].昆明:昆明理工大学,2005.
[9]大连理工大学无机化学教研室.无机化学[M].北京:高等教育出版社,2010:145-146.
[10]刁微之,张凡.以β-萘酚钴渣为原料制取氧化钴的工艺研究[J].云南冶金,2008,37(4):23-27.

