系统性红斑狼疮患者血清中Tim-1蛋白水平及其基因多态性①
陈 杰 胡 娜 苏斌涛 崔天盆(武汉市第一医院检验科,武汉 430022)
人T细胞免疫球蛋白黏蛋白分子(T cell immunoglobulin domain and mucin domain protein,Tim)只有3个基因,分别为Tim-1、Tim-3和Tim-4,定位于染色体的5q33.2区域[1]。Tim-1能调节T细胞的增殖,增强 Th2型细胞因子的产生[2],从而调节Th1/Th2反应;Tim-1还可促进凋亡细胞清除以及调节B调节免疫细胞功能。系统性红斑狼疮(systemic lupus erythematosus,SLE)就是一种自身免疫性疾病,SLE患者Tim-1的mRNA表达水平增高并与疾病的活动程度相关[3]。Kobayashi等[4]在 2007 年报道Tim-1通过磷脂酰丝氨酸结合凋亡的细胞介导凋亡细胞的清除,而 SLE患者存在明显的凋亡紊乱[5]。Tim-1分子第157氨基酸残基的位置有六个氨基酸插入的突变157insMTTTVP,即第四外显子有18个核苷酸的插入。有该突变的个体在感染甲型肝炎病毒后不易患过敏性疾病[6]。SLE与过敏性疾病一样是一种免疫功能紊乱性疾病。因此,本文将探讨Tim-1第4外显子插入与缺失多态性及其血清水平与SLE发病的关系,推测Tim-1在SLE发病中的分子机制。
1 材料与方法
1.1 对象 系统性红斑狼疮患者92例,女性85人,男性7人。平均年龄41.9岁,范围从18岁到81岁。全部来自武汉市第一医院就诊患者,都符合美国风湿病学会(ACR)2009年的系统性红斑狼疮诊断标准。正常对照来自健康体检者。女性76人,男性5人,平均年龄42.3岁,范围从20岁到75岁。没有自身免疫性疾病病史。
1.2 方法
1.2.1 血清的收集 收集受检者静脉血3 ml,离心,取血清,-80℃保存备用
1.2.2 Tim-1蛋白的ELISA检测 ELISA试剂购自R&D公司。共检测健康对照者中26例,SLE患者中47例。鼠抗人的Tim-1蛋白单克隆抗体用0.05 mol/L pH9.6 Na2CO3-NaHCO3包被缓冲液稀释至终浓度为 1 μg/ml,空白 96 孔板,每孔加 100 μl,室温过夜;弃包被抗体,每孔加封闭液(5%BSA-PBS)100 μl,室温放置 1 h;弃封闭液,用 1%的 Tween20的PBS洗板三次,一次5 min;加入血清和系列稀释的标准品100 μl,室温放置1 h;重复上面洗板步骤;加入稀释至工作浓度的生物素化的兔抗人的Tim-1蛋白的多克隆抗体100 μl,室温放置1 h;重复上面洗板步骤;加入1∶5 000稀释的链霉亲和素-HRP结合物,室温放置1 h;重复上面洗板步骤;加入显色试剂TMB显色20 min,加入 H2SO4终止显色反应。450 nm测定OD值。绘制工作曲线,计算样本Tim-1蛋白浓度。
1.2.3 模板DNA的提取 使用血常规采血管收集受检者静脉血2 ml,离心,吸取白膜层细胞。用TIANGEN公司的DNA提取试剂盒(货号:DP304)提取基因组DNA,溶于TE中,-20℃保存备用。
1.2.4 TIM-1的第4外显子插入与缺失多态性分析 自行设计一对引物,上游引物:5'-TCCAGCCTGAGGCTCCTTGTTT-3',下游引物:5'-ATGCTCATTGTTGTTGGAACAG-3'。缺失型 PCR产物大小是201 bp,插入型是 219 bp。
PCR反应体系总体积为25 μl,模板 DNA 100 ng,上下游引物各 1 μl(终浓度为 0.4 pmol/μl),PCR Marster mix(TIANGEN公司货号:KT201-02)12.5 μl,用双蒸水补足反应体系的体积。PCR反应条件:94℃ 预变性3 min,94℃变性30 s,60℃退火30 s,72℃延伸 1 min,30 个循环。
PCR产物5 μl,用3%的含GoldviewⅠ琼脂糖凝胶电泳。伯乐凝胶成像分析仪(Bio-Rad chemiDocTMXRS+)进行拍照。缺失/缺失纯合子出现一条201 bp的条带,缺失/插入杂合子出现201 bp和219 bp的两个条带,插入/插入纯合子只出现219 bp的一个条带。
1.3 统计学分析 采用SPSS18.0软件进行统计分析,计量资料以表示,组间比较采用独立样本的t检验。如果方差不齐,采用两独立样本的Wilcoxon秩和检验。基因型和等位基因频率经哈迪—温伯格平衡定律检验,基因型及等位基因频率比较采用χ2检验,P<0.05为有显著性差异。
2 结果
2.1 血清中Tim-1蛋白浓度 47例SLE患者和26例健康对照组血清中Tim-1蛋白浓度分别为(263.083±276.953)和(58.527±92.424)pg/ml。该资料方差不齐,采用秩和检验(Z=-4.93,P<0.05),两者之间差异具有统计学意义。Tim-1蛋白浓度在SLE患者中的水平高于健康对照组。
2.2 不同基因型个体血清中Tim-1蛋白浓度比较
SLE患者TIM-1的第4外显子缺失/缺失纯合子29例与缺失/插入杂合子18例的Tim-1蛋白的平均浓度分别为(307.360±284.079)和(191.750±256.708)pg/ml,两组之间无显著性差异(t=1.406,P=0.167)。健康对照组TIM-1的第4外显子缺失/缺失纯合子17例与缺失/插入杂合子8例的Tim-1蛋白的平均浓度分别为(70.295±109.917)和(40.468±41.739)pg/ml,两组之间无显著性差异(t=0.736,P=0.469)。因为插入/插入基因型的个体数较少,没有进行统计比较。该突变没有改变Tim-1蛋白在血清中的浓度。

表1 TIM-1外显子4ins/del基因型和等位基因频率Tab.1 The exon 4 of TIM-1 ins/del genotype and allele frequencies
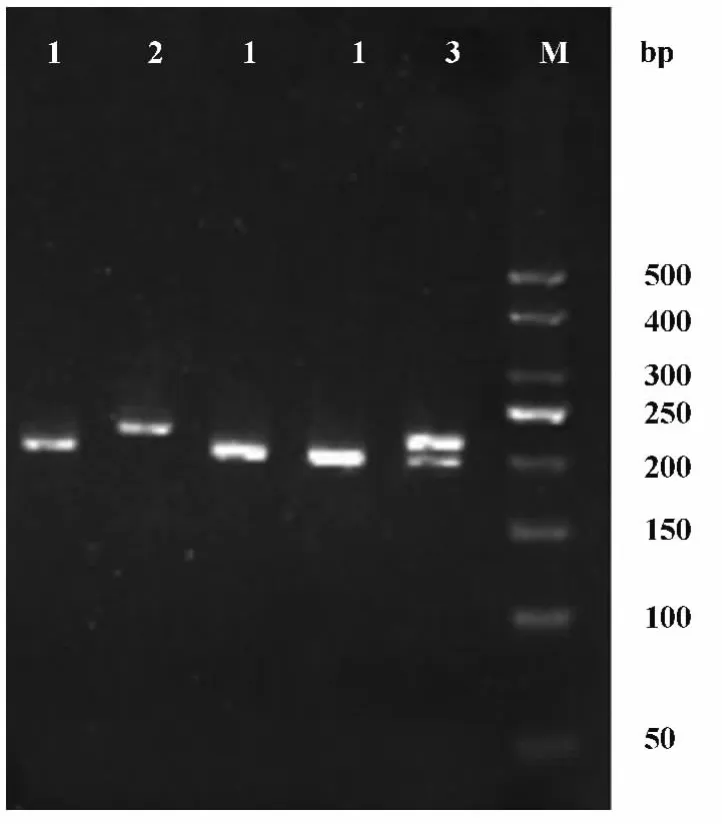
图1 Tim-1第4外显子ins/del基因分析图Fig.1 Ins/del polymorphism of the exon 4 of Tim-1 analysis chart
2.2 基因分型结果图 缺失/缺失(del/del)纯合子出现一条201 bp的条带,缺失/插入(del/ins)杂合子出现201 bp和219 bp的两个条带,插入/插入(ins/ins)纯合子只出现219 bp的一个条带,见图1。
2.3 TIM-1基因的多态性与系统性红斑狼疮的关系的分析 对照组和系统性红斑狼疮组中,缺失/缺失纯合子出现最多,缺失/插入杂合子次之,插入/插入纯合子出现最少。经HWE平衡检验,符合哈迪-温伯格平衡定律,表明该样本具有抽样代表性(χ2=0.060,P=0.806)。经卡方检验,三种基因型组间差别无统计学意义(χ2=1.723,P=0.437)。Tim-1此基因多态性与SLE无相关性,见表1。
3 讨论
人的 Tim基因有三个成员:Tim-1、Tim-3和Tim-4。Tim-3和Tim-1表达于T细胞表面。Tim-3特异性的表达在Th1型细胞上,负性调节Th1细胞反应。Tim-4表达于抗原提呈细胞,是Tim-1的配体。Tim-4与 Tim-1相互作用,调节T细胞的活化增殖[2]。Tim-1是甲型肝炎病毒的受体[7],T 细胞活化共刺激分子。Tim-1分子第157氨基酸残基的位置有6个氨基酸插入的突变157insMTTTVP,即第四外显子有18个核苷酸的插入。有该突变的个体在感染甲型肝炎病毒后不易患过敏性疾病[6]。因此,Tim-1可能参与了免疫系统的调控,该突变可能改变其功能。
SLE是一种多因素的自身免疫性疾病。机体会出现多种自身抗体,补体活化和免疫复合物沉积,导致组织和多器官损伤。辅助性的T细胞主要分化成两型:Th1和Th2。Th1和Th2细胞功能的失衡在SLE的病理机制中起了重要作用[8]。Tim-1是活化T细胞的共刺激分子,大量表达于CD4+T细胞上,促进Th2型细胞介导的免疫反应[9],因此参与Th1和Th2细胞功能平衡的调节。SLE会产生许多抗核成分的自身抗体,特别是抗染色质的自身抗体。由于凋亡的发生异常或者凋亡细胞的清除异常,含有染色质的凋亡碎片被释放。在凋亡的过程中,这些染色质被修饰过,因此增加了自身的免疫原性。树突状细胞吞噬这些碎片,活化自身反应性的T辅助性细胞,接着活化自身反应性的B细胞,产生自身抗体。被修饰过的染色质与这些自身抗体结合形成复合物,沉积在基底膜上,引起炎症。因此,凋亡细胞清除障碍是SLE的一个病因[5]。Tim-1可以结合磷脂酰丝氨酸,促进凋亡细胞的清除[10]。国外Xiao等[11]制作一个Tim-1分子粘蛋白结构域缺失的基因敲除的小鼠,这种突变型的小鼠表现出调节性B细胞分泌IL-10缺陷,这种小鼠随着年龄的增长会自发系统性自身免疫性疾病,血清中INF-γ和自身抗体的量增加,因此,Tim-1在维持调节性B细胞的负性免疫调节功能中起很重要的作用[11]。
本实验中,检测92例SLE患者,81位健康对照个体,没有发现Tim-1的第4外显子插入/缺失多态性与SLE的相关性。同时比较不同基因型个体血清中Tim-1蛋白浓度,发现该突变不影响血清中其蛋白浓度。这可能是Tim-1此种基因多态性与SLE无相关性的原因。47个SLE患者和26个健康对照组血清中Tim-1蛋白平均浓度分别为263.083±276.953和58.527±92.424 pg/ml,其差异具有统计学意义。与Wang[3]等报道SLE患者外周淋巴细胞表达Tim-1 mRNA水平增加相对应,我们发现SLE患者血清中Tim-1蛋白浓度是高于健康对照组的。适量的Tim-1蛋白结合磷脂酰丝氨酸,促进凋亡细胞的清除[4]。SLE患者存在凋亡紊乱,SLE外周血淋巴细胞凋亡增加,且凋亡细胞与正常细胞比例与SLE活动度呈正比;凋亡细胞是核小体的重要来源,而核小体与核小体抗体的结合,核小体与硫酸软骨素的结合是导致狼疮肾炎的病理生理基础[5],肾Tim-1表达水平高,我们推测SLE患者凋亡细胞增加,反馈刺激Tim-1表达增加,导致血清Tim-1蛋白的升高;最近Xiao[11]等研究发现Tim-1是调节性B细胞的表面标记之一,SLE患者血清异常增高的Tim-1可能竞争性干扰调节性B细胞的功能,导致SLE病理进程加速。
总之,Tim-1蛋白在系统性红斑狼疮患者血清中的浓度升高,可能干扰凋亡清除或/和调节性B细胞的功能,可能与系统性红斑狼疮的病理生理机制有关。有关具体机制有待随后的研究进一步证实。
[1]Rennert PD.Novel roles for TIM-1 in immunity and infection[J].Immunol Lett,2011,141(1):28-35.
[2]Meyers JH,Chakravarti S,Schlesinger D,et al.TIM-4 is the ligand for TIM-1,and the TIM-1-TIM-4 interaction regulates T cell proliferation[J].Nat Immunol,2005,6(5):455-464.
[3]Wang Y,Meng J,Wang X,et al.Expression of human TIM-1 and TIM-3 on lymphocytes from systemic lupus erythematosus patients[J].Scand J Immunol,2008,67(1):63-70.
[4]Kobayashi N,Karisola P,Pena-Cruz V,et al.TIM-1 and TIM-4 glycoproteins bind phosphatidylserine and mediate uptake of apoptotic cells[J].Immunity,2007,27(6):927-940.
[5]Bouts YM,Wolthuis DF,Dirkx MF,et al.Apoptosis and NET formation in the pathogenesis of SLE[J].Autoimmunity,2012,45(8):597-601.
[6]Mcintire JJ,Umetsu SE,Macaubas C,et al.Immunology:hepatitis A virus link to atopic disease[J].Nature,2003,425(6958):576.
[7]Feigelstock D,Thompson P,Mattoo P,et al.The human homolog of HAVcr-1 codes for a hepatitis A virus cellular receptor[J].J Virol,1998,72(8):6621-6628.
[8]Chen S,Hu D,Shi X,et al.The relationship between Th1/Th2-type cells and disease activity in patients with systemic lupus erythematosus[J].Chin Med J(Engl),2000,113(10):877-880.
[9]Nakae S,Iikura M,Suto H,et al.TIM-1 and TIM-3 enhancement of Th2 cytokine production by mast cells[J].Blood,2007,110(7):2565-2568.
[10]Chen Z,Qing J,Hu L.Interactions of human T cell immunoglobin mucins with apoptotic cells[J].J Huazhong Univ Sci Technolog Med Sci,2012,32(1):9-16.
[11]Xiao S,Brooks CR,Zhu C,et al.Defect in regulatory B-cell function and development of systemic autoimmunity in T-cell Ig mucin 1(Tim-1)mucin domain-mutant mice[J].Proc Natl Acad Sci USA,2012,109(30):12105-12110.

