阻断p38丝裂原活化蛋白激酶在细胞空泡形成中的作用*
张春燕,冯春红,敬健雄,段春燕,刘友平,夏先明,李 洪,代荣阳,陈绍坤
(泸州医学院:1.生物化学教研室;2.肝胆外科;3.生物教研室,四川泸州646000)
为了适应环境变化,细胞会发生一系列诸如皱缩、膨胀、分裂和空泡形成等形态学的改变。化学和生物活性物质诱导细胞形成的细胞质空泡是一种显著且常见的现象[1-2],此外,细胞空泡也能自发形成[3]。细胞空泡化的程度主要取决于细胞类型[4-5],有些细胞极易发生空泡化,有些细胞则很难形成空泡。
有报道表明[6-7],细胞空泡就好比是细胞内帮助消化的酸性区域。这个酸性区域的组成、来源及形成机制除了取决于细胞类型,也取决于细胞空泡的诱导剂。有学者认为[8-9],细胞的自体吞噬介导了空泡形成,细胞空泡可能代表了某种典型的自体吞噬。但是,有的细胞空泡并非来自于自体吞噬,自体吞噬也并非总 是 介 导 空 泡 形 成[10-11]。 也 有 学 者 认 为[12-13],细 胞 空泡与细胞凋亡密切相关。有些凋亡诱变剂可诱导细胞空泡化,并通过空泡形成参与细胞凋亡的调控。值得注意的是[14],有的细胞空泡并不是因凋亡而产生,有些空泡诱导剂诱导了细胞空泡形成,但并不引发细胞凋亡。丝裂原活化蛋白激酶(mitogen-activated protein kinase,MAPK),如p38MAPK是细胞内重要信号通路,MAPK通路在细胞炎症反应、凋亡、生长和细胞应激等多种生理和病理过程中起着重要的调节作用。虽然目前已明确细胞空泡与细胞应激反应密切相关[15],但是,细胞空泡的形成是否受到细胞应激反应信号通路p38MAPK的调节尚不清楚。
本实验旨在探讨p38MAPK是否参与了细胞空泡形成。研究发现细胞空泡可在HepG2细胞中自发形成,这些空泡可被茴香霉素(Anisomycin)通过活化p38MAPK而消除。此外,阻断p38MAPK可诱导多种肿瘤细胞空泡形成。本实验结果表明p38MAPK在调节细胞空泡形成中发挥了重要作用。
1 材料与方法
1.1 材 料 Anisomycin、放 线 菌 酮 (Cycloheximide,CHX)、SB203580、SP600125购自Merck公司;细胞培养试剂购自Gibco公司;β-actin、p-MAPKAPK2、MAPKAPK2、p38MAPK、磷酸化c-Jun抗体购自CST公司;内质网红色荧光探针及溶酶体红色荧光探针购自Invitrogen公司;电泳试剂均购自Bio-Rad公司;其他为国产分析纯。
1.2 实验方法
1.2.1 细胞培养及处理 肿瘤细胞株 HepG2、LM3、QBC939、Hela和A549于37℃、5%CO2培养箱中常规培养,选取对数生长期细胞进行后续实验。培养细胞分别用anisomycin(0.25、0.5、1.0μg/mL)、SB203580(0、2.5、5.0、10.0 μmol)、SP600125(20nmol)及CHX(5、10、15μmol)处理,并按在对应时间点观察细胞空泡化情况。
1.2.2 Western blot法检测p38MAPK等通路相关分子的表达水平 HepG2细胞常规培养,各实验组给予不同的处理因素后,收集细胞,提取各组细胞蛋白,进行 Western blot检测。总蛋白经十二烷基磺酸钠-聚丙烯酰氨凝胶电泳(SDS-PAGE)分离后,转移到PVDF膜上,脱脂奶粉封闭,加Ⅰ抗:β-actin、p-MAPKAPK2、MAPKAPK2、p38MAPK、p-c-jun、c-Jun,4 ℃过夜,TBST洗膜3次,加Ⅱ抗孵育1h,ECL法显色,凝胶成像系统扫描分析结果。
1.2.3 激光共聚焦显微镜观察内质网及溶酶体形态 LM3、A549细胞常规培养,各实验组给予不同的处理因素后,对照组用二甲基亚砜(DMSO)做相同处理,用内质网红色荧光探针和DAPI探针标记内质网,得到内质网断层扫描图像;溶酶体红色荧光探针标记溶酶体,得到溶酶体荧光染色图像,再经激光共聚焦显微镜观察分析。
2 结 果
2.1 Anisomycin对HepG2细胞空泡的消除作用 实验组应用不同剂量的p38MAPK和JNK的激活剂Anisomycin(0.25、0.5、1.0μg/mL)作用于 HepG2细胞12h,对照组用DMSO做相同处理。光学显微镜下观察比较,可见Anisomycin对HepG2细胞内自发形成的空泡有消除作用,呈剂量-效应关系,见图1A。应用0.5μg/mL Anisomycin分别作用于HepG2细胞0、3、6、12h,该消除作用呈时间-效应关系,见图1B。该结果表明Anisomycin能有效消除HepG2细胞空泡,p38MAPK和JNK信号通路可能参与了细胞空泡化的调节。

图1 Anisomycin对HepG2细胞空泡的消除作用(×400)
2.2 Anisomycin通过活化p38MAPK消除细胞空泡 p38 MAPK抑制剂(SB)组和JNK抑制剂(SP)组分别应用5.0 μmol SB203580、20nmol SP600125作用于 HepG2细胞12h,对照组用DMSO做相同处理,Anisomycin组应用0.5μmol/mL Anisomycin作用12h,Anisomycin+SB组和Anisomycin+SP组分别应用5.0μmol SB203580、20nmol SP600125对HepG2细胞预处理1h,再0.5μmol/mL Anisomycin共同作用12h。光学显微镜下观察比较,可见Anisomycin+SB组的明显空泡化,Anisomycin+SP组与Anisomycin组比较,差异无统计学意义(图2A)。表明SB203580能阻断Anisomycin对HepG2细胞空泡的消除作用,SP600125却不能阻断该消除作用。Western blot结果显示,Anisomycin对p38MAPK和JNK的下游效应产物p-MAPKAPK2和p-c-jun的表达水平均有上调作用。这表明了Anisomycin能活化HepG2细胞内p38 MAPK和JNK通路,SB203580选择性抑制p38MAPK通路,SP600125选择性抑制JNK通路。结果表明Anisomycin是通过活化p38MAPK消除细胞空泡。
实验组应用不同剂量的蛋白合成抑制剂CHX(5、10、15 μmol)作用于HepG2细胞12h,对照组用DMSO做相同处理。光学显微镜下观察比较,CHX不能消除HepG2细胞空泡,表明Anisomycin对空泡的消除作用与它的抑制蛋白合成作用无关(图2B)。
2.3 阻断p38MAPK诱导LM3细胞空泡形成 应用不同剂量的p38MAPK 选择性抑制剂 SB203580(0、2.5、5.0、10.0 μmol)作用于LM3细胞12h,诱导空泡形成,呈剂量-效应关系(图3A)。应用5.0μmol SB203580分别作用于LM3细胞0、6、12、24h,诱导空泡形成,呈时间-效应关系(图3B)。该结果表明阻断p38MAPK可诱导LM3细胞空泡形成,呈剂量-时间双重效应关系。

图2 Anisomycin通过活化p38MAPK消除细胞空泡(×400)

图3 阻断p38MAPK诱导细胞空泡形成(×200)
2.4 阻断p38MAPK诱导多种肿瘤细胞空泡形成 实验组应用5.0μmol SB203580分别作用于QBC939、LM3、Hela细胞12h,对照组用DMSO做相同处理。光学显微镜下观察比较,可见实验组细胞内大量空泡形成(图4)。表明阻断p38 MAPK可诱导多种肿瘤细胞的空泡形成。
2.5 阻断p38MAPK介导的空泡形成破坏内质网结构的整体性 实验组应用5.0μmol SB203580分别作用于LM3、A549细胞12h,对照组用DMSO做相同处理,进行内质网红色荧光探针和DAPI探针标记内质网,得到内质网断层扫描图像。再经激光共聚焦显微镜观察分析,显示对照组细胞的内质网结构完整,实验组细胞的内质网结构不完整(图5)。表明阻断p38MAPK介导的空泡形成破坏了内质网结构的整体性。

图4 阻断p38MAPK诱导多种肿瘤细胞空泡形成(×400)
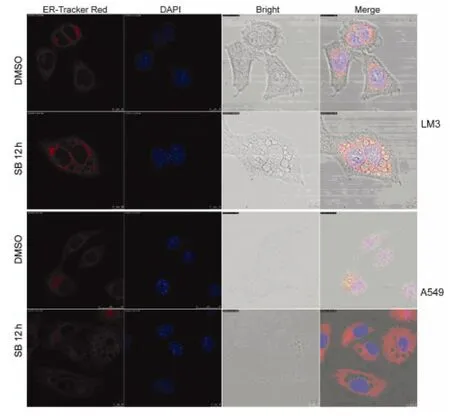
图5 阻断p38MAPK介导的空泡形成破坏内质网结构的完整性
2.6 阻断p38MAPK形成空泡的泡内pH值 应用5.0 μmol SB203580分别作用于LM3、A549细胞12h,进行溶酶体红色荧光探针标记溶酶体,经激光共聚焦显微镜观察分析,显示阻断p38MAPK形成的空泡之中,只有很少一部分呈现荧光染色(图6)。表明阻断p38MAPK形成的空泡,只有少数的泡内pH值为酸性。
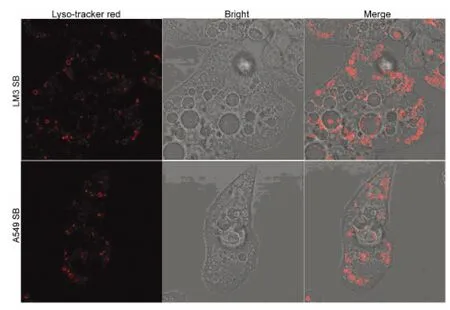
图6 阻断p38MAPK形成空泡的泡内pH值
2.7 阻断p38MAPK介导的空泡形成具有可逆性 实验组应用5.0μmol SBF203580分别作用于LM3、A549细胞12h,再换不含SB203580的培养基继续培养6h,对照组用DMSO做相同处理。光学显微镜下观察,可见实验组经SB203580作用12h,与对照组相比,细胞内有大量空泡形成;而换不含SB203580的培养基6h后,与对照组比较,细胞内空泡化无明显差异(图7)。表明阻断p38MAPK介导的空泡形成具有可逆性。

图7 阻断p38MAPK介导的空泡形成具有可逆性
3 讨 论
细胞空泡化是发生在哺乳类动物细胞中常见的形态学现象之一。细胞局部环境的改变是引起细胞空泡化的根本原因,细胞空泡可自发形成或经诱导刺激而形成。但是,细胞应激信号通路是否参与细胞空泡化,目前尚不明确。本实验旨在探讨p38MAPK通路是否参与了细胞空泡形成。通过研究发现p38MAPK在调节细胞空泡形成中具有重要作用。
应用Anisomycin能有效消除HepG2细胞空泡,因为Anisomycin是p38MAPK和JNK的共同激活剂,这就提示p38 MAPK和JNK信号通路可能参与了细胞空泡化。由于阻断p38MAPK可抑制Anisomycin对细胞空泡的消除作用,阻断JNK却不能抑制Anisomycin的消除作用,提示Anisomycin是通过活化p38MAPK消除细胞空泡的,而不是活化JNK。又因Anisomycin是一种蛋白合成抑制剂,为了确认它对空泡的清除作用是否与抑制蛋白合成有关,本实验应用了另一种经典的蛋白合成抑制剂CHX作用于HepG2细胞,发现CHX不能消除HepG2细胞空泡,表明Anisomycin对空泡的消除作用与它的抑制蛋白合成作用无关,进一步证明了Anisomycin对空泡的消除作用是通过活化p38MAPK来实现的。
本实验应用p38MAPK通路的选择性抑制SB203580阻断p38MAPK通路,发现可诱导多种肿瘤细胞空泡形成,表明阻断p38MAPK在细胞空泡形成中发挥了重要作用。最近有研究报道[14]SB202190可以不依赖p38MAPK信号通路介导细胞空泡形成,分析原因可能是因为所用细胞类型和本实验不同。细胞空泡可在HepG2细胞中自发形成,却不能自发形成于LM3、A549细胞,可能是不同细胞类型中p38MAPK的活化情况不同。此外,不同细胞类型中的p38MAPK通路的功能也不相同,p38MAPK通路并不是惟一调节细胞空泡形成的通路。因此,p38MAPK通路在细胞空泡化的作用,主要取决于细胞类型,而p38MAPK活化或阻断的程度,在很大程度上也取决于细胞类型。
本实验通过激光共聚焦显微镜观察分析内质网断层扫描图像,发现阻断p38MAPK介导的空泡形成破坏了内质网结构的整体性。内质网结构完整性的破坏提示空泡化可能与内质网的应激反应有关。已有报道表明[6-7],细胞空泡就好比是细胞内帮助消化的酸性小区域。本实验对阻断p38MAPK形成的空泡进行溶酶体红色荧光探针标记溶酶体,经激光共聚焦显微镜观察分析,显示阻断p38MAPK形成的空泡之中,只有很少一部分呈现荧光染色。表明阻断p38MAPK形成的空泡,只有少数的泡内pH值为酸性。另外,阻断p38MAPK可介导空泡形成,当去除阻断剂细胞空泡则可消除,表明阻断p38MAPK介导的空泡形成具有可逆性。
本实验结果提示p38MAPK在调节细胞空泡形成中的重要作用,p38MAPK在调节细胞空泡形成中的分子机制有待于后续实验进一步探讨。
[1]Morissette G,Moreau E,C-Gaudreault R,et al.Massive cell vacuolization induced by organic amines such as procainamide[J].Pharmacol Exp Ther,2004,310(1):395-406.
[2]Wang C,Chen T.Intratumoral injection of taxol in vivo suppresses A549tumor showing cytoplasmic vacuolization[J].Cell Biochem,2012,113(4):1397-1406.
[3]Kar R,Singha PK,Venkatachalam MA,et al.A novel role for MAP1LC3in nonautophagic cytoplasmic vacuolation death of cancer cells[J].Onco Gene,2009,28(28):2556-2568.
[4]Ohkuma S,Poole B.Cytoplasmic vacuolation of mouse peritoneal macrophages and the uptake into lysosomes of weakly basic substances[J].Cell Biol,1981,90(3):656-664.
[5]Henics T,Wheatley DN.Cytoplasmic vacuolation,adaptation and cell death:A view on new perspectives and features[J].Biol Cell,1999,91(7):485-498.
[6]Hiruma H,Kawakami T.Characteristics of weak base-induced vacuoles formed around individual acidic organelles[J].Folia Histochem Cytobiol,2011,49(2):272-279.
[7]Funakoshi T,Aki T,Unuma K,et al.Lysosome vacuolation disrupts the completion of autophagy during norephedrine exposure in SH-SY5Yhuman neuroblastoma cells[J].Brain Res,2012,1490(15):9-22.
[8]Martinet W,De Meyer GR.Autophagy in atherosclerosis[J].Curr Atheroscler Rep,2008,10(3):216-223.
[9]Alonso MM,Jiang H,Gomez-Manzano C,et al.Targeting brain tumor stem cells with oncolytic adenoviruses[J].Methods Mol Biol,2012,797:111-125.
[10]Tasdemir E,Maiuri MC,Tajeddine N,et al.Cell cycle-dependent induction of autophagy,mitophagy and reticulophagy[J].Cell Cycle,2007,6(18):2263-2267.
[11]Zhang Y,Yu C,Huang G,et al.Nano rare-earth oxides induced size-dependent vacuolization:An independent pathway from autophagy[J].Int J Nanomed,2010,5(1):601-609.
[12]Dutta R,Das N.Immunomodulation of serum complement(C3)and macrophages by synthetic pyrethroid fenvalerate[J].In vitro study Toxicology,2011,285(3):126-132.
[13]Wang WB,Feng LX,Yue QX,et al.Paraptosis accompanied by autophagy and apoptosis was induced by celastrol,a natural compound with influence on proteasome,ER stress and Hsp90[J].Cell Physiol,2012,227(5):2196-2206.
[14]Menon MB,Kotlyarov A,Gaestel M.SB202190-induced cell typespecific vacuole formation and defective autophagy do not depend on p38MAP kinase inhibition[J].PLoS One,2011,6(8):e23054.
[15]Takebe K,Nishiyama T,Hayashi S,et al.Regulation of p38MAPK phosphorylation inhibits chondrocyte apoptosis in response to heat stress or mechanical stress[J].Int J Mol Med,2011,27(3):329-335.

