多元螯合与多重螯合微量元素的理论及其在饲料业中的应用
冯定远
(华南农业大学动物科学学院,广州 510642)
有机微量元素作为饲料添加剂已经应用多年,从理论上讲,饲料用有机微量元素的作用毋庸置疑。本课题组在2003年也开展了有机微量元素在繁殖母猪上的应用试验,研究其对母猪繁殖性能及仔猪的影响[1-2]。近年来,添加有机微量元素的试验除了直接的生产性能研究外,还探讨了其对畜禽的免疫[3-5]、内分泌[6]、抗热应激[7]、肉品质[8-9]、蛋品质[10-12]、体组织成分[13-15]以及健康[7,16]等方面的影响,同时也评估其相对生物学效价[17]、消化利用[18]和抗营养因子的关系[19],也有研究有机源的铜、铁、锰、锌来评估NRC生长肥育猪的需要水平[20]。但是,目前饲料添加剂有机微量元素产品良莠不齐,高质量的还不多,市场还比较混乱,使用者疑虑仍然比较多。这里的原因有多方面,除了应用者的认识和性价比等因素外,还有一些客观的原因。目前更多所谓的“有机微量元素”或者“螯合物”是有机物、无机物和有机微量元素的混合物,如何提高“高纯度”和“完全化”有机微量元素的程度是未来有机微量元素产品发展的两大方向。
1 目前存在的问题
有机微量元素的合成和生产受到许多因素的影响,这些因素不仅影响产品的质量,也影响产品的成本:1)同一种有机微量元素添加剂生产的反应工艺水平差异大,产品质量有很大的区别;2)有机微量元素种类多,作用差别大,有些没有作用甚至负面作用,如植酸盐、草酸盐也是有机微量元素;3)有机微量元素的化学特性不同,按配位体与配位原子(离子)的不同分简单络合、螯合、多核络合等,产品的稳定性和生物学效价有比较大的差异;4)有机微量元素的理化系数不同,包括络(螯)合率、络(螯)合常数、络(螯)合强度等参数或系数,特别是络(螯)合率,有些比较难得到适合作为饲料添加剂的有机微量元素。
由于在确定的反应体系内,特定的反应条件下,化学反应是不可能完全充分把有机物和微量元素二者同时结合,在没有合适的催化剂的情况尤其如此。单一螯合物的螯(络)合率(反应得率)不可能达到100%,有些生产工艺实际的螯(络)合率不高,不同工艺和生产厂家差别和水平差异很大,有些所谓的“螯合物”产品严格上讲还不是真正意义上的“有机微量元素”,而是少量螯合物和大量无机物的混合物。即使工艺水平高的,也是有机与无机的“混合微量元素”,而不是纯粹的有机微量元素。实际上,目前许多有机微量元素饲料添加剂产品只能是有机与无机的“混合微量元素”。高纯度螯合的螯合物才比较接近真正意义的有机微量元素。
络(螯)合率高低问题,既有生产工艺水平问题,又有2种化学成分的特性问题。即使生产工艺水平的提高,也不可能使2种成分同步完全络(螯)合。从生产效率和成本考虑,针对饲料用有机微量元素,我们提出,可以在单一络(螯)合的基础上,应用多元络(螯)合与多重络(螯)合的理论,生产多元络(螯)合物或多重络(螯)合物,使“混合微量元素”变成更接近纯粹的完全化有机微量元素。
2 有机微量元素、络合物、螯合物、混合物
2.1 有机微量元素
讨论多元络(螯)合和多重络(螯)合时,首先必须理清几个名词和概念,这些名词概念有一定的关联,但是更多的时候是使用混乱。有机微量元素是最基本的概念,螯合物是特殊的有机微量元素。有机微量元素是指有机物与无机微量元素通过化学键或物理氢键结合的产物。营养学意义的微量元素种类为数不多,主要是金属元素如铜、铁、锰、锌等几种。有机物与常量元素(如钙、镁)结合一般称为有机矿物盐。可以与微量元素结合的有机物的种类则非常多,生产饲料用有机微量元素多用有机酸和氨基酸,如富马酸铁、乳酸亚铁、甘氨酸铁、蛋氨酸铁。实际上,不同来源铁的生物有效性差别很大。有机酸中的草酸和植酸是很强的络合剂,对大部分的常量元素和微量元素都有很强的结合能力,而且在常规条件下是不可逆的,所以并不是所有的有机微量元素都有营养意义,相反植酸就有非常强的抗营养作用。金属蛋白(肽)盐的本质是氨基酸与有机微量元素的结合。微量元素也可以与脂肪酸结合,一般称为皂化反应,多表现为抗营养作用。微量元素也可以与糖类或者其他有机物结合,如葡萄糖锌、烟酸铬、吡啶羧酸铬等。
2.2 络合物
微量元素与有机物以化学键或物理键结合一般称为络合,所以有机微量元素常常称为络合物。络合物是由作为中心离子的金属元素与配位体(离子或分子)的有机物通过配位键的结合形成,根据络合物的组成,络合物可分成简单络合物、两核络合物、多核络合物等多种,简单络合物分子或离子只有一个中心离子,每个配位体只有一个配位原子与中心离子成键。
一般的有机微量元素为盐类,也有不是盐类的特异有机微量元素,如营养性微量元素硒取代蛋氨酸中的硫,成为硒代蛋氨酸(或称为蛋氨酸硒,酵母硒的主要成分为蛋氨酸硒)。从严格意义上讲,蛋氨酸硒是有机微量元素,但不是络合物。这是特例,基本上有机微量元素就是络合物。
2.3 螯合物
一般的有机微量元素是简单络合物,特别是有机酸形式的络合物。对于某些氨基酸而言,金属微量元素可以与2个氨基酸或多个氨基酸通过较牢固的化学键(配位键和离子键)形成杂环(五或六环)结构,整个分子结构呈中性。这类两核络合物或多核络合物是特殊的络合物,称为螯合物或者钳合物。氨基酸的氨基和羧基与金属微量元素离子螯合,是氧和氮作配位原子。一般来说,简单络合物的稳定性较差,而环状结构(螯合物也称作内络合物)使螯合物比具有相同配位原子的简单络合物更稳定。
螯合物与普通络合物的差异是特殊的空间结构,“螯合”一词之意是象螃蟹的钳一样固定,很稳定,在通常的消化道的理化条件下不会脱出来,可以以有机或无机形式直接吸收。但是,水解氨基酸的平均分子质量必须接近150 u,螯合物的分子质量不能超过800 u。如果分子质量大于800 u,则螯合物在肠道内不经过水解不能直接穿越细胞膜。只有为数不多的几类有机物可以形成环状结构,目前了解比较多的是氨基酸,也不是所有的氨基酸可以与微量元素螯合,有些只能是络合。在蛋白金属盐或者小肽络合物中,可以同时存在普通络合和特殊螯合2种结合现象。
以最简单的甘氨酸和金属铜结合为例,可以有3种形式(图1):1)1分子甘氨酸通过氨基和1分子铜以共价键结合,形成普通的甘氨酸铜络合物;2)2分子甘氨酸通过对角2个氨基及对角2个羧基和1分子铜结合(其中1个N和1个O以共价键结合,实线表示;一个N和一个O以离子键结合,虚线表示),形成典型的甘氨酸铜螯合物;3)4分子甘氨酸通过相邻2个氨基及相邻2个羧基和1分子铜结合(2个O以共价键结合,2个N以离子键结合),形成复杂的甘氨酸铜小肽螯合物。可以看出,1分子铜可能与1分子、2分子或4分子甘氨酸结合,可能是普通络合,也可能是特殊螯合。
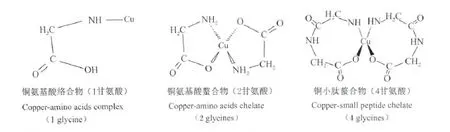
图1 铜氨基酸络(螯)合物分子结构式Fig.1 Structural formula of copper-amino acids complex/chelate
在自然状态下,大部分结合是普通络合和特殊螯合同时存在,即使在专门的氨基酸螯合物生产中,也可能是一般络合物和螯合物都有的产品。所以,关于络合和螯合的名词经常在混用,对于氨基酸源的有机微量元素尤其如此。考虑到许多非氨基酸源的有机微量元素并不是螯合物,而是普通的络合物,所以,以络合物为着眼点。但混用称呼螯合物也是为了大家的习惯,在本文的讨论中,为了方便,后面统一使用螯合物一词称谓包括广义上的“络合物”和狭义上的“螯合物”。
2.4 混合物
在目前实际生产工艺与技术的设计中,更多的是有机物、无机物和有机微量元素的混合物,完全化的有机微量元素并不多见。这里又有多层意思,一是有机物与无机物二者的混合物;二是有机物与有机微量元素二者的混合物;三是无机物与有机微量元素二者的混合物;四是有机物、无机物与有机微量元素三者的混合物。第1种情况很少见,只有完全不涉及反应的工艺条件情况下才有可能,例如直接把粉状的蛋氨酸和硫酸锌混合,第4种类型是目前最常见的情况,而第2种和第3种情况是目前比较好的状态。应用单一螯合技术,即使第2种和第3种情况,也只是实现高纯度螯合物的要求。
最好的状态是完全化的有机微量元素,理想的状态只有通过多元螯合和多重螯合技术与工艺的设计才能实现,特别是多元螯合和多重螯合同时结合的技术与工艺是理想目标。
3 螯合率、转化率、螯合常数、螯合强度
3.1 螯合率
螯合率是指有机微量元素产品中螯合元素量占总元素量的比例,在螯合物的实际应用中人们经常把螯合率看作一种反应得率。螯合率概念是不充分的,络合物化学中没有螯合率概念。通常的螯合率只是考虑金属元素的比例,是从金属元素的角度看,这是不全面的。在络合反应中,有机物有多少比例变成有机微量元素又如何反映出来?特别是有些珍贵的有机物,又特别适合做配位体,一般希望都与金属元素结合。在普通的络合物或者螯合物生产中,螯合率、反应得率都存在一定的问题,只反映了一个方面。
3.2 转化率
在使用更准确的名词“金属元素螯合率”的基础上,是否再增加一个概念“有机物转化率”?我们提出供大家共同讨论。假定组氨酸与钴离子(Co2+)螯合为组氨酸钴,由于钴元素珍贵,希望提高钴元素螯合率,同时,组氨酸目前并不是限制性氨基酸,还不作为添加剂使用,一般需要少,价格高,而多余的组氨酸并不象蛋氨酸、赖氨酸那样有明显的营养价值,也希望提高其螯合过程中的效率,光是钴元素螯合率还是不够的,还需要有一个“组氨酸转化率”的系数来反映工艺水平的高低。
3.3 螯合常数
在不考虑螯合物稳定程度的情况下,配位体螯合金属离子的反应一般容易发生,只要是混合配位体和金属离子的溶液就可以实现螯合。螯合后的稳定情况以螯合物的稳定常数来表示。螯合物的稳定常数是有条件的,也称为螯合条件稳定常数(简称螯合常数)。螯合常数是指有机微量元素产品中已经络合部分的稳定程度,螯合物在溶液中的稳定性通常以螯合物的稳定常数来表示。稳定常数有活度稳定常数和浓度稳定常数,一般常用浓度稳定常数。在一定温度下,只有在溶液中离子强度恒定的条件下,浓度稳定常数才是常数。常数的大小是由化学结构和热力学原理决定的,配位体的分子轨道与金属的轨道耦合作用形成是通过金属中心的离域所致,其电子云的分布是决定络合结构稳定性的主要因素。一般地,简单络合物的稳定性较差。
影响稳定常数主要是配位体的特性,金属离子也有差别,如植酸与钙、镁、铜、钴的络合稳定为镁<钙<铜<钴,原因是钙、镁多以离子键形式成键,钴的成键中多含一些共价键,而铜则居中[21]。共价键比离子键更稳定。
螯合物的稳定常数过低和过高都会影响动物的吸收和利用,动物试验表明,螯合物(内络盐和某些络阳离子)在单胃动物胃中的不溶性,有利于螯合物保持稳定性,然而有些在胃中不易溶解的螯合物可在小肠中溶解吸收,在消化道中溶解的螯合物有利于吸收。
3.4 螯合强度
尽管常用螯合物稳定常数来进行评估,但对于成分较复杂的复杂有机微量元素,如蛋白质或肽类络(螯)合微量元素,测定稳定常数较困难,因为溶液中配位体的浓度、配位数难以准确测定。根据络合平衡关系及络合态和非络合态金属离子的半波电位差△E,Holwerda等[22]提出了螯合强度的参数法。基本原理是金属元素与配位体形成络合物后,在电压作用下还原为金属-汞极的难度加大,电位向更负的方向移动。根据络合物与金属离子还原为金属(Hg)的E1/2差值,即可计算络合物的螯合强度。螯合强度低于10的为弱螯合强度,10~100的为中等螯合强度,100~1 000的为强螯合强度,超过1 000的为极强螯合强度。该法只用于测定饱和溶液中有机微量元素的螯合强度[23],而不能得出游离态和络合态元素的比例,却为鉴别复杂有机微量元素产品质量提供了一种行之有效的检测方法[24]。当然,关于有机微量元素的螯合强度与生物利用率,特别是与有机微量元素溶解度等仍然还有争论。罗绪刚[25]专门探讨了有机锰锌的螯合强度与吸收利用的关系及机制。许甲平等[26]也综述讨论了有机微量元素中螯合率、稳定常数和螯合强度之间的关系。
4 单一螯合、多元螯合、多重螯合、复合型螯合
4.1 单一螯合
单一螯合是指在同一反应体系中,一种有机物与一种无机元素结合的工艺。这是目前一般的螯合物情况。在不考虑螯合物稳定程度的情况下,配位体螯合金属离子都会发生反应,只要是混合配位体和金属离子的溶液就可以实现螯合。但是,有多少比例的金属离子发生了反应?另一个问题是反应以后的稳定性如何?一个螯合物在中性pH时稳定常数很大,但在酸性和碱性受到了H+和OH-浓度的影响,会解离成配位体和金属离子或生成羟合络离子和配位体。由于氨基酸比微量元素价格高,一般在螯合物产品中会含有过剩的金属离子。相反,在一些价格高的金属与某些相对价格低的有机物络合物中,一般含有比较多的单体有机物,有些作为配位体的有机物(如氨基酸和部分有机酸)有营养价值,有些则没有营养价值,有时可能还有一些负作用,如长期使用对肠道健康会产生不良影响。大部分情况下是同时含有螯合物、无机盐和有机物。
4.2 多元螯合
根据有机微量元素中无机微量元素与有机物结合的螯合率、转化率、螯合常数、螯合强度的机理,应用系统动物营养学原理,可以在单一螯合的基础上进行多元螯合。多元螯合是指在同一反应体系中,一种有机物与多种无机元素分别结合的工艺,产生的产物就是多元螯合物。其中与2种元素的结合是两元螯合,与3种元素结合就是三元螯合等。例如,蛋氨酸同时可以与锌和铁结合,形成蛋氨酸锌和蛋氨酸铁。目前实际的螯合物生产工艺是分别单独与锌的螯合或与铁的螯合,是2个单一螯合物。在天然饲料成分中,植酸盐就是一种典型的多元螯合物,只是结合太紧密,稳定系数过高,基本不能够可逆释放,不能够作为营养性化合物,反而是抗营养性复合物。
多元螯合是基于一般的螯合率不是特别高,一种微量元素与氨基酸螯合后,多余的氨基酸可以与另外一种微量元素螯合。氨基酸价格往往比微量元素价格高,为了充分使氨基酸螯合,在螯合物生产中,使用过量的微量元素,使产品中有过剩的金属离子,使螯合率降低。从化学合成角度,氨基酸和微量元素任何一者过量许多都是不合理的。多元螯合物产品是指在同一生产工艺中含有多种微量元素与一种有机物结合的产品,如蛋氨酸锌与蛋氨酸铁。但是,把2种单一螯合物人为复配的蛋氨酸锌与蛋氨酸铁是复合物产品,即有机锌与有机铁预混料。
同一种氨基酸(配位体)与不同金属元素形成的螯合物稳定常数有差别,如蛋氨酸铁的LogK1·K2为6.7,而蛋氨酸铜的 LogK1·K2为14.7。多元螯合的原则是根据螯合物稳定常数大小决定反应的顺序,先反应稳定常数大的元素,后反应稳定常数小的元素。例如,在蛋氨酸铜与蛋氨酸铁的两元螯合物中,生产的工艺是先利用蛋氨酸与硫酸铜反应,然后再与硫酸亚铁反应,目标是充分利用蛋氨酸作为配位体。多元螯合的核心是寻找理想的配位体有机物,有很强的结合能力,而同时又不能稳定性过高,像植酸一样。
4.3 多重螯合
同样,应用系统动物营养学原理,可以在单一螯合的基础上进行多重螯合,多重螯合是指在同一反应体系中,一种无机金属元素与多种有机物分别结合的工艺,产生的产物为多重螯合物。其中与2种有机物的结合是双重螯合,与3种有机物结合就是三重螯合等。如无机铁分别与富马酸、甘氨酸、蛋氨酸结合,形成富马酸铁、甘氨酸铁或蛋氨酸铁。同讨论“多元螯合”的情况一样,目前实际的螯合物生产工艺是分别单独与富马酸、甘氨酸或者蛋氨酸结合。把2种单一螯合物人为复配的蛋氨酸铁与甘氨酸铁是复合物产品,即有机铁预混料。
同一种金属元素与不同氨基酸的螯合物稳定常数不同,如蛋氨酸锌的LogK1为4.38,而甘氨酸锌的LogK1为5.16。金属元素与氨基酸的摩尔比为2时稳定常数增大很多。微量元素氨基酸螯合物的稳定常数(LogK1或LogK1·K2)都在3~6或3~10,而有机酸的稳定常数则一般小于2,乙二胺四乙酸二钠的稳定常数(LogK1)都大于13,抗营养因子的植酸与铜络合的LogK1为10.91。多重螯合的原则同样是根据螯合物稳定常数大小决定反应的顺序,先反应稳定常数大的有机物,后反应稳定常数小的有机物。例如,在富马酸铁与蛋氨酸铁双重螯合物中,生产的工艺是先利用蛋氨酸与硫酸亚铁反应,然后是富马酸与硫酸亚铁反应,目标是充分利用硫酸亚铁,使之变成有机铁。
4.4 复合型螯合
理论上,复合型螯合是同时考虑多元螯合和多重螯合,在同一反应体系中,首先一种有机物与多种无机元素分别结合,经过计算和分析测定,剩余的无机元素再选择一种或者多种有机物反应。或者相反,在同一反应体系中,一种无机元素与多种有机物分别反应结合,经过计算和分析测定,剩余的有机物再选择一种或者多种无机元素进行反应结合,生产出来的产品就是复合有机微量元素。平时使用的复合有机微量元素是通过不同单一螯合物复配而成。实际上,复合型螯合工艺是复杂而很难实现,或者经济价值不合算。
5 多元螯合与多重螯合的意义
多元螯合是为了提高有机物配位体的转化率;多重螯合是为了提高无机元素的螯合率。多重螯合可以生产完全“有机物+螯合物”的有机微量元素,不含有无机物。基本上是完全化的有机微量元素。
多重螯合有2方面的意义:一是更充分提高目标微量元素的利用效率;二是进一步减少微量元素添加剂的污染。同样,多元螯合也有2方面的意义:一是充分利用价值高的有机物的螯合作用;二是减少个别作为螯合配位体的有机物可能对动物肠道健康的抗营养作用。多重螯合的核心是充分把重要的无机金属元素变成有机金属元素,如一些所谓功能性性添加剂,如强补铁、强补锌生产皮红毛亮产品或者高锌蛋等。多重螯合物的另一项潜在重大价值是环境保护,理论上,多重螯合可使添加剂的金属元素低排放甚至零排放。另外,多元螯合物与多重螯合物比,一般的单一螯合物适口性更好,毒副作用小,安全性高。
多元螯合与多重螯合2种工艺结合起来是理想的状态,实际工艺非常复杂,可以简称多元与多重螯合。理论上,多元与多重螯合可以直接生产真正意义上的复合有机微量元素,也是完全化的有机微量元素。
在讨论多元螯合和多重螯合的同时,不能贬低单一螯合的作用和意义,实际上,有机微量元素的主流仍然是单一螯合物。但我们鼓励工艺条件好和技术水平高的机构,探讨研究开发多元螯合物或多重螯合物产品,作为目前单一螯合物的补充,引领有机微量元素朝多元化、系列化和高质量方向发展。
在这里特别强调指出:由于饲料原料的复杂性,饲料本身存在含量变异的多种微量元素,同时,也含有各种抗营养因子,不仅影响饲料原料微量元素的有效供给量,也影响添加的无机微量元素的效率,微量元素完全精准难度很大,使用多元螯合和多重螯合更有意义。而化工及其他领域使用的有机微量元素,更多应该是高纯度单一螯合物。
总之,针对目前更多所谓的“有机微量元素”是有机物、无机物和有机微量元素的混合物的现状,必须思考和重视高纯度和完全化有机微量元素的问题,这是未来有机微量元素发展的两大方向。应用系统动物营养学原理,系统研究和开发单一螯合、多元螯合和多重螯合等系列产品,满足不同目的的需要将越来越被认识和重视。其中,基于多元螯合和多重螯合理论的完全化有机微量元素是饲料有机微量元素领域发展的一个创新。
6 小结
根据无机微量元素与有机物结合的螯合率、转化率、螯合常数、螯合强度的机理,在单一螯合的基础上,有机物与微量元素的反应可以进一步进行多元螯合或者多重螯合的结合。多元螯合是指在同一反应体系中,一种有机物与多种无机元素分别结合的工艺;多重螯合是指在同一反应体系中,一种无机金属元素与多种有机物分别结合的工艺。应用多元螯合物能够充分利用价值高的有机物的螯合作用,同时减少个别作为螯合配位体的有机物可能对动物肠道健康的影响;应用多重螯合物能够更充分提高微量元素的利用效率,同时进一步减少微量元素添加剂的污染。单一螯合、多元螯合和多重螯合的有机微量元素可以组成一个有机微量元素的系列,各自发挥其营养性和功能性作用。
[1]谭会泽.不同复合有机微量元素对经产母猪繁殖性能及血液生化指标的影响[D].硕士学位论文.广州:华南农业大学,2003.
[2]沈思军.母猪添加不同类型有机微量元素对仔猪影响的研究[D].硕士学位论文.广州:华南农业大学,2003.
[3]FERNANDES J I M,BORTOLUZZI C,KOSMANN R C,et al.Assessment of beer yeast diet and organic minerals on the performance and immune reponse of broilers immunized against coccidiosis vaccine[J].Ciência Rural,2013,43(8):1496-1502.
[4]VIEIRA M S V,ZANETTI M A,JUNIOR L C R,et al.Performance and immune response of suckling calves fed organic selenium[J].Animal Feed Science and Technology,2014,188:28-35.
[5]WANG R L,LIANG J G,LU L,et al.Effect of zinc source on performance,zinc status,immune response,and rumen fermentation of lactating cows[J].Biological Trace Element Research,2013,52(1):16-24.
[6]XIE J,TIAN C,ZHU Y,et al.Effects of inorganic and organic manganese supplementation on gonadotropin--releasing hormone-Ⅰ and follicle-stimulatinghormone expression and reproductive performance of broiler breeder hens[J].Poultry Science,2014,93(4):959-969.
[7]OLTRAMARI C E,PINHEIRO M G,DE MIRANDA M S,et al.Selenium sources in the diet of dairy cows and their effects on milk production and quality,on udder health and on physiological indicators of heat stress[J].Italian Journal of Animal Science,2014,13(1),25-30.
[8]OLIVEIRA T F B,RIVERA D F R,MESQUITA F R,et al.Effect of different sources and levels of selenium on performance,meat quality,and tissue characteristics of broilers[J].Journal of Applied Poultry Research,2014,23(1):15-22.
[9]MA Y L,LINDEMANN M D,CROMWELL G L,et al.Evaluation of trace mineral source and preharvest deletion of trace minerals from finishing diets for pigs on growth performance,carcass characteristics,and pork quality[J].Journal of Animal Science,2012,90(11):3833-3841.
[10]SOLOMON S E,BAIN M M.Structural and physical changes in the hen’s eggshell in response to the inclusion of dietary organic minerals[J].British Poultry Science,2012,53(3):343-350.
[11]FERNANDEZ I B,CRUZ V C,POLYCARPO G V.Effect of dietary organic selenium and zinc on the in-ternal egg quality of quail eggs for different periods and under different temperatures[J].Brazilian Journal of Poultry Science,2011,13(1):35-41.
[12]GRAVENA R A,MARQUES R H,PICARELLI J,et al.Supplementation in quail diet with organic minerals on performance and egg quality[J].Arquivo Brasileiro de Medicina Veterinária e Zootecnia,2011,63(6):1453-1460.
[13]BRIENS M,MERCIER Y,ROUFFINEAU F,et al.2-Hydroxy-4-methylselenobutanoic acid induces additional tissue selenium enrichment in broiler chickens compared with other selenium sources[J].Poultry Science,2014,93(1):85-93.
[14]JLALI M,BRIENS M,ROUFFINEAU F,et al.Evaluation of the efficacy of 2-hydroxy-4-methylselenobutanoic acid on growth performance and tissue selenium retention in growing pigs[J].Journal of Animal Science,2014,92(1):182-188.
[15]WANG J,LI D,CHE L,et al.Influence of organic iron complex on sow reproductive performance and iron status of nursing pigs[J].Livestock Science,2014,160:89-96.
[16]HILL G M,MAHAN D C,JOLLIFF J S.Comparison of organic and inorganic zinc sources to maximize growth and meet the zinc needs of the nursery pig[J].Journal of Animal Science,2014,92(4):1582-1594.
[17]MA X Y,LIU S B,LU L,et al.Relative bioavailability of iron proteinate for broilers fed a casein-dextrose diet[J].Poultry Science,2014,93(3):556-563.
[18]JOLLIFF J S,MAHAN D C.Effect of dietary calcium and phosphorus levels on the total tract digestibility of innate and supplemental organic and inorganic microminerals in a corn-soybean meal based diet of grower pigs[J].Journal of Animal Science,2013,91(6):2775-2783.
[19]SCHLEGEL P,SAUVANT D,JONDREVILLE C.Bioavailability of zinc sources and their interaction with phytates in broilers and piglets[J].Animal,2013,7(1):47-59.
[20]GOWANLOCK D W,MAHAN D C,JOLLIFF J S,et al.Evaluating the NRC levels of Cu,Fe,Mn,and Zn using organic minerals for grower-finisher swine[J].Journal of Animal Science,2013,91(12):5680-5686.
[21]冯屏,冯小兵,徐玉佩.植酸与金属离子络合的研究[J].中国油脂,2006,31(8):63-66.
[22]HOLWERDA R A,ALBIN R C,MADSEN F C.Chelation effectiveness of zinc proteinates demonstrated[J].Feedstuffs,1995,67(25):12-13.
[23]HOLWERDA R A.Chelation effectivenedd in zinc,manganese and copper proteinates,complexed minerals products symposium[C]//AAFCO Laboratory Methods and Services Committee,[S.l.]:[s.n.],1997:4.
[24]HOLWERDA R A.‘Quick test’for organmic mineral supplements[J].Feed International,2001,10:28-31.
[25]罗绪刚.有机锰锌的络合强度与其在肉鸡体内吸收利用的关系及机制[J].中国家禽,2011,33(9):40-42.
[26]许甲平,鲍宏云,邓志刚,等.有机微量元素中螯合率、稳定常数和螯合强度之间的关系[J].饲料广角,2012(23):29-30.

