慢性粒细胞白血病BCR-ABL融合基因实时定量检测平台的建立
黄 丹,高贝贝,李 莉,苏晶莹,高 源,闫金松,刘晓晖,邵 静,康志杰
(1.大连医科大学附属第二医院血液科,辽宁大连 116027;2.大连医科大学 公共卫生学院,辽宁 大连 116044)
慢性粒细胞白血病BCR-ABL融合基因实时定量检测平台的建立
黄 丹1,高贝贝1,李 莉1,苏晶莹1,高 源1,闫金松1,刘晓晖2,邵 静2,康志杰1
(1.大连医科大学附属第二医院血液科,辽宁大连 116027;2.大连医科大学 公共卫生学院,辽宁 大连 116044)
目的 建立慢性粒细胞白血病(chronic myelogenous leukemia,CML)患者BCR-ABL融合基因检测及微小残留病变实时定量监测的诊断平台。方法 依据GenBank中编码P210蛋白的融合基因M(b2a2,b3a3)及ABL的基因序列,分别设计引物及Taqman探针,以BCR-ABL阳性的CML患者cDNA为模板,通过PCR扩增出587 bp的基因片段,连入pMD 18-T载体,制备成标准品并绘制标准曲线,运用实时荧光定量PCR(real-time quantitative PCR,RQ-PCR)技术监测BCR-ABL转录水平的变化。结果 成功构建BCR-ABL标准品。应用RQ-PCR探针法,以ABL为内参,对CML患者进行BCR-ABL融合基因的检测,得到比较稳定的定量数据,与定性结果一致。结论 自行构建BCR-ABL质粒为标准品,运用RQ-PCR实时监测BCR-ABL融合基因的表达变化,敏感性好,稳定性高,对临床检验具有普遍意义。
慢性粒细胞白血病;BCR-ABL;标准品;实时荧光定量PCR;诊断平台
慢性粒细胞白血病(chronic myelogenous leukemia,CML)是起源于骨髓多能造血干细胞的恶性增殖性疾病,其细胞遗传学特征是具有Ph染色体 t(9;22)(q34;q11)[1-2],形成 BCR - ABL 融合基因,该融合基因编码的BCR-ABL融合蛋白具有很强的酪氨酸激酶活性,可抑制髓系细胞的粘附和凋亡,促使细胞不依赖于细胞生长因子而过度增殖,引发大量异常细胞的恶性增殖[3]。近年来,随着分子生物学技术的发展和对发病机制的研究,肿瘤靶向治疗已经成为CML治疗的一线方案[3],而针对BCRABL融合基因的检测及监测为CML的诊治提供了可靠的分子依据[4-5]。因此,建立稳定、有效、可行的实时定量检测BCR-ABL融合基因的方法是非常必要的[6]。
1 材料和方法
1.1 材 料
试剂及仪器:RNAiso Plus(D9108A),pMD 18-T Vector(D109A),限制性内切酶EcoRI(D1040A),HindIII(D1060A),质粒纯化试剂盒(DV805A),PCR引物的合成及高保真PCR试剂盒(DR001A)均购自大连宝生物公司;反转录试剂盒及RQ-PCR试剂盒 RocketScript RT PreMix(AccuPower®)和 Accu-Power®DualstarTM qPCR PreMix,均购自 Bioneer公司。PCR仪为Applied Biosystems®GeneAmp®PCR System 9700和 Applied Biosystems®GeneAmp®PCR System 7500等。
1.2 方 法
1.2.1 引物设计:参照欧洲抗癌工作组多中心实验方法[7],以国际广泛应用并认可的ABL基因为内参,根据 GenBank人 BCR-ABL(e14a2)cDNA AJ131466、人v-Abl cDNA NM_007313分别设计上下游引物,构建BCR-ABL基因检测标准品,引物及探针为韩国Bioneer公司合成。分别设计检测BCR-ABL融合基因及内参基因的特异性引物及探针,引物设计示意图及具体序列见图1和表1。
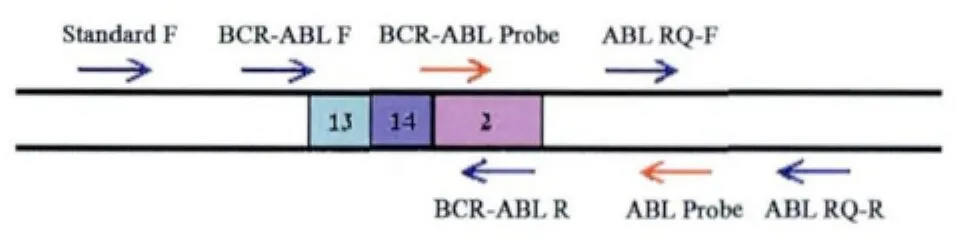
图1 BCR-ABL引物设计示意图Fig 1 Design of primers and probes of BCR-ABL
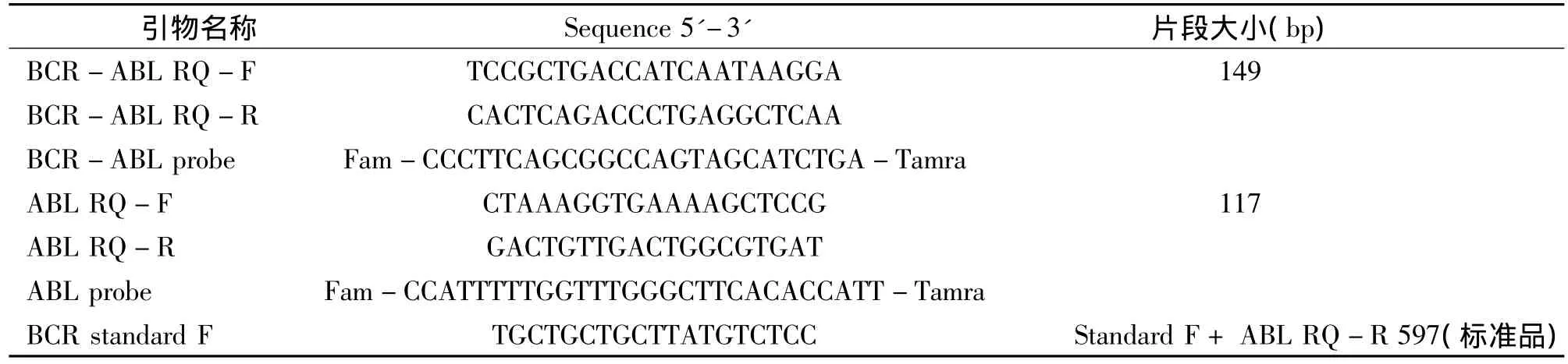
表1 BCR-ABL引物序列Tab 1 Sequences of primers and probes of BCR-ABL
1.2.2 BCR -ABL(S)标准品质粒的构建:提取患者外周血单个核细胞RNA,反转录为cDNA,应用巢式PCR筛查阳性标本[8],将回收的BCR-ABL片断,插入 pMD 18-T载体中,构建 pMD 18TBCR-ABL(S)质粒作为标准品。通过酶切鉴定后送测序,结果回报正确。扩增体系与条件:10×buffer 5 μL,dNTPs 5 μL,引物各2.0 μL,模板 cDNA 2.0 μL,Taq 酶 0.5 μL,H2O 33.25 μL。94 ℃ 变性30 s,56 ℃退火30 s,72 ℃延伸45 s,32 个循环。
1.2.3 标准曲线的制作:将构建成功的质粒转化扩增,根据Avogadro常数和核酸的平均分子量进行计算拷贝数,具体为:拷贝数/μL=(ng/μL ×10-9×6.02×1023)/(DNA碱基数×660)。将质粒稀释为 107/μL、106/μL、105/μL、104/μL、103/μL、102/μL和10/μL,制成标准品,通过实时定量绘制标准曲线。
1.2.4 CML患者标本的实时定量PCR检测与分析:提取CML患者外周血单核细胞总RNA,反转录为cDNA作为模板,以ABL为内参,进行实时荧光定量检测,将检测结果与标准曲线对比,得出拷贝数。为了检测的稳定性和准确性,每批实验需设置阴性对照及空白对照,同时设置3复孔,实验体系为20 μL,cDNA 2 μL、Pre Mix10 μL、RoxⅡ0.4 μL、上游引物 1 μL(10 pmol/μL)、下游引物 1 μL、探针 1 μL、水 4.6 μL,反应条件为解链 95 ℃ 5 s,退火 60℃ 30 s,60℃时采集荧光,共40个循环。
2 结果
2.1 pMD 18T-BCR-ABL(S)质粒的构建
以BCR-ABL(e14a2)阳性患者cDNA为模板,以BCR-ABL S-F+R为引物,成功扩增到597 bp目的片段(图2)。将扩增到的片段进行胶回收纯化,与 pMD 18-T Vector连接构建标准品 pMD 18T-BCR-ABL(S),以EcoR I及Hind Ш双酶切,1.5%琼脂糖凝胶电泳显示378 bp条带,证明扩增引物成功连入pMD 18-T Vector(图3)。将连接产物胶回收纯化送测序,回报序列完全正确,标准品构建成功(图4和5)。
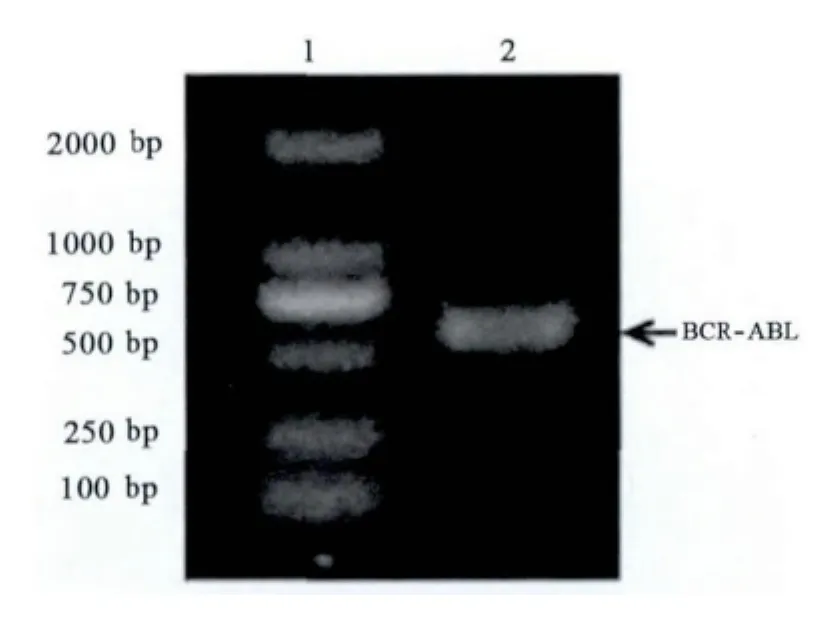
图2 PCR产物电泳图Fig 2 Electrophoretogram of PCR products

图3 酶切图谱Fig 3 Restriction map of standard
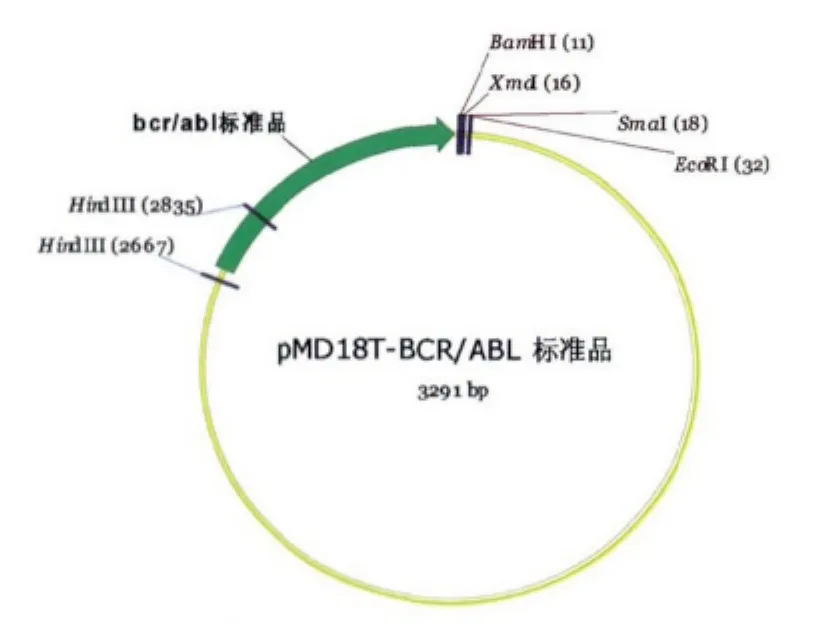
图4 pMD 18T-BCR-ABL(S)示意图Fig 4 Diagram of pMD 18T-BCR-ABL(S)
图5 pMD 18T-BCR-ABL(S)测序结果Fig 5 Sequencing result of pMD 18T-BCR-ABL(S)
2.2 标准品的制备及验证
2.2.1 核酸的定量及拷贝数的计算:pMD 18TBCR-ABL(S)质粒DNA定量结果为3040 ng/μL。故根据计算公式得到拷贝数为8.56×1011(copies/μL)。
2.2.2 标准品的制备:将质粒做10倍梯度稀释,数量分别为 8.56 × 107、8.56 × 106、8.56 × 105、8.56 ×104、8.56 × 103、8.56 × 102、8.56 × 101(copies/μL),以各拷贝梯度样品为模板,进行RQ-PCR扩增,同时设置3复孔及空白对照,图6为不同浓度质粒的扩增曲线,结果显示,不同浓度的模板在PCR扩增后按浓度由高到低的顺序均匀排列,即扩增曲线可以反映起始模板的量,将扩增产物进行1.1%的琼脂糖凝胶电泳,可见明确的目的条带,并随浓度的增加扩增产量增大,证明扩增曲线为特异性扩增。图7为应用质粒标准品绘制标准曲线。结果表明,质粒拷贝数与荧光信号进入设定的阈值时经历的循环数(thresholdcycle,Ct)呈现良好的线性关系,可以用于模板拷贝数的定量。
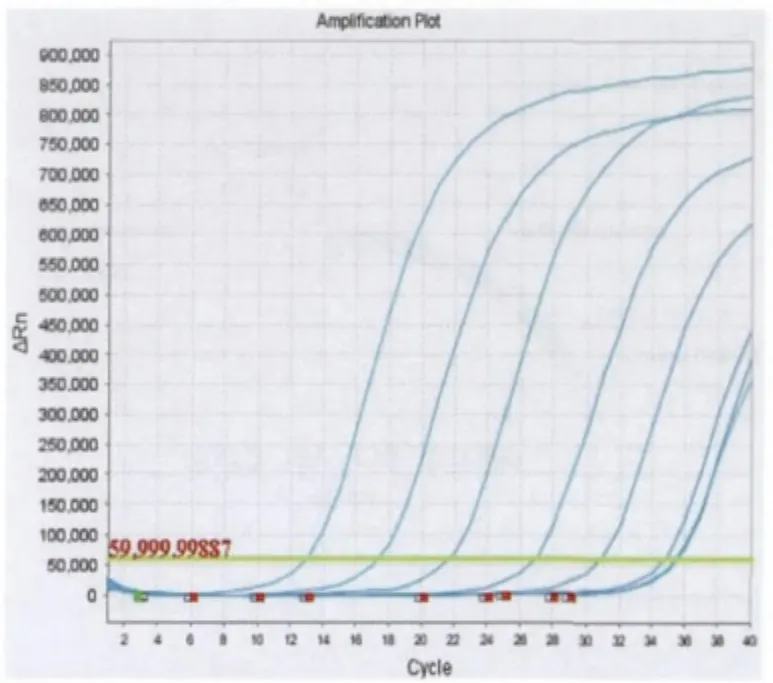
图6 标准品的扩增曲线Fig 6 Amplification plot of the standards
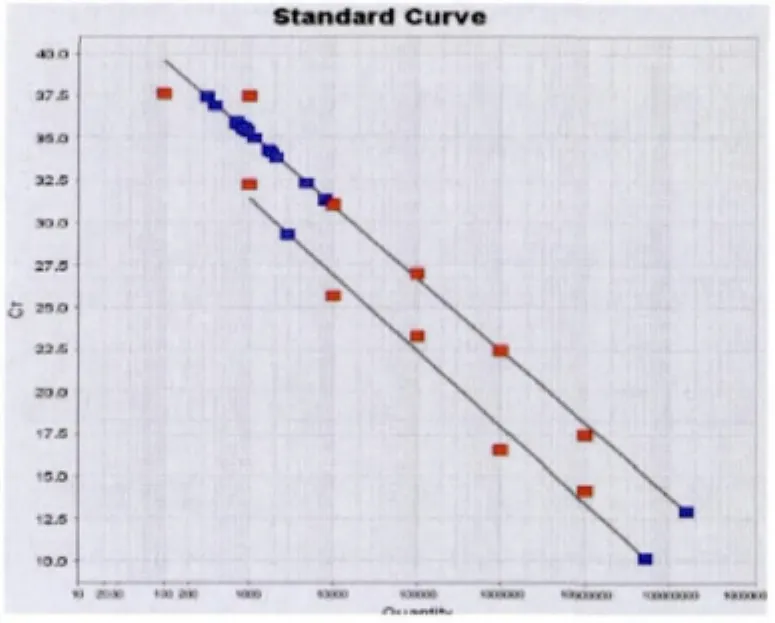
图7 pMD 18T-BCR-ABL(S)为模板建立的标准曲线Fig 7 Standard curve exhibited a good linear relationship between absorbance and pMD 18T-BCR-ABL(S)concentration
2.3 CML患者标本的实时定量PCR分析
以患者cDNA为模板,以构建的 pMD 18TBCR-ABL(S)为标准品,以ABL为内参,应用Taqman探针法,进行患者BCR-ABL融合基因的检测,可以得到比较稳定的定量数据,与定性结果一致(图8和图9)。
3 讨论

图8 利用RQ-PCR实验体系对慢性粒细胞患者血液标本进行BCR-ABL拷贝数检测Fig 8 Monitoring of BCR-ABL copies in CML patients by RQPCR
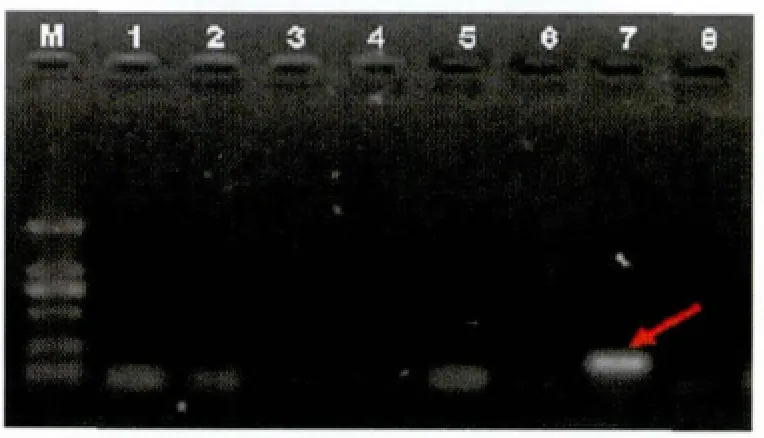
图9 RT-PCR检测患者血液标本DNA扩增产物1.1%的琼脂糖凝胶电泳Fig 9 The samples were amplified with RT-PCR and the products were showed in 1.1%Agar
基因变异是肿瘤形成的根本原因,其中一些特定的突变类型会导致特定的肿瘤,如Ph染色体的形成可直接造成慢性粒细胞白血病的发生。自Ph染色体被发现以来,临床广泛应用细胞遗传学方法检测Ph染色体做CML的诊断和疗效监测。然而基因异常可分为多种形式,染色体核型分析在甄别细微染色体异常时,并不能达到预期的效果。近十余年来,分子生物学方法检测BCR-ABL融合基因的应用逐渐普及。BCR-ABL融合基因的水平与临床疗效有很好的相关性[7],能预先对临床病情变化提出警示,对于白血病微小残留病的监测和及时调整治疗方案都有重要意义,尤其是分子靶向药物的应用,使得分子检测成为CML治疗中不可缺少的一部分,因此,定期检测BCR-ABL融合基因对临床诊疗的意义已经于世界范围内达成共识[9]。
实时定量PCR(RQ-PCR)方法检测灵敏度高,特异性好,能检测到 10-6~10-5个肿瘤细胞,是目前国际上应用检测微小残留病变最普遍的方法,使用实时定量PCR技术监测BCR-ABL分子学水平是评价疗效以及获得完全细胞遗传学反应的最佳方法,但因为已有商品化试剂费用昂贵,故未能广泛应用于临床检验。而以分子生物学技术为基础,自行构建含有BCR-ABL基因的环形质粒为标准品,以国际广泛应用并认可的ABL基因为内参基因,与荧光定量方法相结合,兼顾灵敏性与特异性,经济、快速、稳定,对临床诊断具有潜在价值,值得推广。
目前发现的BCR-ABL融合基因一共有3个亚型[4],ABL的断裂点始终发生在第2号外显子,而BCR的断裂点分别发生在第13、14号外显子,1号外显子及19号外显子,从而形成了不同的亚型,即M(b2-a2,b3-a2),m(e1-a2)及 u(e19-a2),M型编码210 kd的蛋白,主要见于90%以上的CML患者,而m型编码190 kd的蛋白,u型编码230 kd的蛋白,在CML患者中发生率较低。本实验室针对发生于大多数CML患者的M型BCR-ABL融合基因设计引物,成功建立起稳定可行的实时定量PCR检测平台,为CML患者的诊治工作提供了有效的分子支持。
基因检测对临床的诊断及治疗发挥着越来越重要的作用,应用分子生物学方法可以快速建立其他融合基因的特异性检测方法。因此,依托分子生物学实验室,参照欧洲抗癌工作组多中心实验方法,经患者本人同意及伦理委员会审批,利用其BCRABL阳性标本,构建质粒做为标准品,以国际广泛应用并认可的ABL基因为内参基因,以Taqman探针法,设计目的基因引物及探针,应用RQ-PCR技术,监测BCR-ABL融合基因的表达情况,敏感性好,稳定性高,可操作性强,对临床检验具有普遍意义,值得推广。
:
[1]Nowell PC HKA.A minute chromosome in human chronic granulocytic leukemia[J].Science,1960,132(3438):1497.
[2]Heisterkamp NSK,Groffern J.Structural organization of the bcr gene and its role in the Ph,translocation[J].Nature,1985,315(6022):758-161.
[3]Charles LS.Chronic myeloid leukemia[J].N Engl J Med,1999,340(17):1330-1340.
[4]Wong S Witte ON.The BCR -ABL story:bench to bedside and back[J].Annu Rev Immunol,2004,22:247 -306.
[5]Hochhaus AWA.Detection and quantification of residual disease in chronic myelogenous leukemia[J].Leukemia,2000,14(6):998-1005.
[6]孟凡义.慢性粒细胞性白血病的治疗[J].新医学,2004,35(7):392-393.
[7]J Gabert EB.Standardization and quality control studies of'real- time'quantitative reverse transcriptase polymerase chain reaction of fusion gene transcripts for residual disease detection in leukemia-A Europe Against Cancer Program[J].Leukemia,2003,17(12):2318-2357.
[8]李莉,康志杰,武克宇,等.Ph染色体和Bcr-Abl融合基因的动态监测在慢性粒细胞白血病治疗中的临床意义[J].临床和实验医学杂志,2012,11(16):1261-1263.
[9]Ou J VJA,Bagg A.Molecular diagnosis and monitoring in the clinical management of patients with chronic myelogenous leukemia treated with tyrosine kinase inhibitors[J].Am J Hematol,2008,83(4):296 -302.
Development of a diagnosis platform for real time quantitation of BCR-ABL fusion gene in chronic myelogenous leukemia
HUANG Dan1,GAO Bei-bei1,LI Li1,SU Jing -ying1,GAO Yuan1,YAN Jin -song1,LIU Xiao-hui2,SHAO Jing2,KANG Zhi-jie1
(1.Department of Hematology,the Second Affiliated Hospital of Dalian Medical University,Dalian116027,China;2.Department of Public Health,Dalian Medical University,Dalian116044,China)
[Abstract]ObjectiveTo improve clinical diagnosis and treatment of chronic myeloid leukemia(CML),we aim to establish a diagnosis platform for detecting BCR-ABL fusion gene and mornitoring minimal residual disease by constructing a circular plasmid using BCR-ABL fusion gene as a standard.MethodsWe designed primers and Taqman probes specific to BCRABL(b2-a2,b3-a2)and ABL,and used cDNA of the CML patient as the tamplate to amplify a BCR -ABL fragment.The 587bp PCR product of BCR -ABL was cloned into pMD 18T vector and used as a reference standard.The copy numbers was then determined and standard curve derived.The transcriptional expression of BCR/ABL in bone marrow samples from patients was quantitated by real-time quantitative PCR(RQ-PCR).ResultsWe constructed a circular plasmid with BCRABL fusion gene according to the method from cancer groups in Europe.With pMD 18T BCR -ABL plasmid as reference standard and ABL as an internal control,we accurately detected BCR -ABL expression in CML patients using Taqman based RQ-PCR.After further verification on technical feasibility and data reliability,a diagnosis platform for detecting BCR -ABL fusion gene and minimal residual disease in CML patients was then established.ConclusionThe Taqman based RQ -PCR can greatly improve the sensitivity and reliability in detection of BCR -ABL fusion gene expression.With the technical feasibility,the platform could be helpful for the clinical gene diagnosis and provide guidance for CML treatment.
[Key words]chronic myeloid leukemia;BCR-ABL;standard reference;RQ-PCR;diagnosis platform
R446.9
A
1671-7295(2014)01-0013-05
黄丹,高贝贝,李莉,等.慢性粒细胞白血病BCR-ABL融合基因实时定量检测平台的建立[J].大连医科大学学报,2014,36(1):13 -17.
10.11724/jdmu.2014.01.04
大连医科大学附属第二医院青年基金(2011)
黄 丹(1986-),女,辽宁大连人,技师。E-mail:huangdan860901@126.com
康志杰,主治医师。E-mail:cathie1997@sina.com
2013-09-08;
2013-11-30)

