卤素-镁交换法合成2-三氟甲基丙烯酸*
赵 娟,万 洪,冯晓军,徐洪涛,吕 剑
(西安近代化学研究所,陕西 西安 710065)
·研究简报·
卤素-镁交换法合成2-三氟甲基丙烯酸*
赵 娟,万 洪,冯晓军,徐洪涛,吕 剑
(西安近代化学研究所,陕西 西安 710065)
以2-溴-3,3,3-三氟丙烯(1)为原料,经卤素-镁交换反应制得中间体三氟异丙烯基格氏试剂(2);2分别与CO2,正丁醛,苯甲醛和苯甲酰氯反应合成了2-三氟甲基丙烯酸(3a),2-三氟甲基-1-己烯-3-醇(3b),1-苯基-2-三氟甲基-2-丙烯-1-醇(3c)和1-苯基-4-三氟甲基-4-丁烯-1-酮(3d),其中3d为新化合物,其结构经1H NMR,13C NMR,IR,MS和元素分析表征。考察了交换试剂、物料比、温度和反应时间对3a产率的影响。在最优反应条件[以i-PrMgBr/LiCl为交换试剂,150mmol,n(2-溴丙烷)∶n(1)=1.25∶1.00,于-60℃反应2h]下,3a收率64.3%。
卤素-镁交换;2-三氟甲基丙烯酸;三氟异丙烯基格氏试剂;合成
2-三氟甲基丙烯酸(3a)作为一种重要的含氟有机中间体,是合成含氟农药、含氟医药和含氟树脂等多种化工产品的原料,在医学、农业和材料科学等诸多领域均有广泛应用[1]。3a的合成方法已多有文献报道,但是仍存在原料昂贵、毒性大、反应过程复杂和产物分离困难等缺点,需进一步探索和优化。以2-溴-3,3,3-三氟丙烯(1)为原料合成3a是目前最具应用前景的路线之一[2-6]。
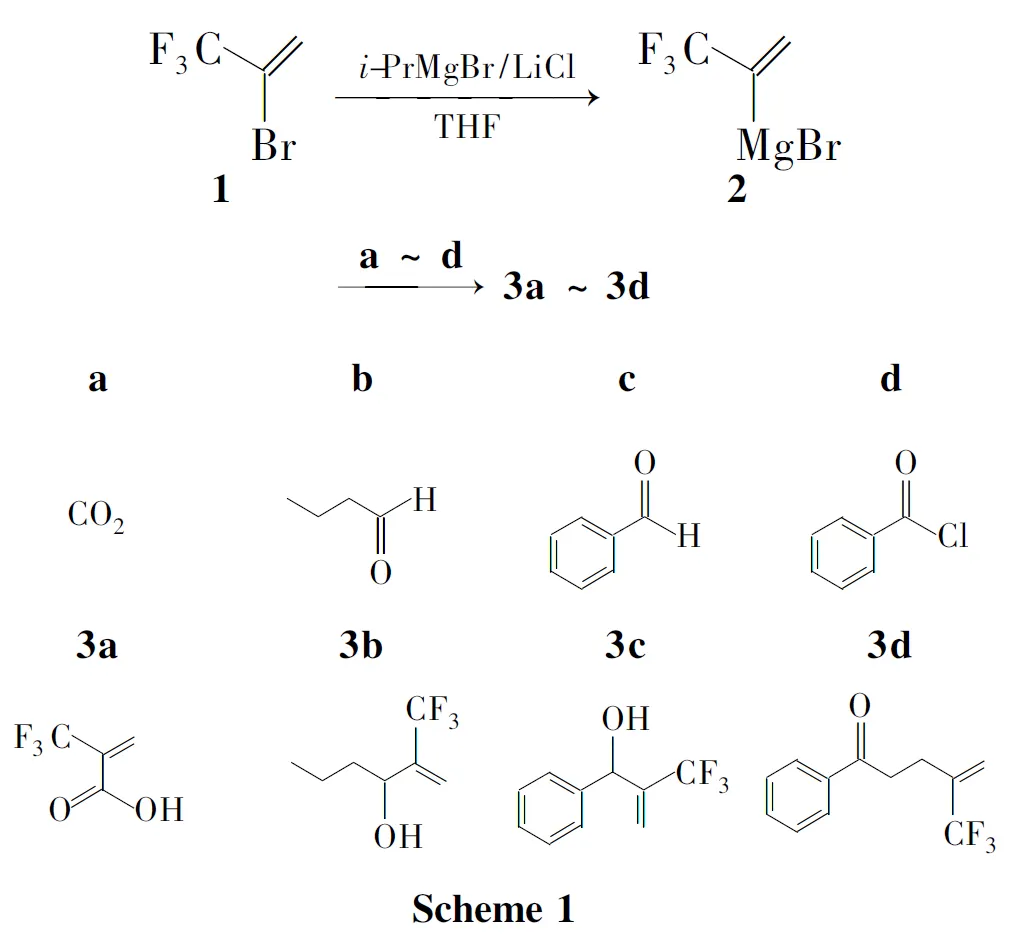
基于此,本文以1为原料,经卤素-镁交换反应制得中间体三氟异丙烯基格氏试剂(2);2与CO2反应合成了2-三氟甲基丙烯酸(3a,Scheme 1),并对反应条件进行了优化。在最佳反应条件[以i-PrMgBr/LiCl为交换试剂,150mmol,n(2-溴丙烷)∶n(1)=1.25∶ 1.00,于-60℃反应2h]下,3a收率64.3%。
本文对该反应进行延伸,将2分别与正丁醛,苯甲醛和苯甲酰氯进行反应,合成了2-三氟甲基-1-己烯-3-醇(3b),1-苯基-2-三氟甲基-2-丙烯-1-醇(3c)和1-苯基-4-三氟甲基-4-丁烯-1-酮(3d),其中3d为新化合物,其结构经1H NMR,13C NMR,IR,MS和元素分析表征。
1 实验部分
1.1 仪器与试剂
INOVA 500MHz型核磁共振仪(CDCl3为溶剂,TMS为内标);Nexus 870型傅立叶变换红外光谱仪(KBr压片);ITQ700TM型气相色谱质谱联用仪;Vario EL CHN型元素分析仪。
所用试剂均为分析纯,使用前经干燥处理。
1.2 合成
(1)3a的合成
氮气保护下,在烧瓶中加入THF 80mL,镁屑1.5g(62.5mmol)和2-溴丙烷7.7g(62.5mmol),搅拌下于室温反应2h。加入无水LiCl 2.6g(62.5mmol),于-60℃滴加18.8g(50mmol)的THF(20mL)溶液,滴毕,于-60℃反应2h得2。于-60℃通入二氧化碳,反应2h。升温至室温,用10%硫酸(25mL)酸化,乙醚萃取,合并有机相,用无水MgSO4干燥后减压蒸馏,收集84℃~86℃/10KPa馏分得白色固体3a4.5g,收率64.3%,纯度99.4%;1H NMRδ:6.60(d,J=1.1Hz,1H),6.88(m,1H),11.67(s,1H);13C NMRδ:121.0(q,J=270.6Hz),130.8(q,J=32.2Hz),135.4(q,J=5.0Hz),166.9;IRν:3418,2680,2591,2512,1718,1149,1107cm-1;GC-MSm/z:140[M+]。
(2)3b的合成
按1.2(1)反应制得2,于-60℃滴加正丁醛3.6g(50mmol)的THF(20mL)溶液,滴毕,于-60℃反应2h;升温至室温,加入饱和氯化铵溶液30mL,用乙醚萃取,合并有机相,干燥后减压蒸馏,收集74℃~76℃/10KPa馏分得淡黄色液体3b6.0g,收率71.4%,纯度98.5%;1H NMRδ:0.95(t,J=7.4Hz,3H),1.38~1.70(m,4H),2.16(s,1H),4.36(m,1H),5.72(s,1H),5.82(d,J=1.4Hz,1H);13C NMRδ:13.8,18.6,38.4,68.9,118.8(q,J=5.6Hz),123.4(q,J=272.2Hz),142.0(q,J=27.6Hz);IRν:3381,2965,2939,2878,1316,1171,1128cm-1;GC-MSm/z:167[M-1]。
(3)3c的合成
按1.2(1)反应制得2,滴加苯甲醛5.3g(50mmol)的THF(20mL)溶液,滴毕,于-60℃反应2h;升至室温,加入30mL饱和氯化铵溶液,用乙醚萃取,合并有机相,干燥后减压蒸馏,收集120℃~122℃/10KPa馏分得淡黄色液体3c7.9g,收率78.2%,纯度97.6%;1H NMRδ:2.14(s,1H),5.41(s,1H),5.79(t,J=1.2Hz,1H),5.92(s,1H),7.31~7.38(m,5H);13C NMRδ:71.3,119.8(q,J=5.4Hz),123.2(q,J=272.1Hz),127.0,127.7,128.6,140.3,140.9(q,J=28.4Hz);IRν:3364,3100,3000,1599,1580,1495,1456,1323,1025,1130,1171cm-1;GC-MSm/z:202[M+]。
(4)3d的合成
按1.2(1)反应制得2,加入CuCN 4.5g(50mmol)和无水LiCl 4.2g(100mmol),于-60℃滴加苯甲酰氯7.0g(50mmol)的THF(20mL)溶液,滴毕,于-60℃反应2h;升温至室温,依次加入饱和氯化铵溶液30mL,10%氢氧化钠溶液20mL,次氯酸钠溶液50mL,抽滤,滤液用乙醚萃取,合并有机相,旋蒸除溶后经硅胶柱层析[洗脱剂:V(石油醚)∶V(CH2Cl2)=3∶1]纯化,收集第二色带,蒸除溶剂后用石油醚(60℃~90℃)重结晶得白色针状晶体3d1.7g,收率14.9%,纯度99.2%;1H NMRδ:2.70(t,J=7.5Hz,2H),3.22(t,J=7.4Hz,2H),5.41(s,1H),5.72(s,1H),7.46~7.98(m,5H);13C NMRδ:24.0,36.5,118.7(q,J=5.8Hz),123.7(q,J=271.9Hz),128.0,128.7,133.3,136.6,137.5(q,J=29.2Hz),198.1;IRν:3100,3000,1681,1597,1580,1486,1450,1158,1109cm-1;GC-MSm/z:228[M+];Anal.calcd for C 62.86%,H 4.92%。
2 结果与讨论
2.13a的合成工艺优化
为优化3a的合成工艺,考察交换试剂(RX)、催化剂、物料比[r=n(RX)∶n(1)]、反应温度和反应时间对3a产率的影响,确定最佳反应条件。
(1)RX与催化剂
150mmol,r=1∶ 1,其余反应条件同1.2(1),考察RX和催化剂对3a收率的影响,结果见表1。
由表1可见,在无催化剂LiCl条件下,以CH3CH2CH2I,CH3CH2CH2Br和CH3CH2CH2Cl为交换试剂,3a收率接近,选用活性适中且价格低廉的溴代物为交换试剂。当RX为直链卤代烷烃时,烷基链越长,反应活性越差,3a收率越低;当RX为带支链的卤代烷烃时,随着烷基碳链增长,空间位阻增大,反应难度增加,从而致使3a收率降低;当RX为卤代芳烃时,3a收率几乎为0,其原因是卤代芳烃制成格氏试剂后,碳负离子与苯环共轭,电荷分散,电负性减弱,较难进行交换反应。可见,不同卤代物作交换试剂对3a收率有很大影响,小分子卤代物由于空间位阻小,反应活性高,易于进行交换反应,故选用i-PrMgBr为交换试剂,即RX=2-溴丙烷。
由表1还可见,加入催化剂LiCl后,当以CH3CHBrCH3为交换试剂时,3a收率从30.9%增至54.2%(No.7)。其原因在于LiCl不仅能够和格氏试剂结合形成电负性更高的结构,还能增加格氏试剂的溶解性,并且减少卤代烃自身的偶联反应,最终提高卤素-镁交换反应效率[7-10]。但对于其它交换试剂,LiCl的催化效果不明显。因此,LiCl的催化效果与交换试剂的分子结构也有着重要关系。
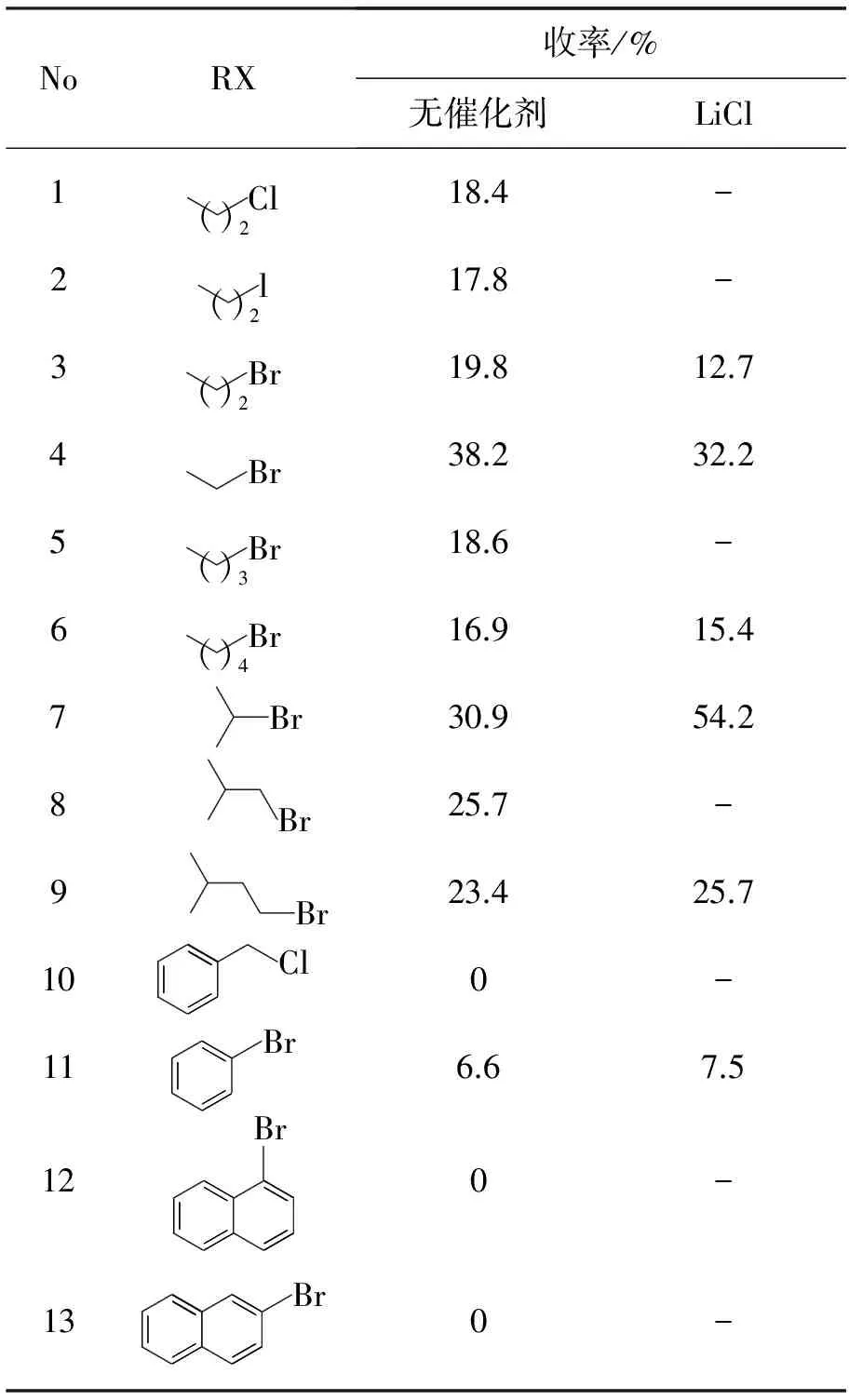
表 1 RX和催化剂对3a收率的影响*Table 1 Effects of exchange reagents and catalyst on yield of 3a
*150mmol,r=1∶ 1,其余反应条件同1.2(1)
(2)反应温度、r和反应时间
以i-PrMgBr为交换试剂,LiCl为催化剂,其余反应条件同1.2(1),考察反应温度、r和反应时间对3a收率的影响,结果见表2。由表2可见,合成3a时,主要副产物为1,1-二氟丙二烯和2,3-二甲基丁烷,前者为2热分解产生,后者为2-溴丙烷与2偶联所产生。由表2可见,反应温度从-50℃降至-80℃的过程中,3a的产率先升高后降低,-60℃时收率最高。这是因为温度升高,2热分解增加,温度过低,反应活性降低。增加2-溴丙烷用量,1转化率增大,有利于提高3a收率,但同时反应体系内2总浓度增加,热分解和偶联等副反应也增多,反应的选择性受到影响[11]。因此,最佳反应温度为-60℃。

表 2 反应温度、 r和反应时间对3a收率的影响*Table 2 Effects of temperature,r and reaction time on yield of 3a
*r=n(2-溴丙烷)∶n(1),其余反应条件同1.2(1)
从表2还可见,r=1.25时,3a收率最高(No.5)。在相同反应条件下(No.5,No.9和No.11),适当延长反应时间,可使交换反应进行更充分,有利于提高3a收率,但反应时间过长也会增大中间体的热分解。最佳反应时间为2.0h。
[1] Daiki I,Yasuko M,Kiyoteru N.Process for preparation of perfluomalkyldihydrouracil derivatives[P].JP 2001302644.
[2] Botteghi C,Lando C,Matteoli U,etal.Study on the preparation of 2-(trifluoromethyl)acrylic acid and its esters from 3,3,3-trifluoropropene via hydrocarbonylation reactions[J].Journal of Fluorine Chemistry,1997,83:67-71.
[3] Matteoli U,Botteghi C,Sbrogio F,etal.Esters andN,N-dialkylamides of 2-(trifluoromethyl)acrylic acid(TFMAA)through Pd-catalysed carbonylation of fluorinated unsaturated substrates[J].Journal of Molecular Catalysis,1999,143:287-295.
[4] Takahsshi M,Shuyams H,Miyano O.Process for producing fluorine-containing aliphatic carboxylic acids[P].US 5004567.
[5] Masaki M,Masatada S,Kazuo M,etal.Preparation of fluorine containing-α,β-unsaturated carboxylic acids from fluorohaloalkenes[P].JP 2001288138.
[6] 徐卫国,徐宇威,陈先进.α-三氟甲基丙烯酸的制备与应用[J].浙江化工,2005,36(5):32-33.
[7] Farnham W B,Calabrese J C.Novel hypervalent(10-1-2)iodine structures[J].Journal of the American Chemical Society,1986,108:2449-2451.
[8] Reich H J,Phillips N H,Reich I L.Lithium-metalloid exchange reactions.Kinetic evidence for an intermediate in the lithium-iodine exchange[J].Journal of the American Chemical Society,1985,107:4101-4103.
[9] Krasovskiy A,Knochel P.A LiCl-mediated Br/Mg exchange reaction for the preparation of functionalized aryl-and heteroarylmagnesium compounds from organic bromides[J].Angewandte Chemie International Edition,2004,43:3333-3336.
[10] Hauk D,Lang S,Murso A.Minimization of side reactions in bromine magnesium exchanges withi-PrMgCl/LiCl ands-BuMgCl/LiCl mixtures[J].Organic Process Research&Development,2006,10(4):733-738.
[11] Tang W J,Sarvestani M,Wei X D,etal.Formation of 2-trifluoromethylphenyl Grignard reagent via magnesium-halogen exchange:Process safety evaluation and concentration effect[J].Organic Process Research &Development,2009,13(6):1426-1430.
Synthesisof2-TrifluoromethylacrylicAcidViaHalogen-MagnesiumExchangeMethod
ZHAO Juan,WAN Hong,FENG Xiao-jun,XU Hong-tao,LÜ Jian
(Xi′an Modern Chemistry Research Institute,Xi′an 710065,China)
An intermediate,3,3,3-trifluoroisopropenyl Grignard reagent(2),was prepared by the bromine-magnesium exchange reaction ofi-PrMgBr with 2-bromo-3,3,3-trifluoropropene(1).2-Trifluoromethylacrylic acid(3a),2-trifluoromethyl-1-hexene-3-ol(3b),1-phenyl-2-trifluoromethyl-2-propylene-1-ol(3c)and 1-phenyl-4-trifluoromethyl-4-buten-1-one(3d)were synthesized by addition reaction of2with CO2,n-butanal,benzaldehyde and benzoyl chloride,respectively.3dwas a novel compound.The structures were characterized by1H NMR,13C NMR,IR,GC-MS and elemental analysis.Effects of exchange agent,mole ratio,temperature and reaction time on the yield of3awere investigated.The optimum reaction conditions of3aat -60℃ for 2h were as follows: exchange reagent wasi-PrMgBr/LiCl,1was 50mmol,n(2-bromopropane)∶n(1)=1.25∶1.00.The yield of3awas 64.3% under the optimum reaction conditions.
halogen-magnesium exchange reaction;2-trifluoromethylacrylic acid;3,3,3-trifluoroisopropenyl grignard reagent;synthesis
2013-08-27;
2014-09-10
陕西省工业科技攻关项目(2010K07-06)
赵娟(1988-),女,汉族,陕西西安人,助理工程师,硕士研究生,主要从事含氟有机化合物的合成研究。Tel.029-88291168,E-mail: canghaiyisu_zj@126.com
吕剑,研究员,中国兵器工业集团首席专家,博士生导师,E-mail: lj_087@126.com
O622.4;O622.5
A
1005-1511(2014)06-0820-04

