特拉匹韦关键中间体{(1S,3AR,6AS)-八氢环戊并[c]吡咯-1-羧酸}的合成*
沈德凤,高 健,魏 来
(佳木斯大学 药学院,黑龙江 佳木斯 154000)
·制药技术·
特拉匹韦关键中间体{(1S,3AR,6AS)-八氢环戊并[c]吡咯-1-羧酸}的合成*
沈德凤,高 健,魏 来
(佳木斯大学 药学院,黑龙江 佳木斯 154000)
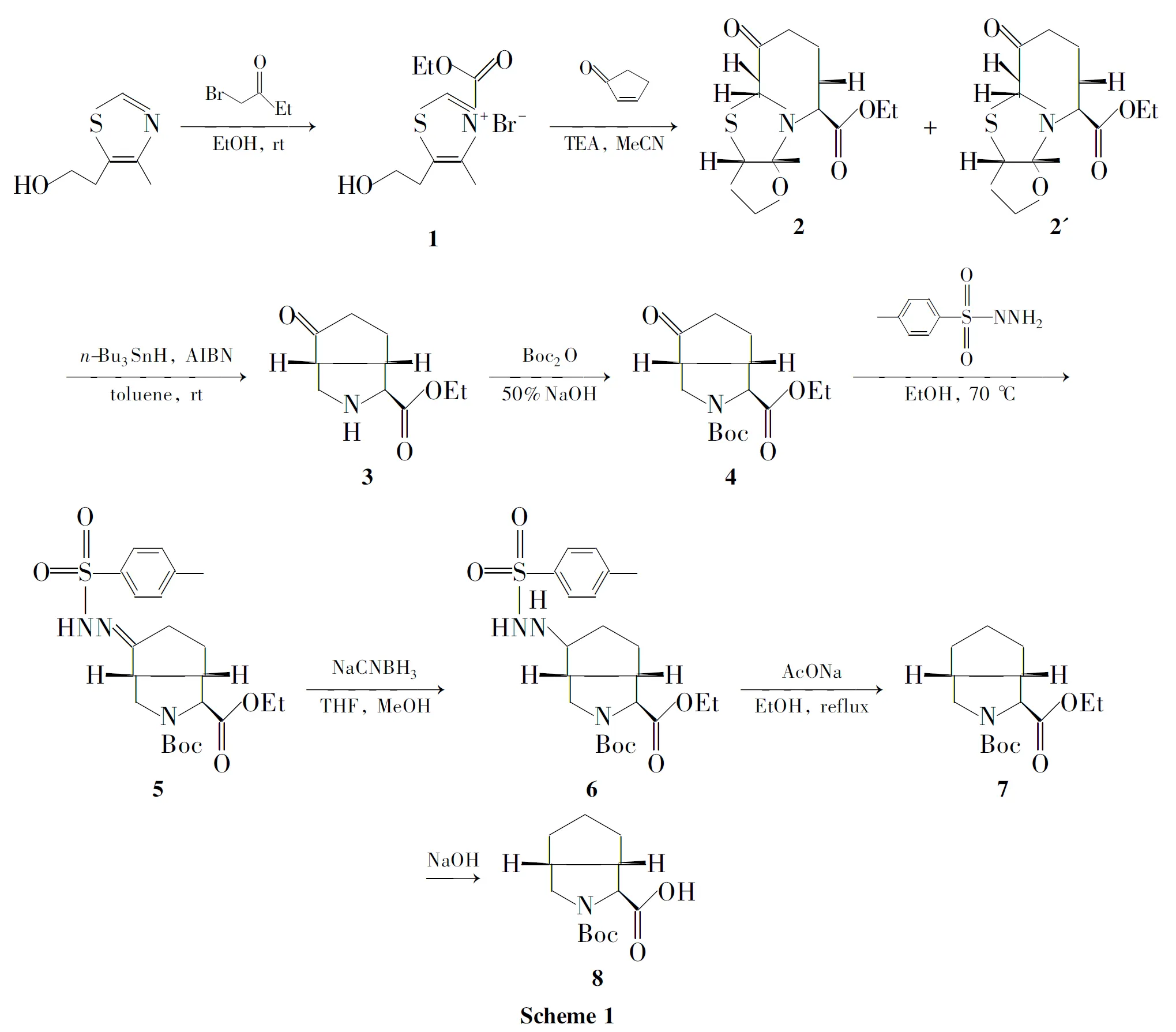
设计了一条合成特拉匹韦重要中间体(1S,3AR,6AS)-八氢环戊并[c]吡咯-1-羧酸(8)的新路线。以4-甲基-5-咪唑基乙醇为原料,经N-烃化、串联加成环化、羰基还原、氨基保护和酯水解等8步反应合成8,总收率24.7%,其结构经1H NMR和MS确证。
特拉匹韦;中间体;药物合成
特拉匹韦是一种可逆性蛋白酶抑制剂,与聚乙二醇α-干扰素和利巴韦林联用,可有效抑制HVC病毒复制,用于慢性丙型肝炎的治疗[1-3]。
(1S,3AR,6AS)-八氢环戊并[c]吡咯-1-羧酸(8)是合成特拉匹韦的关键中间体。文献方法均以(3AR,6AS)-3A,6A-二甲基八氢环戊基[c]吡咯为原料进行合成。Gerald J T等[4]的合成路线相对较短,但在通CO2引入羧基的步骤中,需要保持超低温(-78℃)和使用价格昂贵且危险性较高的仲丁基锂,引入羧基后还需手性拆分,收率较低。Köhler V Z A等[5-6]采用生物法合成8,其操作复杂,条件苛刻且不宜控制。
本文设计了一条合成8的新路线。以4-甲基-5咪唑基乙醇为原料,经N-烃化、串联加成环化、羰基还原、氨基保护和酯水解等8步反应合成8(Scheme 1),总收率24.7%,其结构经1H NMR和MS确证。该方法具有路线条件温和,操作简单,收率较高等优点。
1 实验部分
1.1 仪器与试剂
ZF-7型三用紫外分析仪;Bruker-300MHz型核磁共振波谱仪(CDCl3为溶剂,TMS为内标);Agilent LC/MSD型高效液相质谱联用仪。
所用试剂均为分析纯。
1.2 合成
(1)3-(2-乙氧基-2-氧代乙基)-5-(2-羟乙基)-4-甲基噻唑-3-溴化物(1)的合成
在单口瓶中加入4-甲基-5-咪唑基乙醇19.4g(0.14mol),溴乙酸乙酯22.6g(0.14mol)和乙醇 500mL,搅拌使其溶解;回流反应4h(LC-MS监测)。减压蒸除乙醇,用混合溶液[V(MeOH)∶V(Et2O)=1.0∶1.8] 590mL重结晶得淡黄色固体140g,收率95%;MSm/z: 310{[M+H]+} 。
(2)(3AS,4AR,4BS,7AS,8S,9AR)-乙基9α-甲基-乙基-5-氧代十氢-2H-环戊二烯并[3,4]吡咯并[2,1-b]呋喃并[2,3-d]噻唑-8-羧酸乙酯(2)和(3AR,4AR,4BS,7AS,8S,9AS)-乙基9α-甲基-5-氧代十氢-2H-环戊二烯并[3,4]吡咯并[2,1-b]呋喃并[2,3-d]噻唑-8-羧酸乙酯(2′)的合成N2保护下,在冰浴冷却的三口瓶中加入140g(0.13mol),2-环戊烯酮50g(0.61mol)和乙腈200mL,搅拌使其溶解;于5min内缓慢滴加TEA 15g(0.15mol),滴毕,反应30min,于室温反应20h至终点(LC-MS监测)。加入AcOEt 200mL,依次用水(3×100mL)和饱和NaCl溶液(200mL)洗涤,用无水Na2SO4干燥,浓缩后经硅胶柱层析[洗脱剂:A=V(乙酸乙酯)∶V(石油醚)=1∶1]纯化得混合物(2+2′)31.5g,产率78%;MSm/z: 312{[M+H]+}。
(3)(1S,3AR,6AS)-乙基-4-氧代八氢环戊并[c]吡咯-1-甲酸叔丁酯(3)和(1S,3AR,6AS)-2-叔丁基-1-乙基-4-氧代六氢环戊二烯并[c]吡咯-1,2(1H)-二羧酸二乙酯(4)的合成
N2保护下,在三口瓶中加入混合物(2+2′)31.5g(0.1mol),Bu3SnH 30mL(148mmol),偶氮二异丁腈(AIBN)2.46g(15mmol)和甲苯120mL,搅拌使其溶解;回流反应14h(LC-MS监测)。减压浓缩,加入Et2O 100mL和2mol·L-1盐酸100mL,剧烈搅拌2h,静止分层,分离水相,用Et2O(2×100mL)洗涤,冷却至<5℃,缓慢加入2mol·L-1NaOH溶液至pH 7,搅拌下加入K2CO315.3g,反应15min;滴加Boc2O 24g(0.11mol)的THF(100mL)溶液,15min滴毕,于室温反应4h(LC-MS监测)。用EtOAc(3×300mL)萃取,合并有机层,依次用1mol·L-1盐酸,饱和Na2CO3溶液,饱和NaCl溶液洗涤,无水Na2SO4干燥,浓缩后经硅胶柱层析(洗脱剂:A=3∶1)纯化得淡黄色液体419.3g,产率65%;MSm/z: 298{[M+H]+}。
(4)(1S,3R,6S)-2-叔丁基-1-乙基-4-(2-对甲苯磺酰基肼基)六氢环戊二烯并[c]吡咯-1,2(1H)-二羧酸二乙酯(5)的合成
在单口瓶中加入419.3g(65mmol),对甲苯磺酰肼13.39g(72mmol)和乙醇200mL,搅拌使其溶解;于70℃反应3h(LC-MS监测)。减压蒸除乙醇,残余物用Et2O 400mL溶解,饱和NaCl溶液200mL洗涤,无水Na2SO4干燥,浓缩得棕黄色液体525.8g,收率85%;MSm/z: 466{[M+H]+}。
(5)(1S,3AR,6AS)-2-叔丁基-1-乙基-4-(2-甲苯磺酰基肼基)六氢环戊二烯并[c]吡咯-1,2(1H)-二羧酸二乙酯(6)的合成
冰浴冷却,在反应瓶中加入525.8g(55mmol)和混合溶液[V(THF)∶V(MeOH)=1∶1]200mL,分批加入氰基硼氢化钠5.2g(83mmol),加毕,反应至终点(LC-MS监测)。用饱和氯化铵溶液调至pH 7,减压浓缩,分液,水相用DCM(3×300mL)萃取,合并有机相,依次用1mol·L-1盐酸100mL,饱和Na2CO3溶液100mL和饱和NaCl溶液100mL洗涤,用无水Na2SO4干燥,浓缩得淡黄色液体624.4g,产率90%;1H NMRδ:1.1(t,3H),1.3(d,9H),1.3~1.97(m,5H),2.6(m,2H),3.14~3.25(m,2H),3.9(s,1H),4.15(q,2H);MSm/z: 468{[M+H]+}
(6)(1S,3AR,6AS)-2-叔丁基-1-乙基六氢环戊二烯并[c]吡咯-1,2(1H)-二羧酸二乙酯(7)的合成
在三口瓶中加入624.4g(52mmol),乙酸钠17.1g(208mmol)和乙醇50mL,搅拌下回流反应5h(LC-MS监测)。加水100mL,减压蒸除乙醇。分液,水相用DCM 300mL萃取,合并有机相,用饱和NaCl溶液100mL洗涤,无水Na2SO4干燥,浓缩后经硅胶柱层析[洗脱剂:A=1∶1]纯化得透明液体710.3g,产率70%;1H NMRδ:1.4(s,9H),1.56~1.97(m,5H),2.7(m,2H),3.24~3.66(m,2H),4.00(m,1H),8.24(s,1H)。
(7)8的合成
冰浴冷却,在反应瓶中加入710.3g(36mmol)和THF 400mL,搅拌使其溶解;加入1mol·L-1NaOH溶液50mL,于室温搅拌反应1h(LC-MS监测)。用1mol·L-1盐酸调至pH 3~4,用AcOEt(3×100mL)萃取,合并有机相,用饱和NaCl溶液50mL洗涤,无水Na2SO4干燥,浓缩得透明液体88.8g,收率96%;1H NMRδ:1.4(s,9H),1.56~1.97(m,5H),2.7(m,2H),3.24~3.66(m,2H),4.00(m,1H),8.24(s,1H);MSm/z: 256{[M+H]+}。
2 结果与讨论
以较廉价的4-甲基-5咪唑基乙醇和溴代乙酸乙酯代替文献方法中价格较昂贵的(3AR,6AS)-八氢[c]吡咯为原料,降低了成本。
合成2时,经柱层析纯化得到的异构体2和2′,无需分离,直接在三丁基氢化锡和AIBN的作用下即可得到关键中间体3。此步骤操作简单,反应条件温和,不涉及超低温条件和有机锂试剂的使用,且不需要手性拆分。3只需简单后处理即可直接进行氨基保护反应制备4,两步收率达65%。
合成6时,5只需简单处理后即可直接进行还原,两步收率达85%以上。
用对甲苯磺酰肼法将羰基转化为亚甲基,在特拉匹韦的中间体合成中为首次使用。
[1] 刘兴. 特拉匹韦[J].中国药物化学杂志,2011,21(5):412-413.
[2] Smith L S,Nelson M,Naik S,etal.Telaprevir:An NS3/4A protease inhibitor for the treatment of chronic hepatitis C[J].Ann Pharmacother,2011,45(5):639-648.[3] Modi A A,LIANG T J.Hepatitis C:A clinical review[J].Oral Dis,2008,14(1):10-14.
[4] Gerald J,Tanoury,Hudson,etal.Cochran,Marshfield,MA[P].US 0087973,2007.
[5] Köhler V,Bailey K R,Znabet A,etal.Enantioselective biocatalytic oxidative desymmetrizat-ion of substituted pyrrolidine[J].Angew Chem Int,2010,49(12):2182-2184.
[6] Znabet A.A highly effcient synthesis of telaprevir by strate-gic use of biocatalysis and multicomponent reactions[J].Chem Commun,2010,46(42):7918-7920.
SynthesisofKeyIntermediate{(1S,3AR,6AS)-octahydr-ocyclopenta[c]pyrrole-1-carboxylicacid}forTelaprevir
SHEN De-feng,GAO Jian,WEI Lai
(School of Pharmacy,Jamusi University,Jiamusi 154000,China)
A new route of synthesizing key intermediate(1S,3AR,6AS)-octahydr-ocyclopenta[c]pyrrole-1-carboxylic acid(8)with total yield of 24.76% for Telaprevir was designed.8was synthesized by a eight-step reaction ofN-alkylation,cyclization,carbonyl reduced,amino-protection,ester hydrolysis,etc from 4-methyl-5-imidazole-ethanol.The structure was confirmed by1H NMR and MS.
Telaprevir;intermediate;drug synthesis
2013-09-03;
2014-09-05
沈德凤(1960-),女,汉族,黑龙江兰西人,教授,主要从事新药的开发研究。E-mail: shenjms@163.com
O626.2;R914.5
A
1005-1511(2014)06-0837-03

