1,25-二羟维生素D3调节NF-κB通路对减轻海水吸入型急性肺损伤的作用
张敏龙 王 莉 金发光
1,25-二羟维生素D3调节NF-κB通路对减轻海水吸入型急性肺损伤的作用
张敏龙 王 莉 金发光
目的探讨海水吸入型肺损伤大鼠肺组织中核因子-κB(NF-κB)通路的变化以及1,25-二羟维生素D3对其干预作用。 方法32只大鼠完全随机分为空白对照组、海水处理组、VitD3预处理组和地塞米松处理组,每组8只。采用气管内滴注海水(3 ml/kg)的方法制作海水吸入型急性肺损伤大鼠模型,观察肺部病理变化,用ELISA法检测肺组织中肿瘤坏死因子-α(TNF-α)和白介素-1β(IL-1β)的含量,Western blot检测磷酸化NF-κB的表达变化,免疫荧光观察A549细胞NF-κB核转移情况。 结果海水吸入4 h后,大鼠肺部损伤明显,TNF-α和IL-1β的含量增高,NF-κB磷酸化以及核转移增多;1,25-二羟维生素D3预处理显著减轻了海水吸入导致的急性肺损伤,减少了炎症因子的释放,并且抑制了NF-κB磷酸化以及核转移。 结论NF-κB通路参与了海水吸入型肺损伤的发生发展,1,25-二羟维生素D3能够通过抑制NF-κB信号通路减轻肺损伤。
急性肺损伤; 海水; 1,25-二羟维生素D3; 核因子-κB
淹溺是引起死亡最常见的原因之一。据估计,全世界每年因淹溺导致的死亡接近150万人,而海水淹溺占据了其中的一大部分[1]。尽管经过了几十年的研究,海水淹溺的病死率仍居高不下。海水吸入可以引起急性肺损伤(acute lung injury, ALI),甚至发展为急性呼吸窘迫综合征(acute respiratory distress syndrome, ARDS)。许多海水吸入急性肺损伤动物模型表明,炎症细胞大量渗入到肺泡腔以及肺间质导致了肺组织严重的炎症反应,同时这些炎症细胞分泌大量的炎症因子和活性氧基团,进一步加重了肺损伤。
核因子-κB(nuclear factor-kappa B, NF-κB)通路是被广泛认可的参与炎症反应的细胞内信号通路。NF-κB分子在几乎所有的细胞中都有表达,并且可以调节许多与免疫和急性炎症反应相关的基因[2-3]。许多因素如炎症因子的刺激都可以激活NF-κB通路。NF-κB通路的激活首先通过IκB激酶(IKK)使IκBs(inhibitors of κB)磷酸化,然后下游的NF-κB磷酸化并转移至细胞核,最终引起一系列炎症因子的转录[4-5]。
1,25-二羟维生素D3[1,25-(OH)2VitD3]是维生素D3的生物活性代谢产物,除了调节钙和磷的代谢外,还具有其他的生物活性。最近的研究发现1,25-二羟维生素D3与炎症反应相关。在脂多糖诱导的急性肺损伤中,1,25-二羟维生素D3抑制了中性粒细胞的浸润并且减少了炎症因子的产生[6]。本研究通过复制大鼠海水吸入型急性肺损伤(seawater aspiration-induced, ALI)模型,观察1,25-二羟维生素D3的治疗作用,并进一步探讨NF-κB信号通路参与其中的相关机制。地塞米松能够用于ALI/ARDS的临床治疗,并且已经证实对海水吸入型急性肺损伤具有良好的治疗效果[7]。因此,我们选择地塞米松作为阳性治疗对照。
材料与方法
一、 实验试剂
1,25-二羟维生素D3以及地塞米松购自Sigma公司,高效液相(high performance liquid Chromatography, HPLC)检测纯度达到99%以上,1,25-二羟维生素D3用10%甲醇-1‰Triton X-100溶液制成的混悬液灌胃给药,地塞米松用5‰羧甲基纤维素钠(sodium carboxymethylcellulose)溶液制成混悬液灌胃给药。配方海水按照中国国家海洋局第三海洋研究所海洋生化研究室提供的我国东南沿海海水的主要成分配制:NaCl 26.518 g/L,MgSO43.305 g/L,MgCl22.447 g/L,CaCl21.141 g/L,NaHCO30.202 g/L,KCl 0.725 g/L,NaBr0.083 g/L;pH 8.2,相对密度1.05,渗透压1300 mmol/L。TNF-α和IL-1β ELISA试剂盒购于R&D公司。NF-κB p65和磷酸化NF-κB(pNF-κB) p65 抗体购于Cell Signaling公司,β-actin抗体购于Santa Cruz公司。其他试剂均为国产或进口分析纯。
二、实验动物及分组
健康雄性SD大鼠,清洁级,体重220 g左右,第四军医大学实验动物中心提供。采用完全随机方法将实验大鼠分为四组:A:空白对照组,B:海水淹溺组,C:VitD3预处理组,D:地塞米松预处理组,每组8只。造模前1 h给药,各组大鼠分别灌胃:A和B组:生理盐水;C组:25 μg/kgVitD3;D组:10 mg/kg地塞米松。B、C、D组大鼠制作海水吸入型急性肺损伤模型,造模4 h后放血处死动物收集肺组织标本。动物模型的制备:大鼠腹腔注射3%戊巴比妥钠(1.5 ml/kg)麻醉,仰卧固定,颈正中切口暴露气管,取1 ml的注射器插入气管,在4 min之内缓慢注入3 ml/kg海水。
三、细胞培养及处理
A549细胞用含有100 U/ml青链霉素和10%胎牛血清的RPMI 1640培养液在5% CO2培养箱中37 ℃进行培养。海水刺激前1 h,分别用10-6MVitD3和10-6M地塞米松进行预处理,之后用25%海水(1 ml培养液中含0.25 ml海水)刺激细胞4 h。
四、检测指标及方法
1. 肺组织病理学检查:取各组大鼠左下肺组织迅速放入4%多聚甲醛液中固定24 h,脱水,石蜡包埋,切片,苏木精—伊红染色(hematoxylin-eosin staining, HE),光学显微镜观察。
2. 肺组织湿干比(W/D)测定:取每只大鼠相同部位肺组织,擦拭血迹后立即称量得肺组织湿重,将肺组织标本置于70 ℃烘干箱中72 h至恒重,称量干重,计算湿干比。
3. TNF-α和IL-1β检测:用ELISA的方法检测肺组织匀浆中的TNF-α和IL-1β的含量,具体步骤严格按照试剂盒说明书操作。
4.Western-blot检测NF-κB p65和pNF-κB p65蛋白表达:取适量的肺组织,加入蛋白裂解液冰上匀浆,离心收集上清,定量,沸水煮15 min,电泳,然后转膜。将已做好标记的膜放入封闭液中,室温振荡2 h封闭;加入1︰1000稀释的一抗,4 ℃过夜,加入1︰5000稀释羊抗兔二抗,37℃温育1 h,增强化学发光法 (enhanced chemiluminescence, ECL)显色,避光保存并照相,做灰度扫描处理。
5. 免疫荧光观察A549细胞中NF-κB核转位:进行细胞爬片,并对细胞进行处理,处理后的细胞用4%多聚甲醛液固定10 min,0.1% TritonX-100穿透处理10 min,然后山羊血清封闭30 min,加入1︰100稀释的NF-κB p65抗体4 ℃过夜,之后加入1︰200稀释的异硫氰酸荧光素(fluorescein isothiocyanate, FITC)标记的二抗,最后DAPI染核,封片,荧光显微镜观察并照相。
五、统计学方法
结 果
一、 病理学检测结果
空白对照组大鼠肺泡结构清晰,未见明显的病理结构变化;海水处理组大鼠肺组织结构紊乱,局部肺不张,肺间质可见出血、水肿,并可见大量炎症细胞浸润;VitD3和地塞米松预处理组大鼠肺组织结构尚清晰,间质水肿、出血和炎细胞浸润等改变较海水处理组大鼠明显减轻,见图1。
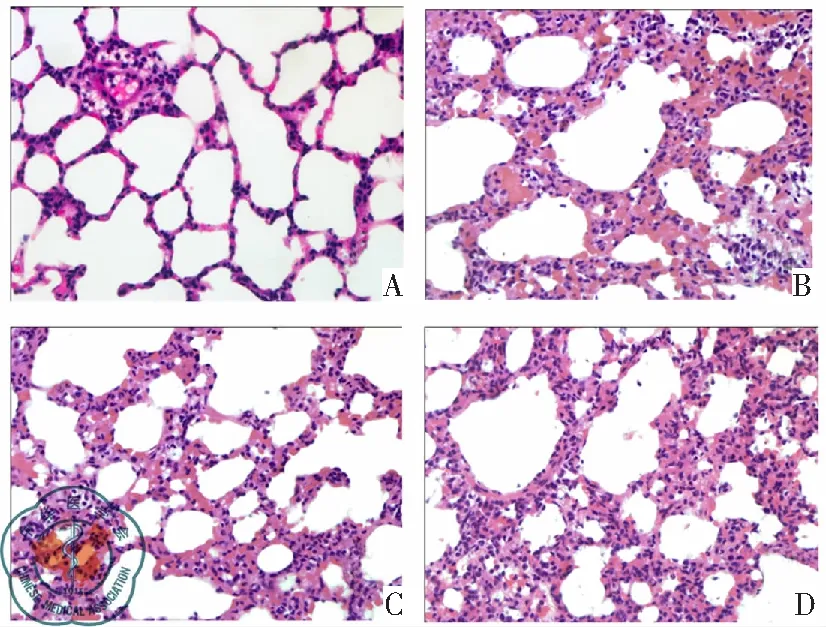
注:A:空白对照组;B:海水4 h组;B;BC:VitD3预处理组;D:地塞米松预处理组
二、肺组织湿干比(W/D)结果
吸入海水4 h后,肺组织湿干比明显增加(P<0.001),VitD3和地塞米松预处理组能够明显降低肺组织含水量,减小湿干比(P<0.05),但VitD3预处理组效果好于地塞米松预处理组,见图2。
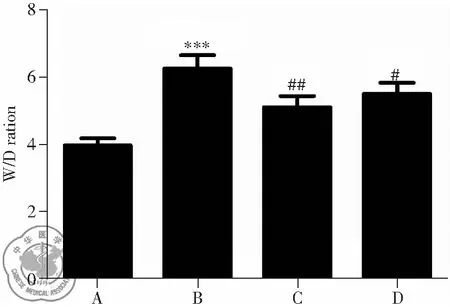
注:A:空白对照组;B:海水4 h组;C:VitD3预处理组;D:地塞米松预处理组;***P<0.001 vs. 空白对照组;##P<0.01,#P<0.05 vs. 海水4 h组
三、ELISA检测结果
与空白对照组相比,海水处理组大鼠肺组织中TNF-α和IL-1β明显升高(P<0.001),VitD3和地塞米松预处理组能够明显降低炎症因子含量(P<0.01),但VitD3预处理组效果好于地塞米松预处理组,见图3。
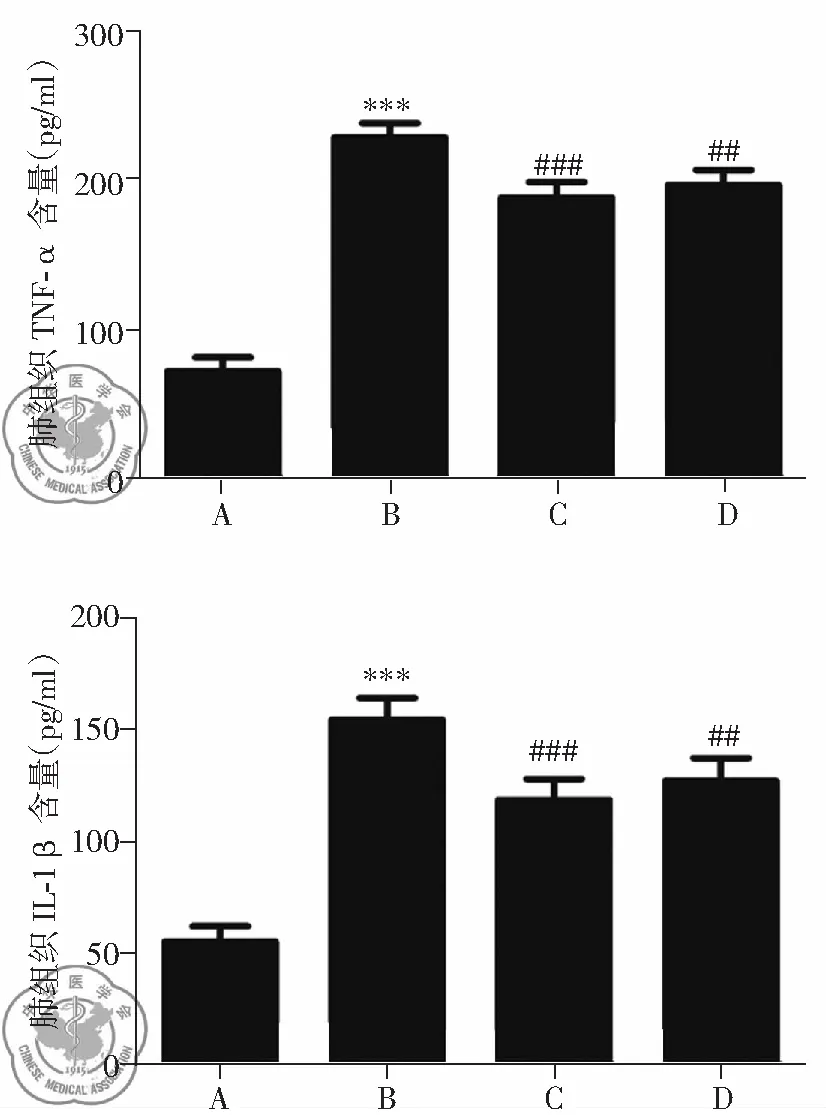
注:A:空白对照组;B:海水4 h组;C:VitD3预处理组;;BD:地塞米松预处理组;***P<0.001 vs. 空白对照组;###P<0.001,##P<0.01 vs. 海水4 h组
四、Western blot检测结果
与空白对照组相比,海水处理组大鼠肺组织中pNF-κB表达显著增加(P<0.001),VitD3和地塞米松预处理组能够明显抑制NF-κB的磷酸化(P<0.05),但VitD3预处理组效果好于地塞米松预处理组,见图4。
五、免疫荧光结果
与空白对照组对比,海水处理A549细胞中NF-κB明显出现核转移,而VitD3和地塞米松预处理组能够抑制NF-κB的核转移,见图5。
讨 论
海水吸入型肺损伤最主要的病理生理变化是炎症反应和肺水肿。由于海水的高渗特性,当其吸入肺泡时会迅速引起肺水肿。肺组织屏障损伤导致炎症细胞大量渗出,多种炎症因子释放,也表明了肺部的急性炎症反应是海水吸入肺损伤的主要发病机制。在本研究中,我们观察到海水吸入4 h后,大鼠肺泡中伴有出血以及大量炎细胞浸润,肺组织伴有明显的水肿,炎症因子的表达也增高。通过1,25-二羟维生素D3的预处理,肺水肿和炎症反应得到了一定程度的减轻。
尽管有很多药物用于治疗ALI和ARDS,但这些治疗并没有明显的降低病死率[8]。1,25-二羟维生素D3是维生素D3的活性代谢产物,最终通过结合维生素D受体进一步调控下游基因[9]。大量研究表明,在许多细胞模型如人类血细胞、树突状细胞、人角质成纤维细胞以及鼻息肉成纤维细胞中,1,25-二羟维生素D3起到了抑制炎症反应的作用[10-13]。另外,1,25-二羟维生素D3在脂多糖诱导的肺损伤中具有抑制炎症细胞渗出的作用。
NF-κB信号通路与炎症反应有密切的联系,在海水吸入型肺损伤中该通路的激活也起到了重要的作用[14-15]。海水刺激后,大量被释放的细胞因子会导致IκBs的降解,与此同时,NF-κB磷酸化并转移至细胞核,从而与目标基因结合并调控这些基因的表达[16]。该过程会引起NF-κB依赖的炎症因子的表达和释放,这些炎症因子最终又会促进肺组织屏障通透性的增加和炎细胞的浸润,从而加重组织的损伤。在我们的试验中,海水吸入导致大鼠肺组织中磷酸化NF-κB表达增加,同时免疫荧光表明,海水刺激后NF-κB核转位增加。而1,25-二羟维生素D3的预处理可抑制肺组织中磷酸化NF-κB表达的增加,同时也可抑制NF-κB的核转位。
本实验结果证明了NF-κB信号通路在海水吸入型肺损伤中发挥了重要的作用。海水吸入刺激诱导了NF-κB的磷酸化和核转位,而1,25-二羟维生素D3的预处理可减轻肺水肿和肺部炎症反应,并且抑制了NF-κB的磷酸化和核转位。这些结果部分的解释了1,25-二羟维生素D3在海水吸入型肺损伤中的作用机制,并且为1,25-二羟维生素D3的临床应用提供了实验依据。
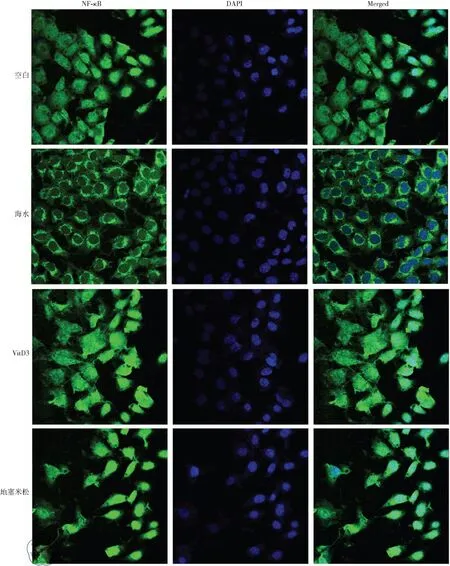
图5 各组细胞免疫荧光检测结果
1 van Beeck EF, Branche CM, Szpilman D, et al. A new definition of drowning: towards documentation and prevention of a global public health problem[J]. Bull World Health Organ, 2005, 83(11): 853-856.
2 Baldwin AS Jr. Series introduction: the transcription factor NF-kappaB and human disease [J]. J Clin Invest, 2001, 107(1): 3-6.
3 Li Q, Verma IM. NF-kappaB regulation in the immune system [J]. Nat Rev Immunol, 2002, 2(10): 725-734.
4 Karin M, Delhase M. The I kappa B kinase (IKK) and NF-kappa B: key elements of proinflammatorysignalling[J]. Semin Immunol, 2000, 12(1): 85-98.
5 Zheng C, Yin Q, Wu H. Structural studies of NF-kappaB signaling [J]. Cell Res, 2011, 21(1):183-195.
6 Takano Y, Mitsuhashi H, Ueno K. 1α,25-Dihydroxyvitamin D(3) inhibits neutrophil recruitment in hamster model of acute lung injury[J]. Steroids, 2011, 76(12):1305-1309.
7 金发光, 郭佑民. 地塞米松调节claudin-4减轻海水淹溺性肺水肿的机制研究[J/CD]. 中华肺部疾病杂志:电子版,2013, 6(2):124-129.
8 Sprung CL, Annane D, Keh D, et al. Hydrocortisone therapy for patients with septic shock [J]. N Engl J Med, 2008, 358(2): 111-124.
9 Lips P. Vitamin D physiology [J]. Prog Biophys Mol Biol,2006,92(1): 4-8.
10 Takahashi K, Horiuchi H, Ohta T, et al. 1 alpha, 25-dihydroxyvitamin D3 suppresses interleukin-1beta-induced interleukin-8 production in human whole blood: an involvement of erythrocytes in the inhibition[J]. Immunopharmacol Immunotoxicol, 2002, 24(1): 1-15.
11 Dong X, Craig T, Xing N, et al. Direct transcriptional regulation of RelB by 1alpha, 25-dihydroxyvitamin D3and its analogs: physiologic and therapeutic implications for dendritic cell function [J]. J Biol Chem, 2003, 278(49): 49378-49385.
12 Fukuoka M, Ogino Y, Sato H, et al. Regulation of RANTES and IL-8 production in normal human dermal fibroblasts by active vitamin D3(tacalcitol)[J]. Br J Pharmacol, 1998, 124(7): 1433-1438.
13 Rostkowska-Nadolska B, Sliupkas-Dyrda E, Potyka J, et al. Vitamin D derivatives: calcitriol and tacalcitol inhibits interleukin-6 and interleukin-8 expression in human nasal polyp fibroblast cultures [J]. Adv Med Sci, 2010, 55(1): 86-92.
14 Ma L, Zhao Y, Li B, et al. 3,5,4′-Tri-O-acetylresveratrol attenuates seawater aspiration-induced lung injury by inhibiting activation of nuclear factor-kappa B and hypoxia-inducible factor-1alpha[J]. RespirPhysiol Neurobiol, 2013, 185(3): 608-614.
15 马李杰, 李王平, 金发光. 急性肺损伤/急性呼吸窘迫综合征发病机制的研究进展[J/CD]. 中华肺部疾病杂志:电子版,2013,6(1):65-68.
16 Hayden MS, Ghosh S. NF-κB in immunobiology [J]. Cell Res, 2011, 21(2): 223-244.
(本文编辑:王亚南)
张敏龙,王 莉,金发光. 1,25-二羟维生素D3调节NF-κB通路对减轻海水吸入型急性肺损伤的作用[J/CD]. 中华肺部疾病杂志: 电子版, 2014, 7(5): 512-517.
1,25-(OH)2VitD3alleviates seawater aspiration-induced acute lung injury by regulating NF-κB pathway
ZhangMinlong,WangLi,JinFaguang
(DepartmentofRespiratoryDisease,TangduHospital,FourthMilitaryMedicalUniversity,Xi′an710032,China)
JinFaguang,Email:jinfag@fmmu.edu.cn
Objective To observe the change of NF-κB pathway in seawater aspiration-induced acute lung injury and the intervention effect of 1,25-(OH)2VitD3. Methods A total of 32 rats were randomly divided into 4 groups: normal control group, seawater group, VitD3pre-treated group and dexamethasone pre-treated group. Every group contains 8 rats. Seawater aspiration-induced acute lung injury model was made by seawater instillation (3 ml/kg) into the airway. Pathology detection was carried out after modeling. The contents of tumor necrosis factor-α(TNF-α) and interleukin-1β(IL-1β) were measured by ELISA and the expression of phospho-NF-κB was measured by western blot. Immunofluorescence was used to detect the nuclear translocation of NF-κB in A549 cells. Results After 4 h seawater stimulation, lung injury was obvious and the contents of TNF-α and IL-1β were increased. The expression of phospho-NF-κB was up-regulated and nuclear translocation was enhanced. However, pre-treatment of 1,25-(OH)2VitD3attenuated lung injury, suppressed the release of pro-inflammation cytokines, and inhibited the expression of phospho-NF-κB and the nuclear translocation. Conclusion NF-κB pathway plays an important part in the seawater aspiration-induced acute lung injury and 1,25-(OH)2VitD3attenuated lung injury by inhibiting NF-κB pathway.
Acute lung injury; Seawater; 1,25-(OH)2VitD3; Nuclear factor-kappa B
10.3877/cma.j.issn.1674-6902.2014.05.009
国家自然科学基金面上项目(81270124)
710032 西安,第四军医大学唐都医院呼吸内科
金发光,Email: jinfag@fmmu.edu.cn
R563
A
2014-05-05)

