不同比例Zr、Al、Ti复合氧化物的制备及其对EDTA-Cr的吸附性能研究
马宏瑞, 马 秀, 郭颖燕, 唐志刚
(陕西科技大学 资源与环境学院, 陕西 西安 710021)
0 引言
国内外的鞣革方法很多,铬鞣革优良的产品性能,如柔软性、耐光性,特别是收缩温度能达到120 ℃以上,是其它任何一种鞣剂所不能达到的.也正因为如此,铬鞣法得到了广泛应用,成为轻革鞣制的主要方法[1].
到目前为止,在生产中单纯使用一种鞣剂鞣制得到的成革性能很难达到消费者的要求,常常使用两种或两种以上鞣剂同时或先后鞣制皮革[2].其中包括单一或多金属 (锆、铝、钛)鞣剂的开发.
目前因锆、铝、钛这类金属尚不属于一类优先控制污染物,故这类金属废水没能单独分流,而是与综合污水一同处理后排入环境.常规的加碱可使这类鞣制废水中组份形成金属氢氧化物从废水中沉淀,这类氢氧化物沉淀能否有效利用是一个值得探讨的问题.
现有处理含铬废水方法主要有吸附法、化学法、生物法、离子交换法、电解法、膜分离法、超临界处理法和离子浮选法等[3-6].鞣制废水呈酸性[7],因此加碱沉淀法是目前鞣制废水中最常用且高效的处理技术,多金属复合鞣制废水中配合物离子多以阳离子型存在,但其价态差异较大,同时还存在Cr(VI)阴离子,同时,Cr2O3、Al2O3、TiO2等又属于两性金属氧化物,在强酸性和强碱性条件下易溶解,尤其当离子大多以配合物或阴离子型存在时,其去除效率较低[8].因此,在确保加碱沉淀大幅度去除废水中高浓度金属的基础上,叠加低浓度脱除技术是完善现有鞣制废水处理体系的基本思路.
Zr、Al、Ti三种金属的氧化物、氢氧化物都具有两性,且都具有一定的吸附特性.设想利用Zr(VI)、Al(Ⅲ)、Ti(Ⅲ)复合鞣制废水沉淀物,去除铬鞣废水中的铬,从而达到“以废治废,循环可控”的目的.目前在利用锆、钛、铝的氧化物去除水体中的重金属已有广泛研究和报道[9-12],这些研究都表明,这类无机氧化物对重金属离子的去除是无选择性的,对于阴、阳离子和金属配合物离子都具有良好的去除效果.
因此,本研究拟通过Zr、Al、Ti三者共同复合(Zr∶Al∶Ti比例分别为2∶2∶1、3∶1∶1、1∶3∶1)制成的沉淀一方面直接利用另一方面在750 ℃下烧结3 h作为吸附剂,进一步深度去除Cr(III)、Cr(VI)等阴阳离子并存、多核、异核配聚体混杂、富含金属有机配合物,且含盐量较高的预沉后鞣制废水.
1 材料和方法
1.1 实验药品

表1 实验药品
1.2 实验方法
1.2.1 多金属复合氧化物吸附剂的制备及表征
采用共沉淀法制备Zr-Al-Ti(2∶2∶1、3∶1∶1、1∶3∶1)且其中最大组分浓度为1 000 mg/L配置所需溶液,使用2 mol/L NaOH快速调节溶液pH至中性7~8之间,并继续快速搅拌1 h.陈化12 h.真空抽滤,并且用去离子水洗涤沉淀,在40 ℃下干燥72 h.研磨至粉体备用.
将上述制备的固体粉末进行热重和热差分析,并将这些粉末置于750 ℃马弗炉中烧结3 h,冷却后采用X射线衍射和比表面积及孔隙度分析,研究烧结后的各复合氧化物的结构特征.
1.2.2 不同吸附剂对不同形态铬的吸附实验
将EDTA与硫酸铬按2∶1.25的摩尔比制备成EDTA-Cr的工作液,确保不产生铬的沉淀,即确定生成EDTA络合态铬.将此溶液分别配制成铬浓度为0~70 mg/L的系列溶液,以模拟制革鞣制废水中可能的情况.各取1.2.1中3种复合金属氧化物10 mg,置于40 mL系列溶液中,在35 ℃恒温、160 r/min条件下震荡3 h,然后测不同吸附剂对总铬的去除效果.
本实验重复3次,测定结果用平均值表示.
1.3 分析测定方法
上述金属氧化物样品的热重和热差分析采用德国NETZSCH 公司STA 409 PC综合热分析仪(高纯氮气保护)进行,扫描速度为10 ℃/min.比表面积及孔隙度分析采用美国Quantachrome公司Nova 2200e进行,测定前将样品300 ℃真空脱气3 h,以N2为吸附质,在-196 ℃测定.同时用BET测定比表面和t法测定各复合氧化物的孔体积.样品晶体结构分析采用D/MAX-2500V型X射线衍射仪(XRD);吸附实验中溶液中铬含量的测定按照GB7466-87二苯碳酰二肼分光光度法测定.
2 结果与讨论
2.1 吸附剂最佳制备条件的确定

(a) Zr-Al-Ti(1∶3∶1)
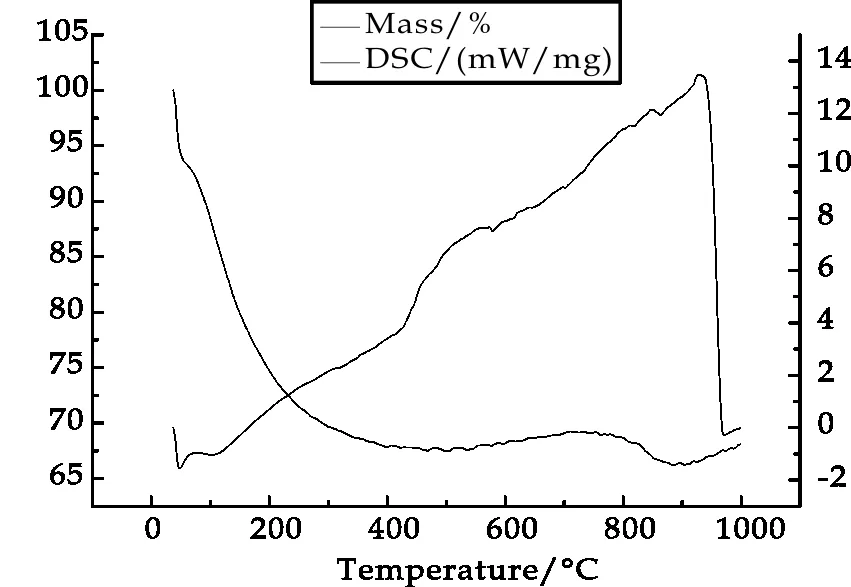
(b) Zr-Al-Ti(2∶2∶1)
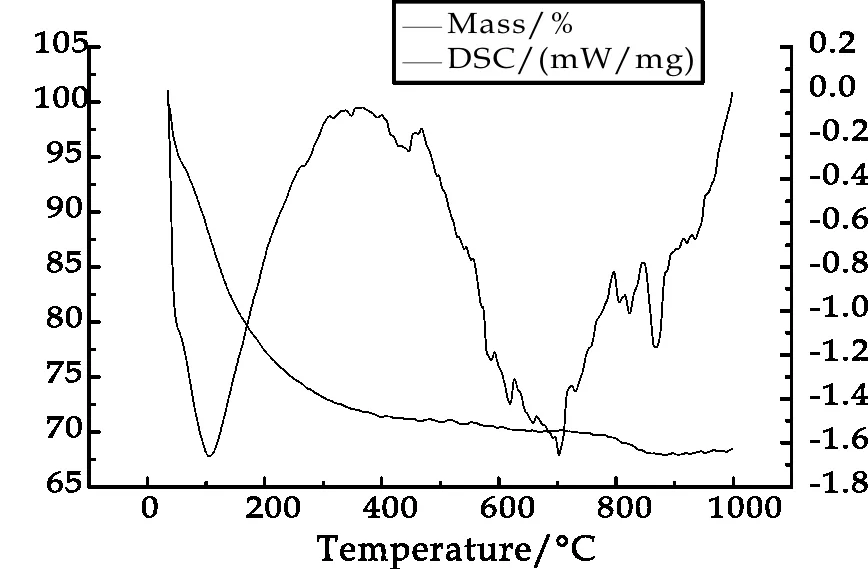
(c) Zr-Al-Ti(3∶1∶1)图1 不同复合氧化物前驱体 TG-DSC热分析曲线
图1中(a)、(b)、(c)分别为Zr-Al-Ti(1∶3∶1)、Zr-Al-Ti(2∶2∶1)、Zr-Al-Ti(3∶1∶1)三个沉淀物在0 ℃~1 000 ℃范围内的TG-DSC测定结果.
由图1可以看出,(a)Zr-Al-Ti(1∶3∶1)中初始TG曲线出现增重,是因为升热过程中部件排开空气的质量在减少,即浮力在减小而形成的加热试样的表观增重[13].0 ℃~200 ℃之间TG曲线一直处于失重,复合物在35 ℃~100 ℃主要是失去了吸附水,相对应的出现了强的吸热峰,且在约100 ℃时达到最快失重速率,失重率约为18%.300 ℃以后曲线趋于平稳,说明沉淀物已经完全转化为氧化物[14].800 ℃出现第二次失重,结合XRD数据,究其原因是氧化物之间发生相互反应,生成了复合氧化物,并释放出燃烧热.同样分析(b)、(c),从TG图上可以看出,在0 ℃~1 000 ℃,都经历了先失去结合水,然后氢氧化物转变为氧化物,从DSC曲线上看出在900 ℃附近各有一强放热峰,应该是氢氧化物完全分解.900 ℃以后都有增重的趋势,可能是由于样品粒径较小,表面能高从而吸附气氛中的氮气引起的[15].整体分析图(a)、(b)、(c),由TG曲线可得,300 ℃~750 ℃之间失重率变化不大,且结合DSC曲线,在此温度下新型复合氧化物已形成,又由于在一定范围内比表面积越大越有利于吸附,而温度越高对于晶型的形成越有利,同时比表面积就会越小,因此,选择750 ℃、烧结3 h作为本实验吸附材料的制备条件.
将图1中测定结果采用Coats-Redfern积分法来进行了动力学过程分析,分析时,将各个数据代入常用的积分动力学函数G(a)及方程ln[G(a) /T2]=ln[(AR/βE)×(1-2RT/E)]-E/RT并以ln(G(a)/T2)对1/T作图,由直线的截距和斜率得到各组动力学参数A和E以及线性相关系数r2.选择具有良好的线性相关系数r2所对应的函数关系G(a)、A和E.结果如表2所示.
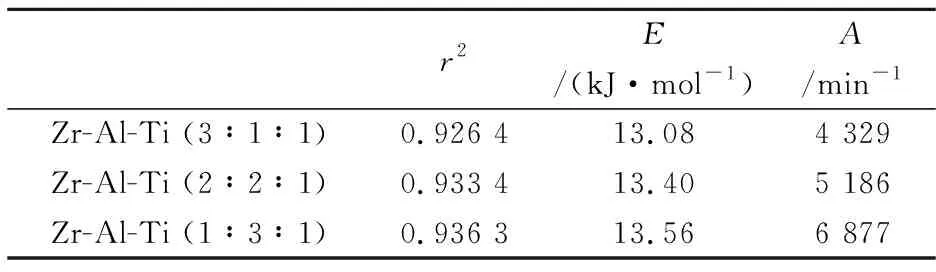
表2 各氢氧化物前驱体的热分解动力学参数
通过对比分析各物质发生了三维球形固膜扩散控制的固相反应,热分解过程遵循Zhuralev-Lesokin-Tempelman三维扩散机理,其函数方程为f(a)=15(1-a)4/3[(1-a)-1/3- 1]-1,g(a)=[(1-a)-1/3-1]2.表1显示,各物质的表观活化能在13.08~13.56 kJ·mol-1之间,表明实验所制备氢氧化物前驱体的热解反应较易发生.
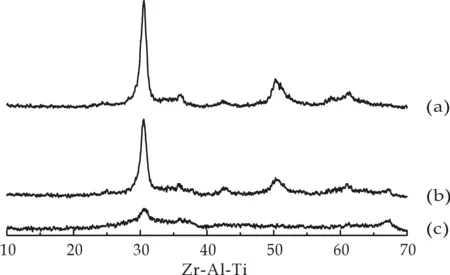
图2 各沉淀物在750 ℃下焙烧3 h 后所得样品的XRD图
图2中(a)、(b)、(c)分别是Zr-Al-Ti(1∶3∶1)、Zr-Al-Ti(2∶2∶1)、Zr-Al-Ti(1∶3∶1)在750 ℃焙烧3 h后的XRD谱图.Zr-A1-Ti经750 ℃焙烧后出现了明显的特征衍射峰 30.6 °的ZrTiO4晶相(特征衍射峰2θ=24.7 °和30.6 °)、67.1 °的γ-Al2O3晶相(特征衍射峰2θ=31.0 °、36.6 °、51.9 °及67.1 °)、ZrO2(PDF=74-1201,34-1084)晶相、TiO2(2θ=36.1 °)晶相及Al0.18Zr0.82O1.91(PDF:53-0572).
2.2 各复合氧化物吸附剂性能及吸附效果
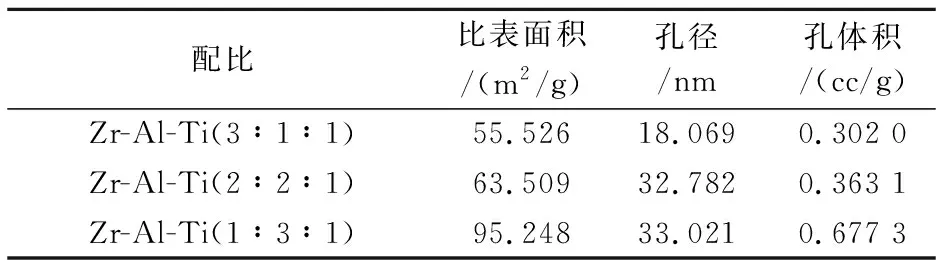
表3 各复合氧化物的比表面积、孔容及孔径
表3为各复合氧化物的比表面积、孔容及孔径检测结果.可以看出这些复合氧化物都属于介孔物质, 且比例为1∶3∶1复合物的比表面积、孔径、孔体积比2∶2∶1、3∶1∶1的大,3∶1∶1的比表面积、孔径、孔体积最小.
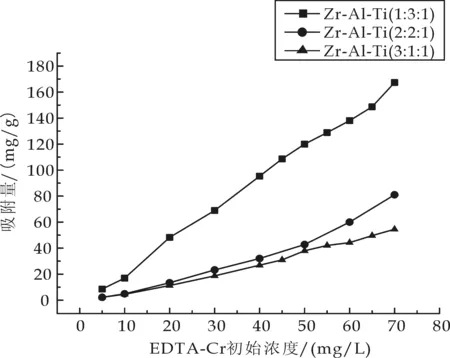
图3 各复合氧化物对EDTA-Cr吸附 特性(吸附剂0.5g/L)
各复合吸附剂对EDTA-Cr的吸附实验表明(如图3所示),在吸附剂用量为0.5 g/L的情况下,在实验浓度范围内均是随着EDTA-Cr浓度的增加而增加.在相同铬浓度条件下,Zr-Al-Ti(1∶3∶1)吸附量优于Zr-Al-Ti(2∶2∶1)、Zr-Al-Ti(3∶1∶1),且Zr-Al-Ti(3∶1∶1)吸附量最低.复合氧化物对EDTA-Cr的吸附量在不同初始浓度条件下各有差异,究其原因是吸附剂自身吸附特性、比表面积及孔径的影响.ZrO2、Al2O3、TiO2属于两性金属氧化物,在强酸和强碱条件下易溶解,形成的复合氧化物的耐酸碱性各不相同[8],吸附剂在相对强酸性条件下的吸附过程发生了自身溶解,从而导致吸附量降低;根据表3测试结果分析,吸附剂比表面积越大越有利于吸附的进行.因此,各吸附剂吸附量之间存在差异.
3 结论
本研究表明,各复合氧化物在750 ℃烧结3 h均发生了物相改变,750 ℃烧结既保证了Zr-Al-Ti(1∶3∶1、2∶2∶1、3∶1∶1)的稳定性又确保了比表面积较大.其中Al含量高的吸附剂具有更大优势.比表面积及孔体积在吸附剂吸附EDTA-Cr过程中,对吸附性能有显著影响.
复合氧化物吸附剂对EDTA-铬吸附在实验铬浓度条件下随着铬浓度的增加而增大,最大吸附量可达到167 mg/g,因此,所制备吸附剂对络合态铬的去除是可行的,这一研究结果完善了现有鞣制废水处理体系,为实际工程中去除络合态铬提供了技术支持,同时为后续实际废水中不同形态铬及总铬的去除研究奠定了基础.
[1] 林 海,但卫华,王坤余,等.无铬多金属配合鞣剂的研究进展[J].皮革科学与工程,2003,13(6):30-33,36.
[2] 陈宗良,李闻欣.金属配合物鞣剂与有机鞣剂结合鞣的研究进展[J].皮革与化工,2008,25(3):13-18.
[3] 王友平, 张焕祯, 于卫花,等.含铬废水吸附材料改性技术探讨[J].环境工程,2012,30(增刊):147-150.
[4] 贾 坤.组合工艺对制革废水的处理效果研究[D].济南:山东大学,2013.
[5] 赵长青,陈武勇,杨秦欢.固定化蜡质芽孢杆菌处理制革废水中Cr(Ⅵ)的条件优化[J].四川理工学院学报,2011,24(4):436-439.
[6] Donghee P,Seong R L,Yeoung S Y,et al.Reliable evidences that the removal mechanism of hexavalent chromium by natural biomaterials is adsorption-coupled reduction[J].Chemosphere,2007(70):298-305.
[7] 霍小平,刘存海.铬鞣废水处理现状综述[J].西部皮革,2009,31(23):37-42.
[8] Dean J.A.Lange′s Handbook of Chemistry[M].New York:McGraw-Hill,1992:340-414.
[9] Bortun A,Bortun M,Pardini J,et al.Effect of competitive ions on the arsenic removal by mesoporous hydrous zirconium oxide from drinking water[J].Materials Research Bulletin,2010,45(11):1 628-1 634.
[10] Rodrigues L A,Leandro J M.Adsorption of Cr(VI) from aqueous solution by hydrous zirconium oxide[J].Journal of Hazardous Materials,2010,173(1-3):630-636.
[11] Debnath S,Ghosh U C,Kinetics.Isotherm and thermodynamics for Cr (III) and Cr (VI) adsorption from aqueous solutions by crystalline hydrous titanium oxide[J].Journal of Chemical Thermodynamic,2008,40(1):67-77.
[12] 马宏瑞,连坤宙,马 秀.Zr(OH)4沉淀物对铬鞣废水Cr3+的吸附试验[J].环境化学,2013,32(1):118-124.
[13] 徐朝芬,孙学信,郭 欣.热重分析试验中影响热重曲线的主要因素分析[J].热力发电,2005,34(6):34-36.
[14] 王 芳.过渡金属氧化物催化剂催化甲醛降解性能研究[D].扬州:扬州大学,2007.
[15] 李兆娜.纳米铝热剂的制备及其表征[D].西安:西北大学,2009.

