淀粉接枝聚丙烯酰胺吸附甲基橙的研究
王煦漫,张彩宁
(西安工程大学 纺织与材料学院,陕西 西安 710048)
印染废水作为有害工业废水之一,因其废水量大、COD值高、生物降解困难的特性,对环境的危害很大.近年来,随着我国纺织印染行业的飞速发展,染料品种和数量的日益增加,印染废水已经成为水环境的主要污染源.国内现有的处理印染废水的方法主要包括生化法、化学絮凝法和吸附法[1].其中吸附法虽然应用较广,但是也存在吸附能力不强和成本高的缺点,因此开发经济、高效、绿色的吸附剂是目前研究的热点.淀粉接枝聚丙烯酰胺共聚物作为一种天然材料改性的功能高分子材料,具有低成本、无毒、易生物降解等优点,在高吸水性树脂、增稠剂和絮凝剂等方面已得到应用[2-3],而在印染废水处理领域尚未见有报道.本文以淀粉和丙烯酰胺为原料,N,N-亚甲基双丙烯酰胺为交联剂,采用水溶液聚合法制备St-g-PAM凝胶,研究其对染料甲基橙的吸附作用,并对其吸附机理和动力学进行了探讨.
1 实 验
1.1 材料与试剂
淀粉、丙烯酰胺、N,N-亚甲基双丙烯酰胺、甲基橙、过硫酸钾、乙醇,均为化学纯,均由西安化玻器械公司提供.
1.2 仪器设备
722型可见分光光度计(上海棱光技术有限公司);AD-12型恒温振荡箱(鹤山精湛染整设备有限公司).
1.3 St-g-PAM凝胶制备、表征
1.3.1 制备 将5g淀粉与100mL蒸馏水加入三口瓶中,于90℃糊化1h.将糊化淀粉溶液冷却至70℃后,依次加入引发剂和交联剂,随后滴加100mL含20g丙烯酰胺单体的水溶液.滴加完毕后于70℃反应4h.对反应产物进行洗涤、干燥及粉碎处理后即得St-g-PAM凝胶.
1.3.2 表征 反应产物用Bruker Vector 70红外光谱仪进行红外分析,采用溴化钾粉末压片法,谱图采集范围为4 000~400 cm-1.
1.4 St-g-PAM凝胶对甲基橙的等温吸附实验
于8只具塞锥形瓶中分别准确称取一定量St-g-PAM,再分别加入100mL不同浓度的甲基橙溶液,置于恒温振荡箱中,在25℃振荡一段时间后离心分离.用分光光度计测定上层清液的吸光度(λ=505nm).利用甲基橙的浓度-吸光度标准曲线算出相对应的甲基橙溶液浓度.以吸附量qe(mg/mg)表征吸附效果:
qe=[(c0-ce)V]/m.
其中c0为甲基橙的初始质量浓度(mg/L),ce为吸附平衡时溶液中甲基橙的质量浓度(mg/L),m为St-g-PAM的质量(mg),V为溶液体积(L).
1.5 吸附动力学实验
准确称取一定量St-g-PAM放入3只具塞锥形瓶中,分别加入100mL不同浓度的甲基橙溶液,置于恒温振荡箱中,在25℃振荡.在不同时间段取样分析,测定溶液中吸附质的浓度,直至达到吸附平衡为止.
2 结果与讨论
2.1 St-g-PAM红外表征

2.2 St-g-PAM的吸附模型
25℃时St-g-PAM凝胶自水中吸附甲基橙的等温线如图2所示.
从图2可以看出,St-g-PAM的吸附量随着甲基橙平衡浓度的增加而增大.在测试的浓度范围,最高可达0.432mg/mg,表明St-g-PAM对甲基橙具有优良的吸附能力.对于固液吸附体系,常用的两种吸附模型有Langmuir等温吸附方程和Freundlich等温吸附方程[4],其公式分别为
其中qm为饱和吸附量(mg/mg),b为与吸附能力有关的吸附常数(L/mg),K和n分别为与吸附剂容量和吸附强度有关的Freundlich常数.
分别用Langmuir和Freundlich方程对图2中的实验数据进行拟合,结果见表1.比较表1中的两种模型相关系数可知,St-g-PAM对甲基橙的吸附行为更符合Freundlich方程.Freundlich模型通常适用于表面具有不同类型吸附位点的情况.因此,可以推断St-g-PAM对甲基橙不是简单的单分子层吸附,而是多层吸附,并且在多个活性位点上均有吸附.St-g-PAM上的活性基团—OH、-NH2分别可以与甲基橙分子形成氢键作用[5].另外,St-g-PAM凝胶为多孔结构,其大比表面积也可产生物理吸附作用.
根据Freundlich理论,K表示吸附量的大小,n表示吸附强度的大小,n>1,则表明该吸附为优惠型吸附,吸附强度较大.根据实验数据计算的n为1.553,故可认为St-g-PAM容易吸附甲基橙,这与实验现象一致.根据n和K的值计算可得出25℃时St-g-PAM对甲基橙的吸附方程如下:
2.3 St-g-PAM吸附动力学

表1 St-g-PAM对甲基橙的等温吸附参数
St-g-PAM吸附动力学曲线如图3所示.可以看出,随着吸附时间的延长,吸附量起初增加很快,但在40min以后,吸附基本达到饱和.根据多孔吸附剂的液相吸附理论[6],可将St-g-PAM吸附甲基橙的过程分为快速吸附阶段、逐步吸附阶段和吸附平衡阶段3个阶段.图3中吸附时间为0~20min的曲线部分对应的是快速吸附阶段,此时甲基橙通过溶液扩散到吸附剂的表面(即液膜扩散);20~40 min为逐步吸附阶段,此时甲基橙分子扩散到吸附剂内部孔隙中,吸附速率降低(即颗粒扩散); 40~120min为吸附平衡阶段,此时St-g-PAM表面以及空洞内部的活性位点被甲基橙分子完全覆盖之后,吸附达到饱和.
常用的吸附动力学方程有准一级动力学方程[7]和准二级动力学方程[8],其公式为
其中qt为t时刻吸附量(mg/L),k1为准一级速率常数(min-1),k2为准二级速率常数(mg/(mg·min)).
对图3中的数据分别用准一级动力学方程、准二级动力学方程进行拟合,结果见表2.

表2 St-g-PAM对甲基橙的吸附动力学参数
注:qe,exp为由实验测出的平衡时的吸附量;qe,cal为由动力学方程计算出的平衡时的吸附量.
从表2可以看出,准二级吸附动力学方程拟合得到的相关系数均优于准一级动力学方程.此外,通过对比拟合的平衡吸附量与实验测得的平衡吸附量, 可知St-g-PAM对甲基橙的吸附过程更符合准二级吸附动力学方程.准二级速率常数k2随着甲基橙初始浓度的增大而减小,这是由于吸附质的浓度增大,分子间的碰撞几率增加,会导致St-g-PAM凝胶内壁微孔堵塞,使得传质阻力加大,从而造成吸附速率的下降.
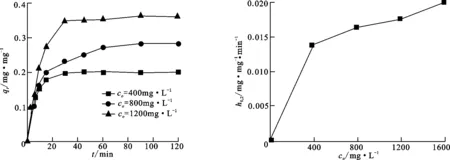
图3 St-g-PAM对甲基橙的吸附动力学曲线 图4 St-g-PAM对甲基橙的初始吸附速率与甲基橙初始浓度的关系
3 结 论
(1) 实验制备的St-g-PAM对甲基橙具有优良的吸附能力,25℃时吸附量可达0.432mg/mg;

(3) 动力学研究结果显示,St-g-PAM对甲基橙的吸附符合准二级动力学方程,而且其准二级速率常数k2随着甲基橙初始浓度的增大而减小.
参考文献:
[1] 李佳,苏宏智.印染废水处理方法及其研究进展[J].污染防治技术,2009,22(6):57-61.
[2] JYOTHI A N.Starch graft copolymers:Novel applications in industry[J].Composite Interfaces,2010,17(2/3):165-174.
[3] FRANCESCO P,FRANCESCA I,GIANFRANCO S,et al.Polymer in agriculture:A review[J].American Journal of Agricultural and Biological Science,2008,3(1):299-314.
[4] HOLMBERG K,JONSSON B,KRONBERG,B,et al.水溶液中的表面活性剂和聚合物[M].韩丙勇,张学军,译.北京:化学工业出版社,2005:312-336.
[5] 王彩,侯朝霞,王美涵,等.聚丙烯酰胺改性羟基磷灰石的制备及吸附Cu2+研究[J].功能材料,2014,45(2):2059-2062.
[6] 近藤精一,石川达雄,安部郁夫.吸附科学[M].李国希,译.北京:化学工业出版社,2006:103-104.
[7] LAGERGREN S.About the theory of so-called adsorption of soluble substances[J].Kungliga Svenska Vetenskapsakademiens,1953,24(3):1-39.
[8] HAMEED B H,AHMAD A A.Batch adsorption of methylene blue from aqueous solution by garlic peel,an agricultural waste biomass[J].Journal of Hazardous Materials,2009,164(2/3):870-875.
[9] WU F C,TSENG R L,HUANG S C,et al.Characteristics of pseudo-second-order kinetic model for liquid-phase adsorption:A mini-review[J].Chemical Engineering Journal,2009,151(1/3):1-9.
[10] 张彩宁,王煦漫.交联γ-聚谷氨酸吸附亚甲基蓝的研究[J].西安工程大学学报,2011,25(3):348-351.

