配方奶粉中克雷伯菌选择性培养方法的研究
胡 萍,魏琳琳,王新华,余大为,许小红,翟育忠,刘爱芳
(1.甘肃省疾病预防控制中心,甘肃 兰州 730020;2.甘肃省庆阳市疾病预防控制中心,甘肃 庆阳745000)
配方奶粉中克雷伯菌选择性培养方法的研究
胡 萍1,魏琳琳1,王新华1,余大为1,许小红1,翟育忠1,刘爱芳2
(1.甘肃省疾病预防控制中心,甘肃 兰州 730020;2.甘肃省庆阳市疾病预防控制中心,甘肃 庆阳745000)
目的 为提高配方奶粉中克雷伯菌的分离鉴定效率,研制专门用于克雷伯菌分离培养的选择性培养基。方法 依据克雷伯菌生化特性,研制成改良麦康凯(MACI)培养基,观察克雷伯菌及其他乳糖阳性的肠杆菌科细菌菌落在MACI平板、SS平板、麦康凯(MAC)平板和结晶紫中性红胆盐琼脂(VRBGA)平板上的生长特点;用产酸克雷伯菌(ATCC13182)和肺炎克雷伯菌(ATCC10031)检测MACI培养基的生长率和最低检出限。结果 克雷伯菌在MACI平板上形成独特的红色菌落,而其他肠杆菌为无色菌落;肺炎克雷伯菌(ATCC10031)和产酸克雷伯菌(ATCC13182)在MACI培养基上的生长率分别为0.936 6和0.898 8;最低检出限均为40 cfu/g。结论 MACI可作为分离克雷伯菌的理想选择性培养基。
配方奶粉;克雷伯菌;选择性培养方法
克雷伯菌属肠杆菌科,营养要求不高。其中的肺炎克雷伯菌及产酸克雷伯菌是重要的条件致病菌和医源性感染菌,且对抗生素易产生耐药性[1~5]。免疫力低下的个体感染此类菌后,可存在罹患肺炎、肠炎、脑膜炎、败血症和食物中毒等风险[2,6~14]。FAO/WHO于2004年5月在日内瓦召开的“婴儿配方奶粉中阪崎杆菌和其他微生物”的联席会议上,将克雷伯菌列为婴儿配方奶粉中B类致病菌[15,16],并要求成员国实施有效的监控。
克雷伯菌分解乳糖,在以往的肠道选择性培养基上,不易与其他乳糖阳性的肠杆菌科的细菌区分。本项目组尝试利用克雷伯菌可分解侧金盏花醇的生化特点[17],对传统肠道菌选择性培养基麦康凯(MAC)加以改良,研制出提高克雷伯菌分离培养效率的改良麦康凯(MACI)培养基,并对市场销售配方奶粉中克雷伯菌进行分离鉴别,比较4种肠道选择性培养基的分离效率,现将结果报告如下。
1 材料与方法
1.1 材料
1.1.1 试剂 营养琼脂(NA)、营养肉汤(NB)、缓冲蛋白胨水(BPW)、SS琼脂、麦康凯(MAC)琼脂、结晶紫中性红胆盐琼脂(VRBGA)、3号胆盐(北京奥博星生物技术有限责任公司);中性红(天津科密欧化学试剂有限公司);生理盐水(甘肃扶正药业科技股份有限公司);琼脂粉、蛋白胨(日本进口分装);侧金盏花醇(国药集团化学试剂有限公司);VITEK 2 GN-菌种鉴定卡(美国bioMerieux.Ine公司)。以上试剂均在有效期内。
1.1.2 仪器 VITEK 2全自动生化鉴定仪(bioMerieux)、恒温培养箱、麦氏浊度比浊仪(法国梅里埃公司)。
1.1.3 试验菌株 产酸克雷伯菌(ATCC13182)、肺炎克雷伯菌(ATCC10031)、产气肠杆菌(NCIMB10102)、阴沟肠杆菌(ATCC23355)、费劳地枸橼酸杆菌(ATCC8090)标准菌株(上海汉尼生物技术有限公司);大肠埃希菌(ATCC25922)标准菌株、产酸克雷伯菌(8株)和肺炎克雷伯菌(12株)临床分离菌株由甘肃省人民医院检验中心馈赠。
1.2 MACI培养基的研制
1.2.1 参照MAC培养基的制备方法[18]将其中的乳糖成分用侧金盏花醇替代,配制方法如下:蛋白胨20 g,氯化钠5 g,琼脂20~25 g,胆盐5 g,蒸馏水1 000 ml,将各成分加入蒸馏水中,加热溶解,调节pH至7.4,加入1%中性红水溶液5 ml,分装适当容器,115℃高压灭菌15 min,温度降至60℃左右,加入侧金盏花醇10 g,充分混匀,制成平板备用。
1.2.2 选择性培养基的分离培养 实验室引进的菌株均经VITEK 2进行鉴定。菌株复活后,分别接种肠道菌选择性培养基SS、MAC、VRBGA和MACI平板,培养后观察菌株在各种平板上的菌落形态。
1.2.3 MACI培养基的质控[19](1)克雷伯菌在MACI培养基上生长率的测定。产酸克雷伯菌(ATCC13182)和肺炎克雷伯菌(ATCC10031)经NB培养后,菌液浓度达到108个/ml。用生理盐水对菌液依次做10倍递增稀释,稀释浓度至100个/ml。各取1 ml菌液,涂布法分别接种于NA平板和MACI平板,检测克雷伯菌在MACI培养基上的生长率(生长率=待测培养基菌落计数/对照培养基菌落计数),结果见表1。

表1 克雷伯菌在不同浓度培养基上的生长试验
(2)克雷伯菌在MACI培养基上最低检出限的测定。无菌取8份配方奶粉(已知无肠杆科细菌),每份25 g,分别加到225 ml NB中,均质。取浓度为100~107个/ml的菌液各1 ml,分别加到8份配方奶粉中,混匀,然后各取1 ml,涂布法接种于MACI平板,结果见表2。

表2 不同浓度克雷伯菌在MACI琼脂上的生长计数情况
1.3 市场销售配方奶粉中克雷伯菌的检测及MACI培养基应用效果的评判
1.3.1 样品 市场销售的1阶段(0~6月)、2阶段(6~12月)、3阶段(1~3岁)和4阶段(3岁以上)18个品牌的配方奶粉,共计98份。
1.3.2 配方奶粉中克雷伯菌的检测步骤 无菌称取配方奶粉100 g置于900 ml BPW中混匀培养后,从中取25 ml置于225 ml NB中混匀培养,分别转种MACI、SS、MAC和VRBGA平板培养。挑取可疑菌落,涂片革兰氏染色,应用VITEK 2全自动生化鉴定仪的GN-菌种鉴定卡对革兰氏阴性杆菌进行鉴定。检测过程中,均带标准菌株作参考。
1.3.3 MACI培养基的应用效果评判 基本程序同1.3.2。分别将MAC、SS、VRBGA、MACI分离到的可疑菌落数与生化鉴定确认的菌落数进行比较,计算出各培养基的分离阳性率(分离阳性率=生化鉴定确认的菌落数/可疑菌落数),并借此对MACI的分离特异性做出评判。
2 结果与分析
(1)实验室引进菌株经VITEK 2鉴定,结果均符合试验要求。
(2)通过对试验菌株菌落的观察发现,在VRBGA、SS和MAC培养基上,菌落均呈湿润、光滑、边缘整齐、红色的形态特点,因此,克雷伯菌不易与其他肠杆菌进行判读和鉴别。MACI平板上,试验菌株进行中的克雷伯菌菌株均形成红色、直径约2 mm、突起、黏稠、相邻融合的菌落,其他肠杆菌的菌落为无色,虽然产气肠杆菌的菌落也为红色,但相邻菌落不发生融合现象。
(3)克雷伯菌在MACI上的生长率。NA是需氧和兼性厌氧菌生长的良好培养基。在此培养基上,肺炎克雷伯菌(ATCC 10031)和产酸克雷伯菌(ATCC13182)不同浓度的菌液均生长良好、计数变化明显。由表1可见,当菌液稀释浓度达到102cfu/ ml时,该菌即可在NA培养基上生长,在MACI培养基上也能达到很好的生长效果。依据食品微生物学检验菌落计数测定的报告原则[20],选择菌落数在30~300的稀释度结果,以NA培养基为对照,计算出MACI培养基的生长率分别为0.936 6和0.898 8。
(4)最低检出限。1 ml菌液加入250 ml含有25 g配方奶粉的NB中,菌浓度被稀释了250倍。表2显示,两种菌在104cfu/ ml稀释度时,均可生长,故MACI平板上的最大稀释生长浓度为104cfu/250 ml,两种克雷伯菌的最低检出限均为40 cfu/g。
(5)市场销售配方奶粉中克雷伯菌的检测。表3显示,在4种不同选择性培养基分离克雷伯菌的试验中,MACI的分离阳性率最高,为75.0%,VRBGA和MAC相同,分别为50.0%,SS为37.5%。
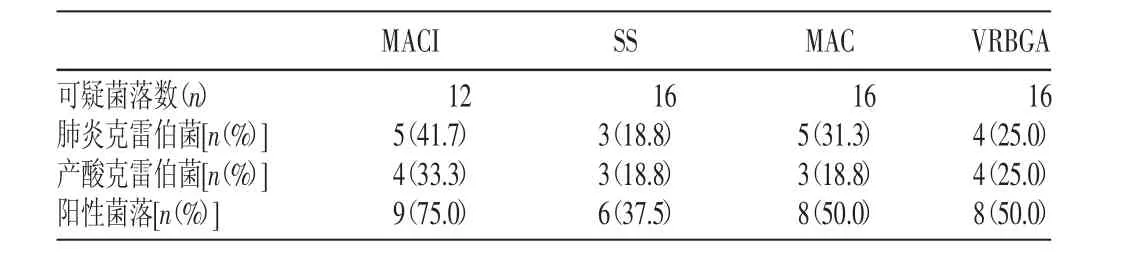
表3 不同选择性培养基分离克雷伯菌效果比较
3 讨论
在肠杆菌科细菌常用的分离培养基MAC、SS、VRBGA上,克雷伯菌与发酵乳糖阳性的细菌菌落均呈红色,不易区分。本项目组依据克雷伯菌可分解侧金盏花醇的特点[17],研制了MACI,经测试,克雷伯菌在MACI上可形成特点显著、易与其他肠杆菌区分的菌落,依据《培养基性能测试实用指南》的要求,经对MACI培养基进行的生长率与最低检出限试验结果表明,肺炎克雷伯菌(ATCC10031)和产酸克雷伯菌(ATCC13182)在该培养基上的生长率及最低检出限均符合预期效果。
对市场销售的98份婴幼儿配方奶粉的检测结果表明,MACI对克雷伯菌的分离阳性率高于其他3种培养基,经对4种选择性培养基组份对比分析,SS琼脂的抑菌剂成分最多,达4种,且含量高[19],而VRBGA琼脂为2种[21],MAC和MACI琼脂仅为1种,且含量都较低[19],是否可以认为,培养基中抑菌剂成分的多寡、含量的高低和可疑菌落挑选是造成克雷伯菌分离效率差异的原因。我们认为MACI培养基为克雷伯菌分离培养的理想培养基。
[1]贤永嫦.肺炎克雷伯菌耐药性分析[J].医学检验,2011,18(3):67.
[2]李景云,马越,姚蕾.内科、外科、儿科、重症监护病房和门诊患者分离的肺炎克雷伯菌耐药性分析[J].中国抗生素杂志,2003,28(9):537-540.
[3]邱清芳.大肠埃希氏菌和肺炎克雷伯氏菌AmpC酶的检测[J].医学检验与临床,2007,18(6):24-26.
[4]华杰,李艳霞.肺炎克雷伯菌医院感染及耐药性监测[J].中华医院感染学杂志,2006,16(10):1172-1173.
[5]尹建雯,徐闻,古文鹏.云南省发现1株携带NDM-1基因的产酸克雷伯菌[J].疾病监测,2012,27(3):211-217.
[6]董捷,于兰,赵郁,等.产酸克雷伯菌引起的食物中毒临床分析[J].中华传染病杂志,2002,21(1):69.
[7]黄锋,严靖,曹金德.儿科病房流行肺炎克雷伯氏菌肠炎一起[J].南通医学院学报,1997,17(2):295-296.
[8]刘如安,刘艳宾.肺炎克雷伯菌下呼吸道感染74例及耐药性分析[J].医学临床研究,2006,23(7):1104-1105.
[9]吴惠.克雷伯菌致婴幼儿腹泻流行病学分析[J].河南医学研究,2004,13(2):178-180.
[10]刘志业,吴景才.婴儿腹泻克雷伯菌的分离鉴定及其临床意义[J].医学综述,1996,2(10):572-573.
[11]孙红,王世平,黄明越.食物中毒样品中检出产酸克雷伯菌的报告[J].中国公共卫生,2001,17(12):1132.
[12]凌勤芳.一起由肺炎克雷伯菌引起的食物中毒[J].中国卫生检验杂志,2008,18(6):1203-1226.
[13]贾艳,孙长江,韩文瑜.肺炎克雷伯菌研究进展[J].微生物学杂志,2006,26(5):67.
[14]丁娟,刘尚才,常世卿.克雷伯氏菌骨伤科感染及药敏分析[J].中医正骨,2003,15(12):37-38.
[15]Joint FAO/WHO Workshop.Enterobacter sakazakii and microorganisms in powdered infant formula[M].Geneva:WHO,2004.
[16]Joint FAO/WHO Workshop.Enterobacter sakazakii and Salmonella in powdered infant formula[M].Rome,Italy:FAO,2006.
[17]张卓然.临床微生物学和微生物检验[M].北京:人民卫生出版社,1988.
[18]中等卫生学校试用教材《微生物学及检验技术》编写组.微生物学及检验技术[M].广州:广东人民出版社,1979.
[19]国家认证认可监督管理委员会.SN/T1538.2-2007培养基制备指南第2部分:培养基性能测试实用指南[S].北京:中国标准出版社,2007.
[20]中华人民共和国卫生部.GB4789.2-2010食品安全国家标准食品微生物学检验菌落总数测定[S].北京:中国标准出版社,2010.
[21]中华人民共和国国家标准.SN/T0738-1997出口食品中肠杆菌科检验方法[S].北京:中国标准出版社,1997.
G424.31
B
1671-1246(2014)07-0114-03
注:本文系2010年甘肃省卫生行业计划项目(GSWST-2010-25)

