不同淋洗剂对污染土娄土中Cu、Pb的淋洗修复研究
邓红侠,刘 霞,王建涛,王 力,杨亚莉,杨亚提
(西北农林科技大学 a 理学院,b 资源环境学院,陕西 杨凌 712100)
目前,我国水资源和土壤中的重金属污染非常严重。2006年之前,环境保护部曾从30万hm2的基本农田保护区中抽取3.6万hm2进行了土壤重金属含量的测定,结果显示重金属超标率达12.1%[1]。由于有毒重金属在土壤环境中的污染过程具有隐蔽性、稳定性及不可逆性等特点,因此土壤中有毒重金属污染的修复研究一直是环境科学领域的热点。用有效淋洗剂淋洗重金属污染土壤,被认为是一项高效、能彻底治理土壤重金属污染的技术[2-3]。常用的淋洗剂有无机酸溶液(HCl和 HNO3等)、有机酸溶液(柠檬酸和酒石酸等)、人工合成的螯合剂(EDTA和DTPA等)和表面活性剂等[4-8]。研究结果表明,无机酸、EDTA和DTPA均能有效去除土壤中的重金属离子[6],但无机酸的使用会导致土壤结构的破坏,化学合成的螯合剂、表面活性剂通常对环境有害,且不易生物降解,会对土壤产生二次污染。目前,人们开始利用对生态环境无毒的生物表面活性剂修复受重金属污染的土壤。生物表面活性剂(biosurfactant)具有羟基、羧基等特征基团,且环境相容性好、化学结构多样、成本低廉、易于回收利用,近年来已成为前景很好的重金属污染修复剂[9-16]。时进钢等[17]研究了鼠李糖脂对沉积物中重金属的去除作用,表明鼠李糖脂对沉积物中的Cd和Pb有明显的去除作用。
目前,在重金属污染土壤的修复研究中,关于不同淋洗剂尤其是表面活性剂对于石灰性土壤淋洗规律和效率的研究还较少。为此,本试验以陕西石灰性土壤土娄土为研究对象,用常用的螯合剂 EDTA、柠檬酸(CIT)以及合成表面活性剂(SDS)和生物表面活性剂鼠李糖脂(RL2)作为淋洗剂,探讨不同淋洗剂对重金属Cu、Pb污染土娄土的最佳淋洗条件以及淋洗效果,分析不同淋洗剂去除重金属离子的机理,以期为石灰性土壤中重金属污染的修复提供一定的理论依据。
1 材料与方法
1.1 主要试剂和土壤
1.1.1 主要试剂 本试验选用2种螯合剂:乙二胺四乙酸二钠盐(EDTA,分析纯,西安化学试剂厂);柠檬酸(CIT,分析纯,天津博远化工股份有限公司)。2种阴离子型的表面活性剂:十二烷基硫酸钠(SDS,分析纯,天津市河北区海晶精细化工厂);鼠李糖脂(RL2,西安罗森伯科技有限公司)。
1.1.2 土 壤 供试原土采集于西北农林科技大学试验农场。采样深度为0~20 cm,样品经自然风干、研碎过孔径1 mm筛,放入烘箱(105 ℃)烘干后储存于广口瓶中备用。供试土壤pH为8.66,CaCO3含量75.5 g/kg,有机质含量11.2 g/kg,物理黏粒(粒径<0.01 mm)含量452.2 g/kg,CEC为20.60 cmol/kg[18];游离Fe2O3含量 59.10 g/kg,矿物组成以伊利石为主,含有少量蛭石[19]。采用王水-高氯酸消煮-火焰原子吸收法(TAS-990原子吸收分光光度计,北京普析通用仪器有限责任公司)测定铜含量为160.68 mg/kg,铅含量为78.25 mg/kg。
1.2 试验方法
1.2.1 Cu、Pb污染土壤的模拟 设置外加重金属Cu、Pb含量分别为400.00 和 500.00 mg/kg。称 30.0 g CuSO4和 23.97 g Pb(NO3)2分别加入到 30.0 kg供试土娄土中。上述污染土壤分别间歇搅拌1个星期后,放置1个月,自然风干,磨细过孔径 1 mm筛备用。模拟污染土娄土中不同形态的重金属采用Sposito顺序提取法[20]提取,采用火焰原子吸收法测定不同形态Cu、Pb的含量(表1),在测定过程中应用插入标准法进行质量控制,以下各项试验内容的测定过程与之相同。
有研究表明,重金属的形态与生物有效性有密切关系[21]。重金属的交换态、吸附态是生物的直接可利用态,可作为重金属生物毒害的直接评价指标;重金属的碳酸盐结合态、有机结合态可作为生物的潜在可利用态,是重金属生物潜在毒害的评价指标;而残余态和硫化物残余态则对生物的可利用性贡献不大。

表 1 污染土娄土中不同形态Cu、Pb的含量
1.2.2 不同浓度淋洗剂对污染土娄土的淋洗 称取原土和污染土娄土各1.00 g,置于一系列100 mL塑料离心管中,分别加入 20 mL不同浓度的 EDTA、CIT、SDS和RL2溶液,使其浓度梯度为 0,0.000 5,0.001,0.005,0.01,0.015,0.02 mol/L。溶液的 pH 均用 0.1 mol/L HNO3和NaOH调至7.0,每处理重复 3 次。将上述溶液于 25 ℃条件下振荡 4 h[22](预试验中此时间下土娄土中Cu、Pb的解吸与吸附达到了平衡状态),5 000 r/min 离心 10 min,过孔径 0.45 μm滤膜,溶液中Cu、Pb的质量浓度用火焰原子吸收法测定。
1.2.3 不同pH淋洗剂对污染土娄土的淋洗 称取原土和污染土娄土各 1.00 g,置于一系列100 mL塑料离心管中,分别加入 20 mL浓度为 0.01 mol/L 的 EDTA、CIT、SDS和RL2溶液,设置 EDTA、CIT、SDS 溶液的pH梯度分别为 2,4,6,8,10,RL2溶液的pH梯度为 6,8,10,12(RL2在酸性溶液中不溶)。其余步骤同1.2.2。
1.2.4 不同浓度背景电解质对淋洗剂淋洗污染土娄土的影响 称取原土和污染土娄土各 1.00 g,置于一系列100 mL塑料离心管中,分别加入 20 mL浓度为 0.01 mol/L的 EDTA、CIT、SDS和RL2溶液,背景电解质NaNO3的浓度分别设为 0,0.005,0.01,0.1,0.5 mol/L,背景电解质NaCl的浓度分别设为 0,0.005,0.01,0.1,0.5 mol/L。其余步骤同1.2.2。
1.2.5 不同水(mL)土(g)比及淋洗次数对污染土娄土淋洗的影响 称取原土和污染土娄土各 1.00 g,置于一系列 100 mL塑料离心管中,分别加入10,20,30 mL浓度为 0.01 mol/L的 EDTA、CIT、SDS和RL2溶液,其余步骤同1.2.2。在离心后的土壤中再加入 20 mL上述溶液,用同样方法连续淋洗 4 次,用火焰原子吸收法测定各次淋洗液中Cu、Pb的质量浓度。
1.2.6 Cu、Pb淋洗量及淋洗百分率的计算 计算公式如下:
q=C×V/m。
(1)
式中:q为淋洗剂对土壤中Cu、Pb 的淋洗量,mg/kg;C为淋洗溶液中Cu、Pb的质量浓度,mg/L;V为淋洗溶液体积,L;m为土样质量,kg。
淋洗百分率=(淋洗量÷土样中重金属总量)×100%。
(2)
2 结果与分析
2.1 不同浓度淋洗剂对污染土娄土中Cu、Pb淋洗效果的影响
图1为EDTA、CIT、SDS和RL2对污染土壤中Cu、Pb 的淋洗曲线。由于不同浓度淋洗剂对原土中Cu、Pb的淋洗百分率均小于5%,且淋洗效果无差异,故略去原土的淋洗曲线。
2.1.1 螯合剂的淋洗效果 从图1可以看出,随着EDTA浓度从0.000 5 mol/L增加到0.005 mol/L,土壤中2种重金属Cu 、Pb的淋洗百分率也相应增加,且增加的幅度较大;当EDTA浓度从0.01 mol/L继续增加到0.02 mol/L时,淋洗百分率增加幅度较小,可见0.01 mol/L为EDTA最适的淋洗浓度,在该浓度下EDTA对Cu、Pb 2种重金属的淋洗百分率分别为63.73%和88.48%,可知 EDTA对Pb 的去除效果明显优于对Cu的去除效果。Mulligan等[23]的研究结果表明,交换态、碳酸盐结合态、氧化物结合态等3种结合形态的重金属离子,其移动能力和生物有效性都比较高,环境风险也较大,通过土壤淋洗能有效去除这3种结合形态的重金属离子;而以有机态和残余态结合的重金属,其移动能力和生物有效性都非常低,环境风险也较低,并且很难去除。通过表1计算可知,污染土娄土中Cu以交换态、吸附态、碳酸盐结合态和有机结合态形式存在的量占Cu总量的63.76%,而Pb为80.21%,这与0.01 mol/L EDTA淋洗Cu、Pb的百分率接近,说明EDTA能有效去除土娄土中交换态、吸附态、碳酸盐结合态和部分有机结合态重金属,而对硫化物残余态和残余态重金属的作用效果不明显。

图 1 不同浓度淋洗剂对污染土娄土中Cu、Pb的淋洗曲线
从图1还可以看出,随着CIT浓度的增加,CIT对污染土娄土中Cu的淋洗百分率的变化趋势与EDTA相同,但其对Cu的淋洗百分率低于EDTA,当CIT浓度为0.02 mol/L时,其对Cu的淋洗百分率最高,为58.68%;随着CIT浓度的增大,CIT对污染土娄土中Pb 的淋洗百分率增加幅度较小,当CIT浓度为0.02 mol/L时,其对Pb的淋洗百分率最高,但仅为23.39%。由此可知,CIT对污染土娄土中Cu的淋洗效果较好,这归因于CIT对Cu 的络合能力(lgK稳=14.2)强于Pb (lgK稳=4.4)[24]。通过表1计算可知,污染土娄土中Cu以交换态、吸附态、碳酸盐结合态形式存在的量占总量的32.59%,而Pb 为9.14%,说明CIT也能有效去除土娄土中交换态、吸附态、碳酸盐结合态和少部分有机结合态重金属Cu和Pb。
2.1.2 表面活性剂的淋洗效果 图1表明,表面活性剂RL2和SDS对污染土娄土中Cu、Pb的淋洗能力远低于EDTA。当RL2浓度从0增加到0.01 mol/L,其对土娄土中2种重金属的淋洗百分率增加幅度很小;当RL2浓度从0.01 mol/L继续增加到0.02 mol/L时,淋洗百分率增加幅度稍大, 0.02 mol/L RL2对土娄土中Cu 、Pb的淋洗百分率分别为13.54%和13.04%,这一结果与Neilson等[15]用鼠李糖脂淋洗铅污染土壤时对铅的去除率(14.2%)接近。Ochoaloza等[25]采用离子交换树脂技术对鼠李糖脂与各种金属离子络合的稳定常数进行了研究,发现当pH=6.9时,鼠李糖脂与各种金属离子络合的稳定常数大小顺序为Al3+>Cu2+>Pb2+>Cd2+>Zn2+>Fe3+>Hg2+>Ca2+>Co2+>Ni2+>Mn2+>Mg2+>K+,由此也说明本研究结果,即RL2对Cu的淋洗能力大于Pb。通过表1计算可知,试验土壤中Cu以交换态、吸附态形式存在的量占总量的12.41%,与RL2淋洗土娄土中Cu的百分率接近,说明RL2能有效去除土娄土中交换态、吸附态结合的Cu;而Pb以交换态、吸附态和碳酸盐结合态形式存在的量占总量的9.14%,说明RL2可以去除土娄土中交换态、吸附态和碳酸盐结合态的Pb。
从图1可以看出,SDS对污染土娄土中Cu的最大淋洗百分率为7.72%,该结果较Ramamurthy等[5]用SDS对污染砂土中Cu的淋洗百分率高;SDS对污染土娄土中Pb的最大淋洗百分率为5.56%,且随着SDS浓度的增加淋洗百分率变化不大。由淋洗百分率值和表1可知,SDS只能淋洗土娄土中部分交换态及吸附态的Cu和Pb。
有研究表明,表面活性剂对于重金属的淋洗作用基于离子交换、沉淀溶解、反电荷离子交换3种机制[26-27]。当表面活性剂浓度低于临界胶束浓度(CMC)时,表面活性剂存在形式为单分子状态,其对重金属的洗脱作用以离子交换为主;而当表面活性剂浓度高于CMC时,洗脱机制则以反电荷离子交换或者沉淀溶解为主,表面活性剂胶束不能直接发生离子交换。Miller[28]提出,生物表面活性剂可能通过2种方式促进土壤中重金属的解吸,一是与土壤液相中的游离金属离子络合;二是通过降低界面张力使土壤中重金属离子与表面活性剂直接接触,从而改变表面性质,削弱金属离子与土壤之间的黏附性,促进金属离子与土壤分离及金属离子与生物表面活性剂的络合。本研究中,当RL2浓度大于其CMC(0.000 1 mol/L)时,金属离子是通过与RL2的胶束结合而得以去除的。而SDS的CMC为0.008 mol/L,本试验中,当SDS浓度小于其CMC时,随着SDS浓度的增加,其对Cu的淋洗百分率增加;当SDS浓度大于其CMC时,重金属的淋洗百分率基本不变并有下降趋势,这与SDS和土娄土中 Ca2+的沉淀损失有关,因为本试验发现,当SDS淋洗液浓度较大时,淋洗后的溶液呈现浑浊现象。
2.2 不同pH淋洗剂对污染土娄土中Cu、Pb淋洗效果的影响
土壤溶液pH是影响土壤吸持重金属离子及重金属离子移动能力的决定性因素之一。由图2可以看出,随着EDTA溶液pH从2增加到8,其对土娄土中Cu的淋洗百分率稍有降低,但变化不大,而对土娄土中Pb的淋洗百分率呈下降趋势,但淋洗百分率在80%以上,说明EDTA溶液能在比较广泛的pH范围(2~8)内对Cu 和Pb进行有效的淋洗。这与Wasay等[29]的研究结果一致,其作用机制在于EDTA对于重金属离子有极强的络合能力,因为EDTA在pH 3~6时仍主要以H2[EDTA]2-的形式存在,而在该pH范围内,土壤重金属离子主要以二价形式存在,因此,EDTA仍能与重金属离子形成稳定的螯合物。考虑到实际土壤的弱碱性,EDTA溶液pH选择在中性范围内比较合理。
图2还表明,当pH<4时,CIT对污染土娄土中Cu的淋洗百分率呈上升趋势;当pH>4时,CIT对污染土娄土中Cu的淋洗百分率呈下降趋势,可能与pH增加导致Cu产生氢氧化物沉淀有关。不同pH CIT对污染土娄土中Pb的淋洗百分率影响不大,主要是由于CIT对Pb的络合能力较小(lgK稳=4.4)。

图 2 不同pH淋洗剂对污染土娄土中Cu、Pb的淋洗曲线
不同pH的2 种表面活性剂SDS和RL2对污染土娄土中Cu、Pb的淋洗百分率影响不大,这与赵保卫等[30]研究的溶液pH对表面活性剂洗脱 Cu有显著影响的结果不同,这可能与土壤类型有关。由于石灰性土壤属于偏碱性,具有较强的对酸碱的缓冲性能,溶液pH的变化对土壤悬液的pH影响不大;而且当pH值较低时,表面活性剂与石灰性土壤中CaCO3溶解产生的Ca2+形成沉淀,从而对土壤中Cu、Pb的淋洗效果变差。总体而言,不同pH淋洗剂对污染土娄土中Cu、Pb的淋洗效果影响不大。
2.3 不同浓度背景电解质对淋洗剂淋洗污染土娄土中Cu、Pb 效果的影响
从图3可以看出,以NaNO3作背景电解质时,随着NaNO3浓度的增加,EDTA和CIT对污染土娄土中Cu的淋洗百分率变化不大。随着NaNO3浓度从0升为0.01 mol/L,RL2和SDS对Cu的淋洗百分率明显降低;之后随着NaNO3浓度的增加,RL2和SDS对Cu的淋洗百分率变化较小。随着NaNO3浓度的增加,4种淋洗剂对污染土娄土中Pb 的淋洗百分率影响不大。而用NaCl作背景电解质时,当NaCl浓度从0变化为0.01 mol/L时,4种淋洗剂对污染土娄土中Cu的淋洗百分率均有明显降低;随着NaCl的浓度从0.01 mol/L增加到0.5 mol/L,Cu的淋洗百分率基本保持不变。4种淋洗剂对土娄土中Pb的淋洗百分率随着NaCl浓度的增加而升高。这是由于随着NaCl浓度的增加, Cl-可以与Pb2+生成络合物而使更多的Pb2+淋洗出来,因此背景电解质浓度的增加导致4种淋洗剂对Pb的淋洗百分率增加,且对EDTA的淋洗效果影响最大。从经济实用角度综合考虑,应选择无背景电解质的淋洗剂。

图 3 不同浓度背景电解质对淋洗剂淋洗污染土娄土中Cu、Pb效果的影响
背景电解质通过影响土壤粒子表面双电层结构而影响土壤对淋洗剂的吸附能力。当背景电解质浓度较高时,土壤粒子表面扩散双电层被压缩,土壤表面动电电势降低,土壤对螯合剂阴离子和阴离子表面活性剂的吸附作用会增加,导致一部分淋洗剂会被固定在土粒表面,因此淋洗剂对重金属的淋洗百分率会有所降低。
2.4 不同水(mL)土(g)比及淋洗次数对污染土娄土中Cu、Pb淋洗效果的影响
2.4.1 水土比 表2显示,当水土比从10(mL)∶1(g)增至30(mL)∶1(g)时,4种淋洗剂对污染土娄土中Cu、Pb的淋洗百分率均增加。这是因为随着螯合剂和表面活性剂液相体积的增大,也相应地增大了螯合剂和表面活性剂胶束对重金属离子Cu、Pb的容纳空间,使Cu、Pb与淋洗剂能够得到充分接触,从而提高了其对Cu、Pb的淋洗百分率。相反,如果加入的土样质量过大,则易形成絮凝沉淀,这使得表面活性剂胶束很难通过土壤颗粒之间的孔隙而聚集[30]。从以上结果看,当水土比为30(mL)∶1(g)时,4种淋洗剂对Cu、Pb的淋洗效果较好。但在实际应用中如果水土比为30(mL)∶1(g)时,会明显增加操作容量和压力,运行成本会增加。因此,较合适的水土比应为20(mL)∶1(g)。
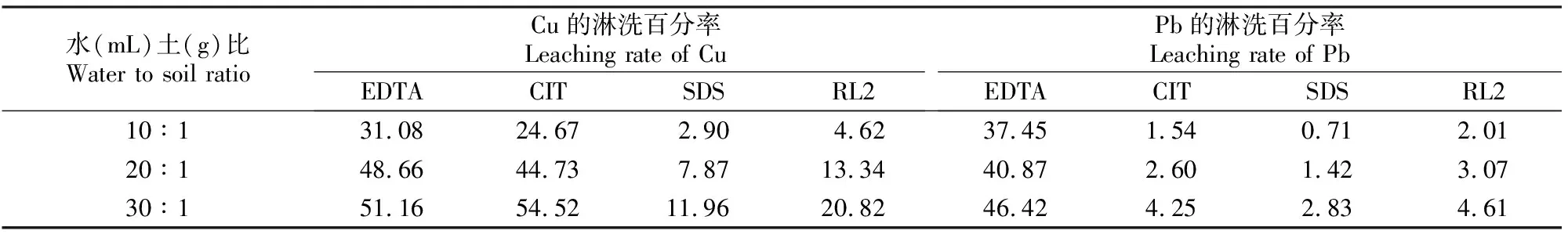
表 2 不同水(mL)土(g)比对污染土娄土中Cu、Pb淋洗百分率的影响
2.4.2 淋洗次数 由表3可知,4种淋洗剂淋洗污染土娄土中的Cu时,螯合剂EDTA和CIT的第1次淋洗对Cu的淋洗百分率分别为68.34%和 50.83%,随后各次对Cu的淋洗百分率远低于第1次淋洗,且随淋洗次数的增加,各次淋洗百分率变化逐渐减小,4次累计对Cu的淋洗百分率达到95%以上;表面活性剂SDS和RL2对Cu的4次淋洗百分率均相差不多,分别在8%和15%左右,4次累计对Cu的淋洗百分率分别为30.95%和60.55%。
因此,从4次累计对Cu的淋洗百分率可以确定,EDTA、CIT和RL2可作为污染土娄土中Cu的淋洗剂。

表 3 淋洗次数对污染土娄土中Cu、Pb淋洗百分率的影响
表3还表明,4种淋洗剂淋洗污染土娄土中的Pb时,第1次淋洗时EDTA对Pb的淋洗百分率就达到了85.52%,随后3次淋洗百分率较低且逐渐减少;CIT、SDS和RL2对Pb的各次淋洗百分率均很小,累计的Pb淋洗百分率均小于20%。说明EDTA是污染土娄土中Pb的最有效的淋洗剂。
从以上结果可见,2种表面活性剂对污染土娄土中的铜、铅有一定的去除能力,但淋洗效果不及2种螯合剂,可能与所选的表面活性剂的化学结构及土壤类型有关[14,17]。
3 结 论
1)淋洗4次后,4种淋洗剂对污染土娄土中Cu的淋洗能力为CIT>EDTA>RL2>SDS,对Pb的淋洗能力为EDTA>RL2>CIT>SDS。
2)EDTA和CIT溶液淋洗污染土娄土中Cu、Pb的最佳条件为:水土比20(mL)∶1(g),淋洗剂浓度0.01 mol/L,pH=7,无背景电解质;当RL2溶液浓度为0.02 mol/L、pH=8、无背景电解质条件下,其对污染土娄土中铜、铅的淋洗效果最佳。
3)多次淋洗结果表明,EDTA、CIT和RL2可以有效地去除污染土娄土中的Cu,EDTA可作为石灰性污染土娄土中Pb的最佳淋洗剂,而SDS则不宜作为污染土娄土中重金属污染修复的淋洗剂。
[参考文献]
[1] 傅国伟.中国水土重金属污染的防治对策 [J].中国环境科学,2012,32(2):373-376.
Fu G W.Countermeasures for water and soil heavy metal pollution in China [J].China Environmental Science,2012,32(2):373-376.(in Chinese)
[2] Van Benschoten J E,Matsumoto M R,Young W H.Evaluation and analysis of soil washing for seven lead contaminated soils [J].Journal of Environmental Engineering,1997,123(3):217-224.
[3] Peters R W.Chelant extraction of heavy metals from contaminated soils [J].Journal of Hazardous Materials,1999,66(2):151-210.
[4] 曾 敏,廖柏寒,曾清如,等.3种萃取剂对土壤重金属的去除及其对重金属有效性的影响 [J].农业环境科学学报,2006,25(4):979-982.
Zeng M,Liao B H,Zeng Q R,et al.Effects of three extractants on removal and availabilities of heavy metals in the contaminated soil [J].Journal of Agro-Environment Science,2006,25(4):979-982.(in Chinese)
[5] Ramamurthy A S,Vo D,Li X J,et al.Surfactant-enhanced removal of Cu and Zn from a contaminated sandy soil [J].Water Air Soil Pollut,2008,190:197-207.
[6] Zhang W H,Lo I M C.EDTA-enhanced washing for remediation of Pb-and/or Zn-contaminated soils [J].Journal of Environmental Engineering,2006,132:1282-1288.
[7] 可 欣,李培军,张 昀,等.利用乙二胺四乙酸淋洗修复重金属污染的土壤及其动力学 [J].应用生态学报,2007,18(3):601-606.
Ke X,Li P J,Zhang Y,et al.Heavy metals removal and its kinetics in contaminated soil under effects of EDTA washing [J].Chinese Journal of Applied Ecology,2007,18(3):601-606.(in Chinese)
[8] 李丹丹,郝秀珍,周东美,等.淋洗法修复铬渣污染场地实验研究 [J].农业环境科学学报,2011,30(12):2451-2457.
Li D D,Hao X Z,Zhou D M,et al.Remediation of chromium residue contaminated soil using a washing technology [J].Journal of Agro-Environment Science,2011,30(12):2451-2457.(in Chinese)
[9] 梁丽丽,郭书海,李 刚,等.柠檬酸、柠檬酸钠淋洗铬污染土壤效果及弱酸可提取态铬含量的变化 [J].农业环境科学学报,2011,30(5):881-885.
Liang L L,Guo S H,Li G,et al.The effects of Cr removal from contaminated soil and the content changes of acid extractable fraction by citric/sodium citrate leaching [J].Journal of Agro-Environment Science,2011,30(5):881-885.(in Chinese)
[10] Mulligan C N,Yong R N,Gibbs B F.Removal of heavy metals from contaminated soil and sediments using the biosurfactant surfactin [J].Journal of Soil Contamination,1999,8(2):231-254.
[11] 孟佑婷,袁兴中,曾光明,等.生物表面活性剂修复重金属污染研究进展 [J].生态学杂志,2005,24(6):677-680.
Meng Y T,Yuan X Z,Zeng G M,et al.Advances in research on remediation of heavy-metal contamination by biosurfactants [J].Chinese Journal of Ecology,2005,24(6):677-680.(in Chinese)
[12] Mulligan C N.Environmental applications for biosurfactants [J].Environ Pollut,2005,133(2):183-198.
[13] Behnaz D A,Mulligan C N.Extraction of copper from mining residues by rhamnolipids [J].Journal of Hazardous,Toxic,and Radioactive Waste,2004,83:166-172.
[14] Hong K J,Tokunaga S,Kajiuchi T.Evaluation of remediation process with plant derived biosurfactant for recovery of heavy metals from contaminated soils [J].Chemosphere,2002,49(4):379-387.
[15] Neilson J W,Artiola J F,Maier R M.Characterization of lead removal from contaminated soils by nontoxic soil-washing agents [J].Environ Qual,2003,32(3):899-908.
[16] 陈 洁,杨娟娟,周文军.皂角苷增强洗脱复合污染土壤中多环芳烃和重金属的作用及机理 [J].农业环境科学学报,2010,29(12):2325-2329.
Chen J,Yang J J,Zhou W J.Simultaneous removal of polycyclic aromatic hydrocarbons and heavy metal from Co-contaminated soils by saponina,a plant-derived biosurfactant [J].Journal of Agro-Environment Science,2010,29(12):2325-2329.(in Chinese)
[17] 时进钢,袁兴中,曾光明.鼠李糖脂对沉积物中Cd和Pb的去除作用 [J].环境化学,2005,24(1):55-58.
Shi J G,Yuan X Z,Zeng G M.Removal of heavy metals from sediment by rhamnolipid [J].Environmental Chemistry,2005,24(1):55-58.(in Chinese)
[18] 孟昭福,杨亚提,龚 宁,等.CTMAB对土娄土表面的修饰机制 [J].土壤通报,2008,39(5):1002-1006.
Meng Z F,Yang Y T,Gong N,et al.Modification mechanism of CTMAB on surface of Lou soil [J].Chinese Journal of Soil Science,2008,39(5):1002-1006.(in Chinese)
[19] 杨亚提,张一平.恒电荷土壤胶体对Cu2+、Pb2+的静电吸附与专性吸附特征 [J].土壤学报,2003,40(1):102-109.
Yang Y T,Zhang Y P.The characteristics of Cu2+and Pb2+electrostatic and specific adsorptions of constant charge colloids [J].Acta Pedologica Sinica,2003,40(1):102-109.(in Chinese)
[20] 孙西宁,张增强,张永涛,等.污泥堆肥过程中重金属的形态变化研究:Sposito浸提法 [J].农业环境科学学报,2007,26(6):2339-2344.
Sun X N,Zhang Z Q,Zhang Y T,et al.Changes of heavy forms in sludge during the composting process:Sposito method [J].Journal of Agro-Environment Science,2007,26(6):2339-2344.(in Chinese)
[21] 雷 鸣,廖柏寒,秦普丰.土壤重金属化学形态的生物可利用性评价 [J].生态环境,2007,16(5):1551-1556.
Lei M,Liao B H,Qin P F.Assessment of bioavailability of heavy metal in contaminated soils with chemical fractionation [J].Journal of Ecology and Enviroment,2007,16(5):1551-1556.(in Chinese)
[22] 刘 霞,邓红侠,张 萌,等.不同解吸剂对污染土娄土中铜铅的解吸动力学研究 [J].西北农林科技大学学报:自然科学版,2011,39(12):159-165.
Liu X,Deng H X,Zhang M,et al.Kinetics of copper and lead desorption from Lou soil as affected by different desorption agents [J].Journal of Northwest A&F University:Natural Science Edition,2011,39(12):159-165.(in Chinese)
[23] Mulligan C N,Yong R N,Gibbs B F.Heavy metal removal from sediments by biosurfactants [J].Journal of Hazardous Materials,2001,85(1/2):111-125.
[24] 李玉红,宗良纲,黄 耀,等.不同有机酸对水稻吸收铅的影响 [J].南京农业大学学报,2002,25(3):45-48.
Li Y H,Zong L G,Huang Y,et al.Effect of different organic acids on lead uptake by rice [J].Journal of Nanjing Agricultural University,2002,25(3):45-48.(in Chinese)
[25] Ochoaloza F J,Artiola J F,Maier R M.Stability constants for the complexation of various metals with a rhamnolipid biosurfactant [J].Environ Qual,2001,30(2):479-485.
[26] Chang S,Wang K,Kuo C,et al.Remediation of metal contaminated soil by an integrated soil washing electrolysis process [J].Soil and Sediment Contamination,2005,14(6):559-569.
[27] Doong R A,Wu Y W,Lei W G.Surfactant enhanced remediation of cadmium contaminated soils [J].Wat Sci Technol,1998,37(8):65-71.
[28] Miller R M.Biosurfactant facilitated remediation of metal contaminated soils [J].Environ Health Persp,1995,103(1):59-62.
[29] Wasay S A,Barrington S F,Tokunaga S.Organic acids to remediate a clay loam polluted by heavy metals [J].Canadian Agricultural Engineering,1998,40:9-15.
[30] 赵保卫,吴咏琪,马婵媛,等.表面活性剂对污染土壤中重金属Cu 的洗脱试验研究 [J].环境科学,2009,30(10):3067-3071.
Zhao B W,Wu Y Q,Ma C Y,et al.Washing copper-contaminated soil using surfactant solutions [J].Environmental Science,2009,30(10):3067-3071.(in Chinese)

