诱导性多能干细胞及其转化医学的信息分析
王 敏,林 杰,孙长凯,许培扬
2006年小鼠诱导多能干细胞(induced pluripotent stem cells,iPSCs)的成功获得以及2007年人类iPSCs的获得改变了科学界对于细胞和机体发育的理解,并因其在药物研发[1]、疾病特异性治疗和再生医学应用[2]的潜力而得到国际高度重视。英国科学家约翰·戈登(John B.Gurdon)和日本科学家山中伸弥(Shinya Yamanaka)由于“成熟细胞可被重编程恢复多能性”的研究成果获得了2012年诺贝尔生理/医学奖。iPSCs已成为国际研究热点,为较全面的把握国际iPSCs科研动态,本研究拟采用文献计量相关方法,分析iPSCs的时间变化、高产国家和机构分布、科研基金资助情况及其热点领域和转化医学研究等,以期为中国开展相关研究及政策制定提供借鉴。
1 材料与方法
1.1 材料
Web of Science(以下简称WOS)数据库由汤森路透集团开发,收录全球8 000多种高质量的期刊,共收录2006年至2013年发表的题名、关键词及摘要中涉及“iPSCs”和“体细胞重编程”相关方面的研究文献2 859篇(检索时间:2013-06-20,限定研究论文、综述、快讯和编者案)。
临床试验数据库(ClinicalTrials)数据库由美国NIH资助开发,共收录184个国家临床试验147 432项,其中iPSCs相关研究18项;Cortellis竞争情报数据库是汤森路透集团开发的用于了解新药研发及市场情报的数据库,共收录药物相关数据52 012条,其中2项iPSCs研究正处于申请临床试验阶段,1项处于临床试验阶段。
1.2 方法
采用文献计量分析方法,利用MS Excel和TDA工具对2 859篇文献进行整理和数据清洗,分析iPSCs的时间、国家、机构分布及其科研基金资助。利于自然语言处理,提取2 859篇文献的题名、关键词和摘要中的高频词,利用TDA对提取的相关词进行数据清洗和共现,采用VOSViewer对56个高频词的共现结果进行聚类分析和可视化展示,挖掘iPSCs研究的主要热点领域。检索ClinicalTrials和Cortellis竞争情报数据库,分析iPSCs相关的转化医学研究。
2 结果
2.1 时间变化
自2006年iPSCs成功诱导后,许多科研机构纷纷开展相关研究。iPSCs研究文献从2006年的3篇增长到2012年的904篇,截至2013年6月iPSCs文献量已达2 859篇,年均增长率达159%,而同期WOS收录文献量年均增长率为4.4%。此外,iPSCs文献占WOS总文献量的比例也由2006年的0.03/10 000增加到2012年的6.76/10 000(图1)。

图1 2006年至2012年国际iPSCs文献量的时间变化Fig 1 International papers of iPSCs published from 2006 to 2012
2.2 国家分布
对开展iPSCs研究人员国别进行分析,2 859篇文献共涉及56个国家,主要集中于北美(1 483篇,51.87%)、亚洲(979篇,34.24%)和欧洲(831篇,29.07%)。在发表文章量排名前10位的国家中(表1),美国居首位,其发文量几乎占到国际iPSCs总文献量的1/2,中国居第3位,其发文量约为美国iPSCs发文量的1/4。
在iPSCs领域,2 859篇文献共被引用77 605次,篇均被引用次数27.14。相对优势指数是各国篇均被引用次数与国际该领域篇均被引用次数的比值。从发表文章量、篇均被引用次数、相对优势指数这3个指标看,日本、美国均居全球首位。

表1 国际发表iPSCs文献数量排名在前10位的国家Table 1 Top 10 countries in international iPSCs area
对发表iPSCs文献的国家科研合作进行分析(图2),美国、英国和德国位于图谱中心位置,是iPSCs国际科研合作的主体;日本、中国及西班牙虽然在发表文章量排名中分别位居第2、第3和第6位,但其位于科研合作图谱的边缘位置,科研合作较少。
2.3 机构分布
在发表文章量前20位的机构中,9家来自美国,4家来自日本。日本京都大学在发表文章量、篇均被引次数和相对优势指数方面均位居首位,体现了其在iPSCs领域的霸主地位。中国科学院和上海交通大学发文量排名进入全球前20位,但从篇均被引次数和相对优势指数看,与国际仍有一定差距(表2)。
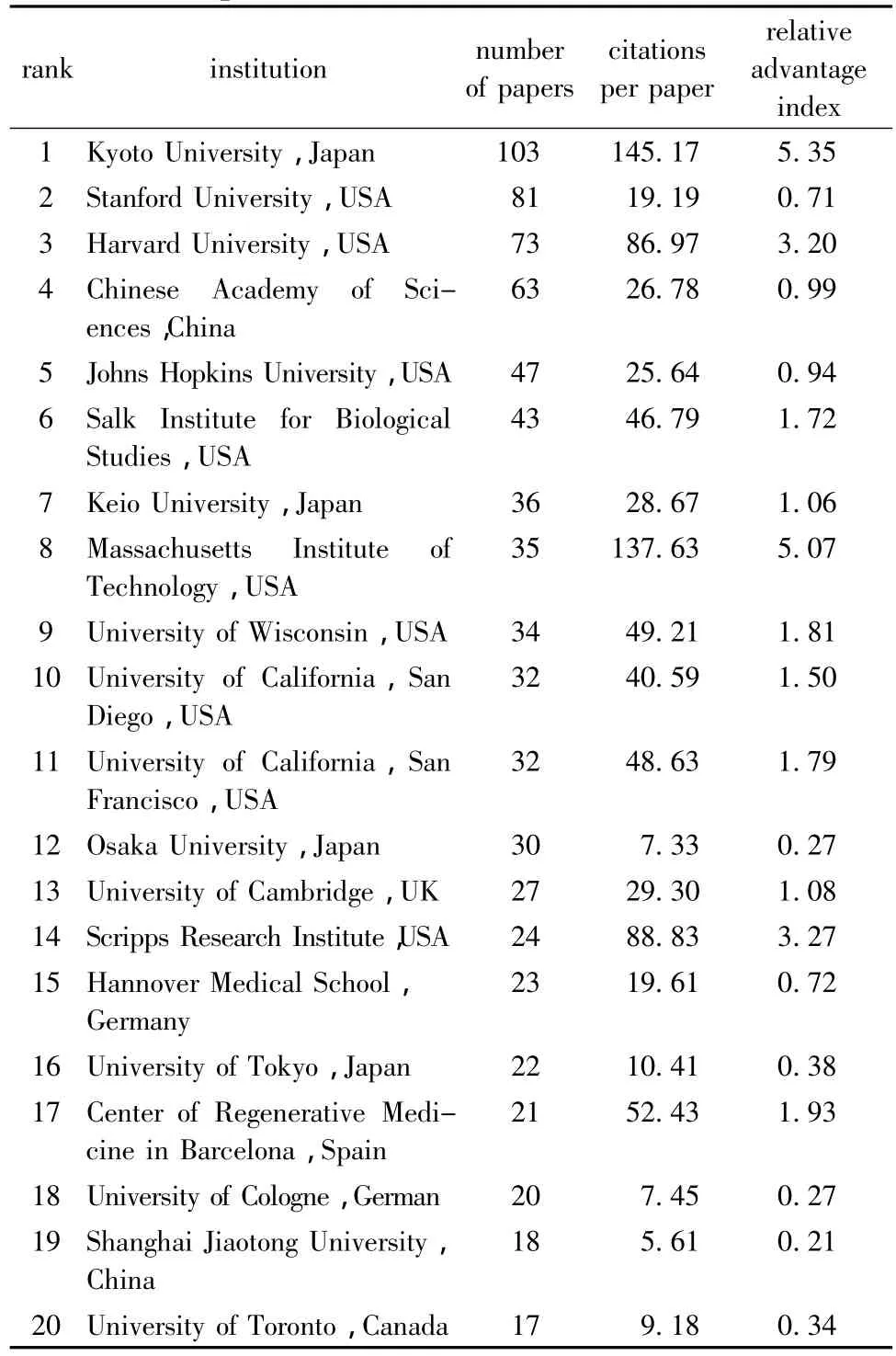
表2 国际iPSCs文献数量排名前20位的机构Table 2 Top 20 institutions in international iPSCs area

图2 iPSCs国际科研合作图谱Fig 2 Cooperative network in international iPSCs area
2.4 科研基金资助
各国在iPSCs领域科研资助逐年增加(图3)。美国国立卫生研究院、日本文部科学省、学术振兴会、科学技术振兴机构和厚生劳动省、中国国家自然科学基金、英国医学研究理事会和惠康基金均对其所在国家iPSCs研究提供了较大比重资金支持(表3)。

图3 国际iPSCs基金资助论文占各年发文量的比例Fig 3 The percentage of funded papers in international iPSCs area

表3 资助iPSCs发表文献排名前10的基金/出资机构Table 3 Top 10 foundations/funding agency in international iPSCs Area
2.5 主要热点研究领域
国际iPSCs研究主要集中在两大方面(图4):
一是影响重编程的因素研究(左侧蓝色和黄色主题)。重编程效率不高及其安全性问题是影响iPSCs由基础向临床转化的基本要素。为提高转化效率及其安全性,科研人员对iPSCs重编程诱导因子及小分子化合物的选择(如OCT4、Sox2和TGF-β等)[3]、安全介导载体体系的建立(如质粒、慢病毒)、重编程过程中的表观遗传学[4]等开展研究。

图4 国际iPSCs研究热点聚类图Fig 4 Cluster mapping of main research works in international iPSCs area
二是iPSCs应用研究(右侧红色和绿色研究主题)。iPSCs为药物研发提供了重要工具,为再生医学提供了广阔前景。目前iPSCs疾病应用领域主要有神经退行性疾病(如阿尔茨海默病、帕金森病、脊髓性肌萎缩症)、心血管疾病(如心肌梗死、长QT综合征)以及糖尿病、视网膜病等[2,5]。
2.6 iPSCs转化医学研究
iPSCs转化研究主要集中在药物研发和再生医学两大领域。
2.6.1 药物研发:药物研发的一个关键问题是制作有效疾病模型。传统制作动物模型一方面建模本身比较困难,同时模型和实际人的疾病也可能相差甚远。直接用患者细胞在体外重编程为疾病特异iPSCs,为药物筛选和疾病特异性治疗提供了重要手段。
目前基于iPSCs已成功建立的疾病模型有神经系统疾病(如帕金森病、脊髓性肌萎缩症、精神分裂症、Rett综合征)、心血管系统疾病(如QT综合征)、遗传性疾病(如LEOPARD综合征、Gaucher病、Huntington病、威尔逊病)及其他疾病(如镰刀型贫血、糖尿病、唐氏综合征)等[6]。利用 ClinicalTrial数据库分析发现,国际上已注册18项与iPSCs有关的研究,如美国佛罗里达大学招募50名高血压患者,抽取静脉血转化为心肌和血管细胞,来研究药物抗高血压效果;以色列Hadassah医学机构招募120名神经疾病患者,利用患者皮肤细胞转化的iPSCs开展疾病模型和药物研发研究。
2012年由10家制药公司及23家学术机构联合开展、涉及11个国家和地区的StemBANCC新药研发项目启动。项目为期5年,旨在招募500名患者建立1 500个iPSCs细胞系,着重开展外周神经系统疾病(尤其疼痛)、中枢神经系统疾病(痴呆症)、神经功能失调性疾病(偏头痛、自闭症、精神分裂症、躁郁症)以及糖尿病的研究,此外还将利用iPSCs寻找药物靶点和生物标记、筛选潜在的治疗药物及开展毒理学实验等[7]。
2.6.2 再生医学:由于iPSCs可分化为不同功能的细胞,为再生医学和组织工程应用提供了可能。
申请及开展人体临床试验的研究。利用Cortellis分析发现,目前有2项iPSCs研究正处于申请临床试验阶段,1项处于临床试验阶段。美国先进细胞科技公司2013年3月向FDA提交临床试验申请,拟利用iPSCs产生的血小板来修复伤口和治疗心血管疾病、血小板减少症;日本京都大学2013年2月向厚生劳动省提交临床试验申请,拟利用患者自体iPSCs产生的多巴胺神经元治疗帕金森病;2013年6月日本厚生劳动省批准日本视网膜研究所应用患者皮肤细胞诱导产生的iPSCs转变为视网膜色素上皮细胞,来抑制与年龄相关的黄斑病变。
组织工程研究。2013年7月,日本研究人员利用3种不同的细胞(肝脏内胚层细胞、间充质干细胞和内皮细胞)合成了人类三维“肝芽”结构[8]。同年8月,美国研究人员利用人类皮肤细胞诱导产生的iPSCs转变为心血管祖细胞,并培养出能自发收缩的人类心脏组织[9]。这些研究代表着人体iPSCs应用的新方向,向寻求制造可移植的器官更迈进了一步。
3 讨论
近年来,干细胞生物学及其临床应用研究领域已取得巨大进步,iPSCs诱导转化及其相关应用研究已成为全球关注的焦点。尤其2007年美国、日本科学家先后利用人成纤维细胞获得iPSCs[10-11],成功避开胚胎干细胞伦理问题后,全球基金资助发表文章的比例由2008年的36%上升至2012年的81%。
一个国家发表文章量反映了其在某领域科研活跃程度,被引用次数一定程度反映了文献质量及被其他学者关注程度,篇均被引用次数可看出在该领域的整体水平,相对优势指数可反映各国科研实力与国际平均水平的关系。从这4个指标看,美国、日本在iPSCs领域科研产出及研究水平处于霸主地位。中国在2006年发布的《国家中长期科学和技术发展规划纲要(2006-2020年)》中提出,“基于干细胞的人体组织工程技术”将成为未来15年中国前沿技术的重点研究领域,目前中国在发文量方面居全球第3位,但篇均被引用次数及相对优势指数低于全球平均水平。
iPSCs由基础向临床应用转化是其研究的必然方向。目前美国、日本已有正处于申请或批准开展人体临床试验的研究,其中2013年6月日本厚生劳动省批准的日本视网膜研究所开展的利用患者视网膜色素上皮细胞来抑制与年龄相关的黄斑病变研究,是国际上首次将iPSCs应用于人体疾病治疗的临床试验,为iPSCs临床应用开辟了先河。但是需要看到的是,iPSCs的临床应用,首先要解决其安全性问题,需要对其稳定性、均一性、致瘤性、毒性和免疫原性等指标进行一系列标准化的检测[12],要解决上述问题,还需不断积累iPSCs安全性、有效性的临床前研究数据。相信在不久的将来,iPSCs的成功应用将对药物研发和再生医学产生重大影响。
[1]Inoue H,Yamanaka S.The use of induced pluripotent stem cells in drug development[J].Clin Pharmacol Ther,2011,89:655-661.
[2]Wu SM,Hochedlinger K.Harnessing the potential of induced pluripotent stem cells for regenerative medicine[J].Nat Cell Biol,2011,13:497 -505.
[3]Rao MS,Malik N.Assessing iPSC reprogramming methods for their suitability in translational medicine[J].J Cell Biochem,2012,113:3061 -3068.
[4]O'Malley J,Skylaki S,Iwabuchi KA,et al.High-resolution analysis with novel cell-surface markers identifies routes to iPScells[J].Nature,2013,499:88 -91.
[5]Oh Y,Wei H,Ma D,et al.Clinical applications of patientspecific induced pluripotent stem cells in cardiovascular medicine[J].Heart,2012,98:443 - 449.
[6]Drews K,Jozefczuk J,Prigione A,et al.Human induced pluripotent stem cells—from mechanisms to clinical applications[J].JMol Med(Berl),2012,90:735 -745.
[7]Gerlin A.Roche,Pfizer,Sanofi Plan$72.7 Million Stem-Cell Bank [EB/OL].[2013-7-30]. http://www.bloomberg.com/news/2012-12-05/
[8]Takebe T,Sekine K,Enomura M,et al.Vascularized and functional human liver from an iPSC-derived organ bud transplant[J].Nature,2013,499:481 -484.
[9]Lu TY,Lin B,Kim J,et al.Repopulation of decellularized mouse heart with human induced pluripotent stem cell-derived cardiovascular progenitor cells[J].Nat Commun,2013,4:2307.doi:10.1038/ncomms3307.
[10]Yu J,Vodyanik MA,Smuga-Otto K,et al.Induced pluripotent stem cell lines derived from human somatic cells[J].Science,2007,318:1917 -1920.
[11]Takahashi K,Tanabe K,Ohnuki M,et al.Induction of pluripotent stem cells from adult human fibroblasts by defined factors[J].Cell,2007,131:861 -872.
[12]Okano H,Nakamura M,Yoshida K,et al.Steps toward safe cell therapy using induced pluripotent stem cells[J].Circ Res,2013,112:523-533.

