血管活性肽优洛可定对自发性高血压大鼠血流动力学影响及与L-型钙通道关系研究
李 鑫,张 迪,郑久明,刘新宇,刘春娜*
(1.辽宁医学院药理学教研室,2.锦州市中心医院,辽宁锦州 121001)
高血压一直是心血管系统疾病研究的热点及前沿。近年来,其患病率不断上升且由此引发的心脑血管病致死率的持续增加,使其越来越受到广泛的重视[1]。长期血压增高可致左室心肌产生重构,左室心肌细胞电生理特性也可发生改变。有研究表明,新型神经血管活性肽优洛可定(urocortin,UCN)在心肌缺血/再灌注损伤中对心肌有保护作用,并可明显而持久的降低血压,但确切的机制目前尚不十分清楚[2-3]。为深入研究UCN对心血管疾病的药理作用,寻找安全而有效的治疗高血压、逆转心室重构的药物,本实验主要应用自发性高血压大鼠(SHR),观察UCN对SHR血流动力学方面、逆转左室重构及相关机制进行研究,从而对UCN在心血管系统中的作用及机制有更深入的了解,为治疗高血压及其他心血管疾病提供新的药物作用靶点。
1 材料与方法
1.1 动物和药品 健康♂ Wistar Tokyo(WKY)大鼠,及spantaneous hypertension rat(SHR)大鼠,体质量(200±20)g,18周龄,由上海中科院动物研究中心提供。优洛可定,sigma公司(美国),批号:171543-83-2。
1.2 实验动物分组 实验动物随机分为6组,包括:WKY对照组(WKY);SHR对照组(SHR):Urocortin小剂量组(UCN1)、中剂量组(UCN2)、大剂量组(UCN3);维拉帕米(VER)组。UCN组及VER组均采用 SHR 大鼠 6 只,Urocortin(1、3、6 μg·kg-1·d-1)每日经尾静脉注射给予,VER(10 mg kg-1·d-1)用三蒸水溶解后每日灌胃给予,用药2周。SHR对照组及WKY组每日经尾静脉注射给予生理盐水0.5 ml。给药期间每日监测各组实验动物尾动脉血压变化情况。
1.3 血流动力学测定 给药2周后,各组实验动物以20% 乌拉坦(1 g·kg-1)麻醉,仰卧位固定,测量术前标准Ⅱ导联心电图并存入电脑,分离左颈总动脉,将压力感受器前端塑料引管自近心端插入左心室,记录血流动力学方面指标,包括平均动脉压(AMP)、左室舒张末压(LVEDP)、左室收缩压(LVSP)以及左心室压力最大变化速率(±dp/dtmax)。
1.4 心肌细胞急性分离 血流动力学实验结束后,立即开胸取出心脏,通过主动脉插管把心脏挂在Langendorff灌流装置上,用台氏液灌流大约30 s;之后用无钙台氏液灌流5~7 min使心脏停跳;用Ⅱ型胶原酶消化液消化15 min,并用无钙台氏液快速冲洗心脏3~5 min停止消化,急性分离心肌细胞。
1.5 全细胞膜片钳记录 将上述一半急性分离的心肌细胞用于记录全细胞跨膜L-型钙通道变化情况,保持电压(holding potential,HP)-40 mv,检测电位(test potential,TP)从-40 mV 到 +50 mV,阶跃10 mV,脉宽200 ms,间隔3 s,以平均膜电流与膜电容之比表示其电流密度(Id),单位为pA/pF。
1.6 自发性高血压大鼠心室肌细胞中荧光钙含量测定 上述急性分离的心肌细胞进行离心,3 000 r·min-1,离心 5 min,弃上清,加入 800 μl普通 PBS缓冲液离心5 min,弃上清,加入300 μl无钙PBS缓冲液离心5 min,再弃去上清,加入10 μl Furo 3,震荡,摇匀,37℃ 水浴15 min之后用流式细胞仪测定心肌细胞内荧光钙含量。
1.7 统计学分析 膜片钳数据采用IGOR软件进行分析。所有数据均以±s表示。两组平均值的比较用非配对t检验。两组以上的均值比较用随机设计的方差分析q检验。
2 结果
2.1Urocortin 对 SHR 大鼠 AMP、LVSP、LVEDP的影响 SHR对照组 AMP、LVSP、LVEDP与 WKY组比较明显升高,二者差异存在显著性(P<0.01)。与SHR对照组比较,UCN 3个剂量组组和VEA组,AMP、LVSP、LVEDP数值均明显降低 (P<0.01)。
2.2 Urocortin对自发性高血压大鼠左室压最大变化速率的影响 +dp/dtmax及-dp/dtmax数值是反映左心室收缩功能的主要指标之一。如Tab 1所示,在SHR对照组中±dp/dtmax数值与WKY组比较明显降低。然而,±dp/dtmax数值在WKY组、UCN组以及VER组都明显升高,与SHR对照组比较差异均存在显著性(P<0.01)。
2.3 UCN对L-型钙通道电流密度影响 与WKY组(3.635±0.156)pA/pF比较,SHR组(5.2967±0.335)pA/pF心室肌细胞L-型钙通道最大电流密度明显升高(P<0.01)。各UCN组及VER(2.465±0.380)pA/pF组与SHR组相比,L-型钙通道最大电流密度明显降低,其中UCN1组降到(4.271±0.392)pA/pF,UCN2 组为(3.087±0.418)pA/pF,UCN3组抑制最为明显,降低到(2.582±0.205)pA/pF(P<0.01),而AST组的电流强度与SHR组比较无明显改变(5.114±0.422)pA/pF(P>0.01)。
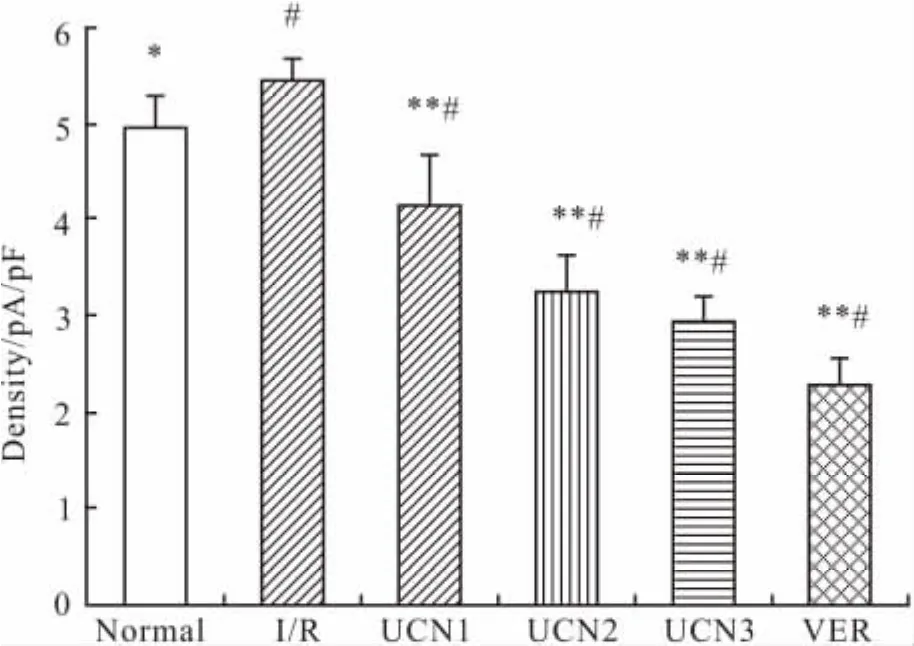
Fig 1 Effects of urocortin on density of SHR cardiomyocytes(±s,n=6)
2.4 细胞内荧光钙含量的测定 流式细胞仪测定急性分离的心室肌细胞内荧光钙含量结果显示,SHR对照组心肌细胞内荧光钙含量(256.1±11.2)mg·L-1明显升高,与 WKY 组(120.5 ±14.4)mg·L-1比较差异存在显著性(P<0.01)。UCN组与VER组中钙含量与WKY组相近。然而,与SHR对照组相比,UCN 组[UCN1,(151.5±12.5)mg·L-1,P<0.01;UCN2,(113.3 ±8.7)mg·L-1,P<0.01;UCN3,(115.6 ±7.3)mg·L-1,P<0.01]与VER组(95.9±5.4)mg·L-1中荧光钙含量明显降低,差异存在显著性。另外,实验中发现,应用CRF-R2受体阻断剂astressin后,再应用urocortin,并不能降低心室肌细胞内荧光钙含量(205.7±12.8)mg·L-1,与SHR对照组比较差异无显著性(P>0.01)。
Tab 1Effects of urocortin on hemodynamic index(±s,n=6)

Tab 1Effects of urocortin on hemodynamic index(±s,n=6)
*P<0.05,**P<0.01 vs SHR group.
WKY SHR UCN1 UCN2 UCN3 VER AMP 69.75 ±2.18 115.4 ±10.63 104.1 ±9.27 69.87±7.58 70.56 ±8.91 72.46 ±6.96 LVSP 118.0 ±4.7 214.5 ±10.4 171.2 ±12.5 123.7 ±9.4 135.8 ±11.6 140.5 ±9.9 LVEDP 0.67 ±0.11 2.51 ±0.59 1.36 ±0.33 0.74 ±0.14 0.87 ±0.25 0.68 ±0.29+dt/dp 8692±351 5621±407 6059±425 6687±394 7746±453 6643±456-dt/dp -8272±269 -4750±473 -5934±652 -6876±619 -7125±542 -7057±539
3 讨论
本实验选用不同剂量UCN,以观察分析UCN对自发性高血压大鼠血流动力学等方面的影响。实验结果显示,SHR组中AMP、LVSP、LVEDP明显升高,同时+dp/dtmax及-dp/dtmax明显降低,表明血流动力学方面损伤明显。应用不同浓度UCN后,AMP、LVSP、LVEDP明显降低,同时 +dp/dtmax及-dp/dtmax明显改善,提示应用UCN能降低血压,解除心肌组织的超负荷状态,不仅心肌力学性质恢复正常,而且也可能为已发生肥厚的心肌组织提供逆转肥厚的可能。

Fig 2 Contents of fluorimetric calcium in cardiomyocytes in SHR(±s,n=6)
实验中发现,UCN能阻断钙离子内流,降低细胞内和线粒体中钙离子浓度,避免细胞内和线粒体钙超负荷;UCN能有效降低心肌细胞内荧光钙离子含量,逆转大鼠心肌纤维化及心肌细胞内Ca2+超负荷现象。随心肌纤维化和细胞内Ca2+超负荷的逆转,不同浓度UCN用药组大鼠左室舒张、收缩功能均明显改善。研究表明,心肌细胞内Ca2+的平衡取决于细胞外Ca2+通过L-型Ca2+通道进入细胞内的速度和数量以及肌浆网(SR)对Ca2+的摄取、储存和释放,而后者更为重要。SR通过钙泵(SERCA-a)、钙泵调节蛋白—受磷蛋白(phospholamban,PLB)等调节心肌细胞内游离Ca2+浓度,维持细胞内钙稳态和正常心肌收缩、舒张功能[4-6]。研究发现肌浆网钙泵活性降低,与Ca2+亲和力降低,因此可导致Ca2+-ATP酶对胞质内游离Ca2+再摄取功能减低,细胞内 Ca2+超负荷,出现心肌舒张功能障碍[7-8]。在心肌细胞膜片钳实验中发现,UCN 能抑制L-型钙通道开放,是抑制心肌细胞内Ca2+超负荷发生的重要分子机制之一。细胞膜L-型钙通道在细胞兴奋-收缩偶联中发挥重要作用,UCN能够阻断血管平滑肌的L-型Ca2+通道,Ca2+减少后引起血管平滑肌去偶联,而产生扩血管效应,进而降低AMP、LVSP、LVEDP,改善血流动力学。UCN减少钙通道开放,减轻钙超载,从而改善高血压大鼠收缩和舒张功能,同时减轻心室肥厚,在高血压及心血管疾病中起保护作用。UCN作为一种新型的小分子血管活性肽,它通过自分泌和/或旁分泌途径,其作用是广泛的,相应作用机制也较复杂[9-10],需要在今后的实验中进一步探讨和研究。
综上所述,在自发性高血压大鼠中UCN将血压降至正常水平时,可消退左室肥厚和改善左室收缩及舒张功能,其可能的机制是UCN与相应的CRF-2R结合,通过抑制L-型钙通道开放,降低心肌细胞内钙离子浓度、减轻钙超载,在高血压等心肌疾病中发挥心肌保护作用。
[1]张根水,罗柳金,侯 宁,等.辛伐他汀对自发性高血压大鼠血管功能作用研究[J].中国药理学通报,2012,28(9):1205-7.
[1]Zhang G S,Luo L J,Hou N,Zhang G P,et al.Effects of chronic treatment with simvastatin on vascular function in spontaneously hypertensive rats[J].Chin Pharmacol Bull,2012,28(9):1205-7.
[2]Scarabelli T M,Pasini E,Stephanou A,et al.Urocortin promotes hemodynamic and bioenergetic recovery and improves cell survival in the isolated rat heart exposed to ischemia/reperfusion[J].J Am Coll Cardiol,2002,40:155-61.
[3]Grandi A M,Imperiale D,Santillo R,et al.Aldosterone antagonist improves diastolic function in essential hypertension[J].Hypertension,2002,40:647-52.
[4]Cai Z,Manalo D J,Wei G,et al.Hearts from rodents exposed to intermittent hypoxia or erythropoietin are protected against ischemiareperfusion injury[J].Circulation,2003,108:79-85.
[5]Bale T L,Hoshijima M,Gu Y,et al.The cardiovascular physiologic actions of urocortinⅡ:acute effects in murine heart failure[J].Proc Natl Acad Sci USA,2004,101:3697-702.
[6]Alsio J,Roman E,Olszewski P K,et al.Inverse association of high-fat diet preference and anxiety-like behavior:a putative role for urocortin2[J].Genes Brain Behav,2009,8(2):193-202.
[7]叶家欣,卢新政,杨晓慧,等.替米沙坦对大鼠动脉血清钙调神经磷酸酶的影响[J].中国药理学通报,2010,26(3):312-6.
[7]Ye J X,Lu X Z,Yang X H,et al.Influence of Telmisartan on peripheral calcineurin of rat with two kidneys one clip hypertension[J].Chin Pharmacol Bull,2010,26(3):312-6.
[8]Brawner J T,Thompson A.Urocortin expression in mouse cochlear nucleus and scarpa’s ganglion[J].Laryngoscope,2008,118(9):1637-44.
[9]Gardiner S M,March J E,Kemp P A,et al.Regional hemodynamic actions of selective corticotropin-releasing factor type 2 receptor ligands in conscious rats [J].J Pharmacol Exp Ther,2005,312:53-60.
[10]Tsotetsi O J,Woodiwiss A J,Netjhardt M,et al.Attenuation of cardiac failure,dilatation,damage,and detrimental interstitial remodeling without regression of hypertrophy in hypertensive rats[J].Hypertension,2001,38:846-51.

