肺硬化性血管瘤的诊断与手术治疗分析
夏宗江
肺硬化性血管瘤(PSH)是临床一种少见的肺部良性肿瘤,其发生率约占肺内良性肿瘤的11%, 患者普遍缺乏临床典型症状, 多在体检或手术中被偶然发现, 易与肺癌相混淆, 误诊率较高[1]。早期正确诊断是确保PSH治疗和预后的关键[2]。本文就2008年6月~2013年6月郑州大学第一附属医院确诊的12例PSH患者的临床特征、影像特点及手术治疗方法进行回顾性分析, 旨在提高本病的诊疗水平。现分析报告如下。
1 资料与方法
1.1 一般资料 选取2008年6月~2013年6月本院收治的12例PSH患者, 男2例, 女10例;年龄28~73岁, 平均(48.7±5.1)岁。4例(33.3%)无症状体检发现肺部阴影, 其余8例出现咳嗽5例(41.7%)、痰中带血2例(16.7%)、咯血1例(8.3%)等非特异性症状。
1.2 诊断方法
1.2.1 病史及体格检查 所有患者均经仔细询问病史, 严格体格检查, 初步判断肿瘤部位、肿瘤大小及性质, 制定出下一步的诊治方案。
1.2.2 影像学检查 X线胸片检查提示边界光滑、无毛刺、与周围组织分界清晰的大小不等团块影;CT扫描发现边界清楚、无或浅分叶、密度均匀、无卫星灶影像(图1), 肿块体积最大4.1 cm×4.6 cm×5.0 cm, 最小1.4 cm×1.5 cm×2.0 cm。发生于右肺5例(41.7%), 其中上叶1例, 中叶2例, 下叶2例;左肺7例(58.3%), 其中上叶2例, 下叶5例;纤维支气管镜检查均未发现新生物, 有2例(16.7%)发现相关肺段支气管外压。
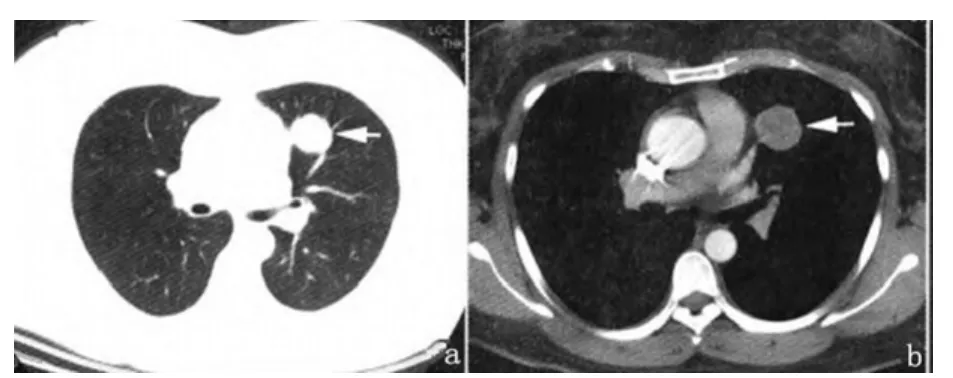
图1 患者女, 45岁。a)行CT扫描显示肺窗示左肺上叶类圆形结节影(←);b)纵隔窗显示密度均匀结节(←)。
1.2.3 细胞学检查 痰细胞学检查均未找到癌细胞;涂片细胞学检查或活检均显示阴性。
1.2.4 术前诊断 术前疑诊为肺癌5例(41.7%), 可疑血管瘤2例(16.7%), 良性瘤2例(16.7%), 炎性假瘤2例(16.7%);转移瘤1例(8.3%)。无一例确诊。
1.3 治疗方法 12例均在全身麻醉下行胸外科手术治疗。其中肿物摘除术4例(33.3%), 肺楔形切除术7例(58.3%), 肺叶切除术1例(8.3%)。均未行肺门及纵隔淋巴结清扫术。对切除肿物作快速冰冻病理检查。术后均重症监护, 常规予以抗生素, 未行放、化疗治疗。
1.4 病理及组织学诊断 12例手术切除标本术后均经病理检查证实为PSH。其中5例(41.7%)经术中冰冻病理检查确诊,其余7例(58.3%)经术后病理及免疫组织化学检查确诊。
1.4.1 肿块 术中见长径2.4~5.8 cm表面光滑、质地软硬适中、圆形或卵圆形肿块, 其中8例(66.7%)包膜完整, 且无周围组织浸润, 4例(33.3%)累及胸膜。
1.4.2 组织学 切开肿块病变呈灰黄或暗红色, 有出血灶。光镜下显示4种标本成分:出血、乳头状突起(表面立方状细胞)、结节(大量致密胶原纤维)及硬化(居于外周, 伴散在出血灶)。肿瘤细胞表面或裂隙可见残存肺泡上皮细胞,少数间质伴有纤维化或钙化。
1.5 统计学方法 数据应用SPSS 13.0统计软件包处理, 计量资料以(±s)表示, 结果采用t检验, 计数资料采用χ2检验,以P<0.05为差异有统计学意义。
2 结果
本组12例均痊愈出院, 住院期间无死亡病例或严重并发症发生。术后随访6~48个月, 均经胸部X线和CT复查,无复发和转移, 生存情况良好。
3 讨论
PSH的组织学起源目前尚未明了, 可能来自于上皮细胞、内皮细胞、肺泡间质间组织和神经内分泌细胞[3]。近年来,有研究指出PSH患者上皮特征性抗原(ESA)TTF0-1与SBP均存在高阳性率表达, 上皮细胞起源说得到了学术界的普遍认可[4]。
而流行病学调查结果显示, PSH好发于女性, 本资料男:女发病率比例约为1:5, 证实了这一点。究其原因, 推测可能与雌、孕激素含量相关。通过长期临床观察发现, PSH生长缓慢, 无明显诱原, 缺乏临床症状, 诊断较困难[5]。本组4例(33.3%)无症状体检发现肺部阴影, 其余8例出现咳嗽5例(41.7%)、痰中带血2例(16.7%)、咯血1例(8.3%)等非特异性症状。但随着影像技术的不断成熟和普及, 临床上对PSH的病理特点有了全新的认识, 诊断率明显提高, 特别是中小血管瘤发现率增多。本组12例X线胸片和CT扫描多表现为边界清楚、无或浅分叶、密度均匀、大小不等的团块影或孤立结节, 肿块体积最大4.1 cm×4.6 cm×5.0 cm, 最小1.4 cm×1.5 cm×2.0 cm, 多发生于肺下叶及周边部位, 但由于本次研究样本数较少, 其病变部位未发现明显的规律性与典型性。
PSH术前较难获得明确的诊断, 本组12例术前痰细胞学检查均未找到癌细胞;涂片细胞学检查或活检均显示阴性。术前疑诊为肺癌5例(41.7%), 可疑血管瘤2例(16.7%), 良性瘤2例(16.7%), 炎性假瘤2例(16.7%);转移瘤1例(8.3%)。无一例确诊。提示PSH与肺癌及其他肺部肿瘤表觋相类似,X线胸片和胸部CT亦缺乏特异性改变, 加上本病在临床上较为罕见, 医师对其临床特征、病理病机认识不够, 易导致误诊、误治。故总结临床实践经验, 加深并本病的认识, 术前仔细询问病史, 严格体格检查及相关影像检查, 十分重要。
由于PSH多位良性, 复发和转移较少(本组仅1例发生转移), 手术切除仍是治疗的主要方法, 患者一旦确诊即考虑开胸探查和手术切除治疗, 其具体术式可根据患者的具体情况选择肺叶全切除或肺楔形切除, 注意尽可能保留肺组织[6]。本组12例均痊愈出院, 住院期间无死亡病例或严重并发症发生。术后随访6~48个月, 均经胸部X线和CT复查, 无复发和转移, 生存情况良好。说明手术治疗PSH的有效性和安全性[7]。
综上所述, PSH多起源于上皮细胞, 好发于女性, 缺乏临床典型症状, 术前明确诊断较为困难。临床诊断应综合评估患者情况、完善体格检查后, 选择合适的影像学检查(X线胸片、胸部CT)方案。手术切除是治疗PSH的有效手段, 以尽可能保留肺组织为原则。
[1]胡爱民,高远,郑华,等.肺硬化性血管瘤26例临床分析.中华临床医师杂志(电子版), 2011(14): 4271-4273.
[2]王建.肺硬化性血管瘤行肺叶切除术的临床价值分析.中国医学创新, 2013, 10(16): 20-21.
[3]高金莉,董志广.肺硬化性血管瘤临床病理及免疫表型特征分析.中国现代医生, 2013, 51(5): 92-93.
[4]方宏洋,何闯,黄学全,等.肺硬化性血管瘤CT表现特征.中华临床医师杂志(电子版), 2012, 6(4): 182-183.
[5]陈淮,曾庆思,周洁,等.肺硬化性血管瘤的影像征象与病理分析.中国医学影像学杂志, 2012, 20(4): 268-271.
[6]袁刈.肺硬化性血管瘤临床病理分析.按摩与康复医学, 2011,2(14): 90-91.
[7]何闯,刘云,郑伟,等.肺硬化性血管瘤临床病理及CT诊断.中华实用诊断与治疗杂志, 2012, 26(5): 417-418.

