5-(2-氯乙基)-6-氯-1,3-二氢-吲哚酮的合成
徐大国 蒋成君
(1.浙江尖峰海洲制药有限公司,浙江 台州 317000;2.浙江科技学院生物与化学工程学院,浙江 杭州 310023)
5-(2-氯乙基)-6-氯-1,3-二氢-吲哚酮(简称吲哚酮)是合成最新非典型广谱抗精神病药齐拉西酮的关键中间[1]。目前报道的吲哚酮的合成方法主要有4条路线:1)以6-氯吲哚-2,3-二酮为原料,经水合肼还原得到6-氯-1,3-二氢吲哚-2-酮,与氯乙酰氯化进傅-克酰化反应制得5-(2-氯乙酰基)-6-氯-1,3-二氢吲哚-2-酮,再经三乙基硅烷/三氟乙酸还原得到吲哚酮[2,3]。 2)5-(2-氯乙酰基)-6-氯-1,3-二氢吲哚-2-酮可先经硼氢化钠还原为5-(2-羟基氯乙基)-6-氯-1,3-二氢吲哚-2-酮,再经三乙基硅烷/三氟乙酸还原得到吲哚酮[4-6]。3)以对氯邻硝基甲苯为原料,与草酸二乙酯缩合,再经水解,经双氧水氧化脱羰、铁粉/盐酸还原,在浓硫酸中高温闭环,再经三乙基硅烷/三氟乙酸还原得到吲哚酮[7,8]。4)以2,4,5-三氟硝基苯为原料,通过氟取代得到2,4-二氟-5-氟基苯,与丙二酸二乙酯钠缩合后,经水解得羧酸,再以氯化亚砜、甲醇酯化得到甲酯,在雷尼镍催化下氢化闭环得到,经溴化锂/硼氢化钠水解还原,最后利用三苯膦、四氯化碳进行氯化反应得到吲哚酮[9-11]。本文以2,5-二氯硝基苯为原料,与丙二酸二乙酯反应,经成环、酰化、还原合成吲哚酮。
1 实验部分
1.1 合成路线
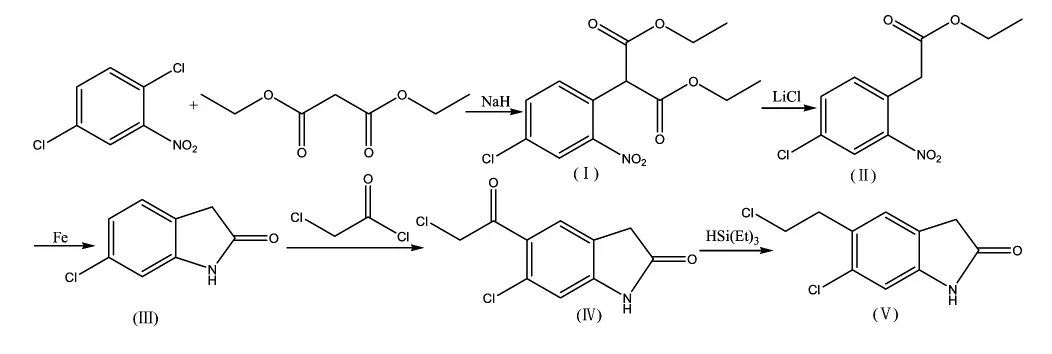
1.2 仪器与试剂
仪器MERCURYDLUS-400型核磁共振仪,美国 Varian公司、Nicolet Avator370傅立叶变换红外光谱仪 美国Vicolet公司、RY-1型熔点仪 天津市分析仪器厂、RE-52CS型旋转蒸发仪 上海泰益医疗仪器设备有限公司、DW-3型电子恒速搅拌器、SHZ-D(III)型循环水式真空泵 巩义市予华仪器有限责任公司。
试剂:石油醚、乙酸乙酯为CP,其它试剂均为工业品。
2 结果与讨论
2.1 4-氯-2-硝基苯基丙二酸二乙酯 (Ⅰ)的合成
将150 mL N,N-二甲基甲酰胺与15 g 50%的钠氢混合,搅拌下滴加43 g丙二酸二乙酯,滴加时温度不超过50℃,滴完后慢慢升温至100℃,搅15 min,停止加热,冷却至室温,滴加25 g 2,5-二氯硝基苯与25 mL N,N-二甲基甲酰胺组成的溶液,滴完后慢慢升温至100℃,并在100℃反应60 min,减压回收N,N-二甲基甲酰胺,剩余物中加入200 g冰水,搅拌,加入200 mL乙酸乙酯,静置分出有机相,水相再加入50 mL乙酸乙酯提取一次,合并有机相,饱和食盐水洗涤一次,加入30 g无水硫酸镁干燥4 h,有机相浓缩得4-氯-2-硝基苯基丙二酸二乙酯(Ⅰ)40 g,收率 97.5%。1H NMR (d-D2O,δ:7.91 (s,1H,ArH),7.87 (d,1H,ArH),7.55 (t,1H,ArH),7.42(t,1H,ArH),3.66(t,4H,CH2NCH2),3.46(t,4H,CH2NCH2)
2.2 4-氯-2-硝基苯基乙酸乙酯(Ⅱ)的合成
将上步所得Ⅰ与7.5 g氯化锂、150 mL N,N-二甲基甲酰胺混合搅拌,升温到100℃,反应3 h后减压回收N,N-二甲基甲酰胺,剩余物中加入200 g冰水,搅拌,加入200 mL乙酸乙酯,静置分层,分出有机相,水相再加入50 mL乙酸乙酯提取,合并有机相,饱和食盐水洗涤一次。加入30 g无水硫酸镁干燥4 h,过滤,有机相浓缩后得4-氯-2-硝基苯基乙酸乙酯 (Ⅱ)26.2 g,收率85.0%。
2.3 6-氯-1 3-二氢-吲哚-2-酮(Ⅲ)的合成
将上步Ⅱ与冰醋酸150 mL混合,分批加入还原铁粉17 g,加完后再在100℃反应2 h,过滤,滤液蒸干后加入100 mL乙酸乙酯,然后以10%的盐酸100 mL洗涤一次,再以饱和食盐水洗涤一次,无水硫酸镁干燥4 h后,浓缩有机相至干得6-氯-1 3-二氢-吲哚-2-酮 (Ⅲ)17 g,收率94.4%。
2.4 5-2-氯乙酰基 -6-氯-1,3-二氢 吲哚酮(Ⅳ)的合成
上述Ⅲ、无水氯化铝35 g、二硫化碳500 mL混合搅拌,再加入氯乙酰氯13 g,加热至回流 10 h,减压回收二硫化碳至干,剩余物中加入30 g冰水,搅拌2 h后过滤,滤层以水洗涤得5-2-氯乙酰基 -6-氯-1,3-二氢 吲哚酮 (Ⅳ)20.0 g,收率80.8%。
1H NMR (d-Acetone),δ:7.70 (s,1H,ArH),7.06 (s,1H,ArH),4.90 (s,2H,ClCH2),3.57(s,2H,CH2);IR (KBr,cm-1):3461,3305,1715,1862。
2.5 5-(2-氯乙基)-6-氯-1,3-二氢-吲哚酮(Ⅴ)的合成
取7 gⅣ,加入100 g三氟醋酸,再加入8 g三乙基硅烷,20℃~30℃反应20~24 h,加入90 g水,搅拌3 h后过滤,滤液回收三氟醋酸,滤层以少量水洗涤用甲醇或乙醇重结晶,得淡黄色成品,5-(2-氯乙基)-6-氯-1,3-二氢-吲哚酮(Ⅴ)5.5 g,收率 78.5%。 mp;218℃~221℃。1H NMR (d-DMSO),δ:10.456 (s,1H,NH),7.260(s,1H,ArH),6.828(s,1H,ArH),3.78 (t,2H,ClCH2),3.469 (s,2H,COCH2,3.086(t,2H,CH2); IR(KBr,cm-1):3224,3077,2956,1712。
[1]成碟,阳凯,刘磊.盐酸齐拉西酮合成路线图解[J].中国医药工业杂志,2012,43(8),709-712.
[2]Reddy M S,Venkatraman S,Rajan S T,et al.Process for the preparation of 5-(2-(4-(1,2-benzisothiazol-3-yl) -1-piperazin-1)ethyl)-6-chloro-1,3-dihydro-2H-indol-2-one-hydro-chloride (ziprasidone hydrochloride)and its intermediate:US,20090047354[P].2009-02-19.
[3]Lowe J A,Nagel A A.Aryl piperazinly-(C2 or C4)alkylene heterocyclie compounds having neuroleptic activity:US,4831031[P].1989-05-16.
[4]Zanon Jacopo,Martini Oscar.A process for the preparation of ziprasidone:EP,1787990[P].2007-05-23.
[5] Giller Eari Lacux,Jr Harrigan edmund.Treatment of bipolar disoroers and associated symptoms: US,2004100957[P].2004-11-25.
[6]郭希,杨艺虹,张绗,等.5-(2-氯乙酰基)-6-氯-吲哚酮的合成[J].武汉工程大学学报,2010,32(11):25-27.
[7]Durgesh V Nadkarni,James F.Hallissey.Improved process for the preparation of 6-chloro-5-(2-chloroethyl)oxindole[J].Org.Process Res.Dev.,2008,12(6):1142-1145.
[8]Mukund K Gurjar,Murugaiah A M S,Dandepally srinivasa reddy.A new route to prepare 6-chloro-5-(2-chloroethyl)oxindole[J]Org.Proc.Res.Dev.,2003,7(3):309-312.
[9]Zanon Jacopo,Martini Oscar.A process for the preparation of ziprasidone:EP,1787990[P].2007-05-23.
[10]Romano Steven Joseph,Anxiety Treatments with ziprasidone:WO,2004100955[P].2004-11-25.
[11]Romano Steven Joseph,Swift Rachel Heather.Method for enhancing cognition using ziprasidone:WO,2004100956[P].2004-11-25.

