HPLC-MS/MS法测定血浆中莫西沙星浓度
梅和坤,王 睿,白 楠,梁蓓蓓,曹 江,汶 柯,唐铭婧,刘银萍,李 悦,王 瑾(解放军总医院药物临床研究中心,北京 100853)
莫西沙星属第四代新型氟喹诺酮类广谱抗菌药物,通过抑制细菌的DNA螺旋酶A亚单位和拓扑异构酶IV的活性,阻断DNA的复制,发挥杀菌作用。莫西沙星对革兰阳性菌、革兰阴性菌、厌氧菌及非典型病原体(支原体、衣原体、军团杆菌)均有良好的抗菌活性,具有组织渗透力强、生物利用度高、作用时间长、不良反应少等优点[1-2]。目前,血浆中莫西沙星浓度的测定主要采用紫外、荧光或质谱法[3-11],而紫外法存在灵敏度低、干扰大和选择性差等问题,质谱法[4,10]测定采用固相萃取技术,固相萃取操作繁琐,成本高。本实验采用直接沉淀蛋白法,快速、灵敏、简捷,为莫西沙星的临床药动学、生物利用度研究及临床患者的血药浓度测定提供方法学基础。
1 材料与方法
1.1 药品、试剂与仪器
莫西沙星标准品(批号:Y0000703,European Pharmacopeaia,纯度96.1%);左氧氟沙星(内标,批号:130455-201005,中国食品药品检定研究院);甲醇为色谱纯。
空白血浆来自解放军总医院输血科。
Agilent 1200高效液相色谱仪,Agilent 6410B型三重四极杆串联质谱仪,配有电喷雾离子源(ESI);METTLER XS105型天平(瑞士METTLER-TOLEDO公司);SIGMA-15PK型高速低温离心机(德国SIGMA公司)。
1.2 色谱条件
色谱柱为ZORBAX EP-C18柱(2.1 mm×100 mm,3.5 μm,美国Agilent公司);流动相为甲醇-水(45∶55,v/v),其中水相中含0.05%甲酸;流速为0.2 mL·min-1;进样量为10 μL;柱温为25 ℃。
1.3 质谱条件
离子源:电喷雾离子化源(ESI),正离子模式;毛细管电压:4000 V;温度:350 ℃;雾化器(N2)压力:35 psi;干燥气流速为10 L·min-1;扫描方式为多重反应离子监测(MRM);莫西沙星的离子对为m/z402.1→m/z384.3,毛细管出口电压为120 V;碰撞能量:CE = 25 ev;左氧氟沙星的离子对为m/z362.4→m/z261.2,毛细管出口电压为135 V;用于分析的离子碰撞能量:CE = 35 ev。
1.4 标准溶液的配制
莫西沙星标准溶液的配制 精密称取莫西沙星标准品26.01 mg(纯度为96.1%,含莫西沙星25 mg),置于25 mL容量瓶,以甲醇定容,配成1 mg·mL-1储备液,避光、恒温4 ℃保存。取该储备液以甲醇依次倍比稀释,配成莫西沙星浓度为50,100,250,500,2000,5000,10 000 ng·mL-1的系列标准溶液,4 ℃保存备用。
左氧氟沙星标准溶液的配制 精密称取左氧氟沙星对照品25.5 mg(纯度为98%),置于25 mL容量瓶中,加甲醇溶解并稀释至刻度,摇匀,即得1 mg·mL-1的内标储备液,取该储备液以甲醇倍比稀释至1 µg·mL-1,作为内标工作溶液置于4 ℃冰箱保存待用。
1.5 血浆样品处理方法
将样品从-80 ℃冰箱取出,室温下自然融化。精密吸取血浆样品100 μL置于洁净EP管中,依次加入1µg·mL-1内标储备液100 µL和甲醇溶液800 µL,涡旋混匀1 min后,在14 000 r·min-1下离心10 min,取上清液200 μL置于一洁净EP管中,加入200 μL去离子水,涡旋混匀,取上清液进样分析。
2 结果
2.1 质谱分析
莫西沙星和左氧氟沙星的子离子扫描图见图1和图2。
2.2 方法的专属性
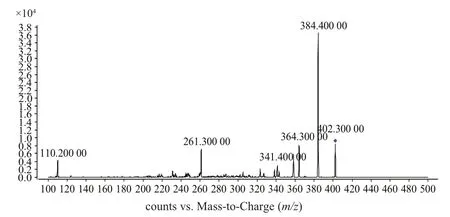
图1 莫西沙星的子离子扫描图Fig 1 Product ion scan of moxifloxacin
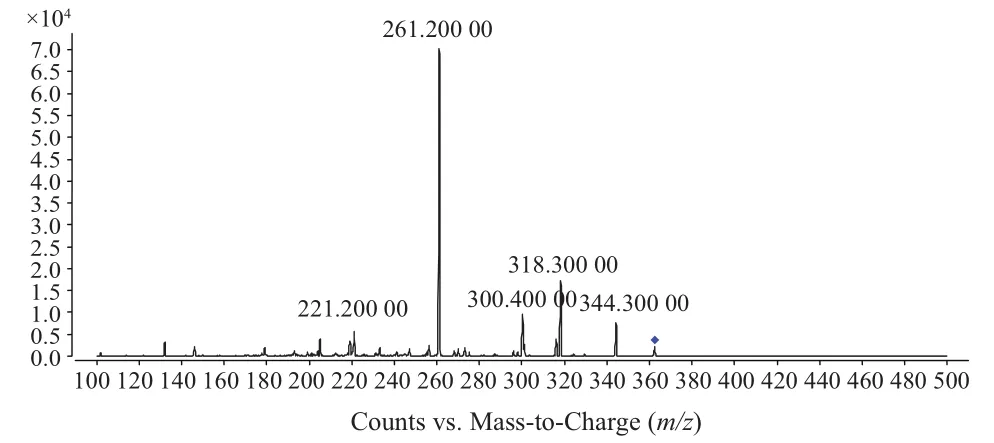
图2 左氧氟沙星的子离子扫描图Fig 2 Product ion scan of levofloxacin
取6名不同健康人的空白血浆,除不加内标外,按照“血浆样品处理方法”处理,得到典型图谱A。取一定浓度的莫西沙星血浆溶液加入内标,按照“血浆样品处理方法”处理,得到色谱图B、C。结果表明,空白血浆中的内源性物质不干扰莫西沙星和内标左氧氟沙星的测定。具体见图3。
2.3 标准曲线和定量范围
取空白血浆100 μL加入莫西沙星系列标准溶液,配制成相当于血浆浓度为50,100,250,500,2000,5000,10 000 ng·mL-1的血浆样品,按“血浆样品处理方法”项下操作,取10 μL进样分析,记录色谱图,以莫西沙星浓度与内标浓度之比为横坐标,系列标准血浆样品测得的莫西沙星的峰面积与内标左氧氟沙星的峰面积比值为纵坐标,采用最小二乘法进行线性回归[12]求得标准曲线回归方程为Y= 2.614 6X+ 0.043 6(r= 0.996),线性范围50 ~ 10 000 ng·mL-1。
2.4 定量下限
将50 ng·mL-1的莫西沙星待测物进行6样本分析,并根据当日的标准曲线求得每一样本的浓度,求得莫西沙星的浓度均值为(56.45±1.91) ng·mL-1,RSD为3.38%,准确度为106.9% ~ 113.6%。结果表明,该方法下莫西沙星待测物浓度定量下限可达到50 ng·mL-1。
2.5 精密度和提取回收率

图3 血浆中莫西沙星和内标左氧氟沙星的色谱图
分别配制浓度为100,500,5000 ng·mL-1的血浆样品作为质控(QC)样品,按血浆样品处理方法项操作,每一浓度平行配制、测定6个样本,连续测定3 d,根据当日的标准曲线计算QC样品浓度,计算准确度和精密度。结果表明,该方法的准确度为90.04% ~109.79%,日内精密度RSD ≤3.81%,日间精密度RSD ≤4.26%,说明该方法的准确度和精密度良好。具体见表1。
精密吸取空白血浆100 μL置于一洁净EP管中,依次加入1 µg·mL-1内标储备液100 μL和甲醇溶液800 μL,涡旋混匀1 min后,再加入莫西沙星系列标准溶液100 μL,混匀,在14 000 r·min-1下离心10 min,取上清液200 μL置于一洁净EP管中,加入200 μL去离子水,涡旋混匀,取上清进样分析。与当日高、中、低三个浓度的QC样本的峰面积比较,计算提取回收率。结果表明,高、中、低三个浓度下药物的提取回收率比较稳定。具体见表2。
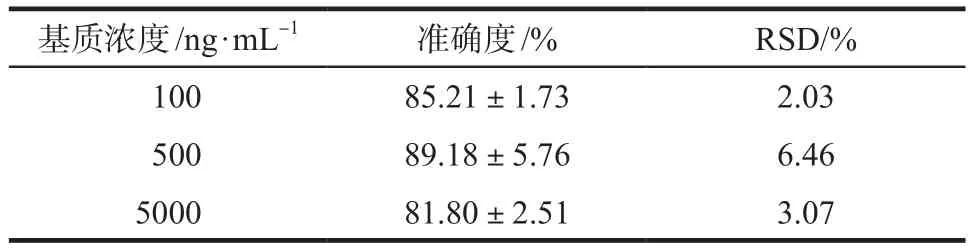
表2 基质效应对莫西沙星血药浓度的影响. n = 9Tab 2 The matrix effect on the concentration of moxifloxacin in human serum. n = 9
2.6 样品稳定性
制备莫西沙星低、中、高三个浓度(100,500和5000 ng·mL-1)的血清样品,分别在室温放置4 h、-80℃反复冻融3次和处理后样本自动进样器放置24 h考察其稳定性,结果表明样品在上述条件下均稳定(RE <9.61%)。
2.7 基质效应
精密吸取去离子水100 μL置于一洁净EP管中,依次加入莫西沙星系列标准溶液100 μL,1 µg·mL-1内标储备液100 μL和甲醇溶液700 μL,涡旋混匀1 min后,再加入莫西沙星系列标准溶液,混匀,在14 000 r·min-1下离心10 min,取上清液200 μL置于一洁净EP管中,加入200 μL去离子水,涡旋混匀,取上清液进样分析,与当日高、中、低三个浓度的QC样本的峰面积比较。结果表明基质效应不影响药物的测定。
3 讨论
本实验建立了HPLC-MS/MS法检测人血浆中莫西沙星浓度的方法,特异性强,定量下限低,灵敏度高,并且本方法较以往的检测方法有如下改进:(1)标准曲线各浓度点与检测系统检测性能相适应,线性良好,定量准确。实验过程中将定量上限提高到10 000 ng·mL-1,定量下限降至50 ng·mL-1,在实际应用中能够检测到给药后5个半衰期以上的药物浓度,完全符合应用中的定量需要,绝大多数药物浓度均落在该线性范围内。(2)在对含药血浆的前处理方面,高效液相法可以采用沉淀能力强的高氯酸、三氟乙酸等沉淀剂,而HPLC-MS/MS法往往不能使用此类沉淀剂,甲醇乙腈沉淀法对血浆的稀释倍数较大,同时为了减小基质效应往往也需要加大稀释倍数,这样甲醇直接沉淀法就可能难以达到所要求的定量下限。本实验改进了血浆前处理方法,未采用以往文献报道的液质联用法的固相萃取[4,10],高效液相色谱法的液液萃取[13-14]和氮气吹干法[11],而采用甲醇直接沉淀法,改进血浆处理方法后,减少了定量操作的步骤,使定量更准确,血浆处理更方便,处理效率更高,提高实际测定样品浓度的实用性。该方法可以高效、准确的测定血浆中莫西沙星的浓度,适用于莫西沙星药代动力学测定。

表1 莫西沙星血浆浓度测定方法的精密度和提取回收率. n = 18Tab 1 Precision and recovery of moxifloxacin in human serum. n = 18
[1] 汪忠亚,靳玉香. 盐酸莫西沙星治疗呼吸道感染40例临床分析[J]. 中国现代实用医学杂志,2007,6(11):10-11.
[2] 宋秀杰,刘又宁,梁蓓蓓,等. 20种抗菌药物对肺炎链球菌的体外抗菌活性研究[J]. 中国药物应用与监测,2010,7(1):20-23.
[3] Ba BB, Etienne R, Ducint D,et al. Determination of moxifloxacin in growth media by high-performance liquid chromatography[J].J Chromatogr B Biomed Sci Appl, 2001, 754(1): 107-112.
[4] Vishwanathan K, Bartlett MG, Stewart JT. Determination of moxifloxacin in human plasma by liquid chromatography electrospray ionization tandem mass spectrometry[J]. J Pharm Biomed Anal, 2002, 30(4): 961-968.
[5] Liang H, Kays MB, Sowinski KM. Seperation of levofloxacin,ciprofloxacin, gatifloxacin, moxifloxacin, trovafloxacin and cinoxacin by high-performance liquid chromatograph: application to levofloxacin determination in human plasma[J]. J Chromatogr B Analyt Technol Biomed Life Sci, 2002, 772(1): 53-63.
[6] 张吟,陈一农,陈文发. 固相萃取-高效液相色谱法测定人血清中莫西沙星浓度[J]. 中国医院药学杂志,2007,27(4):481-483.
[7] 贺德辉,余江平. RP-HPLC法测定人血浆中莫西沙星的浓度[J]. 中国药房,2007,18(32):2506-2507.
[8] 张翠莲,Nightingale CH, Nicolau DP. 反相HPLC测定培养基中莫西沙星含量的方法学研究[J]. 中国药学杂志,2004,39(9):699-701.
[9] Wagenlehner FM, Kees F, Weidner W,et al. Concentrations of moxifloxacin in plasma and urine, and penetration into prostatic fluid and ejaculate, following single oral administration of 400 mg to healthy volunteers[J]. Int J Antimicrob Agents, 2008, 31(1):21-26.
[10] 陈漪,施家威,金米聪. 液相色谱-离子阱质谱法测定人血清中莫西沙星浓度[J].中国临床药学杂志,2009,18(6):345-348.
[11] 林光勇,朱光辉,王增寿,等. 反相高效液相色谱法测定莫西沙星的人体血药浓度[J]. 中国药业,2011,20(22):42-44.
[12] 钟大放. 以加权最小二乘法建立生物分析标准曲线的若干问题[J]. 药物分析杂志,1996,16(5):343-346.
[13] 徐玉红,李玉珍,唐利娟,等. HPLC法测定莫西沙星血药浓度[J]. 中国临床药学杂志,2010,19(3):149-152.
[14] 朱加银,阚歆,楼旦,等. HPLC检测大鼠血浆中莫西沙星浓度及其药动学研究[J]. 中国现代应用药学,2011,28(8):759-762.

