禾谷丝核菌原生质体的制备及遗传转化体系的探索
任向荣, 李 伟, 孙海燕, 陈怀谷, 于汉寿
(1.南京农业大学生命科学院,江苏 南京 210095;2.江苏省农业科学院植物保护研究所,江苏 南京 210014)
由禾谷丝核菌(Rhizoctonia cerealis Van der Hoeven)引起的小麦纹枯病已成为中国小麦主产区小麦高产、稳产的重要威胁[1-2]。该菌通常以菌丝和菌核的形态习居于土壤中,自然条件下只发现无性世代[3-5]。国内外学者对禾谷丝核菌的田间快速检测、化学防治及生物防治等方面做了大量研究[6-10]。但对该病原菌的流行学、基因之间的交流和致病机理等方面的研究远远落后于其他一些病原菌,其主要原因是到目前为止尚未建立禾谷丝核菌有效的遗传转化体系,而制备高质量的与原始菌株遗传背景一致的原生质体是进行遗传转化的前提。
原生质体是通过机械破碎或酶消解细胞壁而得到的裸露细胞,质膜为细胞质和外界环境间的唯一屏障,对外界环境的变化非常敏感。因此,原生质体常被用于生化分析[11]、细胞壁再生过程观察[12]、发育学的研究[13]、标记蛋白质的细胞定位[14]、蛋白质间关系的分析[15-16]以及染色体的改造[17]等。另外,原生质体是丝状真菌细胞融合、诱变育种和遗传转化等的理想材料。随着分子生物学技术在植物病理学研究中的不断应用和发展,真菌的遗传转化越来越受到重视。目前,已有100多种真菌实现了遗传转化[18]。丝状真菌的遗传转化方法有多种,包括PEG-原生质体转化和农杆菌介导转化法 (Agrobacterium tumefaciens mediated transformation,ATMT)等。
有研究结果表明多核的立枯丝核菌(R.solani)原生质体再生菌株无论从形态、生长速率还是分子水平上都与原始菌株有较大差异[19],这一现象对进一步的遗传转化等是不利的。禾谷丝核菌细胞为双核,其原生质体的制备方法,再生菌株与原始菌株之间是否存在差异,以及遗传转化体系的构建等研究目前尚未见报导。本研究采用多种酶消解菌丝细胞壁的方法探索禾谷丝核菌原生质体的制备方法,比较原生质体再生菌株和原始菌株在形态、生长速率、致病力及遗传组成等方面的差异,并利用PEG-原生质体的转化和土壤农杆菌介导的转化等方法尝试构建禾谷丝核菌的遗传转化体系,为进一步研究其致病机理奠定基础。
1 材料和方法
1.1 原生质体制备
采用4种方法获得用于酶解的菌丝:(1)直接从PSA平板上挑取一定量的禾谷丝核菌R0301菌株(该菌株分离自江苏省南京市,是强致病力菌株,保藏于江苏省农业科学院植物保护研究所)的气生菌丝;(2)参照张颖等[20]的方法并有所改进,将挑取的气生菌丝在研钵中研磨后转移到液体TB3(0.3%酵母浸提物,0.3%蛋白胨和20%蔗糖)培养基中,28℃再培养44 h左右,过滤收集菌丝并用无菌水冲洗;(3)参照Liu等[21]的获取菌丝的方法,在铺有玻璃纸的PDA平板上28℃培养44 h左右,将玻璃纸连菌碟一起放进无菌水中从而分离获得菌丝;(4)PDA平板上培养3~5 d后,在菌落边缘打菌碟,转移到铺有玻璃纸的PDA平板上28℃再培养44 h左右,用金属小勺柄或接种针刮取菌丝,该方法是对第3种方法的改良。
将收集得到的菌丝等量转入含2%消化酶(分别是纤维素酶、裂解酶、崩溃酶及溶壁酶)的10 ml 0.7 mol/L渗透压稳定剂(山梨醇、蔗糖、NaCl和MgSO4)中,在30℃、120 r/min条件下酶解。每间隔0.5 h进行显微镜检测。酶解0.5~3.0 h后,3层过滤膜过滤收集原生质体。
1.2 原生质体的计数、核染色及再生
用STC(15%山梨醇,0.7%CaCl2·H2O和5%Tris/HCl,pH 8.0)溶解原生质体沉淀,进行一定的稀释后计数;用10 μg/ml核荧光染料Hoechst 33258(碧云天生物技术研究所产品)对菌丝和原生质体处理5 min后,荧光显微镜(Nikon ECLIPSE E400)下观察核染色情况;将一定量的原生质体加入已冷却至室温的RM(1.6 mol/L蔗糖,0.4%干酪素水解物,0.4%酵母浸提物和0.85%的琼脂粉)固体培养基中,轻轻混匀后倒平板;28℃培养6~7 d后,挑取再生培养基上的单菌落,转接到PDA平板上28℃培养,观察它们与原始菌株在形态和生长速率等方面的差异。
1.3 原生质体再生菌株致病力测定
试验选小麦品种扬麦158,将种子播种于装有灭菌土、口径为8 cm的塑料盆钵中,每钵播25粒,并盖上灭菌土。在人工气候培养箱内20℃培养,待小麦长到二叶期在茎基部接入直径为0.5 cm的菌碟,每个菌株3个重复,接种14 d后参照 Lipps等[22]的分级标准调查病情。计算病情指数,使用DPSv7.05软件对病情指数进行统计分析。
1.4 菌株DNA的提取及AFLP差异分析
从200个再生菌株中随机选取100株进行差异分析。菌株DNA的提取采用快速基因组DNA试剂盒(东盛生物公司产品)。AFLP试验方法参照Ceresini等[23]和 Vos 等[24]的方法,预扩增引物为EcoRI+G(5'-GACTGCGTACCAATTCG-3')和 MseI+G(5'-GATGAGTCCTGAGTAAG-3'),选择性扩增引物为 EcoRI+GT(5'-GACTGCGTACCAATTCGT-3')和 MseI+GT(5'-GATGAGTCCTGAGTAAGT-3')。AFLP选择性扩增产物变性后在6%聚丙烯酰胺凝胶上电泳分离,硝酸银染色显影。
1.5 遗传转化
1.5.1 测定禾谷丝核菌对潮霉素B的敏感浓度设置潮霉素 B 浓度梯度为:0 μg/ml、25 μg/ml、50 μg/ml、75 μg/ml、100 μg/ml,测定禾谷丝核菌对潮霉素B的敏感浓度。
1.5.2 PEG-原生质体转化 按照方法1.1获得的原生质体沉淀,1 ml STC溶解,转入2 ml离心管中;5 000 r/min离心5 min,弃上清;STC悬浮原生质体;转化液:90 μl STC+10 μl质粒 +100 μl原生质体,使原生质体数达到104个、105个和106个,轻轻混匀,室温静置20 min;加1 ml SPTC(STC+50%PEG)轻轻混匀,室温静置20 min;加5 ml TB3混匀,18℃,121 r/min摇培过夜;第2 d倒制平板,先加入一定体积的潮霉素B到RM培养基中,再倒入过夜的转化液,混匀后倒平板;倒置,28℃培养。
1.5.3 土壤农杆菌(A.tumefaciens)AGL-1介导的转化 从新鲜培养的LB平板上挑取土壤农杆菌AGL-1的单菌落,接种到5 ml液体LB培养基中(含50 μg/ml的卡那霉素),200 r/min,28 ℃ 下过夜培养;将 200 μl上述培养液转移到5 ml含50 μg/ml卡那霉素的诱导培养基(IM)中,OD600值约为0.15,加入乙酞丁香酮(AS),浓度为 200 μg/ml,28 ℃ 培养5~6 h使OD600达到0.5~0.6;用TB3悬浮原生质体沉淀;取100 μl经处理的农杆菌菌液和100 μl原生质体,使原生质体数达到104个、105个和106个,混匀后轻轻涂布在含200 μg/ml乙酞丁香酮(AS)的IM固体平板上的玻璃纸上,22℃黑暗培养48 h;把玻璃纸倒置转移到选择培养基上(PSA+50 μg/ml潮霉素 B+400 μg/ml头孢氨苄 +60 μg/ml链霉素),28℃黑暗培养。
2 结果与分析
2.1 菌丝获得方法及细胞壁消解酶和渗透压稳定剂处理对原生质体制备的影响
在以溶壁酶为消解酶和以0.7 mol/L NaCl为渗透压稳定剂的酶解体系中,4种不同方法获得的菌丝用于制备原生质体,得到的原生质体量有很大差异。方法(1)得到的原生质体数为1 ml 101~102个;方法(2)得到的原生质体数为1 ml 0.5×102~1.5×102个;方法(3)制备的原生质体数达到1 ml 5×103~104个;方法(4)得到的幼嫩菌丝制备原生质体时,原生质体数达到1 ml 106个。而其他消解酶和渗透压稳定剂组合的体系中,没有观察到原生质体出现。
采用方法(4)得到的幼嫩菌丝,用0.7 mol/L NaCl为渗透压稳定剂,浓度为2.0%的4种消化酶处理,每间隔0.5 h检测。直到酶解3 h时,在含崩溃酶、纤维素酶和裂解酶3种酶的酶解体系中都没有原生质体出现;而在溶壁酶的酶解体系中,0.5 h就发现大量的原生质体(图1)。结果表明,在本试验条件下,崩溃酶、纤维素酶和裂解酶3种酶对禾谷丝核菌的细胞壁几乎没有消解能力而不能释放原生质体,溶壁酶对禾谷丝核菌的细胞壁的降解起着非常重要的作用。
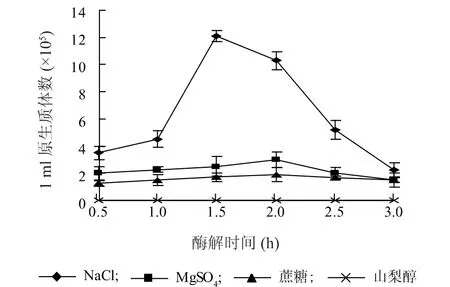
图1 4种渗透压稳定剂对原生质体释放的影响Fig.1 Four kinds of osmotic pressure stabilizers influencing protoplast liberation
同种酶的作用下,不同的渗透压稳定剂对原生质体的释放有很大影响。崩溃酶、纤维素酶和裂解酶3种酶分别在山梨醇、蔗糖、NaCl和MgSO4中酶解直到3 h都没有原生质体出现。在以溶壁酶为细胞壁消解酶的作用体系中,直到酶解3 h,以山梨醇为渗透压稳定剂的体系中原生质体的释放量几乎都为零;而以蔗糖、NaCl和MgSO4为渗透压稳定剂的体系中,酶解0.5 h 1 ml原生质体数已达到105。以蔗糖渗透压稳定剂的体系中原生质体释放量低于以NaCl和MgSO4为渗透压稳定剂的体系(图1)。无机盐渗透压稳定剂NaCl和MgSO4比有机物渗透压稳定剂更有利于禾谷丝核菌原生质体的释放,NaCl尤其明显。酶处理1.5 h时,在NaCl为渗透压稳定剂的体系中,1 ml原生质体数达到106,但随着时间的延长原生质体数并没有增加反而越来越少(图1)。长时间的酶处理可能对原生质体有一定的破坏作用。因此,禾谷丝核菌菌丝酶解处理1.5 h左右是收集原生质体的相对最佳时间。
2.2 原生质体核染色、萌发及再生
所制备的原生质体纯化浓缩后镜检呈规则的球形,大小不一,并有聚集现象(图2a)。原生质体在液体培养基中的萌发类似孢子,先长出牙管,慢慢伸长,长到一定长度开始分叉并小于90°(图2b~d)。在再生培养基(RM)上培养7 d后长出单一分散的白色菌落(图2e)。对菌丝及原生质体细胞核进行染色和镜检,观察到菌丝及原生质体的细胞核数目一致,均为双核(图3)。把再生培养基上(图2e)的单一菌落转接到普通PDA培养基上生长,随机挑取部分原生质体再生菌株,共200株,再生菌株在形态上与原始菌株没有差异。

图2 禾谷丝核菌的原生质体萌发及再生Fig.2 The protoplast germination and regeneration of R.cerealis
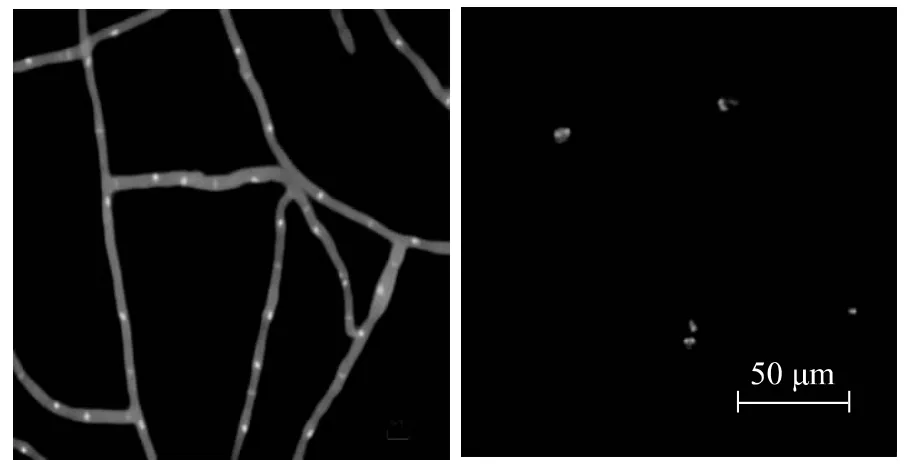
图3 菌丝及原生质体的细胞核Hoechst 33258染色Fig.3 Nuclear staining of hypha and protoplasts with Hoechst 33258
2.3 再生菌株的生长速率及致病力分析
从100个再生菌株(用于后面的AFLP试验)中随机挑选15株,在PDA培养基上培养,测定其生长速率,结果表明原生质体再生菌株与原始菌株的生长速率无显著差异(图4a)。对原始菌株R0301和15个再生菌株进行了致病力测定,病情指数调查结果表明,15个禾谷丝核菌再生菌株的致病力没有明显差异,与原始菌株的差异也不显著(图4b)。
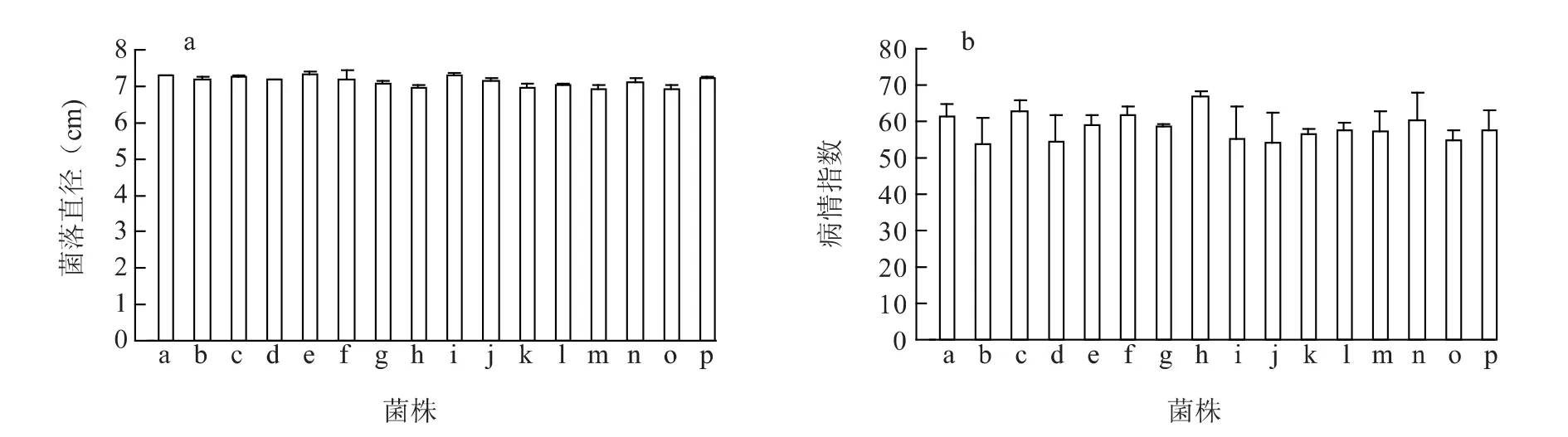
图4 禾谷丝核菌原始菌株和原生质体再生菌株生长速率(a)及致病力(b)比较Fig.4 The growth rate(a)and pathogenicity(b)of regenerated and original strains of R.cerealis
2.4 原生质体再生菌株的AFLP差异分析
随机选择了100个再生菌株,提取其基因组DNA。通过AFLP分子标记差异分析共得到20个片段,分布在50 bp~2 000 bp之间。电泳结果表明再生菌株之间不存在多样性,再生菌株与原始菌株之间也没有差异(图5)。

图5 原生质体再生菌株的AFLP分子标记Fig.5 The analysis of protoplast regenerated strains by AFLP
2.5 遗传转化体系
潮霉素B浓度为50 μg/ml时,对禾谷丝核菌的抑制率已经达到了100%(表1)。因此,选择转化子的潮霉素B浓度为50 μg/ml。原生质体数量为104个、105个和106个时,分别采用 PEG-原生质体转化和农杆菌介导的原生质体转化,多次尝试没有获得转化子。针对禾谷丝核菌的遗传转化,通过多次探究没有成功建立其遗传转化体系。
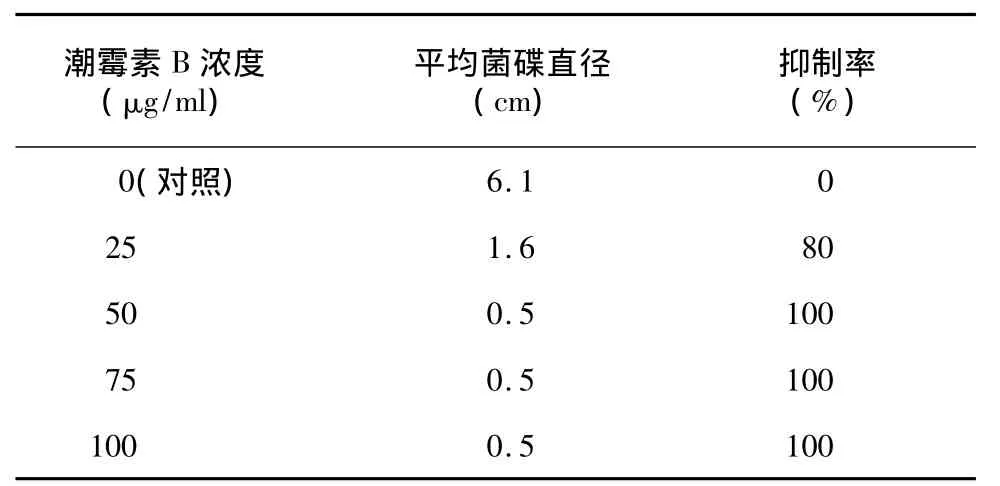
表1 禾谷丝核菌R0301对潮霉素B的敏感性Table 1 The susceptibility of R.cerealis R0301 to hygromycin B
3 讨论
原生质体是遗传转化、融合、诱变育种、观察细胞壁构成及了解内生病毒传播情况等的理想材料,有助于探索丝状真菌的生化特性及遗传学及生理学研究等[19]。原生质体的制备与很多因素有关,如酶的种类、渗透压稳定剂、酶作用时间及温度和菌龄等。
一般处于对数生长期的真菌幼嫩菌丝用于酶解制备原生质体效果最好[25]。幼嫩菌丝的获得对原生质体的制备也非常关键。禾谷丝核菌在实验室培养条件下不产生孢子[3],所以不能像大多数产孢真菌那样通过孢子萌发获得幼嫩菌丝。培养长时间之后的气生菌丝质地过密且已老化,去壁较难不适于原生质体的制备。采用从铺有玻璃纸的PDA培养基上获得的幼嫩菌丝用于酶解,可得到大量的原生质体,并且方法简单易行,耗时短。
原生质体的制备很大程度上依赖细胞壁消解酶的选择,而细胞壁消解酶的选择又和该菌的细胞壁组成相关。禾谷丝核菌是一种担子菌,它的细胞壁主要成分是葡聚糖、几丁质等[26]。纤维素不是禾谷丝核菌的细胞壁主要成分,单一的纤维素酶对禾谷丝核菌几乎没有消化作用。崩溃酶(Driselase)和裂解酶(Lysing enzymes)是立枯丝核菌的高效细胞壁消解酶[21],在本试验中,它们对禾谷丝核菌的细胞壁几乎都没有消解作用。禾谷丝核菌同立枯丝核菌在胞壁组成上可能存在一定的差异。
渗透压稳定剂可维持原生质体细胞膜内外的渗透压平衡,也影响酶的活性[27]。不同的细胞壁消化酶在作用同一底物时,也会有它们适宜的渗透压稳定剂。崩溃酶、纤维素酶和裂解酶3种酶分别在山梨醇、蔗糖、NaCl和MgSO44种渗透压稳定剂中都没有原生质体出现,溶壁酶在本试验所用的渗透压稳定剂(除山梨醇外)中都有大量原生质体产生。无机盐渗透压稳定剂特别是NaCl更有利于禾谷丝核菌原生质体的产生。
显微镜下的原生质体呈规则的球形,并存在聚集现象。有研究结果表明原生质体通过细胞壁的残余物质粘连,这一现象有助于原生质体的细胞壁复原及再生。Liu等[28]制备立枯丝核菌的原生质体,恢复原生质体细胞壁可制成人工孢子。在实验室培养条件下,禾谷丝核菌也不产生任何有性或无性孢子,利用立枯丝核菌制造人工孢子的原理,可能得到禾谷丝核菌的人工孢子,用于筛选禾谷丝核菌的杀菌剂和抗病小麦品种等。另外,根据产孢菌单孢分离的方法,进行单原生质体分离[29],可以对不产孢的禾谷丝核菌进行菌株纯化等应用。
制备得到的原生质体与原始菌株的遗传背景一致是进行遗传转化、诱变育种等的前提。Thomas等[19]的研究结果表明立枯丝核菌的原生质体不仅细胞核数目不同,而且生长速率和形态都有很大差异。本研究通过细胞核染色发现,制备的禾谷丝核菌原生质体都以双核的形式存在,与原始菌株菌丝细胞内的核数目一致。再生菌株的形态、生长速率等与原始菌株也没有差异。AFLP分子标记检测的结果表明,禾谷丝核菌原生质体再生菌株之间遗传组成可能没有差异,并且与原始菌株之间也可能无差异。致病力测定结果也显示原生质体再生菌株与原始菌株之间无显著性差异。以上结果表明,禾谷丝核菌再生菌株和原始菌株之间几乎不存在差异,我们的制备体系没有改变原始菌株的遗传背景。本研究建立的体系可制备大量的与原始菌株遗传背景一致的原生质体,可用于转化及诱变等一系列遗传操作。
本试验通过多次尝试PEG-原生质体转化和土壤农杆菌介导的转化,没有成功建立禾谷丝核菌遗传转化体系。可能原因是,在实验室培养条件下,禾谷丝核菌不产生任何有性或无性孢子,并且细胞内存在双核等[3]。这些现象对禾谷丝核菌遗传转化体系的建立都是非常不利的。另一方面,已经尝试的转化方法或转化条件可能不适合禾谷丝核菌的转化。关于丝核菌属的遗传转化体系,国内外很少有成功的报道,主要原因是很难发现丝核菌的有性态生活阶段,无性态又不产生任何孢子,同时丝核菌属的细胞内存在多核现象等[3]。对于丝核菌属的遗传转化体系的建立有待于人们继续研究。
[1]LIU H X,XIN Z Y,ZHANG Z Y.Changes in activities of antioxidant-related enzymes in leaves of resistant and susceptible wheat inoculated with Rhizoctonia cerealis[J].Agricultural Sciences in China,2011,10(4):526-533.
[2]孔凡彬,李卫海,徐瑞富,等.井冈霉素与其他几种杀菌剂混配对禾谷丝核菌的室内毒力[J].江苏农业科学,2011,39(1):129-131.
[3]GONZÁLEZ G V,PORTAL O M A,SUSAN V R.Biology and systematics of the form genus Rhizoctonia [J].Spanish Journal of Agricultural Research,2006,4(1):55-79.
[4]SHARON M,KUNINAG S,HYAKUMACHI M,et al.Classification of Rhizoctonia spp.using rDNA-ITS sequence analysis supports the genetic basis of the classical anastomosis grouping [J].Mycoscience,2008,49:93-114.
[5]陈 莹,李 伟,张晓祥,等.我国北纬33度地区小麦纹枯病病原菌组成及其致病力研究[J].麦类作物学报,2009,29(6):1110-1114.
[6]GUOY P,LI W,SUN H Y,et al.Detection and quantification of Rhizoctonia cerealis in soil using real-time PCR [J].Journal of General Plant Pathology,2012,78(4):247-254.
[7]陈怀谷,方 正,陈厚德,等.小麦纹枯病的分子检测[J].植物保护学报,2005,32(3):261-265.
[8]SCHROEDER K L,PAULITZ T C.Root diseases of wheat and barely during the transition from conventional tillage to direct seeding[J].Plant Disese,2006,90(9):1274-7253.
[9]HAMADA M S,YIN Y N,MA Z H.Sensitivity to iprodione,difenoconazole and fludioxonil of Rhizoctonia cerealis isolates collected from wheat in China [J].Crop Protection,2011,30:1028-1033.
[10]WEN C Y,YIN Z G,WANG K X,et al.Purification and structural analysis of surfactin produced by endophytic Bacillus subtilis EBS05 and its antagonistic activity against Rhizoctonia cerealis[J].The Plant Pathology Journal,2011,27(4):342-348.
[11]SHEAHAN M B,ROSE R J,MCURDY D W.Actin-filament-dependent remodeling of the vacuole in cultured mesophyll protoplasts[J].Protoplasma,2007,230:141-152.
[12]YANG X Y,TU L L,ZHU L F,et al.Expression profile analysis of genes involved in cell wall regeneration during protoplast culture in cotton by suppression subtractive hybridization and macroarray[J].Journal of Experimental Botany,2008,59(13):3661-3674.
[13]PETERSSON S V,JOHANSSON A I,KOWALCZYK M,et al.An auxin gradient and maximum in the Arabidopsis root apex shown by high-resolution cell-specific analysis of IAA distribution and synthesis[J].The Plant Cell,2009,21:1659-1668.
[14]LOOCK B V,MARKAKIS M N,VERBELEN J P,et al.Highthroughput transient transformation of Arabidopsis roots enables sys-tematic colocalization analysis of GFP-tagged proteins[J].Plant Signaling and Behavior,2010,5(3):261-263.
[15]WU F H,SHEN S C,LEE L Y,et al.Tape-Arabidopsis Sandwich-a simpler Arabidopsis protoplast isolation method[J].Plant Methods,2009,5(16):1-10.
[16]FARACO M,SANSEBASTIANO G P D,SPELT K,et al.One protoplast is not the other[J].Plant Physiology,2011,156:474-478.
[17]HARA S,JIN F J,TAKAHASHI T,et al.A further study on chromosome minimization by protoplast fusion in Aspergillus oryzae[J].Molecular Genetics and Genomics,2012,287:177-187.
[18]高 静,李艳波,柯希望,等.PEG介导的苹果腐烂病菌原生质体转化[J]. 微生物学报,2011,51(9):1194-1199.
[19]THOMAS E,PAKALA S,FEDOROVA N D,et al.Triallelic SNP-mediated genotyping of regenerated protoplasts of the heterokaryotic fungus Rhizoctonia solani[J].Journal of Biotechnology,2012,10:1-7.
[20]张 颖,王 刚,王美南.小麦全蚀病菌原生质体制备的条件及再生菌株的致病性[J].微生物学杂志,2005,25(5):29-32.
[21]LIU T H,LIN M J,KO W H.Factors affecting protoplast formation by Rhizoctonia solani[J].New Biotechnology,2010,27(1):64-69.
[22]LIPPS P E,HERR L J.Etiology of Rhizoctonia cerealis in sharp eyespot of wheat[J].Phytopathology,1982,72:1574-1577.
[23]CERESINI P C,SHEW H D,VILGALYS R J,et al.Genetic diversity of Rhizoctonia solani AG-3 from potato and tobacco in North Carolina[J].Mycologia,2002,94(3):437-449.
[24]VOS P,HOGERS R,BLEEKER M,et al.AFLP:a new technique for DNA fingerprinting [J].Nucleic Acids Research,1995,23:4407-4414.
[25]韩文霞,刘 迪,陈二方,等.氦氖激光、紫外复合诱变天麻素产生菌华根霉LN-A的原生质体[J].微生物学通报,2009,36(12):1849-1855.
[26]GARCIA S B.Cell wall chemistry,morphogenesis,and taxonomy of fungi[J].Microbiology,1968,22:87-108.
[27]李伶俐,严 红,李兴红,等.甘蓝枯萎病菌原生质体的制备与再生条件的优化[J].中国农学通报,2011,27(10):203-207.
[28]LIU T H,LIN M J,KO W H.Development of artificial conidia for ecological studies of Rhizoctonia solani in soil[J].New Biotechnology,2011,28(1):86-91.
[29]QU P,ARATANI A,SYOJI T,et al.Use of single-protoplast isolates in the study of the mating phenomena of Rhizoctonia solani(Thanatephorus cucumeris)AG-1 IC and IA [J].Mycoscience,2008,49:132-137.

