北豆腐中铜残留量的评价
李佩然,阮长青,杨南
(黑龙江八一农垦大学食品学院,大庆 163319)
豆腐作为一种美食有着悠久的历史,具有良好的保健功效,素有“植物肉”的美称[1]。近年来,在食品生产过程中,违法添加非食用物质和滥用食品添加剂已成为影响我国食品安全的突出问题[2]。很多不法商家在利益的驱使下,使用工业氯化镁代替食品氯化镁作为豆腐的凝固剂,或者过量地使用食品级氯化镁[3]。长期食用而造成重金属中毒损害健康[4]。目前,北豆腐中氯化镁引入重金属的检测方法至今未见报道。
铜作为典型的重金属元素具有一定的毒性,长期食用铜含量超标的水及食品,铜就会积累在肝脏中,产生“肝痘”铜代谢及溶血和贫血等疾病[5],因此,铜可作为部分食品重金属污染的监控指标。国家规定食品中铜含量的限量标准为10 mg·kg-1[6]。目前,食品中微量铜的测定方法有①原子吸收火焰光谱法[7-8],其敏度高、选择性好,但仪器昂贵、分析费用高;②分光光度法[9-10],其操作简便、精密度良好、仪器价格低,易于普及;③其他方法,如利用传感器测定铜等[11-12]。
采用二乙基二硫代氨基甲酸钠法(分光光度法)和火焰原子吸收光谱法,通过检测梯度添加食品级与工业级氯化镁豆腐中的铜残留量,确定其来源,为利用铜、铅、砷等重金属残留量综合评价过量使用食品级氯化镁或违法使用工业级氯化镁提供研究基础。
1 材料与方法
1.1 材料与试剂
黄豆(东北非转基因大豆),食品级氯化镁(MgCl2·6H2O含量46%;连云港益康佳化工有限公司),工业级氯化镁(MgCl2·6H2O含量44.5%;天津长芦汉沽盐场有限责任公司),铜标准溶液(天津光复精细化工研究所),铜试剂(天津大茂试剂厂),硝酸,高氯酸,四氯化碳,柠檬酸铵,乙二胺四乙酸二钠,硫酸,氨水,酚红指示剂,所用试剂等级均为分析纯及去离子水。
1.2 仪器设备
紫外可见光分光光度计(T6,北京普析通用有限公司),马弗炉,电加热板,原子吸收分光光度计(GC-112A,北京普析通用有限公司)。
1.3 标准溶液的配制
分光光度法:用0.5%硝酸溶液将1.0 mg·mL-1铜标准溶液逐级稀释至浓度为 0、5.0、10.0、15.0、20.0和 25.0 μg·mL-1。铜标准溶液(1.0 mg·mL-1)用 0.5%的硝酸溶液多次稀释,定容到10mL容量瓶,使铜标准使用液的终浓度分别为 0、5.0、10.0、15.0、20.0 和25.0 μg·mL-1,测定吸光度,并绘制标准曲线。
选择最佳的仪器参数制作火焰原子吸收光谱法的标准曲线,铜标准使用液的终浓度分别为0、1.0、2.0、4.0、6.0、8.0 和 10.0 μg·mL-1,测定吸光度,并绘制标准曲线。
1.4 样品溶液的制备
分别称取10份150 g黄豆加入1000mL水浸泡12 h后制浆,滤除豆渣。凝固剂添加量分别为黄豆干物质重量的2.4%、2.6%、2.8%、3.0%和3.2%,预先配制成浓度为8%工业级与食品级氯化镁水溶液,在豆浆85℃时点浆,凝乳后将其破脑、压榨,制成豆腐[13-14]。同时,收集压榨的黄浆水待测定。
参照铜检测标准GB/T 5009.13-2003制备样品[15],略作修改,方法如下。准确称取2.0 g试样,精确至0.0001 g,置于100mL瓷坩埚中,加入10mL浓硝酸,密封静置24 h,小火蒸干,继续加热炭化至无烟后,移入马弗炉中,500±25℃灰化4 h,取出放冷,再加5mL硝酸浸湿灰分,小火蒸干,再移入马弗炉中2 h,冷却后取出,如此反复灰化直至试样无炭粒为止,以1mL硝酸(1+4)溶解4次,移入10.0mL容量瓶中,用水定容备用。
1.5 样品的测定
分光光度法:采用二乙基二硫代氨基甲酸钠法检测,于试样消化液、试剂空白液和铜标准液中,各加入5mL柠檬酸铵,乙二胺四乙酸二钠溶液和3滴酚红指示剂,混匀,用氨水(1+1)调至红色。各加2mL铜试剂溶液和10.0mL四氯化碳,剧烈振摇2min,静置分层后,四氯化碳层经脱脂棉滤入2 cm比色杯中,以四氯化碳调节零点,于波长440 nm处测吸光度值[15]。
试样在紫外-可见分光光度计扫描到铜元素在440 nm处有最大吸收峰,在此波长下测定试样的吸光度值,计算公式如下:

式中:X 为试样中铜的含量,mg·kg-1;A1为试样消化液中铜的吸光度值;A2为空白液中铜的吸光度值;m为试样的质量,g;V1为试样消化液的总体积,mL;V2为测定所用试样消化液体积,mL。
原子吸收光谱法:将处理后的样液、试剂空白液和标准溶液分别导入调至最佳条件火焰原子化器进行测定。仪器选择最佳工作条件:波长324 nm,灯电流 3.0 mA,狭缝宽度 0.4 nm,乙炔流量 12.0 L·min-1,空气流量 15.0 L·min-1,燃烧头高度 6.0 mm[15]。
试样在原子吸收火焰光度计扫描铜元素在324 nm处有最大吸收峰,在此波长下测定试样的吸光度值,计算公式如下:

式中:X 为试样中铜的含量,mg·kg-1;A1为样品中铜的吸光度值;A2为空白中铜的吸光度值;V为试样处理后的总体积,mL;m为试样的质量。
1.6 方法的加标回收试验与精密度试验
回收率试验:准确称取3份一定量的豆浆样品,分别加入 Cu2+浓度为 1.0 mg·kg-1的铜标准溶液1、5mL和10mL,按照上述试验的方法分析测定Cu残留量,进行加标回收实验[16]。
精密度试验:分别在7份样品中添加1mL 1.0 mg·kg-1铜标准使用液[17],按上述实验方法进行分析测定,验证该方法的精密度和准确性。
1.7 方法的最低检出限
在最佳的实验条件下,对试剂空白溶液进行11次测定,用3倍空白样品吸光度值的标准偏差除以标准曲线斜率即为本方法的最低检出限[18]。
2 结果与分析
2.1 标准曲线的绘制
分光光度法对应的吸光度值分别为0.00、0.144、0.276、0.420、0.588 和 0.768,铜含量在 0.8~21.5 mg·L-1范围内,浓度与吸光度值呈现良好的线性关系,回归方程为Y=0.0304X-0.0137,R2=0.9965。
原子吸收光谱法对应的吸光度值为0.000、0.018、0.038、0.078、0.117、0.153 和 0.208,铜含量在 0.01~0.155 mg·L-1范围内,浓度和吸光度值呈现良好的线性关系,回归方程为Y=0.0203X-0.0026,R2=0.9967。
2.2 样品的测定
本实验对样品制作过程中的铜含量进行追踪分析,点样前豆浆铜含量为3.75 mg·kg-1,食品级氯化镁中铜含量1.8 g·kg-1,工业级氯化镁中铜含量4.0 g·kg-1,分别用分光光度法和原子吸收光谱法检测豆腐以及黄浆水铜含量,结果如表1所示。

表1 样品中铜含量分析结果(mg·kg-1)Table 1 The copper content analysis results of the samples(mg·kg-1)
表1中凝固剂的添加量在2.4%~3.2%,由分光光度法的检测结果可知,氯化镁添加量在铜含量随着豆腐及黄浆水中两种氯化镁添加量的增加而逐渐增大;梯度添加食品级、工业级氯化镁的豆腐中铜含量范围分别为 7.15~9.08 mg·kg-1和 10.79~12.87 mg·kg-1,黄浆水中分别为 2.69~2.72 mg·kg-1和 3.38~3.45 mg·kg-1,添加工业级氯化镁的豆腐和黄浆水中铜含量偏高。通过单因素方差分析所得的P值可知,豆腐中随着两种凝固剂添加浓度的增加,导致铜含量明显上升,P<0.0001差异极显著。而黄浆水中的铜含量并没有因氯化镁添加量而升高,P>0.05差异不显著。
测定结果表明,当食品级氯化镁添加量大于3.2%时,豆腐中铜的残留量才会超出国家限量;而工业级氯化镁添加含量大于2.4%时,铜残留量就超出了国家限量。为达到蛋白变性而使豆腐凝固的目的,工业氯化镁的添加量应该高于2.4%,即由杂质引入的铜的含量必然超标。因此,根据豆腐中氯化镁添加量的要求以及铜含量的测定结果,可以评价豆腐中是否存在过量使用食品级氯化镁甚至使用工业氯化镁作为凝固剂。
2.3 精密度实验
验证该方法的精密度和准确性,结果见表2。

表2 精密度实验Table 2 The experiment of precision
由表2可知光光度法试验铜含量结果相对标准偏差为9.43%,原子吸收光谱法试验铜含量结果相对标准偏差为3.59%,两种方法的精密度良好,均可满足试验要求。
2.4 加标回收试验
加标回收实验结果见表3。

表3 加标回收率Table 3 The recovery rate of copper
由表3可知,分光光度法测得铜的回收率在95.0%~103.4%之间,其平均回收率为98.5%;原子光谱法测得铜的回收率在99.0%~100.6%之间,其平均回收率为99.7%,两种方法结果可靠,均可用于铜残留量的分析。
2.5 最低检出限的测定
本方法的最低检出限结果见表4。
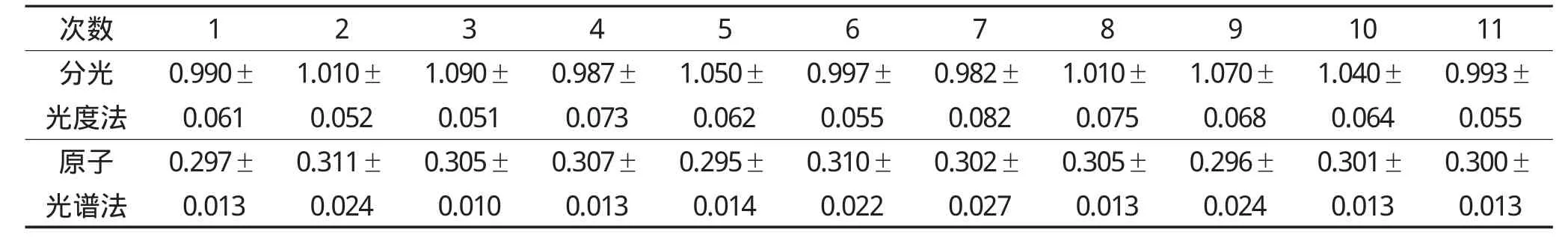
表4 最低检出限Table 4 Theminimum detection limit of method
计算出分光光度法铜的检出限为0.106 mg·kg-1,以1.00 g样品消化后定容至10mL,样品最低检出限为 1.06 mg·kg-1;原子吸收光谱法的检出限为0.00504 mg·kg-1,以 1.00 g样品消化后定容 10mL,样品最低检出限为0.0504 mg·kg-1。
3 讨论
3.1 北豆腐制作工艺过程中,凝固剂氯化镁的添加量直接影响豆腐成型及其品质,凝固剂添加量占黄豆干物质重的2.4%~3.2%之间,豆腐凝固成型具有良好的口感;超出此梯度区间范围直接影响豆腐品质,凝固剂添加量小于2.4%,豆腐水嫩不成易型;凝固剂添加量大于3.2%,豆腐过老无口感,试验失去意义。因此试验选取2.4%、2.6%、2.8%、3.0%和3.2%凝固剂添加量为测定指标,检测豆腐中工业氯化镁与食品氯化镁之间的差异,探索检测违法添加物工业氯化镁的分析方法,同时对黄浆水中铜残留量进行对比分析。
3.2 试验以分光光度法和原子吸收光谱法进行检测分析,并通过回收率、精密度和最低检出限等试验进行验证。试验结果表明,两种方法均满足试验的分析要求并取得良好的结果。由于原子吸收光谱法所用仪器昂贵,分析费用较高,一般的检测机构及食品生产厂家尚不具备此条件;而分光光度法操作简便,仪器检测费用较低,适用于大多数检测机构,食品生产企业应用分光光度法进行检测更具有现实可行性。
3.3 试验分别检测梯度添加工业氯化镁与食品氯化镁制成豆腐中铜的残留量,通过对比分析发现:添加食品氯化镁和工业氯化镁的豆腐,检测值差异显著;黄浆水中铜残留量的检测结果差异较小,二者基本上呈现持平的趋势,因此试验选择检测豆腐中铜残留量区别添加工业氯化镁与食品氯化镁。试验结果分析表明,由于豆腐中蛋白质的凝结作用,导致黄浆水中重金属铜残留量相对较低,大部分铜离子都被阻隔在豆腐当中,不能随着压力的作用随黄浆水流出,因此黄浆水中铜含量差异微小,豆腐中铜含量差异显著。
3.4 研究结果表明,添加食品级氯化镁的豆腐中,铜残留量已接近国家规定的限量标准10 mg·kg-1,出于对食品安全的考虑,建议生产厂家在添加氯化镁的过程中降低添加量或选取其他凝固剂复合添加[19];添加工业氯化镁的豆腐中,铜残留量超出国家规定的限量标准,因此,检测豆腐中铜残留量可作为区分豆腐中是否添加工业氯化镁的一种方法。添加食品氯化镁与工业氯化镁豆腐中铜残留量差异显著,证明通过检测重金属的方法鉴定违法添加凝固剂的试验具有可行性,今后将继续综合分析豆腐中As、Pb、Hg等重金属元素的含量,为评价豆腐中违法添加物提供方法指导。
4 结论
利用分光光度法与原子吸收光谱法检测了梯度添加工业氯化镁与食品氯化镁豆腐中铜的残留量,获得了方法的精密度、回收率和最低检出限。研究结果证实了豆腐中铜残留量超过食品中铜限量标准源于过量使用食品级氯化镁或违法使用工业级氯化镁,该方法对于利用铜与氯化镁中的其他重金属的残留量评价氯化镁的使用情况具有指导意义。
[1]徐渡新,郑文年,徐洪,等.实验探究豆腐的主要成分与性质[J].阜阳师范学院学报,2010,27(3):88-90.
[2]徐立青,孟非.中国食品安全研究报告[M].北京:科学出版社,2012.
[3]中华人民共和国卫生部.食品中可能违法添加的非食用物质和易滥用的食品添加剂名单:第四批[EB/OL].[2012-03-22].http://www.moh.gov.cn/mohwsjdj/s9164/201004/46534.shtml.
[4]Islam EU,Yang X E ,He Z L ,et al.Assessing potential dietary toxicity of heavy metals in selected vegetables and food crops [J].Journal of Zhejiang University Science B(Life Science),2007,8(1):1-13.
[5]刘柯,何君,张瑞斌,等.德州市郊蔬菜中重金属的含量检测及对策研究[J].安徽农业科学,2009,37(1):346-348.
[6]GB15199-94.食品中铜限量卫生标准[S].
[7]万正杨,闫江虹.微波消解-原子吸收分光光度法测定茶叶中的微量元素[J].中国卫生检验杂志,2006,16(12):1459-1460.
[8]董丙坤,徐慧琴.原子吸收分光光度法测定蔬菜水果中的微量元素铜[J].河南农业,2008,22:51-52.
[9]Moyaa H D,Dantonib P,Rocha F R P,et al.A multicommuted flow-system forspectr-ophotometric determination of tannin exploiting the Cu(Ⅰ)/BCA complex formation[J].Microchemical Journal,2008,88(1):21-25.
[10]Liang P,Yang J.Cloud point extraction preconcentration and spectrophotometric determination of copper in food and water samples using amino acid as the complexing agent[J].Journal of Food Composition and Analysis,2010,23(1):95-99.
[11]Yuce M,Nazir H,Ddnmez G.A voltammetric rhodotorula mucilaginosa modified microbial biosensor for Cu(II)determination[J].Bioelectrochemistry,2010,79(1):66-70.
[12]Narayana L S ,Reddy J K ,Reddy A S ,et al.Extractive spectrophotometric reagent for the determination of Cu(II) in food and water samples [J].Food Analytical Methods,2008(4):293-299.
[13]曾洁,赵秀红.豆类食品加工[M].北京:化学工业出版社,2010.
[14]范志军,江连洲.豆浆生产中提高大豆蛋白质抽出率的研究[J].黑龙江八一农垦大学学报,2011,23(6):64-68.
[15]GB/T 5009.13-2003.食品中铜的测定方法[S].
[16]李志熙,王瑞斌.蔬菜中微量铜的测定方法[J].食品科学,2009,30(18):258-260.
[17]周志,唐巧玉,汪兴平,等.微波消解—原子吸收法快速测定莼菜中铜、锌的含量[J].食品科学,2007,28(6):285-287.
[18]傅书林,蓝洁娜.焙烤咖啡豆中铜的测定[J].现代食品科技,2007,23(7):84-85.
[19]谢微,车康,汪春,等.低嘌呤脱脂豆腐粉凝固剂凝固效果研究[J].黑龙江八一农垦大学学报,2012,24(2):71.

