草酸镁的合成与应用研究*
张 静,沈国良,马晓雨,刘红宇,徐铁军,陈远南
(沈阳工业大学a.石油化工学院;b.辽阳校区图书馆,辽宁辽阳111003)
草酸镁是最重要的草酸盐之一,也是非常重要的镁盐[2]。草酸镁最早发现在人体的结石中,波菜、甜菜、番茄、草莓、花生、茶等大多数植物中含有草酸,与体内金属Mg2+、Ca2+易生成难溶的固体草酸镁、钙盐,慢慢沉聚形成结石。实际上,在自然界中,存在草酸镁、草酸钙等二价草酸盐矿物,研究发现这些二价草酸盐矿物是由苔藓生长形成的[3,4]。
二十世纪70年代初,人们开始研究草酸镁的合成与应用。随着科学技术的发展,草酸镁的应用领域越来越广泛,在化工、材料等领域具有重要应用,是制备纳米氧化镁最常用的前驱物[5]。
1 草酸镁的合成方法
1.1 液相法
1.1.1 金属镁与草酸的直接反应 草酸属于中等强度的有机酸,可以与金属镁直接反应。反应方程式为:
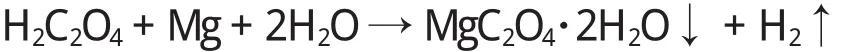
该反应是典型的置换反应,有H2产生,并放出大量热。由于草酸、草酸镁均不易溶于水中,所以反应产物分离比较困难。在以金属镁为原料制取草酸镁的工艺方法中,金属镁也不易获得。
1.1.2 Mg(OH)2与草酸的直接反应 Mg(OH)2为无机中强碱。在水溶液中,Mg(OH)2与草酸可以进行中和反应,生成草酸镁盐和水。反应方程式为:
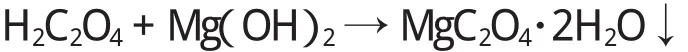
仇晓丰[6]分别将150gMg(OH)2、150g草酸用去离子水配成浓度为5%~30%的水溶液,然后按等物质的量比,在强搅拌下将草酸水溶液滴加到Mg(OH)2水溶液中,控制反应液pH值为4~5,反应生成草酸镁。蒸发反应液中的水分,过滤得到草酸镁细颗粒晶体。该方法采用低浓度反应物制备浓度较低的草酸镁,草酸镁析出缓慢,不团聚,得到的晶体草酸镁颗粒细小均匀,晶形良好。
武艳妮[7]将草酸配制成浓度为0.8mol·L-1的溶液和将Mg(OH)2配制成2mol·L-1的浆液,按草酸与Mg(OH)2物质的量之比为1∶1进行反应。在40℃下,将Mg(OH)2浆液滴加到草酸溶液中,滴加结束后反应20min,得到白色沉淀物,经抽滤、烘干,得草酸镁。
在以Mg(OH)2为原料制备草酸镁的反应中,Mg(OH)2在水中为白色膏状物或浆状液,不易进行反应和后处理。
1.1.3 硝酸镁与草酸的反应 在水中,可溶性硝酸镁可以与草酸反应制备草酸镁。

胡建华[5]用蒸馏水将Mg(NO3)2配成浓度为1. 42g·mL-1的溶液、将草酸配制饱和溶液,在不断搅拌的条件下,按照草酸饱和溶液与Mg(NO3)2溶液重量比为1∶1.2,把草酸饱和水溶液缓慢加入到Mg(NO3)2溶液中,产生大量白色沉淀。当沉淀完全时,于90~100℃下加热5~8min,然后自然冷却,将沉淀物离心甩干,洗涤5~6次,甩干、干燥得草酸镁。
反应中副产的HNO3能使草酸镁在水、有机溶剂中形成胶体。Ashok Kumar[6]以硝酸镁六水合物为原料,将其和草酸溶解在乙醇中形成凝胶体,然后凝胶体在100℃下烘干24h,可制得草酸镁。
1.1.4 MgSO4与草酸的反应
(1)MgSO4与草酸的直接反应 MgSO4为可溶性镁盐,在水溶液中能够与草酸反应制取草酸镁。

从反应式可以看出,反应过程中副产大量H2SO4,有人以此作为制备H2SO4的方法。
林传明等[7]在研究草酸镁分解脱水动力学的过程中,首先选用MgSO4为原料,在酸性条件下,与草酸反应合成了草酸镁。
颜文斌等[8]向浓度为1.5mol·L-1的MgSO4溶液中加入草酸作为沉淀剂,草酸与MgSO4物质的量比为1∶1.5,控制pH值为2.0~3.0,在反应温度70℃下,搅拌反应生成白色沉淀,抽滤分离,沉淀物用蒸馏水洗涤至无,再用少量无水乙醇洗涤。在烘箱中于80℃下干燥2h得草酸镁粉体。
(2)硫酸镁与草酸的间接反应 郭丽丽等[9]研究了在加热和搅拌下,将一定浓度的(NH4)2C2O4溶液以1D·s-1的速度加入到MgSO4水溶液中,用聚乙二醇作分散剂(按3%的质量比加入),滴加完毕后应使pH值为6.5~7.2,再恒温搅拌0.5h,真空抽滤得白色沉淀,然后分别用稀氨水、去离子水、无水乙醇充分洗涤沉淀,直到用饱和的BaCl2溶液检测不出为止,沉淀于150℃下干燥2h即可得到草酸镁。
1.1.5 MgCl2与草酸的反应
(1)MgCl2与草酸的直接反应 凌程凤等[10]报道了以MgCl2为原料,直接与草酸反应制取草酸镁。
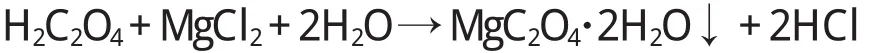
将MgCl2溶液加热至40℃,加入表面活性剂CTMAB,充分搅拌,再按MgCl2与草酸物质的量比为2∶1加入草酸固体,恒温搅拌20min,充分反应,产生沉淀。将反应液过滤,得到的白色沉淀物,放入烘箱内,80℃干燥1h,得到草酸镁晶体。
(2)MgCl2与草酸的间接反应 由于MgCl2与草酸的直接反应将副产大量HCl,在水中HCl不易被蒸出,易形成盐酸,所以产品产率较低。为了得到高产率的草酸镁,通常情况下,先将草酸与NaOH或氨水反应生成草酸钠或草酸铵,然后再与MgCl2反应,生成草酸镁和NaCl、NH4Cl,反应彻底,副产物易于分离。
①MgCl2与草酸钠的反应 卢荣丽[11,12]以草酸钠和MgCl2为原料,采用低温水热法制备草酸镁。实验按物质的量比1∶1取配成水溶液,使的浓度为0.25mol·L-1,放入内衬聚四氟乙烯的高压釜中,在100℃下进行水热反应,控制反应时间为3h。反应结束后,高压釜自然冷却至室温,取出其中的白色沉淀,离心分离,用蒸馏水和无水乙醇反复洗涤数次,至没有Cl-(用AgNO3检验)后,真空常温干燥24h,得白色粉末状的草酸镁固体。
李培刚等[13]以草酸钠和MgCl2为原料,采用模拟生物矿化中无机物在有机物模板剂调制下形成的仿生合成技术,利用有机大分子聚苯乙烯马来酸钠和聚苯乙烯磺酸钠调节草酸镁的成核和生长,制备出花生状和球状草酸镁颗粒。实验先分别配制0.2M草酸钠水溶液、0.2M MgCl2水溶液、0.1g·L-1聚苯乙烯马来酸钠水溶液以及0.1g·L-1聚苯乙烯磺酸钠水溶液,然后将草酸钠水溶液加入到聚苯乙烯马来酸钠与聚苯乙烯磺酸钠的混合液中(体积比为4∶1或1∶1),并调节混合液的pH值为9,再将MgCl2水溶液加入到混合液中,充分搅拌1min。最后将混合液放置于60℃恒温水浴中,经静置一定时间后用去离子水清洗产物,干燥,得花生状、花球状草酸镁。该法优点是试剂均为商业产品,无需繁琐制备,工艺可控性强,易操作,成本低,制得的产物纯度高。
②MgCl2与草酸铵的反应 王爱萍等[14]将300mL煮沸并充分除尽CO2的高纯水冷却至70℃,缓慢加入140g已提纯的中,在水浴上加热,在激烈搅拌下,徐徐加入草酸铵饱和溶液,至滴入草酸铵饱和溶液不产生白色沉淀为止。静置,使草酸镁沉淀充分陈化,倾出溶液,在草酸镁沉淀中加入热水,充分搅拌、静置,再次倾出溶液,重复3次。然后,将沉淀用砂芯漏斗吸滤过滤,用150mL热水分3次洗涤草酸镁沉淀,将草酸镁沉淀连同砂芯漏斗一起放入110℃干燥箱中,干燥2h,得草酸镁。1.1.6 乙酸镁与草酸的反应 管洪波[15,16]以乙酸镁和草酸为原料,采用溶液法制备草酸镁。
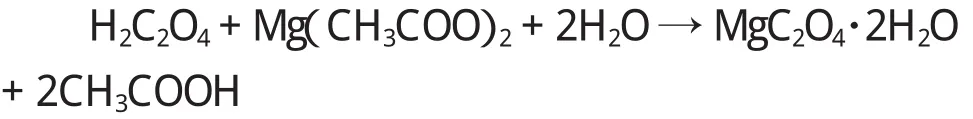
Subramania等[20]以乙酸镁、草酸为原料,乙二醇为还原剂,在197℃回流反应2h,得到白色草酸镁晶体。
1.2 固相法
固相法具有反应无需溶剂、产率高和反应条件易掌握等优点,在配位化合物、纳米材料、金属簇合物以及复合金属氧化物的合成中已经得到了广泛的应用。近年来,有文献报道采用固相法合成草酸盐,主要以乙酸盐和草酸为原料,低温固相法合成草酸盐。
1.2.1 乙酸镁与草酸的反应 二十世纪90年代,北京理工大学与贵州师范大学合作以草酸和乙酸镁为原料,采用室温固相化学反应法制备草酸镁。

廖莉玲等[18]以乙酸镁和过量草酸为原料,采用低温固相法制备草酸镁。实验分别称取4g Mg固体混合于研钵中,充分研磨,研磨过程中有乙酸释放。研磨2h后,置于80℃烘箱内干燥4h,得到草酸镁。
曹亚丽[19]取置于玛瑙研钵中研细,然后加入0.02mol研细的,混合研磨1h后放置2h,使反应进行完全。然后将该反应产物用去离子水、无水乙醇洗涤,抽滤后于空气中自然干燥,得到白色固体草酸镁。
管洪波等[20]按物质的量比1∶1.5称取研磨好的和H2C2O4·2H2O,在球磨机中混合研磨60min,90℃烘干12h后,得到草酸镁。
贾殿赠等[21]采用一步低热固相化学法合成了空心纳米结构的草酸镁。将乙酸镁和草酸固体分别在玛瑙研钵中研磨5min,然后混合均匀研磨50min,在70℃下恒温2h,确保反应完全。室温下进一步研磨,然后再用乙醇在超声波震荡中洗涤,70℃干燥2h,得到空心纳米球状草酸镁,直径为50~100nm。在混合研磨过程中,加入一定量PEG400,按上述步骤操作,可得到空心纳米棒状草酸镁,直径为100~200nm,长达几微米。
1.2.2 氯化镁与草酸钠的反应 高长华[22]以氯化镁和草酸钠为原料,采用固相法制备草酸镁。称取物质的量分别为0.01mol的MgCl2·6H2O和Na2C2O4,分别研磨10min后,在中加入3mL的PEG,继续研磨10min,再转入同一研钵中,共同研磨20min使之充分反应,加入一定量的去离子水溶解副产物形成悬浊液,转入砂芯漏斗中,用真空泵抽滤,用去离子水洗涤至检测不到Cl-后,再用无水乙醇洗涤3次,将所得滤饼转入蒸发皿中并于预先升温至100℃的烘箱中干燥4h,取出冷却、研细,即得前驱物
2 草酸镁的应用
2.1 用作催化剂
在以二元醇和二元酸为原料生产高粘度聚酯方法中,一般经历酯化反应、缩聚反应和固相缩聚反应,其中酯化反应、缩聚反应时需添加催化剂。至今,90%以上都采用锑系催化剂,但值得注意的是:由于锑本身属于重金属,具有一定的毒性;在自然界中,锑又与剧毒的砷共存。因此,锑系催化剂的应用受到一定限制。同时,含锑的二元醇残渣必须处理;锑在织物染色工序中会被浸出,造成对工艺水的污染。近年来,毒物学家和环境专家反复提到锑可能危害人身健康。因此,许多公司正在研究无锑非重金属催化剂。目前,研究最多的非重金属催化剂为钛系催化剂。但是,单用钛系催化剂,在生产高粘度聚酯过程中所表现出的固相缩聚速率只有原锑系催化剂的1/3左右,远远不能满足工业化生产的需要,成为制约钛系催化剂应用产业化的瓶颈。朱振达[23]以钛为主催化剂,草酸镁为助催化剂,当助催化剂添加量为50~250×10-6时(以镁离子在聚酯总重量中的含量为基准),固相缩聚速率达到甚至超过原锑系催化剂聚酯缩聚速率,能满足工业化生产需要和生产出不含重金属的高粘度聚酯,且成品质量和生产效率高于现有产品。
以氯化钯为主催化剂,选用亚铁盐作助催化剂,草酸镁粉体为催化剂载体,环戊二烯选择加氢得到聚合级环戊烯[24],该催化体系催化效率高、性能稳定、成本低。
2.2 制备镁铝尖晶石
镁铝尖晶石是最要的耐火材料。镁铝尖晶石的饱和结构使其具有绝缘性好、热膨胀系数小、耐蚀性高、耐磨性良好、硬度高、化学稳定性好、热稳性高等许多优良性能[25]。
张显等[26]以异丙醇铝、草酸铝或硝酸铝为铝源,以草酸镁为镁源,按Al与Mg物质的量比为2的比例,配制0.5~2M摩尔浓度的镁铝前驱体溶胶,经600~1200℃保温处理1~6h,反应得到纳米镁铝尖晶石粉。所得粉体分布均匀,性能优异。
2.3 制备纳米氧化镁
草酸盐作为制备金属氧化物的前驱物,具有热分解温度低、纯度高、成本低等优点。近10多年来,对各种草酸盐制取纳米金属氧化物开展了研究。用TG、DTA、XRD、SEM等技术对单一草酸盐或混合草酸盐的热性能、热分解动力学及其制备纳米金属氧化物过程中晶相、形貌等方面的研究,在国际上已成为一个非常活跃的研究领域。
纳米MgO具有不同于本体材料的光、电、磁、化学等特性。由于其颗粒直径小、比表面积大,纳米氧化镁具有高的活性、强吸附性、良好的低温烧结性、高电阻率等优良性质,可用作高绝缘材料、高质量陶瓷材料、高性能阻燃纤维、环境保护的吸附剂、负载型甲醇和低碳醇合成的催化剂载体等,是一种有广泛应用价值的新型无机功能材料。
纳米MgO的制备方法很多,诸如化学气相沉积法、液相均匀沉淀法、金属镁醇盐水解法、溶胶一凝胶法等,这些方法得到的纳米MgO容易发生团聚,不易制得纯度高、粒径小、颗粒尺寸分布范围窄、无硬团聚的纳米MgO。
采用草酸镁作为前驱体,500℃下直接在马弗炉中焙烧即可制得超细的MgO纳米晶体。草酸镁焙烧反应温度较低,所得MgO颗粒超细均匀。
3 结语
在有机酸中,草酸的酸性是属于中强酸,且草酸根离子具有很强的配合能力,所以很容易制取稳定的草酸镁。在化工生产中,尽管制备草酸镁的方法多种多样,但到目前为止,能够应用于工业生产的方法比较少,其主要原因有:(1)原料、规模、投资成本等因素的影响;(2)有些工艺方法尚处于实验室研究阶段,属探索性的,甚至有些根本不可能实现工业化生产。根据中国的资源条件、工艺水平,采用液相间接法比较容易实现规模化工业生产。
随着科学技术的快速发展,草酸镁的应用领域越来越多,国内外对草酸镁的需求量迅速增加。因此,一方面要求我们尽快开发出草酸镁新型的、适合大规模工业化生产的合成工艺;另一方面需要我们进一步开发草酸镁的应用领域。
[1] 郭子成.草酸及其产品的开发与利用[J].河北轻工业学院学报,1992,13(3):45-50.
[2] 胡庆福,宋丽英,胡晓湘.镁化合物工业产品及其发展趋势[C]. 2011年全国镁盐行业年会暨环保阻燃镁肥研讨会论文集,2011.20-35.
[3]仇晓丰.高纯度纳米级金属镁粉的生产工艺[P].中国:CN1027 28853A,2012-10-17.
[4] 武艳妮,左白艳,李领,等.工业草酸与氢氧化镁制备纳米氧化镁的研究[J].无机盐工业,2011,43(7):29-31.
[5]胡建华.一种光谱纯氧化镁的制备方法[P].CN:101885497B,2012-12-05.
[6]Ashok Kumar,Jitendra Kumar.溶胶凝胶法制备的MgO粉末通过电子束蒸发形成作为绝缘体保护体应用在PDP领域的MgO[J].薄膜电子器件,2008,31(1):192-196.
[7] 林传明,袁誉洪,关春秀,等.二水固态草酸镁脱水的热分析动力学[J].中南民族大学学报(自然科学版),2003,22(3):17-19.
[8] 颜文斌,石爱华,高峰,等.轻烧菱镁矿制备高纯纳米氧化镁[J].硅酸盐学报,2010,38(1):110-113.
[9] 郭丽丽,师新阁,冯勋,等.超细氧化镁的制备[J].洛阳师范学院学报,2009,28(2):72-74.
[10] 凌程凤,高雪艳,杨姣,等.草酸镁分解法制备纳米氧化镁[J].无机盐工业,2005,(9):106-108.
[11] 卢荣丽,低温水热法制备纳米氧化物及其性质研究[D].上海:华东师范大学,2007.
[12] 卢荣丽,胡炳元,王麟生,等.低温水热法制备氧化镁纳米晶[J].功能材料,2007,38(5):825-828.
[13] 李培刚,雷鸣,沈静琴.一种利用仿生合成金属制备草酸镁颗粒的方法[P].中国:CN102093202A,2011-06-15.
[14] 王爱萍,王少明,梁秀丽,等.氧化镁标准物质的研制[J].化学分析计量,2003,12(2):4-6.
[15] 管洪波,王培,王晖.高比表面纳米MgO的制备及其影响因素研究[J].物理化学学报,2006,22(7):804-808.
[16] 管洪波,王培,赵璧英,等.低温固相法制备高比表面积的纳米MgO[J].催化学报,2006,27(9):793-798.
[17]Subramania A,Vijaya C K,Sathiya R P,et al.Polyolmediated thermolysis process for the synthesis of MgO nanoparticles and nanowires[J].Nanotechnology,2007,18:5601-5608.
[18]廖莉玲,刘吉平.固相法合成纳米氧化镁[J].精细化工,2001,18(12):696-698.
[19] 曹亚丽.特殊形貌纳米材料的低热固相化学合成及其表征[D].乌鲁木齐:新疆大学,2004.
[20]Guan Hongbo,Wang Pei,Zhao Biying,et al.Preparation of nanometermagnesiawith high surface area and study on the influencing factorsof the preparation process[J].Acta Phys-Chim Sin,2006,22(7):804-808.
[21]Jia Dianzeng,Zhang Li,Cao Yali,et al.Characterization ofmagnesium oxalate and cobaltous hydroxide nanostructures prepared through one-step solid-state chemical reaction at low-heating temperature[J].JElectroceram,2008,21:218-221.
[22] 高长华.纳米MgO粉体的制备与改性及其在内墙涂料上的抗菌应用研究[D].南昌:南昌大学,2007.
[23] 朱振达,宗建平,傅伟铮,等.一种高粘度聚酯切片的生产方法[P].中国:CN101508767A,2009-03-12.
[24] 尹荣鋆,周耀坤.环戊二烯选择加氢制聚合级环戊烯[J].合成橡胶工业,1979,2(5):404-408.
[25] 沈国良,董优嘉,刘红宇,等.镁铝双金属醇盐合成工艺的研究[J].化学世界,2012,53(2):76-80.
[26] 张显,郝富锁.利用草酸盐溶液处理铝质耐火材料颗粒的方法[P].CN:101891409A,2010-11-24.

