基于布卢姆教育目标分类学(修订版)的分析应用——化学教学案例分析
杨超杰
(西北师范大学教育学院 甘肃 兰州 730070)
2001 年美国布卢姆教育目标分类学(修订版)问世。其影响力远高于1956 版。 已经在许多国家的课程编制、教育目标设计、 教学评价等领域发挥了至关重要的作用。 而反观国内有关布卢姆认知领域教育目标分类的研究与论述,多数仍采用旧版资料,特别是在化学教学领域。 随着基础教育课程改革的深入,化学教学方面的新研究也势在必行。 本文借用2001 年布卢姆教育目标分类学(修订版)理论来分析一篇教学案例,对其教学目标、教学活动和教学评价及这三者之间的一致性进行分析。
一、2001 版布卢姆教育目标分类学(修订版)简介
20 世纪90 年代中期,在1956 版布卢姆教育目标分类学长期应用的经验和效果的基础上,以课程理论专家安德森(L.W.Anderson)为首的教育专家团队开始酝酿,并于2001 年完成出版了《面向学习、教学和评价的分类学—布卢姆教育目标分类学的修订》。 与布卢姆1956 版的一个维度分类(知识、领会、应用、分析、综合和评价)不同,新的分类学采用了“知识维度”和“认知过程维度”二维框架(见表1)。修订版以知识维度为纵轴(事实性知识、概念性知识、程序性知识和元认知知识),认知过程维度为横轴(记忆、理解、运用、分析、评价和创造)构成了一个二维表。 对于相同的知识类型来说,可以有多种不同的认知过程,形成不同的教学目标。 教师可以根据教育目标中的动词和名词分别确定“知识维度”和“认知过程维度”的类别,将教育目标置于相应的交叉单元格中。
因此,使用了分类表之后,就能更完整清晰地理解教学目标。 教师根据这教学目标设计相应的教学过程和评价方法。 将会更有针对性的指导学生认知活动,促进教学目标的达成。 这就是新版分类表的价值所在。
二、化学教学案例分析
本节笔者借用江苏某高级中学高一化学备课资料的教学案例(略作修改)。

表1 2001 版布卢姆教育目标分类学表
第二节 化学计量在实验中的应用(一)
——物质的量和摩尔质量
教学目标
(一)知识与技能
1.记忆物质的量的基本单位——摩尔;了解物质的量与微观粒子之间的关系,了解摩尔质量的概念;懂得阿伏加德罗常数的涵义。
分析:该目标包含3 个子目标。 “记忆”是认知过程的记忆水平,“了解”和“懂得”都是理解水平。 “物质的量的基本单位——摩尔”和“阿伏加德罗常数”隶属事实性知识。 “物质的量与微观粒子之间的关系”,“摩尔质量的概念”是概念性知识。 即目标1 可以转换为记忆事实性知识(目标1.1)、理解概念性知识(目标1.2)、理解事实性知识(目标1.3)。
2.了解物质的量、摩尔质量、物质的质量之间的关系;并能用于简单的化学计算。
分析:前半个子目标即理解概念性知识(目标2.1),后半个子目标即运用程序性知识(目标2.2)。
(二)过程与方法
初步培养学生演绎推理、归纳推理、逻辑推理和运用化学知识进行计算的能力
分析:“初步培养学生……”没有明确的说明认知水平的动词,因此这个目标很模糊,不容易被操作,因此这个目标暂不做考虑。 后半个子目标中“化学知识”过于宽泛,但根据本课题,姑且将其归为运用程序性知识(同目标2.2)。
(三)情感态度与价值观
通过对概念的透彻理解,培养学生严谨、认真的学习态度。
教学重点与难点:物质的量及单位;摩尔质量的概念和有关摩尔质量的计算;物质的量及单位——摩尔。
将以上六个教学目标归类于表2。

表2 物质的量和摩尔质量教学目标分析
教学过程
1.引入课题(活动1)
我们在初中时知道,分子、原子、离子等我们肉眼看不见的粒子,可以构成客观存在的、具有一定质量的物质, 这说明在我们肉眼看不见的粒子与物质的质量之间,必定存在着某种联系,那么,联系他们的桥梁是什么呢? 要解决这个问题,我们来学习第二节化学计量在实验中的应用。
分析:教师通过知识回顾,引发学习兴趣,引出把微小物质扩大倍数形成一定数目的集体以便于方便生活,有利于初高中知识的有效衔接。 这一活动属于回忆概念性知识。
2.物质的量的概念(活动2)
物体的长短,物体的冷热程度如何表示? 同样的,物质的量可用来表示物质所含粒子数的多少,其符号为n,它是国际单位制中的基本物理量, 四个字缺一不可,不可简写。物质的量单位:摩尔,符号mol,简称摩。(教师板书)
分析:这一教学活动中教师引导学生主动回忆并积极提取已有知识, 为新旧知识的迁移做好更充分的准备,引入了物质的量的概念。 活动2 属于记忆、理解事实性知识,理解概念性知识。
3.阿伏加德罗常数概念(活动3)
1mol 物质的量表示的粒子数目是多少呢?这个数值是以什么为依据得出的? 请阅读教材45 页上内容,理解物质的量在粒子数目上的大小关系(学生回答,老师点评得出结论)。
结论:1mol 任何粒子的数目是0.012kg12C 中所含的碳原子数目约为6.02×1023个。1mol 任何粒子的数目也叫阿伏加德罗常数。
阿伏加德罗是意大利物理学家。 因他对科学研究有着很大的贡献, 故用他的名字来表示1mol 任何粒子的粒子数,以示纪念。 化学上,我们用NA来表示阿伏加德罗常数,其单位mol-1,它表示1mol 任何粒子的粒子数,其数值近似等于6.02×1023个(教师板书)。
分析:学生自学,师生一问一答,检验自学成果,并进行化学史的教育, 培养学生良好的科学态度。 活动3属于理解概念性知识。
例题(评价1)
(1)应用阿伏加德罗常数。
①1mol H2所含氢气分子的个数_________。
②2mol 氢分子含_________个氢原子。
(2)判断正误,说明理由。
A. 1mol 氢 B. 1mol CO2C. 1mol 小米
(3)根据摩尔有关知识进行计算。
①1.204×1024个H,合________mol。
②N 个水分子的物质的量是___________。 (已知,阿伏加德罗常数为NA)
分析:这是对教学过程的评价。 了解学生是否理解了上述两个概念。 因此属于理解概念性知识的评价。
4.N、NA与n 的关系(活动4)
由以上练习得出粒子总个数N、 阿伏加德罗常数NA、物质的量n 三者之间的关系,写出公式。
注意:摩尔是一个巨大数量粒子集合体,可以是整数,也可以是小数,例如可以有0.5mol 氧气,但分子、原子等具体的粒子,只能是整数,就不能说0.5 个。 (教师板书)
分析:此教学内容是本节课的重点,教师根据几道例题就引出公式,得到结论,可能效果不会太好,需要改进教学方法。 此过程属于理解概念性知识并运用程序性知识。
随堂练习1(评价2)
(1)0.5mol 水中含有_________个水分子。
(2)1mol HCl 溶于水,水中存在的溶质粒子是什么?它们的物质的量各是多少?
分析: 本练习主要让学生在上述例题的基础上,进一步运用公式:N=nNA。 属于对运用程序性知识的评价。
5.摩尔质量概念(活动5)
前面我们学习了物质的量,它表示含有一定数目的粒子集体。 那么,1mol 粒子的数目是以什么为标准得出来的? 其数目约为多少? 我们初中所学某种原子的相对原子质量也是以碳-12 原子为标准得出来的, 它是怎样定义的?
思考:假如一原子的质量为m1,碳-12 原子的质量为mc,则该原子的相对原子质量A1怎样表示? (学生答案A1=12m1/mc,教师评价)。 若另一种原子的质量为m2,则它的相对原子质量A2又该怎样表示? (学生回答)。 A1比A2与m1与m2的关系是什么呢?(教师推导得出:原子的质量比=原子的相对原子质量比)。
由此得1mol 任何原子的质量比, 就等于它们的相对原子质量比。
根据上述推导1mol 氢原子的质量是多少? 由此可得出什么结论? 1mol 氢分子呢? 与它的相对分子质量有什么关系?为什么?(学生回答)那么,对于粒子中的离子来讲,又将怎样呢? 请大家阅读课本12 页最后一段后回答(学生回答)。
结论:1mol 任何粒子或物质的质量是以克为单位,在数值上就等于该粒子的相对原子(分子、离子)质量。
定义:单位物质的量的物质所具有的质量——摩尔质量,符号为M,公式:M=m/n,单位g/mol。
依据此式,我们可以把物质的质量与构成物质的粒子集体——物质的量联系起来。
分析:在此活动中,教师采用类比的方法引入新知识,再由教师推导得出结论,最后引出摩尔质量的概念。这过程中通过紧凑的提问和学生自学,从而记住并理解结论以及概念。 这一活动属于回忆概念性知识,理解概念性知识,运用程序性知识。
随堂练习2(评价3)
(1)Na 的摩尔质量_____________。
(2)1mol NaCl 的质量是_________。
例题(评价4)
(4)24.5g H2SO4的物质的量是_____。
解:H2SO4的相对分子质量为98,则M(H2SO4)=98g/mol。 n(H2SO4)=0.25mol。
随堂练习3(评价5)
5mol CuSO4·5 H2O 的质量是多少?
分析: 评价3 就是对摩尔质量概念的简单套用,并适当引申,属于理解概念性评价;评价4、5 都是在理解摩尔质量的基础上对公式:n=m/M 的应用同属于应用程序性知识的评价活动。
课堂小结:略
三、教学目标、活动、评价一致性分析
将以上教学活动和评价归类于表3 中。
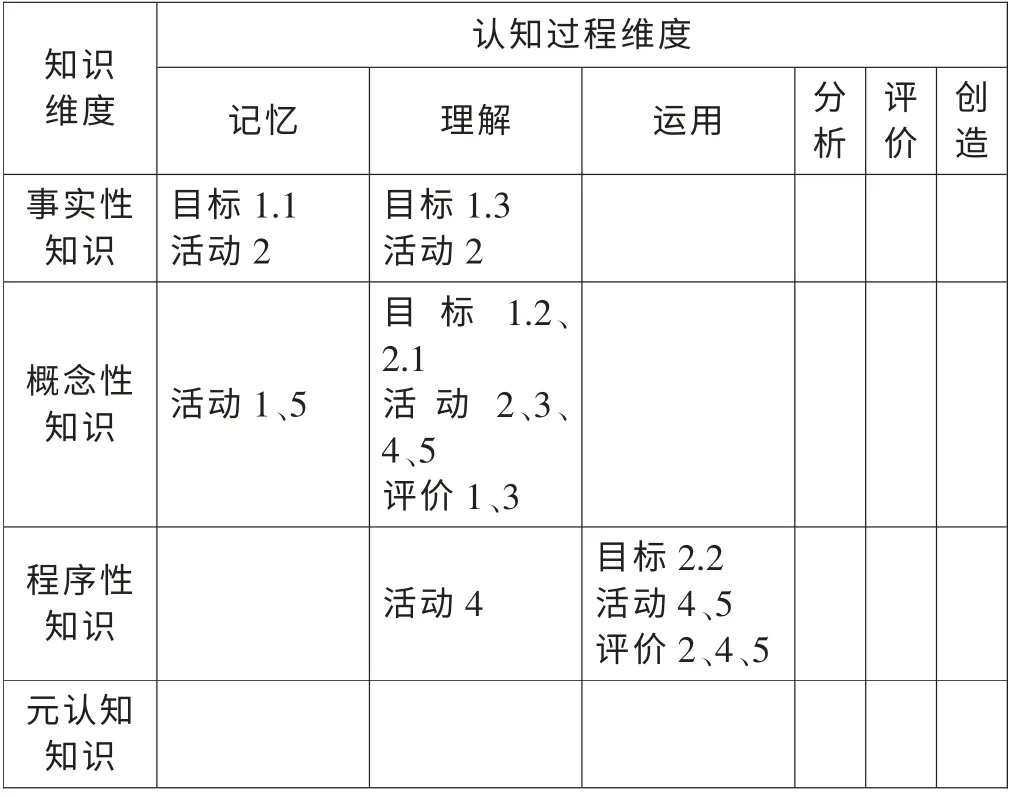
表3 教学目标、活动、评价的一致性分析
由表3 可知, 这一教学过程具有良好的一致性,教师在每一个教学活动之后几乎都有及时的教学评价,这些评价选题与所授知识相对应,对学生的学习成果提供了及时反馈。 虽然活动1 和2 没有评价过程,但后续的评价中有涉及。 至于活动4、5 的单独列出,笔者认为它们都是为进一步认识的基础,鉴于本节课知识点的连贯性,相应的评价也可以相互利用。 但从表中也发现一些不足:教师在结束课堂时没有布置作业,进一步的评价没有及时跟上,有待改进。
四、结语
根据布卢姆教育目标分类学理论能较好地确保教学目标、过程和评价三者之间的一致性。 化学教师可以适当借鉴,建立一个教学设计、活动和评价的讨论平台,必将会在化学教学中起到一定的效果。
同时我们也要意识到科学是无止境的,教育目标分类学研究也不例外,仍有需要改进的地方,如:布卢姆教育目标分类学理论没有较好地落实情感态度方面的目标;由于分类表的指导,对学生的活动和内心体验不够重视等都是有待改进的重要课题。 自布卢姆教育目标分类学问世至今,仍不断地进行着改进研究,不断地取得新的进展,我们化学教育者也要与时俱进,不断更新已有的理论研究,并付诸于实践。
[1] 安德森等著,皮连生译.学习、教学和评估的分类学:布卢姆教育目标分类学修订版(简缩版)[M].上海:华东师范大学出版社,2008:26-29,86-87
[2] 中华人民共和国教育部.义务教育化学课程标准(2011 版)[S].北京:北京师范大学出版社,2011
[3] 屈程.布卢姆教育目标分类学修订版在小学数学教学中的应用[D].华东师范大学,2008

