海藻酸纤维对碱性品红的吸附性能研究
孙 哲,夏延致,全凤玉,李海宁,朱立华
(青岛大学纤维新材料与现代纺织国家重点实验室培育基地,山东青岛266071)
海藻酸纤维对碱性品红的吸附性能研究
孙 哲,夏延致*,全凤玉,李海宁,朱立华
(青岛大学纤维新材料与现代纺织国家重点实验室培育基地,山东青岛266071)
以自制海藻酸纤维为吸附剂,考察了吸附剂用量、溶液温度、吸附时间和溶液pH值等因素对海藻酸纤维吸附碱性品红的吸附效果的影响。结果表明:脱色率随海藻酸纤维加入量的增加而提高,随着溶液温度升高而迅速下降;加酸或加碱都不利于海藻酸纤维对碱性品红的吸附;对于40 mg/L的碱性品红溶液,当海藻酸纤维的加入量为5 g/L,室温下振荡40 min既能达到吸附平衡,脱色率可达96%;Freundlich等温方程能很好地描述海藻酸纤维对碱性品红的吸附,其吸附行为是物理吸附,吸附过程为熵减过程;海藻酸纤维经过8次再生后,对碱性品红的脱色率仍可达到93%以上,可重复利用。
海藻酸纤维 碱性品红 吸附 吸附热力学
印染行业每年需消耗近108t的工业水,每加工100 m2织物,会产生3~5 t废水,且废水色度大、有机物含量高,对生态系统和人类健康造成了极大的危害[1]。目前应用最广的染料废水脱色方法是吸附法。活性炭作为一类有效的吸附剂,其再生比较困难,而且价格昂贵[2]。海藻酸纤维是以海藻酸钠为原料,氯化钙为凝固浴,经过湿法纺丝工艺得到海藻酸钙纤维,然后用盐酸浸泡而制得的。在水溶液中,碱性品红失去氯离子而带正电荷,海藻酸纤维易失去质子而带负电荷,二者可以通过静电吸引力结合而达到脱色的目的。海藻酸纤维的原料来源于海带、紫菜、褐带菜等丰富的褐藻类海藻植物中提炼的海藻多糖,来源广泛,提取简单,表面积大,吸附迅速,且吸附材质极易降解不会对环境造成二次污染[3-4]。作者用实验室自制的海藻酸纤维作为吸附剂,研究了海藻酸对碱性品红的吸附性能。
1 实验
1.1 试剂与仪器
海藻酸纤维:实验室自制[5];碱性品红:天津凯信化学工业有限公司产;浓盐酸,氢氧化钠:均为分析纯,市售。
TU-1901双光束紫外可见分光光度计:北京普析通用仪器有限公司制;pH计:上海精密科学仪器有限公司制;SHA-B型水浴恒温振荡器:上海国华企业制。
1.2 绘制碱性品红标准曲线
配制浓度为40 mg/L的碱性品红溶液,分别移取1,2,3,4,5,6 mL 于50 mL 容量瓶中,加水定容至刻度,测定溶液在其最大吸收波长543 nm处的吸光度(A)。以其浓度(C)为横坐标,A为纵坐标绘制标准曲线,其线性回归方程及相关系数(r)如下:

1.3 吸附实验
准确称取一定量海藻酸纤维加入到50 mL浓度为40 mg/L的碱性品红溶液中,室温下振荡到设定时间,然后取出纤维,在染料最大吸收波长543 nm处测量溶液的A,计算吸附后染料的浓度(Ct)。通过式(2)计算脱色率(d):

式中:Co为染料的初始浓度。
1.4 吸附等温线
室温下,取0.02 g纤维,测定不同初始浓度下达到吸附平衡时的平衡吸附量(qe)和平衡吸附浓度(Ce),qe和Ce的关系式如下:

式中:V为染料溶液的体积;m为吸附剂的质量。
以qe对Ce作图得吸附等温线,分别用Langmuir等温吸附方程式、Freundlich等温吸附方程式和Temkin等温吸附方程式来描述海藻酸纤维对碱性品红的吸附等温线[6-7]。
1.5 热力学实验
用Van't Hoff方程式[8]研究海藻酸纤维吸附碱性品红的热力学性能。
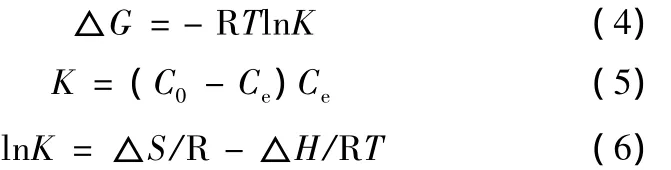
式中:K为亨利常数,可以从Langmuir方程中直线截距得到;△G为标准吉布斯自由能;R为通用气体常数;T为绝对温度;△S为吸附过程的熵变;△H为吸附过程的焓变。
以lnK对1/T得到一条直线,由此直线的斜率和截距可以求得吸附过程的△S和△H。
2 结果与讨论
2.1 海藻酸纤维用量
从图1可知,海藻酸纤维对碱性品红有很高的吸附性,纤维用量为1 g/L时,碱性品红的d高达90%。碱性品红的d随着纤维用量的增加而增大,当纤维用量增加到5 g/L时,d达到96%,继续增加纤维用量,d增幅很小。因为增加纤维用量时,能与染料结合的吸附点增加,从而吸附更多的染料分子,使d升高,之后绝大多数染料分子被纤维吸附,继续投加纤维d不再升高。

图1 海藻纤维用量对d的影响Fig.1 Effect of alginate fiber dose on d
2.2 振荡时间
称取0.25 g海藻酸纤维加入50 mL浓度为40 mg/L的碱性品红溶液中,室温下振荡,每隔一定时间取样分析。从图2可知,由于海藻酸纤维与碱性品红之间静电吸引力的存在,在较短时间内,海藻酸纤维能迅速吸附大量的碱性品红,5 min时d达85%。当振荡时间小于40 min时,随着振荡时间的延长,d大幅增加,之后d趋于稳定达到96%。所以,海藻酸纤维对碱性品红的吸附平衡时间为40 min。
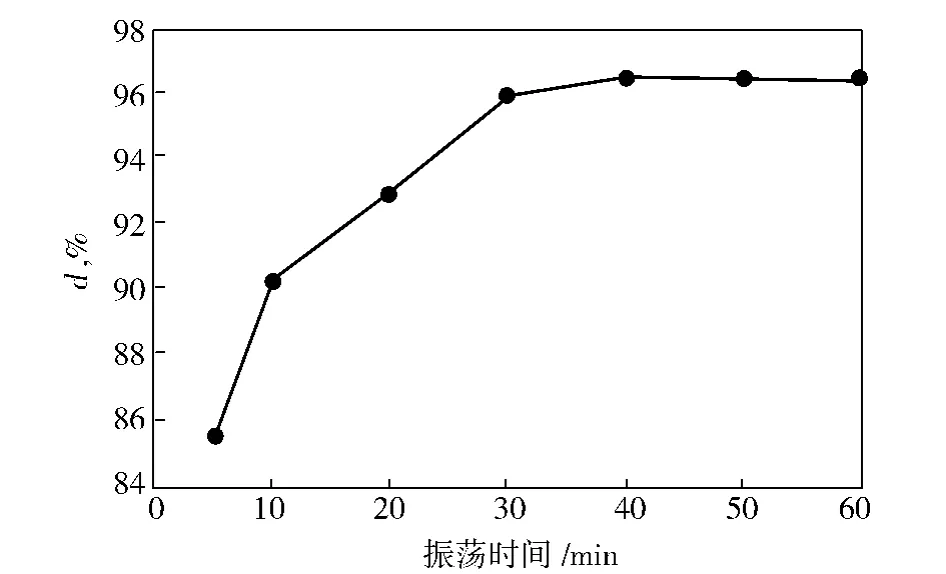
图2 振荡时间对d的影响Fig.2 Effect of oscillation time on d
2.3 溶液温度
取50 mL浓度为40 mg/L的碱性品红溶液,加入0.25 g海藻酸纤维,在不同温度下振荡,结果见图3。随着溶液温度的升高,碱性品红的d迅速降低。从25℃升高到75℃时,d从96%降低到13%。温度的变化对d的影响很大。这是由于海藻酸纤维对碱性品红的吸附是由于二者静电引力(即库仑力)的作用,温度增加,分子运动加剧,二者作用力减弱,d降低。
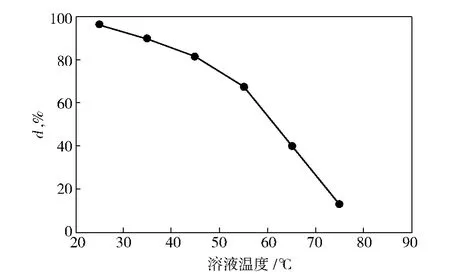
图3 溶液温度对d的影响Fig.3 Effect of solution temperature on d
2.4 溶液pH值
用盐酸和NaOH溶液调节碱性品红溶液的pH值,在溶液pH值大于9时,碱性品红结构发生改变而褪色,因此考察溶液pH值小于9时的吸附效果。从图4可以看出:pH值的变化对碱性品红的d影响较大;pH值减小时,d大幅度下降;增大pH值时,d也会降低;未调节时(pH值大约5.7),海藻酸纤维对染料的吸附效果最好,d最高。这是因为在水溶液中,海藻酸纤维分子上有—COOH,经过电离而带负电荷,碱性品红带正电荷,往溶液中加入H+,溶液中大量的H+也能与纤维上有限的吸附点结合从而使更少的碱性品红分子与海藻酸纤维结合,从而d降低;同样增大pH值,溶液中的OH-能与带正电荷的碱性品红分子产生静电吸引力,也使与海藻酸纤维结合的染料减少,d降低。所以,实验只需要维持原pH值即可。

图4 溶液pH值对d的影响Fig.4 Effect of pH value of solution on d
2.5 吸附等温线
以qe对Ce作图得吸附等温线,结果见图5。采用Langmuir模型、Freundlich模型和Temkin模型进行线性拟合的结果见表1。由图5可知,达到吸附平衡时,纤维上的染料浓度随染液中染料浓度的增加而不断增加,没有明显的极限。由表1可知,线性拟合后Freundlich等温吸附方程的r明显高于Langmuir方程和Temkin方程的,而且r值很高。所以海藻酸纤维吸附碱性品红的过程更符合Freundlich等温吸附模型,为物理吸附[9]。其中,1/n大于0.1小于1,说明海藻酸纤维对碱性品红有较强的吸附能力,吸附容易进行[10]。碱性品红吸附在纤维上是以扩散吸附层存在的,染料分子既吸附在纤维分子的无定形区,还有些分布在孔道溶液中与它保持动态平衡,染料浓度呈扩散状分布,即离纤维分子链近的浓度高,离分子链远的浓度低[9]。所以,海藻酸纤维吸附碱性品红并不是单分子的吸附,纤维表面吸附点不均匀,这一过程主要是物理吸附,即非定位吸附。

图5 吸附等温线Fig.5 Adsorption isotherm

表1 海藻酸纤维吸附碱性品红的Langmuir与Freundlich及Temkin模型的拟合结果Tab.1 Langmuir,Freundlich and Temkin fitting results of alginate fiber adsorption for basic fuchsin
2.6 吸附热力学
根据图3作lnK~1/T图,由Van't Hoff方程拟合海藻酸纤维对碱性品红的吸附方程为:
lnK=-30.635+10 162.147/T,r=0.985 6 (7)
由方程求得各参数,结果见表2。由表2可以看出,当吸附温度在55℃以下时,△G小于0,这说明此时反应是自发进行的,当温度在55℃以上时,△G大于0,此时反应不能自发进行。且温度越高,△G逐渐增大,这说明温度越高,吸附反应自发进行的程度越小,升高温度不利于吸附反应的进行[11]。
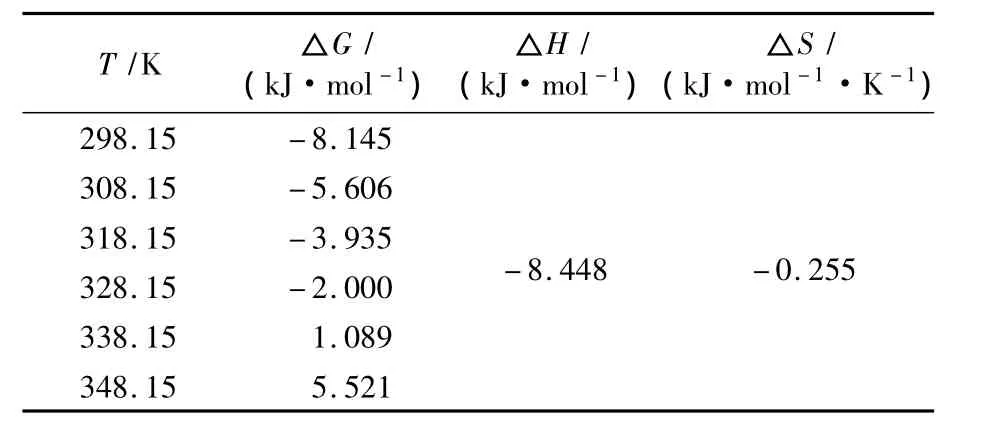
表2 海藻酸纤维对碱性品红的吸附热力学参数Tab.2 Thermodynamic parameters for alginate fiber adsorption for basic fuchsin
吸附过程的△H小于0,表明吸附是放热过程。Mahir Alkan指出,当△H在40~120 kJ/mol之间时主要为化学吸附,否则主要为物理吸附[12]。由此可知,海藻酸纤维对碱性品红的吸附主要为物理吸附。此结果表明,吸附作用力大部分是由纤维与染料间的静电引力即库仑力产生,少部分是分子间作用力。△S小于0,说明整个吸附过程熵减小,体系的无序度减小,吸附质在吸附剂表面的随意运动性能比在溶液中的低,吸附过程为熵减过程。
2.7 海藻酸纤维的再生
为了提高海藻酸纤维的利用率,解决吸附剂的后处理及其二次污染问题,对海藻酸纤维进行再生实验。将吸附碱性品红的海藻酸纤维用pH值为1的盐酸浸泡1 h,取出洗净烘干后反复用于吸附实验。结果发现随着再生次数的增加,碱性品红的d并没有降低,进行8次再生后d仍可达到93%以上,因为海藻酸纤维与碱性品红的静电引力很弱,在盐酸溶液中,碱性品红几乎全部发生解吸附而脱离下来。这表明海藻酸纤维能反复利用,可以多次吸附去除废水中的碱性品红。
3 结论
a.自制的海藻酸纤维对碱性品红染料有较好的吸附性能。碱性品红的d随纤维加入量的增加而提高,随温度的升高而大幅度降低。溶液的酸碱性对d的影响较大,实验中维持原pH值更有利于吸附的进行。对于40 mg/L的碱性品红溶液,当海藻酸纤维的投加量为5 g/L时,室温下吸附平衡时间为40 min,d为96%。
b.Freundlich等温方程能很好地描述这一吸附行为。海藻酸纤维对碱性品红的吸附是自发的放热的物理吸附过程,△S为-0.255 kJ/(mol·K),吸附过程为熵减过程。
c.海藻酸纤维再生性能良好,可以多次重复利用。
[1]朱虹.印染废水处理技术[M].北京:中国纺织出版社,2004:152-155.
[2]Song Jiyun,Zou Weihua,Bian Yangyang,et al.Adsorption characteristics of methylene blue by peanut husk in batch and columnmodes[J].Desalination,2011,265(1/2/3):119 -125.
[3]李嘉宁,孔庆山,高继贤,等.海藻酸对水溶液中Cu2+的吸附动力学研究[J].科学技术与工程,2010,10(4):942 -945.
[4]郭春香.海藻酸纤维对阳离子染料吸附性能的研究[D].青岛:青岛大学,2011.
[5]Ahmad A L,Sumathi S,Hameed B H.Adsorption of residue oil from palm oil mill effluent using powder and flake chitosan:E-quilibrium and kinetic studies[J].Water Res,2005,39(12):2483-2494.
[6]Han Runping,Wang Yuanfeng,Han Pan,et al.Removal of methylene blue from aqueous solution by chaff in batch mode[J].J Hazard Mater,2006,137(1):550 -557.
[7]Chiron N,Guilet R,Deydier E.Adsorption of Cu(II)and Pb(II)onto a grafted silica:isotherms and kinetic models[J].Water Res,2003,37(13):3079 -3086.
[8]孔庆山,姜丽萍,高继贤,等.海藻酸纤维对Zn2+的吸附性能研究[J].合成纤维,2008,37(11):12-16.
[9]赵涛.染整工艺学教程[M].第二分册.北京:中国纺织出版社,2005:120-123.
[10]Raji C,Anirudhan T S.Batch Cr(Ⅵ)removal by polyacrylamid-egrafted sawdust:kinetics and thermodynamics[J].Water Res,1988,32(12):3772 -3780.
[11]Fu Qingling,Deng Yali,Li Huishu.Equilibrium,kinetic and thermodynamic studies on the adsorption of the toxins of Bacillus thuringiensis subsp Kurstaki by clay minerals[J].Appl Surf Sci,2009,255(8):4551 -4557.
[12]Alkan M,Demirbas Ö,Celikcapa S,et al.Sorption of acid red 57 from aqueous solution onto sepiolite[J].J Hazard Mater,2004,116(1/2):135 -145.
Adsorption properties of alginate fiber for basic fuchsin
Sun Zhe,Xia Yanzhi,Quan Fengyu,Li Haining,Zhu Lihua
(State Key Laboratory Cultivating Base of Advanced Fibers and Textile Materials,Qingdao University,Qingdao266071)
Using self-made alginate fiber as an adsorbent,the effects of adsorbent dosage,solution temperature,adsorption time and solution pH value on the adsorption effect of alginate fiber for basic fuchsin were investigated.The results showed that the decoloration rate rose with the addition of alginate fiber and rapidly dropped with the increase of solution temperature;the addition of acid or alkali could block the adsorption of alginate fiber for basic fuchsin;the adsorption equilibrium could be achieved for 40 mg/L basic fuchsin solution after oscillating for 40 min at room temperature and the decoloration rate could reach 96%when the addition of alginate fiber was 5 g/L;the Freundlich adsorption model qualified to describe the adsorption behavior of alginate fiber for basic fuchsin,which was a physical adsorption and entropy decreasing process;the alginate fiber can acquire the basic fuchsin decoloration rate above 93%after regenerating 8 times,which proved that it can be used repeatedly.
alginate fiber;basic fuchsin;adsorption;adsorption thermodynamics
TQ342.86
A
1001-0041(2012)04-0004-04
2011-10-27;修改稿收到日期:2012-05-18。
孙哲(1988—),女,硕士研究生,从事合成纤维及吸附方面的研究。E-mail:gnjsz@163.com。
国家自然科学基金(50908120);山东省自然科学基金(Q2008B04)及泰山学者人才工程资助。
* 通讯联系人。E-mail:qdxyzh@163.com。

