长春瑞宾单药与长春瑞宾联合卡铂治疗≥75岁的老年晚期非小细胞肺癌患者的临床研究
李爱武,周彩存,徐建芳,任胜祥,陈晓霞,朱 韧
(同济大学附属肺科医院肿瘤科,上海 200433)
肺癌是全球发病率和死亡率最高的恶性肿瘤,其中非小细胞肺癌(non-small-cell lung carcinoma,NSCLC)约占肺癌总数的80%。NSCLC患者中大部分是老年人,其中65岁以上的患者占50%以上,70岁以上患者甚至占40%以上[1-2]。
长春瑞宾是肺癌常用的化疗药物,单药长春瑞宾可以延长老年(≥70岁)晚期NSCLC患者的生存期和提高生活质量[3]。但一些研究结果显示,老年患者也可以从含铂类的两药方案化疗中获益,由于相对于顺铂,卡铂较少引起肾毒性以及无需水化等而更适合老年患者[4-6],因而含卡铂的联合方案也是老年患者常用的化疗方案。本研究旨在探讨长春瑞宾与长春瑞宾联合卡铂在治疗≥75岁的晚期NSCLC患者的有效性和安全性。
1 资料与方法
1.1 一般资料
对同济大学附属肺科医院肿瘤科2006年1月至2008年12月收治的细胞学或组织学确诊的51例老年(≥75岁)初治晚期NSCLC患者进行回顾性分析研究。入选本研究的标准:按UICC(1997)肺癌临床病理分期均为无手术指征和无根治性放疗指征的Ⅲb或Ⅳ期,ECOG行为状态评分(PS)≤2,患者均有可测量病灶,造血系统功能基本正常[WBC(4~12)×109/L,HB >90 g/L,PLT>100×109/L],血清Cr<20 mg/L,APT、GOT<1.5 倍正常上限,总胆红素<15 mg/L,paO2>70 mmHg,合并有急性严重感染、严重的心脏疾患、伴有其他恶性肿瘤、有症状的脑转移患者除外。
1.2 治疗方法
患者分为单药组和联合组,分别接受长春瑞宾单药(第1、8天 25 mg/m2)或长春瑞宾(第1、8天25 mg/m2)联合卡铂(AUC=5,第1天)静脉点滴,化疗前后予以包括5-HT3受体拮抗剂预防性止吐等对症治疗。21 d为1个周期,除非患者出现不可接受的毒副反应或患者本人拒绝进一步化疗,化疗周期最多可至4个周期。
1.3 合并症、疗效和毒性评价标准
根据Charlson等[7]合并症评分表的改编版本对合并症进行分类,由于本研究中仅1例患者无合并症,为了统计方便,根据合并症的数量将患者分为两组:轻度(0~2)组、重度(≥3)组。近期疗效参照RECIST1.0关于实体瘤评价系统统一评定,分为完全缓解(complete remission,CR)、部分缓解(partial remission,PR)、疾病稳定(stable disease,SD)和疾病进展(progression disease,PD),CR+PR 为有效,疾病控制率为CR+PR+SD的率。总生存时间定义为患者签署化疗知情同意书到死亡或最后一次随访时间。毒性反应安CTC3.0关于毒性反应评价标准分为1~5级。每6周进行RESICT疗效评价。
1.4 统计学分析
资料结果应用SPSS13.0统计软件包进行分析处理,率的比较采用卡方检验,生存率采用寿命表法,多因素COX回归分析不同临床因素与生存期关系,不同治疗方案与生存期的关系采用 Kaplan-Meier法分析,Log-Rank检验判断差异性,P<0.05为差异有统计学意义。
2 结 果
2.1 患者的一般特征
5例≥75岁的老年患者中,单药组31例,联合组20例。其中大于80岁的比例较少,两组分别有4(12.9%)例和1(5.0%)例。两组患者均以男性,PS 0~1,非鳞癌以及转移性肺癌(Ⅳ期)为主,1例患者无合并症,30例存在1~2种合并症,20例(39.2%)存在重度合并症,而大多数患者没有接受二线(靶向)治疗,患者特征在两组间没有显著的统计学差异(见表1)。
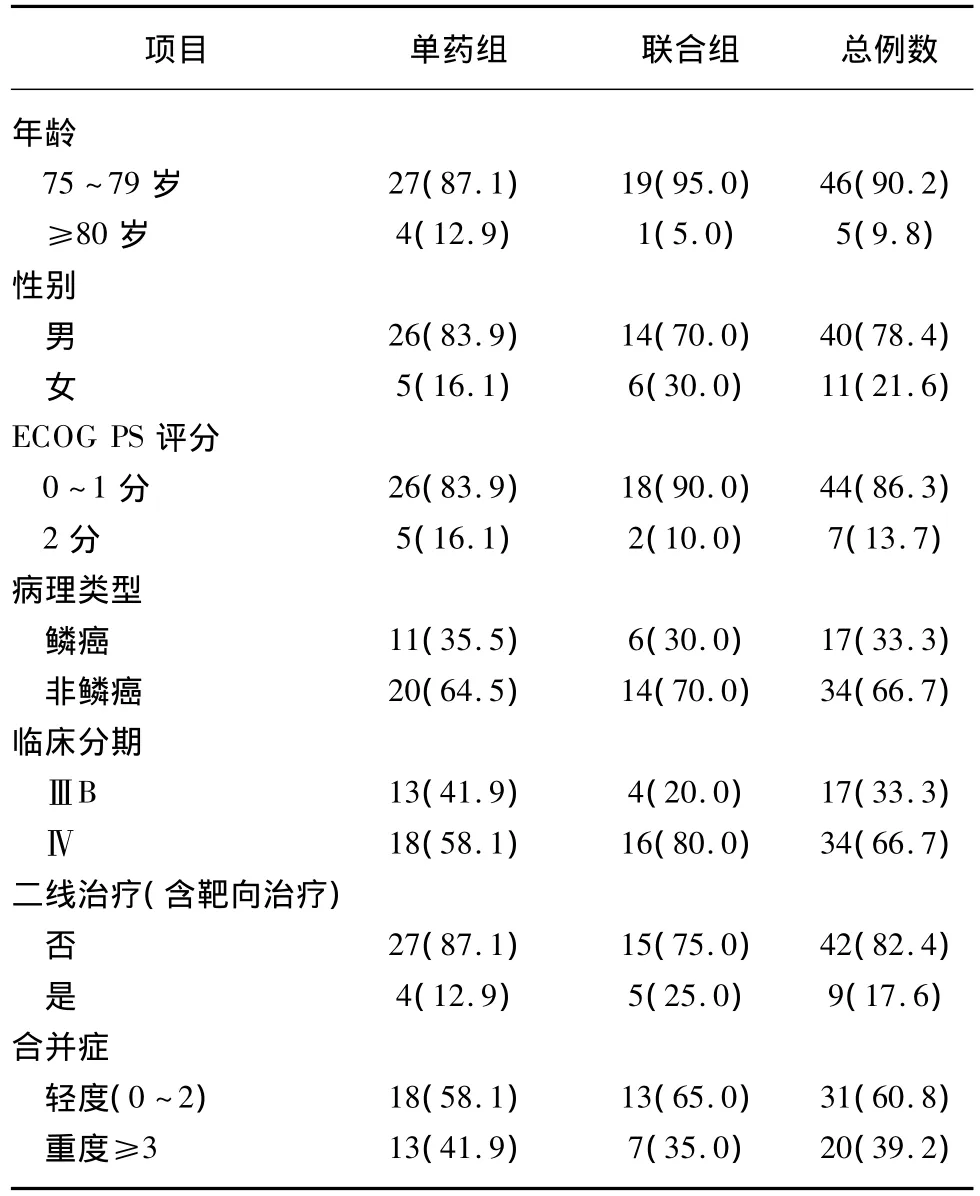
表1 51例≥75岁老年NSCLC患者的一般特征Tab.1 Comparison of general features of 51 elderly NSCLC patients(≥75 y) [n(%)]
2.2 患者的治疗状况、临床疗效和生存时间
2.2.1 治疗状况 本研究中51例患者共接受了105个周期的化疗,平均化疗周期数为2.1±0.9,其中单药组的平均化疗周期为 1.9±0.7,联合组为 2.1±1.1(P=0.295)。单药组完成3~4周期的比例为16.1%,联合组为40%,差异无统计学意义(P=0.056)。
2.2.2 临床客观疗效 两组可评价疗效的患者分别为21例和14例,PR单药组2(9.5%)例,SD 8(38.1%)例,联合组分别为 4(28.6%)例,6(42.8%)例,两组的有效率和疾病控制率均没有统计学差异(P=0.191,0.296),见表 2。
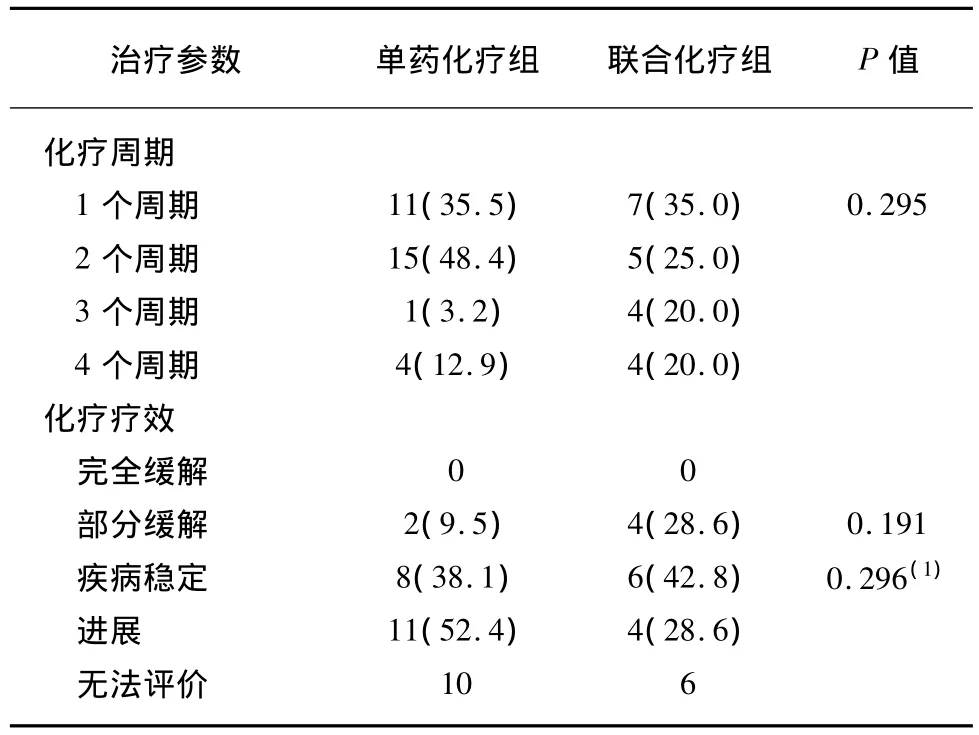
表2 51例≥75岁老年NSCLC患者治疗周期和疗效Tab.2 Comparison of chemotherapy cycles and response of 51 NSCLC patients(≥75 y)[n(%)]
2.2.3 生存时间 本研究显示,单药组与联合组失访病例数分别为6例和2例,占总数的19.4%和10.0%。两组的中位生存时间分别为7.2个月(95%CI 4.9,9.5)和 9.3 个月(95%CI 4.3,15.7),1、2年生存率分别为 39.7%、10.0% 和 45.0%、13.0%(Log Rank P=0.679),见图1。
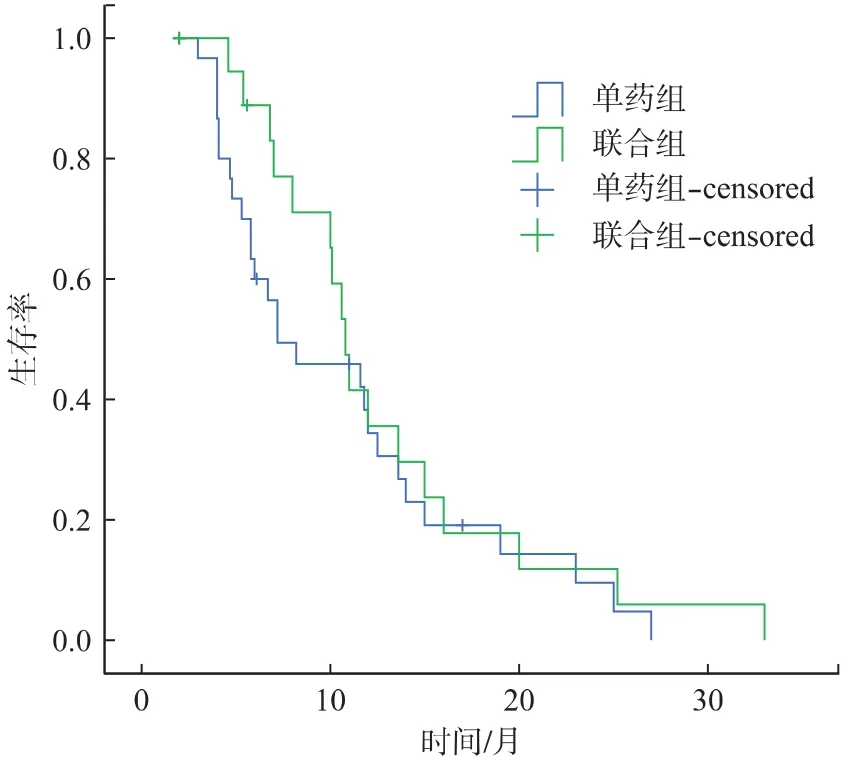
图1 不同治疗组的≥75岁老年晚期NSCLC患者的生存时间曲线图Fig.1 Comparison of Kaplan-Meier curve for survival of NSCLC patients(≥75 y)in different time(Log Rank,P=0.679)
2.3 化疗毒副反应
所有患者均可评价毒副反应,结果发现两组的毒副反应均较轻,无Ⅳ级不良反应(表3),主要的Ⅲ度毒副反应是骨髓抑制,分别为贫血、白细胞下降、中性粒细胞下降和血小板下降,联合组的发生率稍高于单药组,但两组间差异无统计学意义,而且可能与联合组的治疗周期较多等因素有关。胃肠道及肝肾功能的毒副反应发生率较低,主要为Ⅰ~Ⅱ度的胃肠道反应及肝肾功能毒性,大多患者经过对症治疗后可缓解。
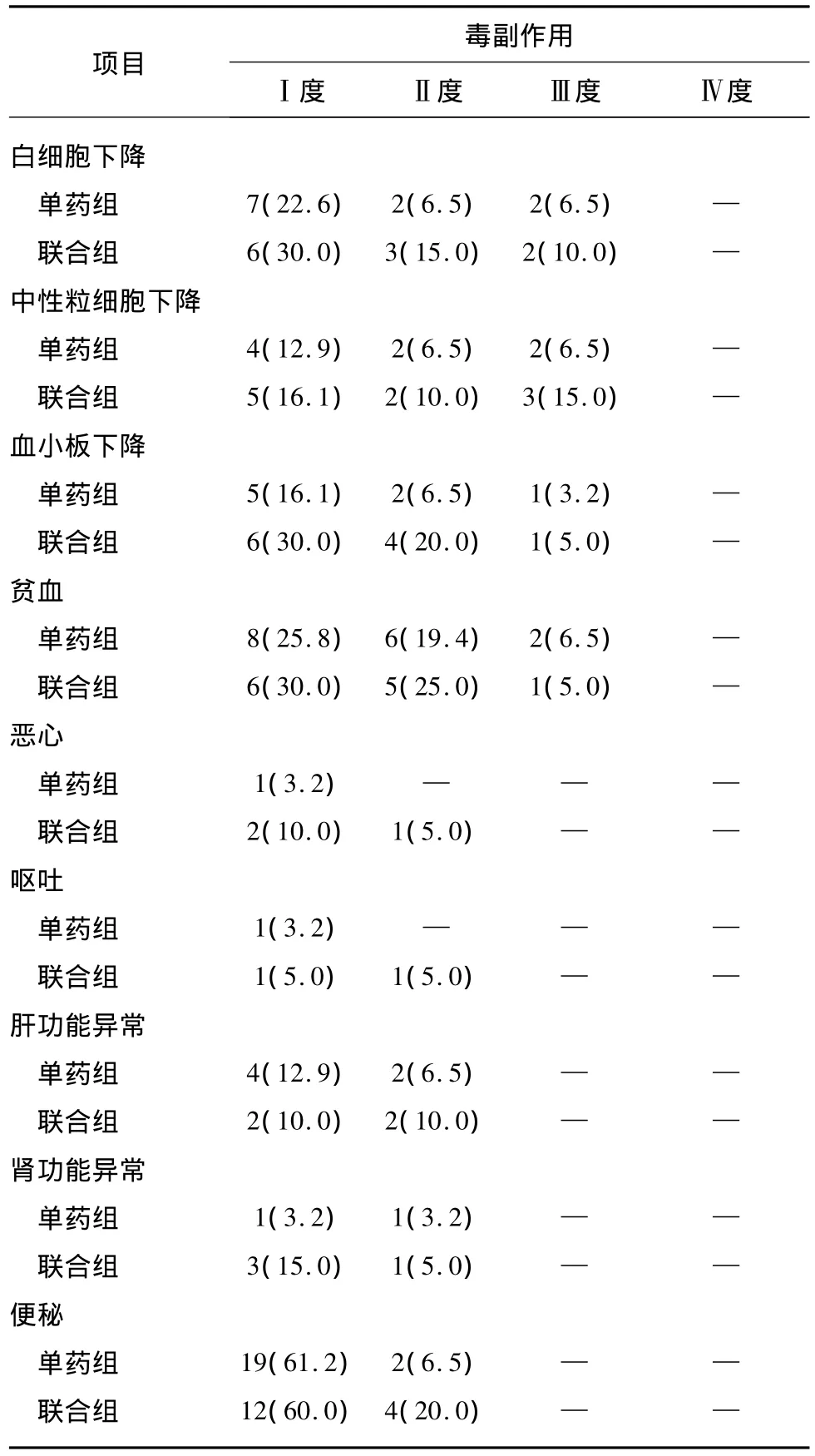
表3 51例≥75岁老年NSCLC常见毒性反应分级的数量及比例Tab.3 Comparison of toxicities of 51 NSCLC patients(≥75 y) [n(%)]
2.4 患者的临床特征与生存期
针对临床特征与生存期的多因素探索中,没有发现与生存期显著相关的临床特征。但PS评分可能是其中最为重要的临床因素:PS为2的患者1年生存率不足30%,低于PS为0~1的患者的45.5%(P=0.067),见表 4。
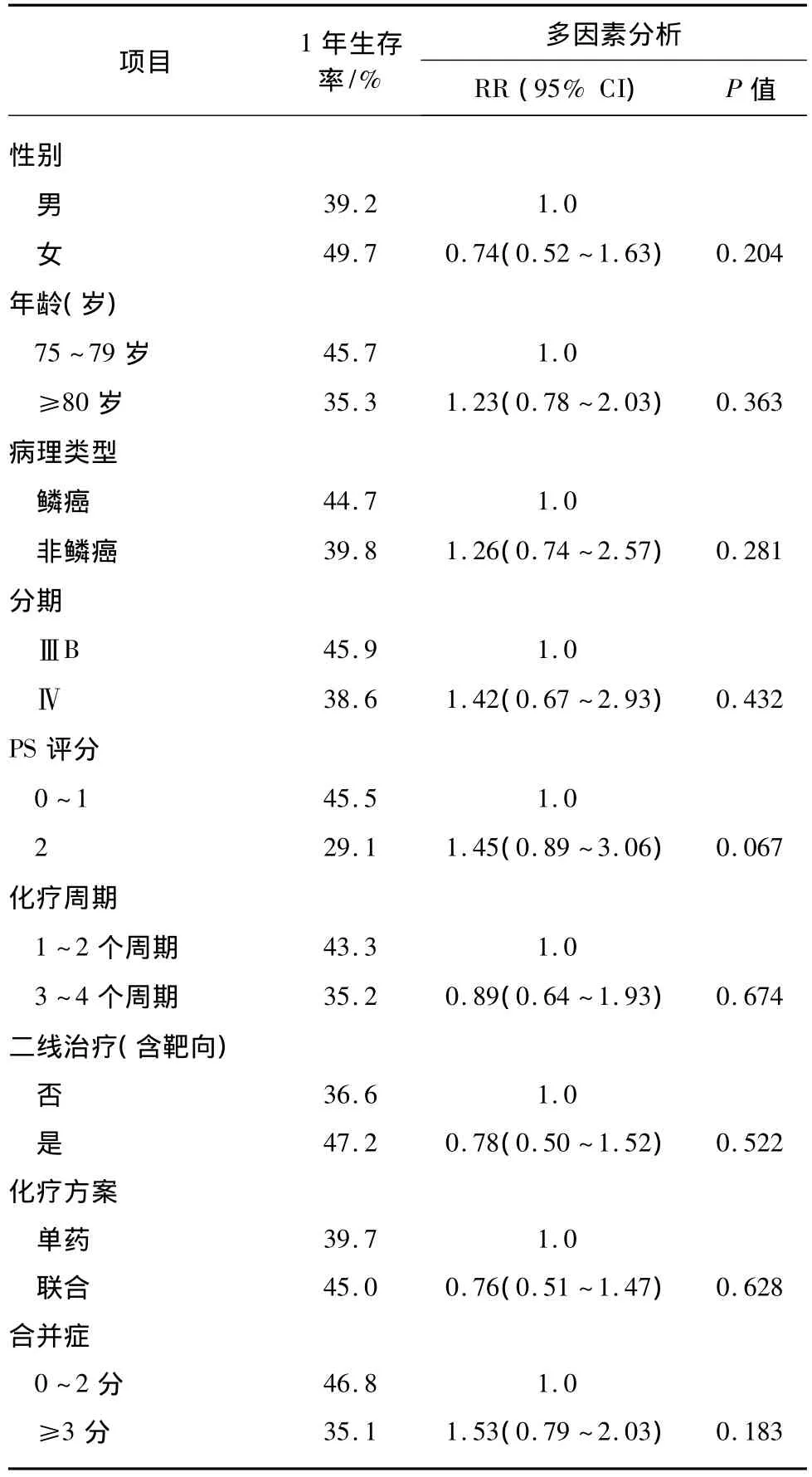
表4 51例≥75岁老年NSCLC的临床特征与生存期的多因素COX回归分析Tab.4 Comparison of multivariate COX regression analysis of 51 NSCLC patients(≥75 y)
3 讨 论
由于老年患者常常存在着许多正常生理和器官功能的改变和衰退,同时存在着较高比例的合并症,如COPD、心血管或脑血管性疾病等;以及一些老年特有的现象,如抑郁等精神状态、认知程度、家庭和社会支持等[8]。所有这些老年现象常常影响患者或者家属甚至临床工作者对老年患者治疗的态度。
长春瑞宾单药的临床研究显示,长春瑞宾可以显著地提高老年患者的生活质量以及延长生存期,从而初步确立了老年晚期肺癌患者可以从化疗中受益的观点[3]。但是,这些研究主要针对于70岁以上的老年患者,部分对于75岁以上的患者的分层分析发现,该类患者的疗效和生存期与70~74岁组患者相似,但在化疗药物的组合、剂量以及给药方案上应该更加优化或调整[9-11]。
临床研究显示,长春瑞宾联合卡铂方案治疗老年晚期NSCLC的有效率为20%,1年生存率为25%,而且耐受性较好[12]。Okamoto 等[11]的关于紫杉醇联合卡铂在老年晚期肺癌中的研究中发现75岁以上与70~74岁的患者疗效和毒副反应均相似,PR率分别为26%与30%,Ⅲ度血液学毒性分别为73%和60%。所以,含卡铂类的联合方案可作为包括75岁以上的合适的老年晚期肺癌患者的治疗方案之一。
本研究的结果显示,75岁以上的老年患者接受长春瑞宾和长春瑞宾联合卡铂的方案的OR分别为9.5%和28.6%,MST分别为7.2个月和9.3个月,1、2年OS分别为39.7%、10.0%和45.0%、13.0%,联合组的疗效稍优于单药组,但均无统计学差异。此外,多因素分析发现,PS评分与合并症可能是影响老年患者生存预后的最重要临床因素(P=0.067,0.183)。
在毒副反应方面,总体的发生率比相关资料[3,10-11]低,未见Ⅳ级以上不良反应,主要的Ⅲ度毒副反应是骨髓抑制,分别为贫血、白细胞下降、中性粒细胞下降和血小板下降,大多患者经过对症治疗后可缓解。本研究认为毒性反应率较低的原因之一可能由于部分患者的治疗周期较少等原因没有观察到相应的毒副作用。有8例患者第1周期治疗后出现白细胞及血小板的Ⅱ度以上下降而拒绝第2周期治疗,另有5例患者因为治疗中间出现合并症的加重而拒绝进一步化疗,最终导致本研究患者毒性反应发生率低和总治疗周期低。由于较多患者的化疗不能按计划方案进行,因而,影响了本组患者治疗的最终疗效、生存期以及毒性反应的分析,这一方面的研究还有待进一步深入。
总之,本研究发现对于≥75岁的老年NSCLC患者,长春瑞宾与卡铂的联合方案化疗似乎疗效更高,而且毒副反应易于耐受。PS评分与合并症可能是该类患者化疗时需要考虑的主要指标之一。由于本研究是一项回顾性的研究,存在着一些临床和治疗因素的不对称性等,因而还不能对该类老年患者的化疗方案得出完整的结论,尚需要进一步研究予以证实。
[1] Owonikoko TK,Ragin CC,Belani CP,et al.Lung cancer in elderly patients:an analysis of the surveillance,epidemiology,and end results database[J].J Clin Oncol,2007,25(35):5570-5577.
[2] Pallis AG,Gridelli C,van Meerbeeck JP,et al.EORTC elderly task force and lung cancer group and International Society for Geriatric Oncology(SIOG)experts'opinion for the treatment of non-small-cell lung cancer in an elderly population[J].Ann Oncol,2010,21(4):692-706.
[3] Gridelli C.Effects of vinorelbine on quality of life and survival of elderly patients with advanced non-smallcell lung cancer[J].J Natl Cancer Inst,1999,91(1):66-72.
[4] Maionea P,Rossia A,Sacco Pc,et al.Treating of advanced non-small cell lung cancer in the elderly[J].Ther Adv Med Oncol,2011,2(4):251-260.
[5] Kelly K,Crowley J,Bunn PA,et al.Randomized phaseⅢ trial of paclitaxel plus carboplatin versus vinorelbine plus cisplatin in the treatment of patients with advanced non-small-all lung cancer:a Southwest Oncology Group trial[J].J Clin Oncol,2001,19(3):3210-3218.
[6] Mazzanti P,Massacesi C,Rocchi MB et al.Randomized,multicenter,phaseⅡ study of gemcitabine plus cisplatin versus gemcitabine plus carboplatin in patients with advanced non-small cell lung cancer[J].Lung Cancer,2003,41(1):81-89.
[7] Charlson ME,Pompei P,Ales KL,et al.A new method of classifying prognostic comorbidity in longitudinal studies:development and validation[J].J Chronic Dis,1987,40(5):373-383.
[8] Deppermann KM.Influence of age and comorbidities on the chemotherapeutic management of lung cancer[J].Lung Cancer,2001,33(Suppl 1):S115-S120.
[9] Gridelli C,Perrone F,Gallo C et al.Chemotherapy for elderly patients with advanced non-small-cell lung cancer:the Multicenter Italian Lung Cancer in the Elderly Study(MILES)phase Ⅲ randomized trial[J].J Natl Cancer Inst,2003,95(5):362-372.
[10] Sakakibara T,Inoue A,Sugawara S,et al.Randomized phaseⅡ trial of weekly paclitaxel combined with carboplatin versus standard paclitaxel combined with carboplatin for elderly patients with advanced nonsmall-cell lung cancer[J].Ann Oncol,2010,21(4):795-799.
[11] Okamoto I,Moriyama E,Fujii S.et al.Phase Ⅱ study of carboplatin-paclitaxel ccombination chemothe-rapy in elderly patients with advanced non-small cell lung cancer[J].Jpn J Clin Oncol,2005,35(4):188-194.
[12] LeCaerH,Delhoume JY,ThomasPA,et al.Multicenter phaseⅡtrial of carboplatin/vinorelbine in elderly patients with advanced non-small-celllung cancer efficacy and impact on quality of life:Groupe Francais de Pneumo-Cancerologie Study 9902[J].Clin Lung Cancer,2005,7(2):114-120.
[13] 娄广媛,李铁,古翠萍,等.吉西他滨单药及联合卡铂治疗初治的老年晚期非小细胞肺癌疗效观察[J].中华医学杂志,2010,90(2):100-102.
[14] Crinò L,Cappuzzo F,Zatloukal P,et al.Gefitinib versus vinorelbine in chemotherapy-naive elderly patients with advanced non-small-cell lung cancer(INVITE):a randomized,phase Ⅱ study[J].J Clin Oncol,2008,26(26):4253-4260.
[15] Chen YM,TsaiCM,FanWC,et al.Phase Ⅱrandomized trial of erlotinib or vinorelbine in chemonaire,advanced,non-smallcelllung cancer patients aged 70 years or older[J]J Thorac Oncol,2012,7(2):412-418.
[16] Mok TS,Wu YL,Thongprasert S,et al.Gefitinib or carboplatin-paclitaxelin pulmonary adenocarcinoma[J].N Engl J Med,2009,361(10):947-957.

