CNAS T0612 能力验证中pH值对测定终点判断的影响
北京市海淀区药品检验所(100083)刘志杰 张静 李东辉
《CNAS T0612 滴定法测定药品中氯化钠含量》能力验证推荐采用《中国药典》2010年版的方法[1]。本方法以0.1M硝酸银溶液为滴定液,吸附指示剂荧光黄指示终点。采用本方法测定能力验证样品氧氟沙星氯化钠注射液,颜色变化不明显,无突越,终点很难判定。
1 试剂与试药
氧氟沙星氯化钠注射液(CNAS T0612 能力验证样品),0.1M硝酸银滴定液(购于北京市药品检验所)。
2 指示剂指示原理
2.1 滴定反应原理 荧光黄指示剂,是一种有机酸,在溶液中离解。
2.2 化学计量点前 溶液中Cl-过量,AgCl胶体微粒对构晶离子Cl-吸附能力强,指示剂的阴离子不被吸附,此时溶液呈黄绿色。
2.3 化学计量点后 Cl-消耗,AgCl胶体微粒吸附指示剂的阴离子,在胶体表面形成了荧光黄银化合物而呈淡红色,使整个溶液由绿色变为淡红色,指示终点到达。
3 结果
能力验证中氧氟沙星氯化钠注射液pH值约为5,为考察溶液pH对滴定终点判定的影响。本实验对比加入2.5%硼砂溶液4ml(此时溶液pH约为7),与不加硼砂溶液的结果,见附表。
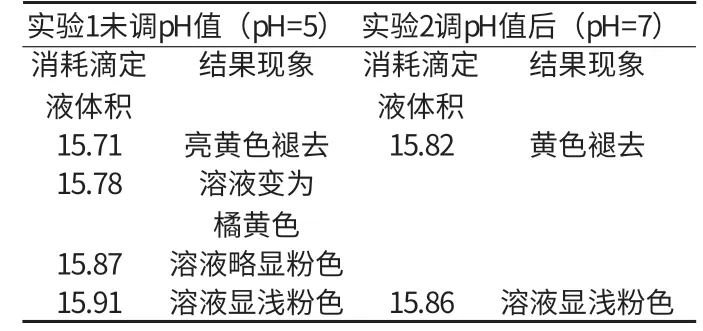
附表 不同pH值下,滴定反应的现象
从附表可以看到在未调pH值时,从亮黄色褪去到溶液显浅粉色,大约消耗0.2ml滴定液,结果相差大约0.1mg/ml。在调pH值后,从黄色褪去到溶液显浅粉色,大约消耗0.04ml滴定液,结果相差大约0.02mg/ml。在实验1中,滴定终点不灵敏,很难判定终点,这对检测人员就提出了更高的要求。在实验2中,颜色变化清晰,人员的误差小。
4 结论
在近滴定终点时,部分解离的指示剂阴离子被硝酸银胶体微粒吸附,打破了解离平衡,促进了指示剂分子的解离。这必然造成了指示终点的滞后。这一点在实验中也得到了进一步的证明,实验1的结果较实验2的结果稍偏大。控制被滴定溶液的pH值,保证指示剂主要以阴离子形式存在,可增加显色剂的灵敏度,减少了人员误差,从而保证了实验结果的准确可靠。

