移植肾长期存活受者体内人白细胞抗原抗体对移植肾功能的影响
曾毅刚 刘志宏 范昱 秦燕 丁言德 沈瑾 邱建新
(上海交通大学附属第一人民医院泌尿外科,上海 200080)
抗体介导的排斥反应是影响移植肾长期存活的主要因素之一。Colvin[1]的研究表明,人白细胞抗原(human leukocyte antigen,HLA)抗体与术后早期出现的移植物组织损伤及移植物失功有关。但是,关于HLA抗体对移植肾长期存活的影响目前仍存在争论[2]。Loupy等[3]的研究表明,不论移植前还是移植后患者体内存在的HLA抗体,都可以导致移植物的损伤。Iwasaki等[4]的研究却发现,某些HLA抗体可以保护移植物免受抗体介导的损伤作用。Terasaki等[5]对4763例肾移植患者的研究发现,移植术后20.9%受者体内出现HLA抗体,但作为一个横断面的调查有其局限性。关于肾移植受者术前体内已经存在的HLA抗体在术后体内如何变化及其对移植物长期存活的影响,目前尚缺乏深入的研究。本研究检测了肾移植10年后患者体内的HLA抗体,并与移植前HLA抗体检测的结果进行对比,以了解HLA抗体对移植肾长期存活的影响。
1 资料与方法
1.1 研究对象 本研究的长期存活肾移植受者定义为:术后移植肾带功存活10年以上且血清肌酐<177μmol/L的受者。2011年1月—2011年10月在我院治疗的符合长期存活肾移植标准的患者92例,其中男性49例,女性43例;年龄31~75岁,中位年龄(53.00±9.12)岁。92例均为初次肾移植受者,并均应用环孢霉素A、吗替麦考酚酯和醋酸泼尼松为免疫抑制药物。
1.2 HLA抗体的检测方法及分组 抽取肾移植受者外周血5 mL,分离血清,备检。应用莱姆德抗原板(LAT1240,美国One Lambda公司)、采用酶联免疫吸附法检测HLA抗体,用Bio-Tek800NB型酶标仪测定并读取结果[6]。根据移植10年后HLA抗体的检测结果,将HLA抗体阳性的肾移植受者归为阳性组,HLA抗体阴性的归为阴性组。术前HLA分型所用试剂及方法详见参考文献[7]。
1.3 移植肾功能的评价 采用日本OLYMPUS AU2700全自动生化分析仪,对92例肾移植受者进行血清肌酐检测。采用肾脏病膳食改善(the modification of diet in renal disease,MDRD)方程[8]计算估计肾小球滤过率(eGFR)。
1.4 统计学处理 采用SPSS 19.0统计软件进行统计学分析。计量资料组间比较采用One-Way ANOVA方差分析,计数资料采用卡方检验,以P<0.05为差异有统计学意义。
2 结 果
2.1 移植术前及术后10年HLA-Ⅰ、HLA-Ⅱ类抗体的变化 92例肾移植受者中,移植术前检出Ⅰ类抗体27例,而10年后仅3例检出Ⅰ类抗体;移植术前检出Ⅱ类抗体16例,10年后仅2例检出Ⅱ类抗体;并且10年后检出的抗体种类均与移植前的抗体种类不同,见表1。移植术10年后检出Ⅰ类抗体12例,其中仅3例移植前存在Ⅰ类抗体;检出Ⅱ类抗体18例,其中2例移植前存在Ⅱ类抗体,见表2。移植术前和移植术10年后,HLA抗体均为阳性的患者,其抗体种类并不相同,提示长期存活的肾移植患者体内存在的抗体均为术后新出现的HLA抗体,与移植前患者体内存在的抗体无关。

表1 肾移植前HLA抗体阳性的患者肾移植术后抗体的变化
2.2 长期存活的肾移植患者当前体内的HLA抗体对移植肾功能的影响 根据移植术10年后患者体内HLA抗体情况进行分组,抗体阳性组23例(25.0%),阴性组69例(75.0%)。两组患者的年龄、性别、术前透析时间、淋巴细胞毒活性、供肾冷/热缺血时间、术后免疫抑制治疗方案、移植术后时间等差异无统计学意义(P>0.05),见表3。阳性组患者移植术后1个月和10年的eGFR分别为(65.43±13.11)mL/(min·1.73 m2)和(66.52±14.52)mL/(min·1.73 m2),阴性组则为(52.51±16.27)mL/(min·1.73 m2)和(69.09±25.54)mL/(min·1.73 m2),组间比较差异无统计学意义(P>0.05),提示长期存活的肾移植患者体内存在的HLA抗体对移植肾功能的影响低微。
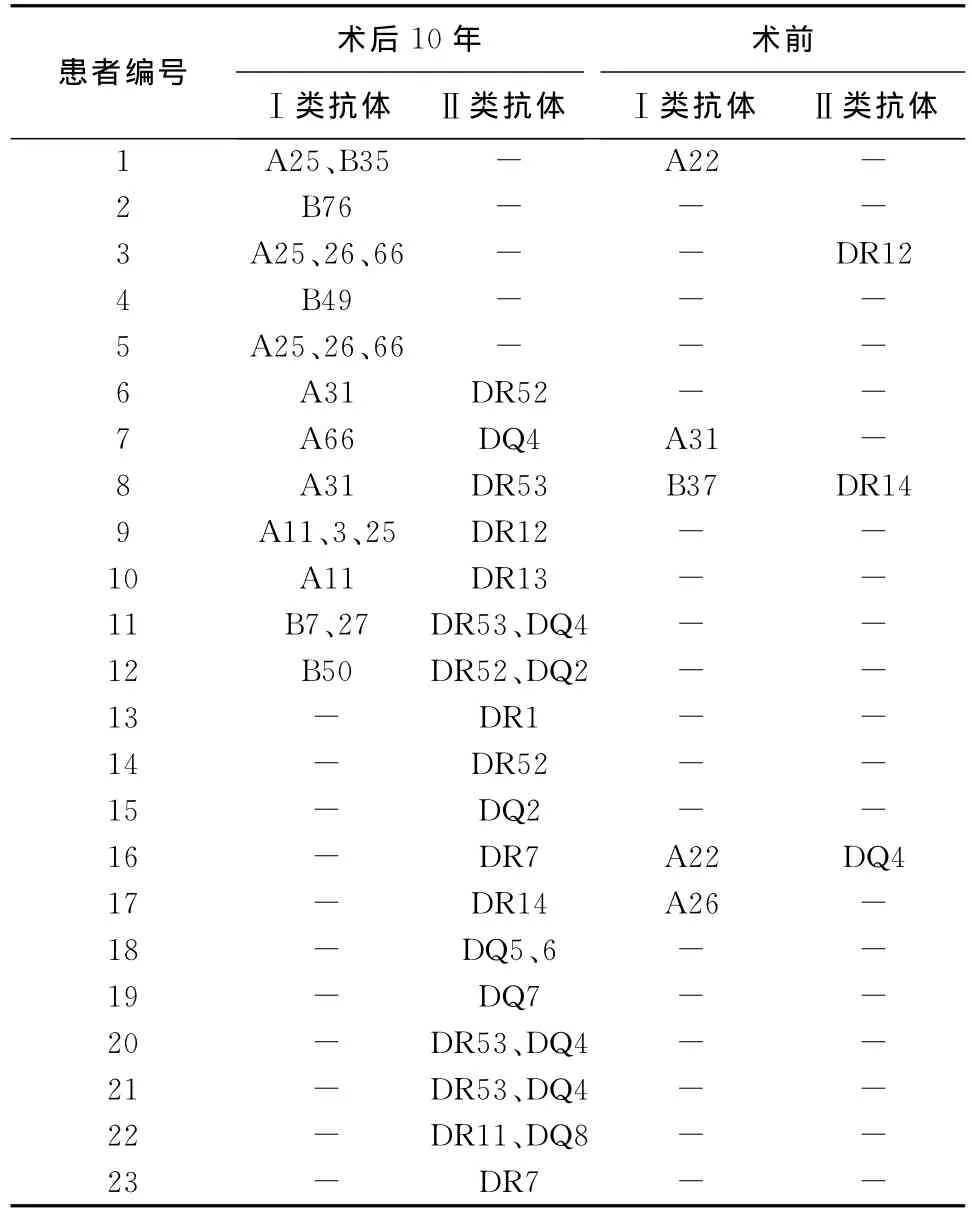
表2 肾移植10年后HLA抗体阳性的患者及其术前抗体情况
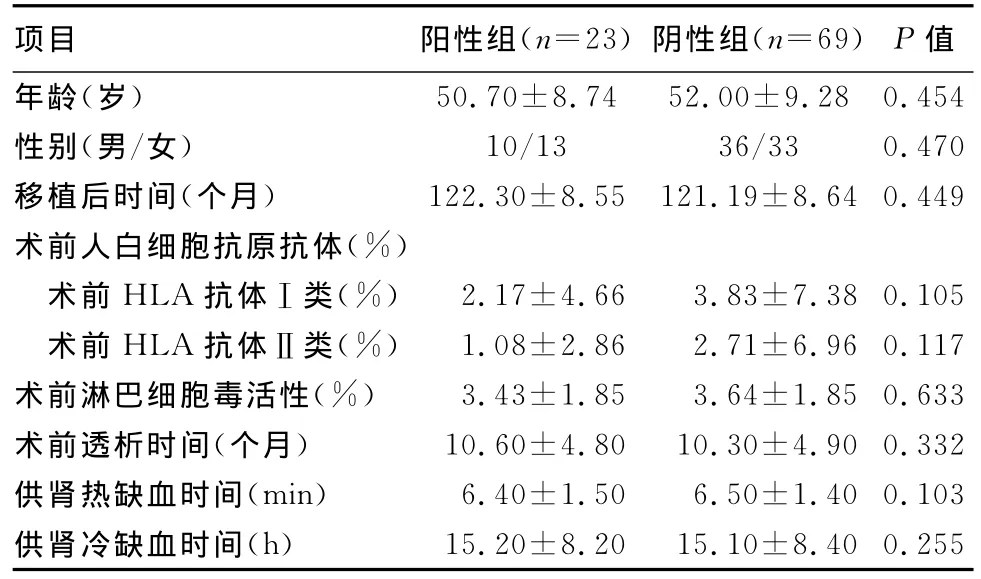
表3 HLA抗体阳性组与阴性组患者一般资料比较
2.3 移植术后供者特异性抗体(donor specific HLA antibodies,DSA)对移植肾长期存活的影响 92例患者中,DSA阳性者仅3例,占3.26%。刘志宏等[9]发现,肾移植术后1年中出现DSA的患者比例为17.4%(16/92)。唐敏英等[10]报告,在一般汉族人群中,肾移植术后DSA的阳性率为38.1%。本研究发现,在长期存活的肾移植患者中,DSA阳性患者的比例显著低于普通肾移植人群。
3 讨 论
以往研究[11]表明,HLA抗体在移植术后早期会损害移植肾甚至使移植物失功。HLA抗体出现的时点或强度都会影响移植物的近期存活[12]。2011年Banff标准[13]将HLA抗体作为移植物的体液排异反应的诊断标准之一。KDIGO(Kidney Disease:Improving Global Outcomes)指南建议,移植肾功能的评价主要以eGFR为指标。本研究通过eGFR监测发现,长期存活的肾移植患者当前体内的HLA抗体对移植肾功能的影响低微。对特异性HLA抗体进行定性分析后发现,这些抗体多为术后新出现的HLA抗体,提示对于长期存活的肾移植受者而言,移植后新出现的HLA抗体并不一定会引起移植物的损伤,甚至可能是“有益”的。Iwasaki等[4]的研究表明,肾移植患者移植后新出现的HLA抗体可以增强移植物抗排异的能力。这也可能与肾移植患者应用了有效的免疫抑制治疗方案有关。Trivedi等[14]的研究发现,免疫抑制剂尤其是蛋白酶抑制剂,可以有效抑制抗HLA抗体。也有研究[15]认为,在出现移植肾功能不全的症状之前,术后检测出与术前不同的HLA抗体并不能代表排异反应的存在。
本研究中,长期存活的肾移植人群中Ⅰ类抗体的检出率较肾移植术前显著降低,且术后检出的Ⅰ类抗体的种类与术前不同;而Ⅱ类抗体的检出率与肾移植术前无显著差异,但术后检出的Ⅱ类抗体的种类亦与术前不同。一项包括107例移植肾受者的研究[16]结果显示:血液循环中的HLA特异性抗体,尤其是Ⅰ类抗体,与抗体介导的急性排异反应或急性细胞性排异反应有关;而抗体介导的慢性损伤与抗体的特异性无关。由此可以推断:术前体内存在HLA特异性抗体,尤其是Ⅰ类抗体的移植受者大多在移植后早期发生排异反应,甚至有可能发生移植物失功,随着移植物存活时间的延长,术前体内存在的预致敏抗体渐渐消失,这可能与免疫抑制剂的应用以及抗体的吸收有关[17-18]。我们的研究发现,肾移植后患者体内可检出与术前的抗体类型不同的HLA抗体,长期存活的肾移植患者当前体内的HLA抗体对移植肾功能的影响低微。这些新出现的抗体可能来自外界抗原与HLA的交叉致敏反应,并且这种致敏性似乎只针对少数特定的抗原,也就是说这些新产生的HLA抗体所致的免疫损伤对移植肾的影响低微[19]。
除此之外,本研究还发现,移植10年后DSA阳性患者仅占3.26%。目前的研究[20]对于肾移植后患者中DSA阳性的比例颇有差别,这可能与应用不同的抗体检测技术以及不同类型的免疫抑制剂、包含不同的样本例数、对移植人群随访时间不同和移植术前存在不同的HLA特异性抗体有关。本研究对肾移植术后10年时的患者采用了与术前相同的技术方法检测HLA抗体(包括DSA),结果显示,在移植肾长期存活的肾移植患者中,DSA阳性患者的比例显著低于普通肾移植人群,这可能是因为术后出现DSA的大部分患者在长期随访中移植肾已失功。在移植肾失功的患者中,DSA介导的移植肾损伤很常见,这在一定程度上影响移植肾的长期存活[21]。文献[22]报告,肾移植患者发生排斥反应时,清除DSA可以降低移植物失功的发生率,促进移植物的长期存活。另有研究[20]发现,肾移植后DSA的检出率随时间的延长而降低,这可能是因为患者机体的自适应调节机制可以抑制抗体的产生。我们的研究发现,长期存活的肾移植患者,其当前体内的HLA抗体对移植肾功能影响不显著,这些抗体多为术后新出现的HLA抗体,以Ⅱ类抗体为主,与移植前患者体内存在的抗体无关;而肾移植后出现的DSA可能会影响移植肾的长期存活。
本研究中,我们仅检测了移植肾长期存活患者术后产生的HLA抗体,有必要进行前瞻性、多中心、大样本的研究以明确术后产生的HLA抗体与移植肾长期存活之间的关系。
[1]Colvin RB.Antibody-mediated renal allograft rejection:diagnosis and pathogenesis[J].J Am Soc Nephrol,2007,18(4):1046-1056.
[2]Leffell MS,Zachary AA.Anti-allograft antibodies:some are harmful,some can be overcome,and some may be beneficial[J].Discov Med,2010,9(48):478-484.
[3]Loupy A,Suberbielle-Boissel C,Hill GS,et al.Outcome of subclinical antibody-mediated rejection in kidney transplant recipients with preformed donor-specific antibodies[J].Am J Transplant,2009,9(11):2561-2570.
[4]Iwasaki K,Miwa Y,Haneda M,et al.Significance of HLA class I antibody-induced antioxidant gene expression for endothelial cell protection against complement attack[J].Biochem Biophys Res Commun,2010,391(2):1210-1215.
[5]Terasaki PI,Oz awa M.Predicting kidney graft failure by HLA antibodies:aprospective trial[J].Am J Transplant,2004,4(3):438-443.
[6]Toresan R,Manfro RC,Proenca MC,et al.Association between the presence of anti-HLA antibodies with acute rejection and chronic allograft nephropathy in the first year after kidney transplantation[J].Transplant Proc,2008,40(3):718-719.
[7]Opelz G,Wujciak T,Mytilineos J,et al.Revisiting HLA matching for kidney transplantation[J].Transplant Proc,1993,25(1):173-175.
[8]Levey AS,Coresh J,Greene T,et al.Expressing the Modification of Diet in Renal Disease Study equation for estimating glomerular filtration rate with standardized serum creatinine values[J].Clin Chem,2007,53(4):766-772.
[9]刘志宏,谭建明,胡志林,等.肾移植术后供者特异性抗体对移植肾近期效果的影响[J].中华器官移植杂志,2003,24(6):356-458.
[10]唐敏英,王庆华,尚乐乐,等.采用单抗原微珠抗体检测肾移植受者体内供者特异性抗体[J].中华器官移植杂志,2011,32(10):596-599.
[11]Terasaki PI,Cai J.Human leukocyte antigen antibodies and chronic rejection:from association to causation[J].Transplantation,2008,86(3):377-383.
[12]Hidalgo LG,Campbell PM,Sis B,et al.De novo donor-specific antibody at the time of kidney transplant biopsy associates with microvascular pathology and late graft failure[J].Am J Transplant,2009,9(11):2532-2541.
[13]Mengel M,Sis B,Haas M,et al.Banff 2011 Meeting report:new concepts in antibody-mediated rejection[J].Am J Transplant,2012,12(3):563-570.
[14]Trivedi HL,Terasaki PI,Feroz A,et al.Abrogation of anti-HLA antibodies via proteasome inhibition[J].Transplantation,2009,87(10):1555-1561.
[15]Gill JS,Landsberg D,Johnston O,et al.Screening for de novo anti-human leukocyte antigen antibodies in nonsensitized kidney transplant recipients does not predict acute rejection[J].Transplantation,2010,89(2):178-184.
[16]Zhang Q ,Reed EF.Non-MHC antigenic targets of the humoral immune response in transplantation[J].Curr Opin Immunol,2010,22(5):682-688.
[17]Mao Q,Terasaki PI,Cai J,et al.Analysis of HLA class I specific antibodies in patients with failed allografts[J].Transplantation,2007,83(1):54-61.
[18]Everly MJ,Terasaki PI,Trivedi HL.Durability of antibody removal following proteasome inhibitor-based therapy[J].Transplantation,2012,93(6):572-577.
[19]Morales-Buenrostro LE,Terasaki PI,Marino-Vazquez LA,et al."Natural"human leukocyte antigen antibodies found in nonalloimmunized healthy males[J].Transplantation,2008,86(8):1111-1115.
[20]Ntokou IS,Iniotaki AG,Kontou EN,et al.Long-term follow up for anti-HLA donor specific antibodies postrenal transplantation:high immunogenicity of HLA classⅡgraft molecules[J].Transpl Int,2011,24(11):1084-1093.
[21]Gaston RS,Cecka JM,Kasiske BL,et al.Evidence for antibody-mediated injury as a major determinant of late kidney allograft failure[J].Transplantation,2010,90(1):68-74.
[22]Everly MJ,Everly JJ,Arend LJ,et al.Reducing de novo donor-specific antibody levels during acute rejection diminishes renal allograft loss[J].Am J Transplant,2009,9(5):1063-1071.

