无溶剂条件下Brnsted酸离子液体催化丙三醇与醋酸的酯化反应
马慧媛,武 跃,刘秀梅,王 畅,颜佩芳
(1.辽宁师范大学化学化工学院,辽宁大连116012;2.中国科学院大连化学物理研究所中国离子液体实验室,辽宁大连116023)
无溶剂条件下Brnsted酸离子液体催化丙三醇与醋酸的酯化反应
马慧媛1,2,武 跃1,刘秀梅2,王 畅2,颜佩芳2
(1.辽宁师范大学化学化工学院,辽宁大连116012;2.中国科学院大连化学物理研究所中国离子液体实验室,辽宁大连116023)
在无溶剂条件下,以Brnsted酸离子液体为催化剂催化丙三醇与醋酸酯化反应,考察了离子液体的循环使用效率,比较了不同结构离子液体的催化性能,并讨论了离子液体的相对酸强度与其催化性能的相关性,同时对反应时间、反应物摩尔比、反应温度以及离子液体用量等条件进行了优化。结果表明,在n(Acetic acid)/n(Glycerol)=8、n([HSO3-bmim][HSO4])/n(Glycerol)=0.02、反应温度100℃、反应时间30min的优化条件下,丙三醇转化率达到97%。
离子液体(IL);酯化;酸催化;丙三醇;醋酸
随着化石资源的高强度开发利用,其储量日趋衰竭,导致原油和石化产品价格居高不下[1],而且石化资源的开采与使用带来严重的环境污染,因此发展新能源对其进行补充和替代势在必行。近年来,生物柴油作为新型可再生、可降解的清洁能源受到广泛关注[2],成为化石燃料的重要替代品。生物柴油多采用脂肪酸甲酯(FAME)与甲醇经酯交换反应制得。随着生物柴油产量的增加,副产物丙三醇大量过剩,将过量丙三醇转化为高附加值化学品具有重要的意义[3-6]。
丙三醇与醋酸酯化反应制备醋酸甘油酯是其有效的转化途径之一。酯化产物用途非常广泛[7],单醋酸甘油酯(MAG)可作为燃料的溶剂及增塑剂,二醋酸甘油酯(DAG)可用作乳化剂、水泥添加剂及硝化纤维的溶剂[8],而三醋酸甘油酯(TAG)可应用于化妆品、医药、染料、卷烟滤嘴棒的增塑剂等。
传统的醋酸甘油酯制备多采用硫酸催化法。该法严重腐蚀设备、污染环境,且催化剂回收困难。为了开发“绿色清洁”的催化丙三醇酯化转化新工艺,人们分别将酸性介孔材料[9]、TPA/Nb2O[10]5、Amberlyst-15[11]等催化剂用于该反应过程。这些催化剂在一定程度上克服了硫酸催化过程中存在的缺点,但反应时间长,催化剂易碳化、用量大和催化剂回收困难等问题仍待解决。
Brnsted酸性离子液体作为一类环境友好的新型催化材料,不但对水和空气稳定,而且同时兼具液体酸高活性和固体酸易回收的双重优点,被广泛用于催化酯化反应过程[12-14]。2007年,离子液体([HSO3-pmim][HSO4])首次被用于催化丙三醇酯化转化过程[15],获得了令人满意的三醋酸甘油酯收率(95%),但是对于离子液体的用量以及离子液体的酸性与其催化活性的关联规律问题没有进行深入讨论。
为了研究离子液体的结构、酸性与催化活性之间的相关性,以及离子液体的用量对反应的影响,笔者选择一系列结构不同的Brnsted酸离子液体为催化剂,在无溶剂条件下催化丙三醇与醋酸酯化反应,并对反应条件进行了优化。
1 实验部分
1.1 离子液体的制备
[16-17]方法合成离子液体。代表性合成步骤如下:在室温下,将N-甲基咪唑与1,4-丁烷磺内酯反应制得离子液体前驱体,然后将前驱体与硫酸等强酸等摩尔混合,在80℃下反应8h。溶剂洗涤除去非离子液体残余物,真空干燥(100℃,真空度<133Pa)4h,得到无色透明黏稠状液体即为离子液体。
1.2 离子液体的表征
采用Brucker DRX-400核磁共振波谱仪进行1H NMR和13C NMR测试,采用HP1100LC/MSD色谱-质谱联用仪测得样品的质谱数据。得到下面各离子液体样品的1H NMR和13C NMR和质谱数据。
(1)[HSO3-bmim][HSO4]
1H NMR(400MHz,D2O,δ):1.575(m,2H),1.855(m,2H),2.759-2.795(t,2H),3.726(s,3H),4.079(t,2H),7.273(d,1H),7.329(d,1H),8.559(s,1H)。
13C NMR(400MHz,D2O,δ):20.359,27.524,35.111,48.337,49.511,121.594,123.097,135.376。
ESI-MS positive mass peaks(m/z)(+):219.1[M]+;437.0[2M++HSO-4]+。
(2)[HSO3-bmim][tos]
1H NMR(400MHz,D2O,δ):1.41(m,2H),1.68(m,2H),2.07(s,3H),2.64(t,2H),3.56(s,3H),3.86(t,2H),7.04(s,1H),7.02(s,1H),7.09(s,1H),7.14(s,1H),7.38(s,1H),7.40(s,1H),8.36(s,1H)。
13C NMR(400MHz,D2O,δ):20.34,20.80,27.93,35.48,48.69,49.95,121.92,123.44,125.13,129.23,135.54,139.60,142.04。
ESI-MS positive mass peaks(m/z)(+):219.1[M]+;437[2M++tos-]+。
(3)[HSO3-bmim][NTf2]
1H NMR(400MHz,D2O,δ):1.484~1.561(m,2H),1.744~1.819(m,2H),2.682~2.72(q,2H),3.646(s,3H),3.974~4.010(t,2H),7.180~7.184(d,1H),7.240~7.244(d,1H),8.446(s,1H)。
13C NMR(400MHz,D2O,δ):20.919,29.106,36.559,49.859,51.039,115.462,118.642,121.820,123.115,124.600,125.000,136.749。
ESI-MS positive mass peaks(m/z)(+):219.1[M]+。
(4)[HSO3-bmim][OTf]
1H NMR(400MHz,D2O,δ):1.447~1.525(m,2H),1.721~1.796(m,2H),2.657~2.696(q,2H),3.628(s,3H),3.959~3.995(t,2H),7.170(d,1H),7.227~7.236(d,1H),8.452(s,1H)。
13C NMR(400MHz,D2O,δ):21.895,29.065,36.603,49.838,51.040,119.028,122.180,123.098,124.594,136.825。
ESI-MS positive mass peaks(m/z)(+):219.1[M]+。
(5)[Hmim][HSO4]
1H NMR(400MHz,DMSO,δ):3.929(s,3H),7.674(d,1H),7.740(s,1H),9.087(s,1H)。
ESI-MS positive mass peaks(m/z)(+):83.1[M]+。
(6)[Bmim][BF4]
1H NMR(400MHz,DMSO,δ):0.899~0.936(t,3H),1.255~1.313(q,2H),1.751~1.825(m,2H),3.866(s,3H),4.158~4.194(t,2H),7.686(s,1H),7.750(s,1H),9.113(s,1H)。
ESI-MS positive mass peaks(m/z)(+):139.1[M]+。
该6种离子液体符合如图1所示的分子结构。

图1 6种离子液体的分子结构Fig.1 Molecular structures of six ionic liquids
1.3 离子液体酸性检测
将离子液体配成相同浓度的水溶液(16mmol/L),以4-硝基苯胺为指示剂(2.9×10-2mmol/L),采用SHIMADZU2550紫外可见光谱仪(UV-Vis)测定指示剂与离子液体作用后的吸光度。
1.4 Brnsted酸离子液体催化丙三醇酯化反应
将离子液体(0.4mmol,0.13g)、丙三醇(40mmol,3.68g)、醋酸(320mmol,19.22g)依次加入装有回流装置的100mL圆底烧瓶中,在100℃下磁力搅拌反应30min。分别采用Agilent 6890/5973GC-MS联用仪和Agilent 7890A气相色谱仪进行产物定性和定量分析。
2 结果与讨论
2.1 离子液体的Hammett酸度函数H0
近年来对离子液体酸性测定有一些报道[18-22],其中Hammett酸性函数被认为是测定质子酸酸性的途径之一,其定义如式(1)所示。
H0=pK(I)aq+log([I]/[IH+])(1)
式(1)中,pK(I)aq为指示剂的解离常数;[I]和[IH+]分别为未被质子化的指示剂摩尔浓度和质子化的指示剂摩尔浓度。笔者选择4-硝基苯胺(pKa=0.99)为碱性指示剂,采用紫外-可见吸收光谱法测定指示剂与离子液体作用后的吸光度,结果示于图2。加入酸性离子液体后,指示剂在溶液中被质子化,未被质子化的指示剂摩尔浓度降低,吸光度值下降,因此根据指示剂吸光度值的变化可计算[I]/[IH+],再利用式(1)计算离子液体的Hammett酸度函数H0。
从图2可以看出,空白指示剂最大吸光度值出现在382nm处,不同分子结构离子液体可以使4-硝基苯胺的吸光度有不同程度的减弱。随着4-硝基苯胺吸光度下降,与之作用的离子液体的酸性逐渐增强,离子液体酸性大小顺序为[HSO3-bmim][HSO4]、[HSO3-bmim][NTf2]、[HSO3-bmim][OTf]、[HSO3-bmim][tos]、[Hmim][HSO4]、[Bmim][BF4]。这一结果表明,分子中SO3H—基团的引入对离子液体酸性提高有很大帮助,阳离子结构中有SO3H—基团的离子液体,酸性明显强于不含SO3H—基团的离子液体([HSO3-bmim][HSO4]vs[Hmim][HSO4])。SO3H—基团是提高离子液体酸性的有效功能基团。当阳离子结构相同时,阴离子结构对离子液体的酸性有很大影响,阴离子为NT和的离子液体酸性要强于阴离子为tos-和OTf-的离子液体。
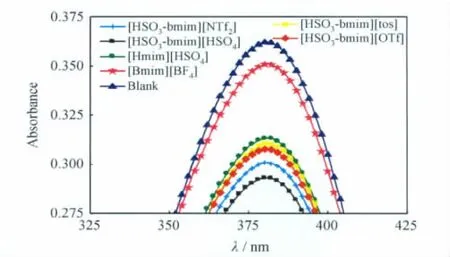
图2 4-硝基苯胺在不同离子液体水溶液中的吸光度Fig.2 Absorption spectra of 4-nitroaniline in aqueous solutions containing various ILs
2.2 Brnsted酸离子液体催化丙三醇酯化反应性能
2.2.1 离子液体的重复利用
丙三醇与醋酸酯化反应是一个典型的酸催化反应,酯化反应产物主要有单醋酸甘油酯、二醋酸甘油酯和三醋酸甘油酯,反应如方案1所示。

方案1 丙三醇和醋酸的酯化反应Scheme 1 The esterification of glycerol and acetic acid
离子液体是否能够循环利用,是其作为优秀催化材料的前提。反应结束除去未反应的乙酸,加入乙酸乙酯在冰浴中静置10h,待离子液体析出后倾倒出上层乙酸乙酯,下层离子液体在100℃下真空干燥8h后重复利用,实验结果列于表1。由表1可见,[HSO3-bmim][tos]重复使用5次后,丙三醇转化率仍保持在92%以上,说明该离子液体在催化丙三醇酯化反应中保持较高的催化活性。

表1 离子液体([HSO3-bmim][tos])在催化丙三醇酯化反应中的循环使用Table 1 Recycling of ionic liquid[HSO3-bmim][tos]in esterification of glycerol
2.2.2 离子液体酸性与其催化丙三醇酯化反应性能的关系
为了选择合适的离子液体优化反应条件,比较了不同结构离子液体催化丙三醇酯化反应性能,并将离子液体的酸性与其催化性能进行关联,结果如图3所示。从图3可以看出,当离子液体的相对酸度H0大于1.74时,丙三醇的转化率随H0的下降而上升;当H0小于1.74时,丙三醇酯化反应转化率达到高位平台。阳离子结构含SO3H—基团的离子液体在催化丙三醇酯化反应中具有非常高的催化活性,不含SO3H—基团的离子液体([Hmim][HSO4])的催化活性远不及前者,而酸性很弱的离子液体([Bmim][BF4])对该反应几乎没有催化活性;阴离子结构为HSO-4和NTf-2的SO3H—功能化离子液体催化活性优于阴离子为tos-和OTf-的SO3H—功能化离子液体,即离子液体的催化活性从高到低的顺序为[HSO3-bmim][HSO4]、[HSO3-bmim][NTf2]、[HSO3-bmim][OTf]、[HSO3-bmim][tos]、[Hmim][HSO4]、[Bmim][BF4],其中前三者的催化活性几乎相当。当Brnsted酸离子液体的相对酸度H0大于1.74时,离子液体对丙三醇酯化反应的催化活性与其酸性强弱顺序一致;当相对酸度H0小于1.74时,酸性的增强对催化活性的提高意义不大。

图3 离子液体相对酸度H0与其催化丙三醇酯化反应活性的关系Fig.3 The relationship between the relative acidity H0and catalytic performance of ionic liquids in glycerol esterification Reaction conditions:n(Acetic acid)/n(Glycerol)=8;n(IL)/n(Glycerol)=0.001;θ=100℃;t=30min
2.3 反应条件对[HSO3-bmim][HSO4]催化丙三醇酯化反应的影响
根据上述实验结果,选择离子液体([HSO3-bmim][HSO4])作为催化剂,对反应时间、原料比例、反应温度及离子液体用量等条件进行优化。
2.3.1 反应时间的影响
图4为反应时间对离子液体催化丙三醇酯化反应的转化率和选择性的影响。从图4可以看出,随着反应时间的延长,丙三醇转化率和TAG选择性逐渐上升,MAG选择性逐渐下降,而DAG选择性先上升后下降。当反应时间超过30min,丙三醇转化率及各产物的选择性基本不再变化。反应初期主要由动力学控制反应的进程,丙三醇迅速转化为MAG,MAG在强酸性条件下迅速发生深度酯化反应,生成DAG和TAG,结果导致MAG选择性下降,DAG和TAG选择性上升;而当反应时间超过10min后,反应体系接近热力学平衡,反应速率逐渐下降,同时根据反应产物组成推测,随着时间的延长,MAG、DAG会进一步与醋酸作用,发生深度酯化反应,生成三取代产物TAG。因此表现出MAG、DAG选择性下降,而TAG选择性上升。综合考虑转化率和产物分布,确定最佳反应时间为30min。

图4 反应时间对离子液体催化丙三醇与醋酸酯化反应的影响Fig.4 Effect of reaction time on the esterification of glycerol with acetic acid catalyzed by IL Reaction conditions:n(Acetic acid)/n(Glycerol)=8;n([HSO3-bmim][HSO4])/n(Glycerol)=0.05;θ=100℃
2.3.2 醋酸与丙三醇摩尔比的影响
醋酸与丙三醇摩尔比(n(Acetic acid)/n(Glycerol))对离子液体催化丙三醇与醋酸酯化反应性能的影响如图5所示。丙三醇的转化率和DAG选择性随着n(Acetic acid)/n(Glycerol)的增加而上升,在n(Acetic acid)/n(Glycerol)>4时,基本维持稳定;TAG选择性随着n(Acetic acid)/n(Glycerol)的增加而上升,当n(Acetic acid)/n(Glycerol)>6时,变化趋势减缓,继续增加n(Acetic acid)/n(Glycerol)至8后,TAG选择性几乎不再变化。MAG选择性随着n(Acetic acid)/n(Glycerol)的增加而下降,当n(Acetic acid)/n(Glycerol)>8时,基本维持恒量。增大n(Acetic acid)/n(Glycerol),有利于反应正向进行,但过量醋酸会使离子液体酸性下降。综合以上因素,选择n(Acetic acid)/n(Glycerol)为8。
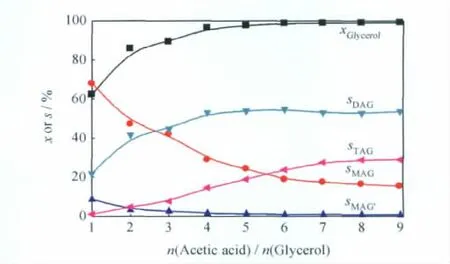
图5 n(Acetic acid)/n(Glycerol)对离子液体催化丙三醇与醋酸酯化反应的影响Fig.5 Effect of n(Acetic acid)/n(Glycerol)on the esterification of glycerol with acetic acid catalyzed by IL Reaction conditions:n([HSO3-bmim][HSO4])/n(Glycerol)=0.05;θ=100℃;t=30min
2.3.3 反应温度的影响
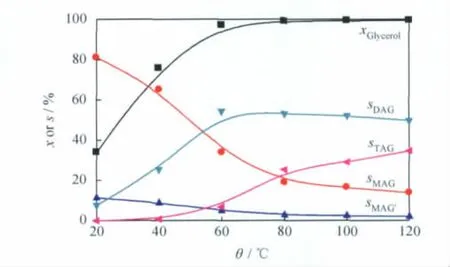
图6 反应温度对离子液体催化丙三醇与醋酸酯化反应的影响Fig.6 Effect of reaction temperature on the esterification of glycerol with acetic acid catalyzed by IL Reaction conditions:n(Acetic acid)/n(Glycerol)=8;n([HSO3-bmim][HSO4])/n(Glycerol)=0.05;t=30min
反应温度对离子液体催化丙三醇与醋酸酯化反应的影响如图6所示。由图6可看出,随着反应温度的升高,丙三醇转化率、DAG和TAG选择性逐渐上升,而MAG的选择性逐渐下降。在高温条件下MAG容易与醋酸发生深度酯化反应,生成二、三取代产物,所以导致MAG选择性下降,DAG和TAG选择性上升。即低温有利于MAG生成,高温有利于TAG生成。综合考虑丙三醇的转化率、各产物选择性等因素,反应温度选择100℃为宜。
2.3.4 离子液体用量的影响
离子液体用量(n([HSO3-bmim][HSO4])/n(Glycerol))对丙三醇与醋酸酯化反应转化率和选择性的影响如图7所示。随着n([HSO3-bmim][HSO4])/n(Glycerol)的增加,丙三醇转化率逐渐上升直至几乎完全转化,MAG选择性下降,DAG和TAG选择性先上升;当n([HSO3-bmim][HSO4])/n(Glycerol)超过0.02时,不再有明显变化。随着n([HSO3-bmim][HSO4])/n(Glycerol)的增加,反应体系的酸性增强,促进酯化反应向正反应方向进行。由图7可知,在离子液体n([HSO3-bmim][HSO4])/n(Glycerol)为0.02时,丙三醇的转化率和产物选择性几乎趋于稳定,说明其有较好的催化活性。

图7 离子液体[HSO3-bmim][HSO4]用量对丙三醇与醋酸酯化反应的影响Fig.7 Effect of[HSO3-bmim][HSO4]amount on the esterification of glycerol with acetic acid Reaction conditions:n(Acetic acid)/n(Glycerol)=8,θ=100℃,t=30min

方案2 SO3H-功能化离子液体催化丙三醇与醋酸酯化反应可能的反应历程Scheme 2 Possible reaction mechanism of the esterification of glycerol with acetic acid catalyzed by SO3H-functional ionic liquids
2.4 离子液体催化丙三醇酯化反应机理推测
根据上述结果与讨论,提出了SO3H-功能化离子液体催化丙三醇与醋酸酯化反应可能的反应机理,见方案2。离子液体SO3H-基团上的质子先和醋酸中的羧基形成钖盐,此步反应很快完成,这样就使羧基的碳原子带有更高的正电性,有利于亲核试剂的进攻;丙三醇中的1个伯羟基作为亲核试剂对羰基碳进攻,酸的酰氧键断开,脱去1分子H2O,再失去1个H+,形成单醋酸甘油酯;脱下的H+继续进攻醋酸中的羧基形成钖盐,单醋酸甘油酯中的另一个伯羟基对羰基碳原子进行亲核进攻,导致醋酸的酰氧键断开,脱去1分子H2O形成二醋酸甘油酯,同时失去1个H+。同理,二醋酸甘油酯中的仲羟基与质子化的乙酸发生亲核反应即得到三醋酸甘油酯。然而由于亲核试剂空间位阻过大,进攻困难,导致三取代产物收率低。
3 结 论
(1)SO3H—功能化离子液体在无溶剂条件下催化丙三醇与醋酸酯化反应表现出较好的重复使用性能,循环使用5次后,仍保持较高的催化活性。
(2)离子液体的酸性由阴、阳离子共同决定,SO3H—基团的引入对酸性的提高至关重要。在一定酸度范围内,酸性与催化活性呈正相关。当Brnsted酸离子液体的相对酸度H0大于1.74时,随着离子液体酸性的增强,丙三醇的转化率逐渐上升;当H0小于1.74时,增强酸性对催化活性无明显改善。
(3)在离子液体([HSO3-bmim][HSO4])作为催化剂,n(Acetic acid)/n(Glycerol)=8时:在n([HSO3-bmim][HSO4])/n(Glycerol)=0.001、100℃条件下反应30min,MAG收率可达51.9%(选择性为63.5%);在n([HSO3-bmim][HSO4])/n(Glycerol)=0.05、100℃条件下反应7min,DAG收率可达59.8%(选择性为60.4%);在n([HSO3-bmim][HSO4])/n(Glycerol)=0.05、120℃条件下反应30min,TAG收率可达34.4%(选择性为34.6%)。
(4)在n(Acetic acid)/n(Glycerol)=8、n([HSO3-bmim][HSO4])/n(Glycerol)=0.02、反应温度100℃、反应时间30min的优化条件下,丙三醇转化率达到97%。
(5)根据实验结果推测了该反应可能的机理。由于亲核试剂受空间位阻的影响,导致三取代产物(TAG)收率低,酯化反应停留在生成二取代产物(DAG)阶段。
参考文献
[1]闵恩泽.利用可再生农林生物质资源的炼油厂——推动化学工业迈入“碳水化合物”新时代[J].化学进展,2006,18(2-3):131-141.(MIN Enze.Developing biorefinery by utilizing agriculture and forestry biomass resources:Striding forward[J].Progress In Chemistry,2006,18(2-3):131-141.
[2]MA F R,HANNA M A.Biodiesel production:A review[J].Bioresource Technology,1999,70(1):1-15.
[3]ZHOU C H,BELTRAMINI J N,FAN Y X,et al.Chemoselective catalytic conversion of glycerol as a biorenewable source to valuable commodity chemicals[J].Chemical Society Reviews,2008,37(3):527-549.
[4]CORMA A,IBORRA S,VELTY A.Chemical routes for the transformation of biomass into chemicals[J].Chemical Reviews,2007,107(6):2411-2502.
[5]BARRAULT J,POUILLOUX Y,CLACENS J M,et al.Catalysis and fine chemistry[J].Catalysis Today,2002,75(1-4):177-181.
[6]JONES M C,TEWARI P,BLEI C,et al.Selfassembled nanocages for hydrophilic guest molecules[J].Journal of the American Chemical Society,2006,128(4-5):14599-14605.
[7]BEHR A,EILTING J,IRAWADI K,et al.Improved utilisation of renewable resources:New important derivatives of glycerol[J].Green Chemistry,2008,10(1):13-30.
[8]TAGUCHI Y,OISHI A,IKEDA Y,et al.Copolymerization structure of biodegradable macromolecular aliphatic polyester-has aliphatic polyester expressed by specific formula involving divalent aliphatic groups:US,6180751-B1[P].2001.
[9]MELERO J A,GRIEKEN R,MORALES G,et al.Acidic mesoporous silica for the acetylation of glycerol:Synthesis of bioadditives to petrol fuel[J].Energy Fuels,2007,21(3):1782-1791.
[10]BALARAJU M,NIKHITHA P,JAGADEESWARAIAH K,et al.Acetylation of glycerol to synthesize bioadditives over niobic acid supported tungstophosphoric acid catalysts[J].Fuel Processing Technology,2010,91(2):249-253.
[11]VALTER L C GONCALVES,BIANCA P PINTO,JOAO C SILVA,et al.Acetylation of glycerol catalyzed by different solid acids[J].Catalysis Today,2008,133-135:673-677.
[12]ZHU H P,YANG F,TANG J,et al.Brnsted acidic ionic liquid 1-methylimidazolium tetrafluoroborate:Agreen catalyst and recyclable medium for esterification[J].Green Chemistry,2003,5(1):38-39.
[13]FRAGA-DUBREUIL J,BOURAHLA K,RAHMOUNI M,et al.Catalysed esterifications in room temperature ionic liquids with acidic counteranion as recyclable reaction media[J].Catalysis Communications,2002,3(5):185-190.
[14]MIAO J M,WAN H,GUAN G F.Synthesis of immobilized Brnsted acidic ionic liquid on silica gel as heterogeneous catalyst for esterification[J].Catalysis Communications,2011,12(5):353-356
[15]LU L,YU S T,XIE C X.Synthesis of glycerol triacetate using functionalized ionic liquid as catalyst[J].Journal of Chemical Technology and Biotechnology,2009,84(11):1649-1652.
[16]COLE A C,JENSEN J L,N TAI I,et al.Novel Brnsted acidic ionic liquids and their use as dual solvent-catalysts[J].Journal of the American Chemical Society,2002,124(21):5962-5963.
[17]GU Y L,SHI F,DENG Y Q.SO3H-functionalized ionic liquid as efficient,green and reusable acidic catalyst system for oligomerization of olefins[J].Chemical Communications,2003,4(11):597-601.
[18]XU D Q,WU J,LUO S P,et al.Fischer indole synthesis catalyzed by novel SO3H-functionalized ionic liquids in water[J].Green Chemistry,2009,11(8),1239-1246.
[19]THOMAZEAU C,OLIVIER-BOURBIGOU H,MAGNA L,et al.Determination of an acidic scale in room temperature ionic liquids[J].Journal of the American Chemical Society,2003,125(18),5264-5265.
[20]GU Y L,ZHANG J,DUAN Z Y,et al.Pechmann reaction in non-chloroaluminate acidic ionic liquids under solvent-free conditions[J].Advanced Synthesis &Catalysis,2005,347(4):512-516.
[21]XING H B,WANG T,ZHOU Z H,et al.The sulfonic acid-functionalized ionic liquids with pyridinium cations:Acidities and their acidity-catalytic activity relationships[J].Journal of Molecular Catalysis A:Chemical,2007,264(1-2):53-59.
[22]WANG Y Y,JIANG D,DAI L Y.Novel Brnsted acidic ionic liquids based on benzimidazolium cation:Synthesis and catalyzed acetalization of aromatic aldehydes with diols[J].Catalysis Communications 2008,9(15):2475-2480.
Brnsted Acidic Ionic Liquids Catalytic Performance for Esterification of Glycerol and Acetic Acid Under Solvent-Free Condition
MA Huiyuan1,2,WU Yue1,LIU Xiumei2,WANG Chang2,YAN Peifang2
(1.School of Chemistry and Chemical Engineering,Liaoning Normal University,Dalian116012,China;2.China Ionic Liquid Laboratory,Dalian Institute of Chemical Physics,Chinese Academy of Sciences,Dalian116023,China)
Esterification of glycerol with acetic acid was carried out by using a series of Brnsted acidic ionic liquids as catalyst in solvent-free condition.The recycling of ionic liquid was evaluated.The catalytic performance of different kinds of ionic liquids was measured.The relationship between the Brnsted acidity-catalytic activity and the relative acidity were studied.Moreover,the reaction conditions of reaction time,molar ratio of reactants,reaction temperature and ionic liquid amount were optimized.The results indicated that under the optimized reaction conditions of 100℃,30min,n(Acetic acid)/n(Glycerol)=8,n([HSO3-bmim][HSO4])/n(Glycerol)=0.02,the conversion of glycerol was 97%.
ionic liquid;esterification;acid catalysis;glycerol;acetic acid
book=2012,ebook=1
O643.32
A
10.3969/j.issn.1001-8719.2012.03.008
1001-8719(2012)03-0399-08
2011-06-10
国家自然科学基金(21006102)、中国科学院知识创新工程领域前沿项目(DICP K2009D03)和大连理工大学精细化工国家重点实验室开放课题基金项目(KF1009)资助
马慧媛,女,硕士,从事新型功能化离子液体的设计合成与应用研究;E-mail:keaihuiyuan@163.com
刘秀梅,女,助理研究员,博士,从事新型功能化离子液体的设计合成与应用研究;Tel:0411-84379167;E-mail:liuxiumei@dicp.cn

