华蟾素胶囊中5-羟色胺的含量测定方法研究
宋愿智 宋 哲 李秋菲
1.陕西省食品药品检验所,陕西西安 710061;2.西安市红十字会医院,陕西西安 710054
华蟾素胶囊是由华蟾素片改变剂型而成的制剂,华蟾素片收藏于中华人民共和国卫生部药品标准中药成方制剂标准第14册,标准代号为WS3-B-2564-97。本品由单味干蟾皮经提取精制而成,具有解毒、消肿、止痛功效,主要用于中、晚期肿瘤,慢性乙型肝炎等的治疗[1]。原片剂质量标准中无含量测定项,为有效控制本品质量,依据SFDA《药品注册管理办法》及相关技术指导原则[2-4],本资料对其质量标准,特别是对含量测定方法进行了研究。据资料报道[5-6],干蟾皮中含有多种化学成分,如华蟾蜍毒素、华蟾蜍素及次素、去乙酰华蟾素、蟾蜍配基、脂蟾毒配基、吲哚类生物碱(如蟾酥碱,蟾酥甲碱)等。吲哚类生物碱具有一定的药理作用,特别是5-羟色胺(Serotonine),因此笔者以此为指标对其含量测定进行研究,研究结果证明,该方法简便易行,结果准确、可靠,方法重现性较好,可以作为其制剂质量控制的一种方法。
1 仪器与试剂
1.1 仪器
TU-1810紫外可见分光光度计(北京普折通用仪器有限责任公司);赛多利斯BP211D电子天平。
1.2 试药
5-羟色胺对照品(批号111656-200401,中国药品生物物品检定所,供含量测定用);华蟾素胶囊(市场购得,陕西东泰制药有限公司,Z20056846);所用试剂均为分析纯(西安化学试剂厂)。
2 方法与结果
2.1 溶液的配制
2.1.1 对照品溶液的制备 精密称取在五氧化二磷干燥器中真空干燥至恒重的5-羟色胺对照品2 mg,置50 mL量瓶中,加水溶解并稀释至刻度,摇匀,即得。
2.1.2 供试品溶液制备 取本品装量差异项下的内容物,研细,取约0.5 g,精密称定,置索氏提取器中,加三氯甲烷适量,加热回流至提取液近无色,放冷,弃去三氯甲烷液,药渣挥干三氯甲烷。再加甲醇适量,加热回流2 h,放冷,甲醇液水浴上蒸干,残渣加水适量使溶解,转移至25 mL量瓶中,并用水稀释至刻度,摇匀,滤过,即得。
2.2 测定波长选择
分别取对照品、供试品溶液按拟定的含量测定方法操作,显色后在500~600 nm进行扫描,结果两者均在556 nm处有最大吸收,故选此波长为测定波长。见图1。
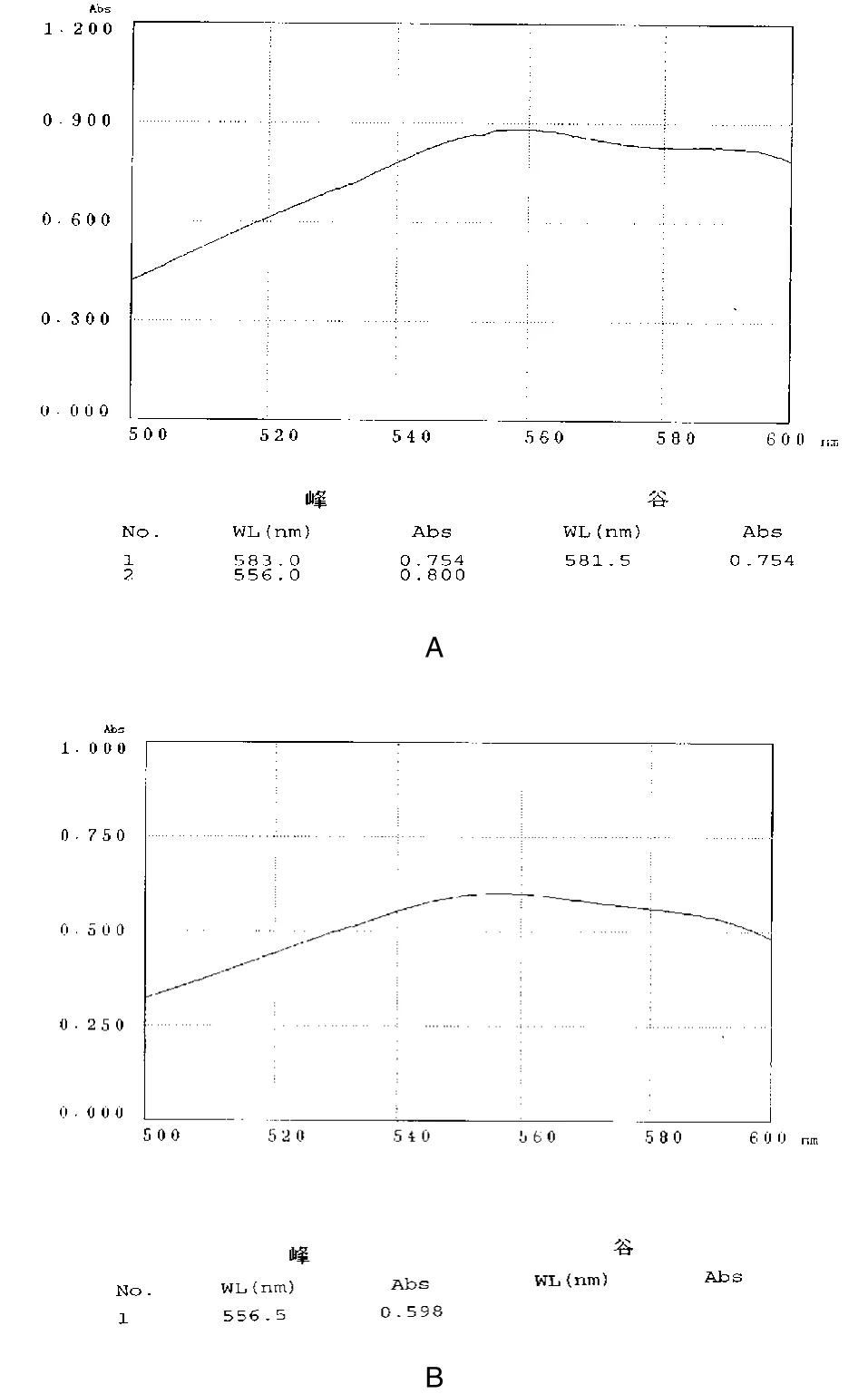
图1 对照品、供试品溶液波长测定
2.3 线性关系考察
精密量取对照品溶液 1.0、2.0、3.0、4.0 和 5.0 mL,分别置10 mL量瓶中,各加水使5.0 mL,摇匀,加15%对二甲氨基苯甲醛盐酸溶液(2→3)至刻度,摇匀,放置30 min。按照分光光度法,在556 nm波长处测定吸收度,以吸收度值为纵坐标,5-羟色胺量为横坐标,绘制标准曲线。见图2。结果5-羟色胺在0.044 5~0.222 5mg范围内,线性关系良好,回归方程为:y=3.891 2x+0.087 1,相关系数为:r=0.998 8。

表1 5-羟色胺加样回收率试验结果表(n=6)
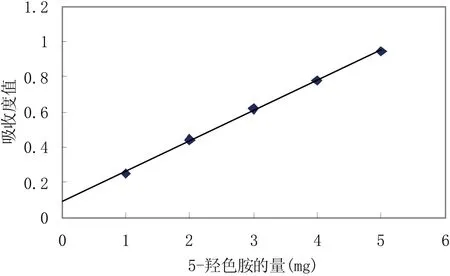
图2 5-羟色胺的吸收度曲线
2.4 精密度试验
取供试品溶液,按拟定的含量测定方法操作,5次连续测定其吸收度值,计算RSD为0.66%。试验结果表明,精密度良好。
2.5 稳定性试验
取供试品溶液,按拟定的含量测定方法操作,于0、30、60、90、120、150和180 min测定吸收度值。结果在本试验条件下,供试品在3 h内稳定,显色30 min后就基本稳定,RSD为1.66%。
2.6 重现性试验
取同一批华蟾素胶囊5份样品,按供试品溶液制备方法制备和测定,结果RSD为2.38%,说明重现性良好。
2.7 加样回收率试验
取同一批已知含量的华蟾素胶囊6份样品,精密加入一定量的5-羟色胺对照品溶液,按拟定的含量测定方法测定吸收度值,计算回收率。结果平均回收率为96.77%,RSD为1.42%。见表1。
2.8 样品测定
取10批样品,按供试品溶液的制备方法制备并测定,结果10 批样品中 5- 羟色胺含量为 0.303、0.289、0.255、0.295、0.257、0.263、0.281、0.256、0.273和 0.239 mg/粒,平均含量为0.271 mg/粒。
3 讨论
3.1 供试品溶液的制备
由于吲哚类生物碱在三氯甲烷、乙酸乙酯等有机溶剂中不溶,而在水、甲醇中溶解度较大;但用水提取供试品溶液中杂质较多。故笔者先用三氯甲烷除去一些脂溶性和甾体类成分(特别是后者可与对二甲氨基苯甲醛显色剂反应显色),再用甲醇回流提取吲哚类生物碱,与显色剂反应后,测定其含量。
3.2 提取方法的考察
取本品内容物适量,研细,精密称取4份,每份约0.5 g,置索氏提取器中,加三氯甲烷适量,加热回流至提取液为无色,放冷,弃去三氯甲烷液。将药渣挥干三氯甲烷,加甲醇适量,分别用超声和回流两种不同的方法提取1 h,过滤,用甲醇适量分次洗涤容器及残渣,滤液和洗涤液置同一蒸发皿中,水浴上蒸干,残渣加水适量使溶解,并转移至25 mL量瓶中,加水稀释至刻度,摇匀,过滤,即可。按拟定的含量测定方法测定每份含量。结果回流提取吲哚类总生物碱的含量最高,所以提取方法确定为回流提取。为保证提取完全,采用索氏提取器中提取。同时对加热回流提取时间进行了考察,分别于加热回流1、2、3、4 h,按拟定方法测定含量。结果回流提取2 h,提取液颜色变浅,且含量最高,所以确定回流提取时间为2 h。
[1] 中华人民共和国卫生部药典委员会.卫生部药品标准·中药成分制剂[S].第14册.1997:42.
[2] 国家食品药品监督管理局.药品注册管理办法(局令28号)[S].2007-7-10.
[3] 国家食品药品监督管理局.药物研究技术指导原则(2005)[M].北京:中国医药科技出版社,2005:196.
[4] 国家药典委员会.中国药典2010年版一部[S].北京:中国医药科技出版社,2010:205.
[5] 江苏新医学院.中药大辞典[M].上海:上海科学技术出版社,1986:5688-5690.
[6] 杨力宏.中华大蟾蜍皮化学成分的研究[J].药学学报,1992,27(9):679.

