环戊烯水合法制环戊醇的研究Ⅰ.催化剂和溶剂对水合反应的影响
杨晓辉,宋 健,吴 杰,孙树娟,冯荣秀
(天津大学 化工学院,天津 300072)
精细化工
环戊烯水合法制环戊醇的研究Ⅰ.催化剂和溶剂对水合反应的影响
杨晓辉,宋 健,吴 杰,孙树娟,冯荣秀
(天津大学 化工学院,天津 300072)
以强酸性阳离子交换树脂为催化剂、苯酚为溶剂、环戊烯为原料采用直接水合法合成了环戊醇,考察了12种强酸性阳离子交换树脂催化剂在90℃和135℃下的催化活性,初步筛选出6种耐高温阳离子交换树脂催化剂,研究了这6种催化剂的催化活性与温度的关系,同时考察了溶剂种类对水合反应的影响,得到了适宜的反应条件。实验结果表明,Amberlyst 36催化剂的活性最高;丁醇是该水合反应的最佳溶剂。以Amberlyst 36为催化剂、丁醇为溶剂,在水与环戊烯摩尔比为6∶1、环戊烯与丁醇质量比为1∶1、反应温度160℃、反应压力1.20 MPa、反应时间4 h、搅拌转速600 r/min的条件下,环戊醇选择性为97.46%,环戊烯转化率为 11.13% 。
强酸性阳离子交换树脂催化剂;环戊烯;环戊醇;苯酚;丁醇;水合反应
环戊醇是一种重要的精细化工中间体[1],主要用于制备溴代环戊烷、氯代环戊烷、抗菌药、抗过敏药等产品。目前工业上主要以己二酸为原料生产环戊醇,该方法转化率和选择性均较高,但由于己二酸成本高、工艺路线长、环境污染严重,导致产品的价格较高,限制了该工艺的进一步发展。以环戊烯为原料制备环戊醇的方法有间接水合法和直接水合法两种,其中,间接水合法的转化率较高(70%以上)、选择性较好(90%以上)[2-3],但催化剂硫酸对设备腐蚀严重,在硫酸回收套用时浓缩过程能耗大。直接水合法虽然转化率较低,但解决了设备腐蚀、能耗大等问题,因此越来越受到人们的关注,目前正处于研究阶段。
文献[4-9]报道了烯烃直接水合制备有机醇的技术,其中所用的催化剂有强酸性阳离子交换树脂、分子筛和沸石等。Nuntasri等[10-11]以分子筛为催化剂合成了环戊醇,环戊烯转化率为10.1%,环戊醇选择性为99.5%,此方法的缺点是反应时间长、耗水量大。分子筛是环戊醇脱水的有效催化剂,这表明以分子筛为催化剂合成环戊醇时,环戊烯的转化率不会太高。文献[12-13]以PCR145H(一种质子型苯乙烯基磺酸阳离子交换树脂)为催化剂合成了环戊醇,但都存在环戊烯转化率低、原料环戊烯循环量大等缺点。
本工作以苯酚为溶剂,采用环戊烯直接水合法合成了环戊醇,考察了12种强酸性阳离子交换树脂催化剂对水合反应的影响,筛选出适宜的催化剂,同时对苯酚体系下存在的副反应进行了研究。此外还考察了溶剂种类对水合反应的影响,确定了较优的溶剂体系。
1 实验部分
1.1 原料
环戊烯:纯度99%,上海共禾化工有限公司;蒸馏水:天津市蓝水晶净化制冷设备技术有限公司;苯酚:工业纯,中国石油吉林石化分公司;DNW -Ⅰ,DNW-Ⅱ催化剂:工业级,丹东明珠特种树脂有限公司;D72,001×7,NKC-9催化剂:工业级,南开大学化工厂;ZGC107,CD350,CD450催化剂:工业级,杭州争光树脂有限公司;Ameberlyst 15,Ameberlyst 35,Ameberlyst 36,Ameberlyst 45 催化剂:工业级,Rohm and Haas Company。树脂催化剂的各项技术指标见表1。

表1 树脂催化剂的各项技术指标Table 1 Specification of the strong acidic cation exchange resin catalysts
1.2 分析方法
采用ThermoFisher Scientific公司HPG1800A型气相色谱-质谱联用仪和北京北分瑞利分析仪器(集团)有限责任公司SP-1000型气相色谱仪对试样进行定性、定量分析。
1.3 实验方法
在反应釜中依次加入43.20 g蒸馏水(2.40 mol)、27.20 g 溶剂、9.70 g 催化剂和 27.20 g(0.40 mol)环戊烯,密封反应釜,用N2置换体系3次,升高压力至1.20 MPa,边慢速搅拌(搅拌转速300 r/min)边将温度升至反应温度,然后将搅拌转速调至600 r/min并保持4 h。反应结束后,将反应体系自然冷却至50℃以下,然后分别用水和冰水冷却至10℃以下,停止搅拌,压力降至常压。用160 μm的标准筛滤去催化剂,反应液分层,将水层和有机层分别进行GC分析。蒸馏有机层得到环戊醇。
2 结果与讨论
2.1 催化剂种类对水合反应的影响
以强酸性阳离子交换树脂为催化剂催化环戊烯进行水合反应时,反应在树脂相内进行,反应速率由反应物环戊烯和生成物环戊醇在树脂相中的扩散速率和颗粒内进行的反应速率共同决定。Wulff等[14]认为树脂催化剂的活性是由其本身的酸性和活性点的可接近度决定的,影响酸性和可接近度的主要因素与树脂的性能(交换容量、交联度、孔结构和颗粒大小)有关。
水合反应是可逆的放热反应,反应温度低于90℃时,体系提供的能量低于反应活化能,反应难以进行,且催化剂的活性较低,反应速率较慢,在一定的反应时间内收率太低;反应温度太高时平衡对逆反应有利,若反应温度超过树脂催化剂的使用温度,树脂催化剂的活性也会下降。根据树脂催化剂的性质,选择90℃和135℃两个反应温度对催化剂的活性进行初步考察,实验结果见表2。由表2可见,无论使用何种树脂催化剂,在反应温度为90℃时,环戊烯的转化率均较低,且部分树脂催化剂的环戊醇选择性也较低。GC分析结果表明,90℃下,主要副反应是烷基化反应。当反应温度为135℃时,环戊醇选择性及环戊烯转化率均较高。这是因为随反应温度的升高,树脂催化剂膨胀度增大,活性点的可接近度也增大,环戊烯传质容易,更易于接近活性基团,使催化剂表现出较高的活性。因此,在一定范围内升高反应温度有利于水合反应的进行。
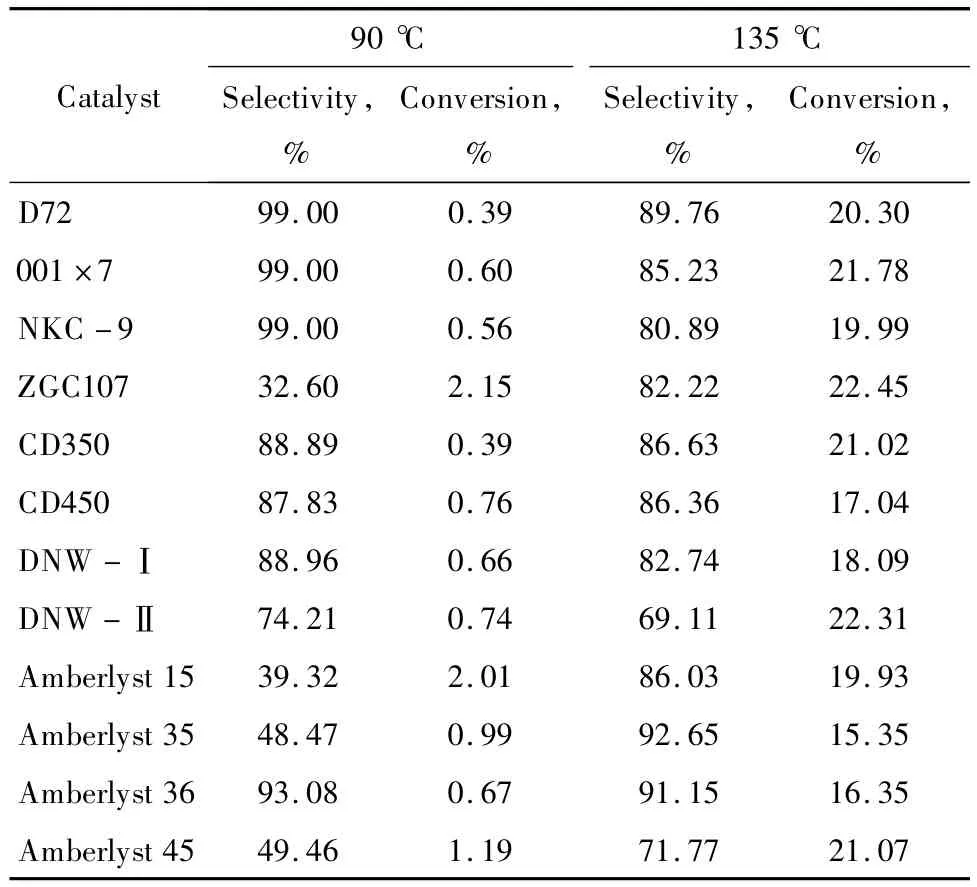
表2 不同树脂催化剂的水合反应催化活性Table 2 Catalytic activities of the resin catalysts in the hydration of cyclopentene to cyclopentanol
在筛选用于该反应的树脂催化剂时,不仅要考虑催化剂的活性,还必须考虑树脂本身的特性,尤其是反应温度的限制。结合表1可知,D72,001×7,NKC -9,ZGC107,CD350,CD450,Ameberlyst 15等树脂催化剂的最高使用反应温度都低于135℃,均不宜长期在135℃或更高的反应温度下进行催化反应。考虑到工业可行性,重点考察了稳定性好且机械强度强的耐高温树脂催化剂DNW-Ⅰ,DNW-Ⅱ,Amberlyst 35,Amberlyst 36,Amberlyst 45 的催化活性。虽然Ameberlyst 15催化剂的最高使用温度为120℃,但为考察Ameberlyst系列产品的性能,也对Ameberlyst 15催化剂的性能进行了考察。
2.2 耐高温树脂在不同温度下的催化活性
树脂催化剂的活性由树脂的交换容量和孔结构等因素决定,而这些因素与温度有关,因此温度是影响树脂催化剂稳定性和催化活性的重要因素。为进一步筛选催化剂,考察了DNW-I,DNW-Ⅱ,Amberlyst 15,Amberlyst 35,Amberlyst 36,Amberlyst 45这6种耐高温树脂催化剂分别在90,120,135,150,160℃下的催化活性,得到了这6种树脂催化剂在最佳温度下的催化活性,实验结果见表3。由表3可见,以Amberlyst 45树脂和DNW-Ⅱ树脂为催化剂时,环戊醇的选择性均低于90%,主要是由于这两种催化剂的孔径和交换容量较小,影响了环戊烯、环戊醇及苯酚的传质扩散,使三者滞留在树脂内部,发生醚化、烷基化等副反应,致使环戊醇的选择性较低,所以不适合用作该反应的催化剂。
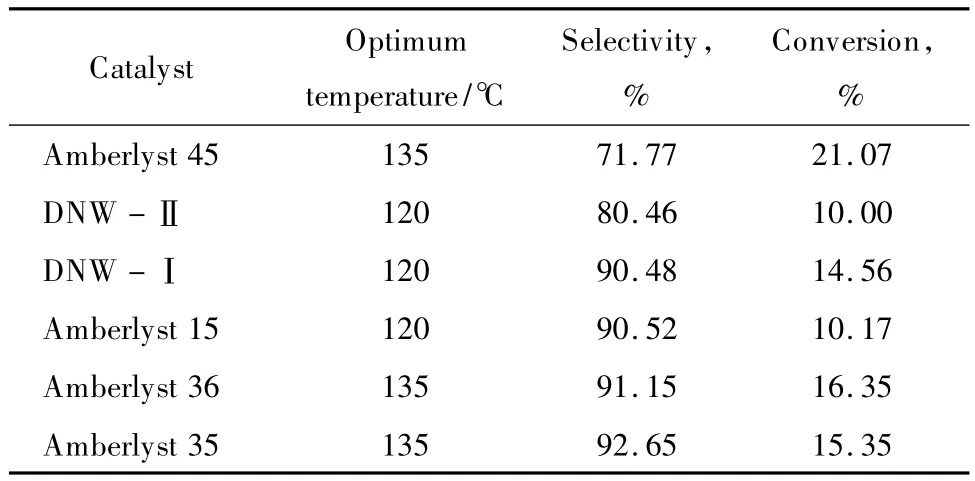
表3 不同耐高温树脂催化剂在最佳温度下的催化活性Table 3 Catalytic activities of the different resin catalysts under optimum temperature
DNW - Ⅰ,Amberlyst 15,Amberlyst 35,Amberlyst 36催化剂得到的环戊醇选择性都在90%以上,但DNW-Ⅰ树脂的孔径和比表面积较小,环戊烯向催化剂内部的扩散速率较慢,与环戊烯接触的活性点较少,催化效率较低。综合考虑环戊醇选择性、环戊烯转化率及催化剂的稳定性可知,以Amberlyst 36或Amberlyst 35为催化剂较适宜,其中Amberlyst 36具有更大的交换容量,树脂表面的磺酸基浓度更大,有利于提高反应速率,所以优选Amberlyst 36作为该水合反应的催化剂。此时,环戊烯转化率为16.35%,环戊醇选择性为91.15%。
2.3 苯酚体系下的副反应
在2.2节筛选催化剂的过程中,以苯酚为溶剂,此时反应体系存在大量副反应,导致环戊醇的选择性较低,为此对反应体系中的主要成分进行了GCMS分析,分析结果见表4。由表4可见,反应产物中除生成目的产物环戊醇外,还存在苯酚的烷基化副产物(一烷基化产物和二烷基化产物)和醚化副产物(苯酚环戊醚和二环戊醚),表明该水合反应的主要副反应为醚化反应和烷基化反应。而产生烷基化副反应的主要原因在于以苯酚为溶剂,因此苯酚不适合作为该水合反应的溶剂,有必要对溶剂种类进行深入研究。

?
2.4 溶剂种类对水合反应的影响
环戊烯水合反应是液-液-固三相反应,传质是影响反应的关键因素。研究发现,在不加溶剂时,不论何种催化剂,环戊烯转化率和环戊醇收率均较低,因此加入溶剂是必要的。参考文献[15]的研究结果,在研究初期向反应体系中加入苯酚溶剂,它增加了环戊烯与水分子之间的互溶性,使催化剂表面形成的水分子液膜变薄,降低了环戊烯向催化剂的扩散阻力,提高了反应速率。但以苯酚为溶剂存在如下缺点:(1)苯酚不稳定,易发生烷基化、醚化、氧化等副反应,且烷基化、醚化反应的产物均为高沸点化合物,黏度大,后处理困难;(2)副产物若不经处理而随苯酚循环使用,则在反应体系中累积,增大了体系黏度,使搅拌困难;(3)苯酚沸点高,与环戊醇分离需采用精馏方式,能耗大;(4)苯酚毒性大,易带来环境污染问题。
针对以上缺点,选取一些同时具有亲水官能团和亲油官能团的溶剂,这些溶剂能增加环戊烯与水分子之间的互溶性,且都是工业上常用的溶剂。考察了溶剂种类对水合反应的影响,实验结果见表5。由表5可见,以甲醇、乙二醇甲醚、乙醇为溶剂时,环戊醇选择性均低于20%,主要是因为甲醇、乙醇在较高温度下都能与环戊烯、产物环戊醇发生醚化反应,降低环戊醇的选择性,而乙二醇甲醚的羟基也可与环戊醇发生醚化反应,所以这些物质不适合作为该水合反应的溶剂。
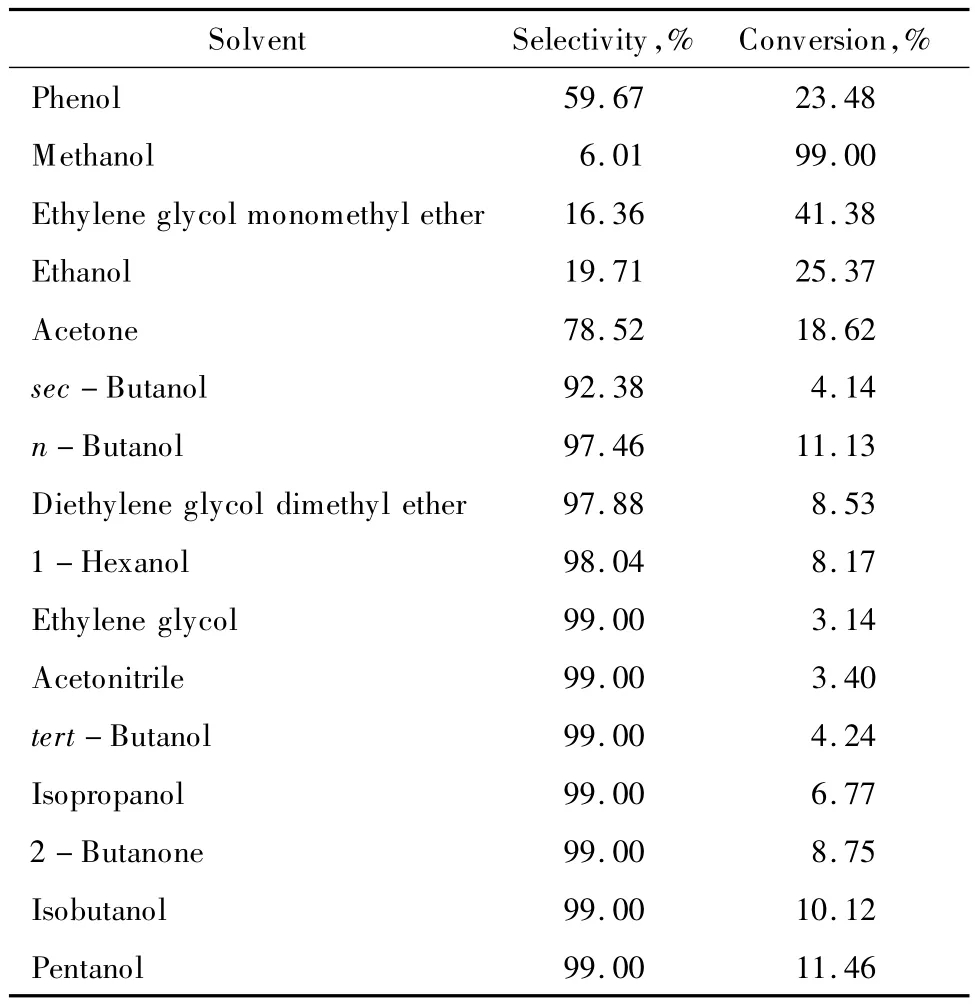
表5 溶剂种类对水合反应的影响Table 5 The effect of solvent type on the hydration of cyclopentene
以丙酮为溶剂时,环戊醇选择性低于80%,丙酮在反应条件下易发生自身缩合反应,使得环戊醇选择性降低,也不适合作为该反应的溶剂。
以异丙醇、仲丁醇、叔丁醇、乙二醇、乙腈为溶剂时,虽然环戊醇的选择性较高,但环戊烯的转化率太低,均低于8%,且以异丁醇、仲丁醇、叔丁醇为溶剂时,这些溶剂可在磺酸基催化下脱水生成相应的烯烃,使体系压力升高,带来安全问题;乙二醇溶解环戊烯的性能较差,不能增加环戊烯和水的互溶性,导致环戊烯的转化率较低;乙腈则易发生水解反应生成乙酸等副产物,增加了后处理工序,所以这些物质也都不适合作为该反应的溶剂。
以丁醇、丁酮、己醇、戊醇、乙二醇二甲醚为溶剂时,环戊醇选择性均在97%以上,环戊烯转化率在8%以上,在环戊醇选择性相差不大的情况下,优选环戊烯转化率较高的丁醇、戊醇为溶剂。但戊醇的沸点(138.0℃)与环戊醇的沸点(140.8℃)接近,使产物分离困难。而丁醇则具有随温度的升高能与强极性的水和非极性的烃类互溶、常温时又能从水中析出的特点,反应结束后,可作为萃取剂,有效地将环戊醇萃取到有机相,不仅提高了环戊醇的收率,而且水相又可循环使用,整个工艺几乎不排放废弃物。所以,选用丁醇为溶剂较适宜。此时,环戊烯转化率为11.13%,环戊醇选择性为97.46%。
3 结论
(1)在苯酚体系中,对环戊烯直接水合法合成环戊醇的催化剂进行筛选,以Amberlyst 36耐高温强酸性阳离子交换树脂为该反应的催化剂较适宜。
(2)针对以苯酚为溶剂易发生醚化和烷基化等副反应的问题,考察了溶剂对该水合反应的影响,优选稳定性更好的丁醇为溶剂。在以Amberlyst 36为催化剂、丁醇为溶剂、水与环戊烯摩尔比为6∶1、环戊烯与丁醇质量比为1∶1、反应温度 160℃、反应压力1.20 MPa、反应时间4 h、搅拌转速600 r/min的优化条件下,环戊醇选择性为97.46%,环戊烯转化率为11.13%。
(3)环戊烯直接水合法制备环戊醇,虽然环戊烯的转化率较低,但由于环戊烯沸点较低可回收循环使用,所产生的污染物较少,属于环境友好工艺。
[1]徐克勋.精细有机化工原料及中间体手册[M].北京:化学工业出版社,1998:2215.
[2]徐泽辉,顾超然,郭世卓.环戊烯合成环戊醇的研究[J].化学世界,2002,(4):200 -202.
[3]上海石化公司化研所开发环戊烯合成环戊醇新工艺.石油化工,2002,31(8):685.
[4]Nippon Zeon Co,Ltd.Method for Producing Cyclopentanol by Using Solid Acid Comparing Zirconium Compound as Catalyst:JP,2002326968[P].2002-11-25.
[5]Nippon Zeon Co,Ltd.Method for Producing Cyclopentanol:JP,2002326967[P].2002 -11 -25.
[6]Nippon Zeon Co,Ltd.Method for Producing for Cyclopentanol:JP,2002154997[P].2002 -05 -28.
[7]Nippon Zeon Co,Ltd.High- Purity Cyclopentene and Method for Producing Cyclopentanol Using the Same:JP,2001270842[P].2001-10-02.
[8]Nippon Zeon Co,Ltd.High Purity Cyclopentene,Method for Producing the Compound and Method for Producing Cyclopentanol by Using the Compound:JP,2001261592[P].2001-09-26.
[9]Nippon Zeon Co,Ltd.Method for Producing Cyclopentanol:JP,2001181222[P].2001-07-03.
[10]Nuntasri D,Wu Peng,Tatsumi Takashi.Highly Selective Formation of Cyclopentanol Through Liquid-Phase Cyclopentene Hydration over MCM - 22 Catalysts[J].Chem Lett,2002,31(2):224-225.
[11]Nuntasri D,Wu Peng,Tatsumi Takashi.Highly Selectivity of MCM-22 for Cyclopentanol Formation in Liquid-Phase Cyclopentene Hydration[J].J Catal,2003,213(2):272 -280.
[12]Nippon Zeon Co,Ltd.Preparation of Cyclopentyl Alcohol:JP,2003171322A[P].2003-06-20.
[13]Nippon Zeon Co,Ltd.Preparation of Cyclopentanol from Cyclopentene:JP,2003212803[P].2003 -07 -30.
[14]Wulff G,Dhal P K.Syntheses and Seperation Using Functional Polymers[M].New York:Chichester,1988:149.
[15]中国石化上海石油化工有限公司.环戊醇制备及精制的方法:中国,1676507A[P].2005-10-05.
Preparation of Cyclopentanol by Direct Hydration of CyclopenteneⅠ.Effects of Catalysts and Solvents on the Hydration
Yang Xiaohui,Song Jian,Wu Jie,Sun Shujuan,Feng Rongxiu
(College of Chemical Engineering ,Tianjin University,Tianjin 300072,China)
The preparation of cyclopentanol by direct hydration of cyclopentene was studied with strong acidic cation exchange resins as catalysts and phenol as solvent.The catalytic activities of 12 strong acidic cation exchange resins were investigated at 90℃ and 135℃ separately,among which the relationships of the catalytic activities of six heat-resistant cation exchange resins with temperature were researched. The influence of solvent type on the hydration reaction was studied also.Experimental results showed that catalytic activity of Amberlyst 36 was the highest andn-butanol was the best solvent.Under the reaction conditions of Amberlyst 36 as catalyst,n- butanol as solvent,mole ratio of H2O to cyclopentene 6 ∶1,mass ratio of cyclopentene ton-butanol 1 ∶1,reaction temperature 160 ℃,pressure 1.20 MPa,reaction time 4 h and stir speed 600 r/min,the conversion of cyclopentanol was 11.13%and the selectivity to cyclopentanol was 97.46%.
strong acidic cation exchange resin catalyst;cyclopentene;cyclopentanol;phenol;n-butanol;hydration
1000-8144(2011)04-0414-05
TQ 223
A
2010-10-17;[修改稿日期]2010-12-28。
杨晓辉(1984—),男,山东省烟台市人,硕士生,电话13920861372,电邮 yangxhfacai@126.com。联系人:冯荣秀,电话15602155062,电邮 rxfeng7091@tju.edu.cn。
(编辑 李明辉)

