消旋氧氟沙星抗体制备及其手性识别特性研究
王伟华,雷红涛,孙远明,王利英,王保玲
(华南农业大学食品学院/广东省食品质量安全重点实验室,广东广州510642)
消旋氧氟沙星抗体制备及其手性识别特性研究
王伟华,雷红涛*,孙远明*,王利英,王保玲
(华南农业大学食品学院/广东省食品质量安全重点实验室,广东广州510642)
采用活泼酯法(A)和直接EDC(1-乙基-3-(3-二甲氨丙基)碳二亚胺盐酸盐)法(D),合成两种包被抗原(OFL-A-OVA和OFL-D-OVA)和两种免疫抗原(OFL-A-BSA和OFL-D-BSA),然后分别用两种免疫抗原免疫小鼠获得与其对应的多克隆抗体,建立消旋氧氟沙星残留免疫检测方法。研究结果表明:紫外扫描图谱证明四种抗原均合成成功,OFL-A-BSA、OFL-D-BSA、OFL-A-OVA 和 OFL-D-OVA 的偶联比分别为19.67、3.03、1.93 和 0.99。消旋氧氟沙星的间接竞争ELISA法的线性检测范围为16.35~444.10ng/mL,IC50为5.42ng/mL,最低检测限为6.23ng/mL。消旋氧氟沙星抗体与恩诺沙星、环丙沙星、加替沙星等其他同类药物的交叉反应率较低,表明消旋氧氟沙星抗体具有较高的特异性,且消旋氧氟沙星抗体对左旋氧氟沙星和右旋氧氟沙星的识别并非对等,对左旋的识别能力较大,左旋氧氟沙星对抗体的产生起主要作用。
氧氟沙星,人工抗原,多克隆抗体,交叉反应率,手性识别
食品安全问题已成为全世界关注和担忧的焦点,关系到广大消费者的身体健康与生命安全,关系到社会稳定与经济发展。我国的食品安全并不容乐观,每年因农药、渔药、兽药和其他污染物残留而造成的农产品、水产品及加工食品的经济损失巨大。氧氟沙星是一种在畜禽、水产养殖等农业领域中应用较广的喹诺酮类抗菌药物,主要作用于细菌体内DNA促旋酶,抑制该酶的活性,干扰DNA合成,从而起到抗菌作用,氧氟沙星的药理研究表明,S型异构体的抗菌活性比R型高2个数量级,是外消旋体的2倍,不良反应比外消旋体低。Morrissey等发现氧氟沙星两个手性异构体对DNA促旋酶的亲和力大小基本相似,但二者与酶的摩尔结合比差异很大,S型与酶结合时有4个单体装配在结合口袋,而R型却只有2个;结合口袋内结合的多个S型单体优化了药物和酶的作用,通过计算机分子模拟发现,DNA促旋酶将DNA双链变性形成口袋后,S-氧氟沙星的喹诺酮母环与该口袋结合,同时喹诺酮C-7取代基又与DNA促旋酶的b亚基相互作用,从而进一步增强了S型对映体的结合力[1]。该药物长期使用,会在动物体内大量积聚,从而危害人类健康。氧氟沙星是已上市的13个喹诺酮类抗菌药中最为优秀的、可再开发的新品种之一,也是迄今国际上临床使用的480余种含手性因素的药物之一。手性对映体的性质在各向同性的环境中完全一样,而在各向异性的环境中则往往不同,具有生理活性的一些对映体,往往一种活性很高,另一种活性很小或者没有活性,这种现象在农药[2]、治疗药物[3]中很常见。本文以氧氟沙星为对象,制备消旋氧氟沙星的多克隆抗体,对该抗体的交叉反应和手性识别特性进行评价,探索消旋氧氟沙星抗体的识别特性,为阐述半抗原类物质的手性识别机制提供参考。
1 材料与方法
1.1 材料与仪器
动物材料 Balb/c纯种雌性小鼠,7~8周龄,体重20~22g,中山医科大学实验动物中心;牛血清白蛋白(BSA)、卵清蛋白(OVA)、Freund氏完全和不完全佐剂 Sigma公司;HRP标记的羊抗小鼠IgG抗体武汉博士德生物工程有限公司;脱脂奶粉 内蒙古伊利实业集团股份有限公司;消旋氧氟沙星、左旋氧氟沙星、恩诺沙星、环丙沙星、加替沙星、1-乙基-3-(3-二甲氨丙基)碳二亚胺盐酸盐(EDC)、二环己基碳二亚胺(DCC)、N-羟基琥珀酰亚胺(NHS)、N,N-二甲基甲酰胺(DMF)、四甲基联苯胺(TMB)、柠檬酸、吐温-20 北京鼎国生物技术有限责任公司;其他化学试剂 均为国产分析纯。
透析袋、低温高速离心机 Sigma公司;BP61S型电子天平 德国Sartorius公司;Ultraspec4000型紫外/可见分光光度仪 Pharmacia Biotech公司;Multiskan MK3酶标仪、Wellwash MK2洗板机 美国Thermo labsystems公司;BP61S电子天平 瑞士Sartorius公司;微量可调移液器 法国Gelson公司;82-5控温磁力搅拌器 金坛市恒丰仪器厂;94-2磁力搅拌器 国华电器有限公司;TGL-16高速台式离心机 上海医用分析仪器厂。
1.2 实验方法
1.2.1 人工抗原制备
1.2.1.1 活泼酯法合成人工免疫原(OFL-A-BSA)和人工包被原(OFL-A-OVA) 称取39.4mg(0.1mmol)OFL放入小烧杯,加入6mL的DMF,再分别加入 122.0mg(0.6mmol)的 EDC、46.4mg的 NHS(0.4mmol)、6mL双蒸水,用保鲜纸封口,磁力搅拌下室温反应24h制成 A液。将158.4mg(0.02mmol)BSA溶于20mL 0.1mol/L、pH9.6的碳酸盐缓冲液中,得B液。将A液逐滴加入B液中,磁力搅拌器搅拌下室温反应6h。用生理盐水在4℃下透析3d,透析完全后,测定人工抗原浓度,分装,-20℃冻存,即得人工免疫原OFL-A-BSA。
人工包被原OFL-A-OVA的制备基本同免疫原OFL-A-BSA,仅将 BSA 换成105.6mg(0.0024mmol)OVA。
1.2.1.2 直接 EDC法合成人工免疫原(OFL-DBSA)和人工包被原(OFL-D-OVA) 将 3.9mg(0.01mmol)OFL溶于 3mL蒸馏水,加入 10.2mg(0.05mmol)EDC、10mg(0.001mmol)BSA,室温搅拌反应3h,用生理盐水在4℃下透析3d。透析完全后,测定人工抗原浓度,分装,-20℃冻存,即得人工免疫原OFL-D-BSA。
人工包被原OFL-D-OVA的制备基本同免疫原OFL-D-BSA,仅将 BSA 换成3.3mg(0.000075mmol)OVA。
1.2.2 人工抗原的鉴定方法
1.2.2.1 人工免疫原和包被原浓度的测定 采用Braford 法[4]。
1.2.2.2 紫外光谱鉴定[5]将合成的OFL-A-BSA、OFL-D-BSA、OFL-A-OVA、OFL-D-OVA、BSA、OVA分别用生理盐水配制成适当浓度的溶液,用生理盐水作对照在200~400nm波长下扫描。参照陈新建等[6]的计算方法,计算分子结合比。
1.2.3 OFL多克隆抗体的制备 将OFL-A-BSA和OFL-D-BSA分别与等量的弗氏佐剂混合,充分乳化后皮下多点注射免疫小鼠,每只100μg免疫原;第二次以后用弗氏不完全佐剂,免疫间隔为3周,第3次免疫后7d尾部取血,4℃冰箱放置过夜,3000r/min离心10min,取上清,-20℃冰箱内保存。用 OFL-ABSA免疫的小鼠编号分别为 A1、A2,用OFL-D-BSA免疫的小鼠编号分别为D1、D2。
1.2.4 免疫抗血清效价的测定 采用间接ELISA方法。
1.2.5 抗体的识别特性鉴定
1.2.5.1 数据处理和曲线拟合 用PBST分别溶解左旋氧氟沙星、恩诺沙星、环丙沙星、加替沙星作为竞争抗原,采用间接竞争ELISA法作检测曲线,采用Origin7.5软件的四参数对数函数式(1)对ciELISA数据进行处理和曲线拟合[7-8]。

式中,A为曲线渐进线最大值,等于0浓度时的吸光度值,即Amax;B为曲线回折点处的斜率,即50%的Amax在曲线上对应点的斜率;C为曲线回折点对应的x值,等于50%的Amax所对应的药物浓度,即IC50;D为曲线渐进线最小值,等于背景值,即Amin。
1.2.5.2 识别特性评价 根据下式计算交叉反应率[9-10],以交叉反应率评价识别特性。

2 结果与分析
2.1 人工抗原的紫外光谱法鉴定
将各溶液进行适当的稀释(偶联产物按蛋白计),经紫外扫描得各溶液的紫外吸收光谱图(图1、图2)。OFL分子结构中至少有3个基团可作为偶联的部位,即哌嗪环上的亚氨基、3-位碳原子的羧基和4-位碳原子上的羰基。本实验选择OFL分子结构中3位碳原子上的羧基作为偶联反应所需的基团。BSA与OVA是两种常用的载体[11],它们分别有60和20个游离的氨基,这些氨基可以和OFL分子结构中3位碳原子上的羧基发生偶联反应,形成肽键,从而形成稳定的合成产物。由图1、图2可以看出,BSA、OFL、OFL-A-BSA三者的紫外吸收光谱均有显著的差异,合成的抗原的最大特征吸收峰与OFL和BSA均不同,人工抗原在340nm左右明显呈现出OFL 的特征,说明 OFL 偶联成功[6]。同理,OFL-DBSA、OFL-A-OVA及 OFL-D-OVA 三者的紫外光谱图也证明抗原偶联是成功的。
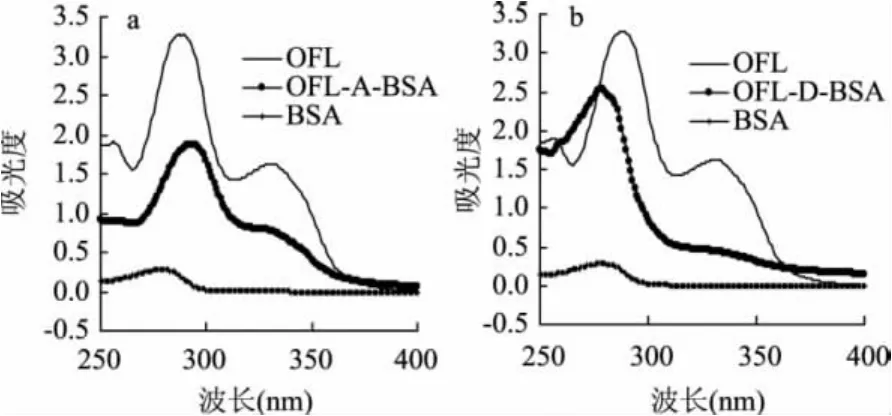
图1 免疫原的紫外吸收光谱
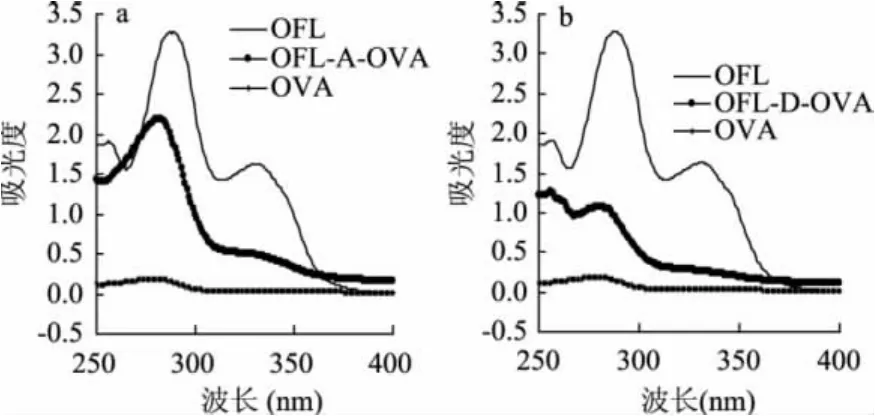
图2 包被原的紫外吸收光谱
根据文献方法[6]计算可知,OFL-A-BSA、OFLD-BSA、OFL-A-OVA 和 OFL-D-OVA 的偶联的结合比分别为19.67、3.03、1.93 和0.99。
2.2 免疫血清的效价和抑制的测定
OFL-A-BSA免疫所得抗血清用 OFL-A-OVA包被的酶标板检测后,发现效价曲线与抑制曲线有明显差别,且阴性对照数值都比较低(图 3-a、图3-b),说明OFL-A-BSA抗血清产生了消旋氧氟沙星的抗体。但是OFL-D-BSA免疫所得抗血清用OFL-D-OVA包被的酶标板检测后,效价曲线与抑制曲线却没有明显差别,说明OFL-D-BSA抗血清特异性较差。

图3 免疫抗血清A1和A2的效价和抑制
2.3 多克隆抗体的交叉反应性的测定
OFL-A-BSA抗血清的交叉反应条件如下:取A1小鼠血清以1∶16000稀释。其中消旋氧氟沙星的药物浓度从10000ng/mL开始,按10倍稀释梯度稀释;左旋氧氟沙星、环丙沙星、恩诺沙星和加替沙星的药物浓度都从10000ng/mL开始,15倍稀释梯度稀释。由表1可以看出,用间接竞争ELISA法检测消旋氧氟沙星,线性检测范围为 16.35~444.10ng/mL,IC50为5.42ng/mL,最低检测限为6.23ng/mL。
消旋氧氟沙星抗体与左旋氧氟沙星的交叉反应率为120.08%,与右旋氧氟沙星的交叉反应率为101.30%,说明消旋氧氟沙星抗体对左旋氧氟沙星和右旋氧氟沙星的识别并非对等,对左旋的识别能力大于对右旋的识别力,左旋氧氟沙星对抗体的产生起主要作用。消旋氧氟沙星抗体与恩诺沙星的交叉反应率为2.88%,从结构上看(表1),恩诺沙星由环丙烷替代了消旋氧氟沙星上3环的结构,4环结构中增加1个CH3基团,侧链结构发生较大变化,其性质随之变化,恩诺沙星交叉反应率低,说明侧链的结构对交叉反应有较大影响。环丙沙星与消旋氧氟沙星的结构相比,环丙烷替代了消旋氧氟沙星上3环的结构,结构差异较大,导致半数抑制浓度IC50值增加,交叉反应率降低。加替沙星的结构与环丙沙星相比,4环上多一个CH3基团,2环上多一个CH2O基团,这两个基团同时存在,使加替沙星与环丙沙星在结构上消除了空间位阻效应,因此,消旋氧氟沙星对加替沙星和环丙沙星的交叉反应率几乎相等,但加替沙星和环丙沙星都与消旋氧氟沙星在侧链结构上有很大的差异,所以对这两者的交叉反应率都很低。综上所述,消旋氧氟沙星抗体与恩诺沙星、环丙沙星、加替沙星等同类其他药物的交叉反应率很低,说明该抗体具有很好的特异性。
3 讨论
建立灵敏特异的氧氟沙星的ELISA方法需要灵敏特异的抗氧氟沙星抗体。氧氟沙星是小分子物质,属半抗原,只具有反应原性而没有免疫原性,不能直接刺激动物机体产生抗体,必须与大分子载体蛋白进行偶联才能作为免疫原。氧氟沙星分子结构中含有羧基,因此可通过中间物NHS在EDC等有机溶剂的作用下与蛋白质的氨基结合形成蛋白质与小分子的偶联物。本实验采用直接EDC法和活泼酯法两种方法进行偶联,用直接EDC法合成的免疫原免疫小鼠没有产生针对消旋氧氟沙星的抗体,其原因是由于直接EDC法易形成蛋白质间的聚合物,而不是均一产物,也可能是偶联比较低所致;而活泼酯法,在直接EDC法的基础上,使用NHS,避免了载体间的偶联,产物比较单一。
消旋氧氟沙星抗体的特异性可以通过与各种喹诺酮类化合物的交叉反应来评价。理论上,抗原同抗体结合时,距离同半抗原与载体蛋白结合点最远的分子部分优先被抗体识别。喹诺酮类药物在结构上相近,有共同特征,因此喹诺酮类药物抗体往往会与同类药物产生交叉反应。在本实验中,免疫原是通过消旋氧氟沙星上的羧基与载体蛋白上的氨基连接合成的,在这个连接中,氧氟沙星上离连接点最远的基团是哌嗪基部分。左旋氧氟沙星的哌嗪基通过一个氮原子与甲基相连,因此与消旋氧氟沙星抗体表现出较高的交叉反应。
长期以来,人们一直把对映体当作同一种物质来看待。事实上,对映体的性质在各向同性的环境中完全一样,而在各向异性的环境中则往往不同。研究表明,不同的对映体在人体内的药理、代谢过程、毒性和疗效存在着显著差异,大致有以下6个类别:两种对映体的药理活性可相互协同,具有互补作用[12];对映体活性不同,可开发成 2 个药物[13];两种对映体一种有治疗药理活性,另一种产生毒副作用[14];对映体具有相反的活性[15];一个对映体具有显著的活性但其对映体活性很低或无活性[16];两种对映体有等同或相类似的药理活性,但作用强度有差异[17]。在自然状态下,手性药物的多种构型虽然化学组成一样,但它们各自的毒性、生理活性和药理作用往往存在着差别,产生这种差别的主要原因是:生命机体本身是由具有高度不对称性的生物大分子组成,这种不对称性赋予生物大分子通过一定的信息去识别不同的对映性的能力,使得与之契合者才能发生相互作用,从而产生生理活性。

表1 不同种药物的抑制中浓度和交叉反应
1894年,Fisher报道了一种底物的结构对酶活性的影响,1904年,激素受体的立体选择性(手性)被报道。从那以后,有许多关于蛋白质立体选择和对应选择的事例被发现。许多科学家认为,手性是蛋白质内在的性质,在某种程度上,抗体对研究蛋白质的立体选择性来说是一个非常好的模型系统[18]。Landsteiner的经典抗体理论表明,如果一个蛋白质能跟连在手性中心上的配位体中的原子相互作用,那么它就可能具有立体选择性。氧氟沙星是喹诺酮抗生素中的一员,它能抑制II型异构酶的活性,II型异构酶能使松弛的DNA超螺旋结构转变为负的超螺旋形式。在对这些药物抑制机制及DNA异构酶相互作用的一系列研究中,发现左旋氧氟沙星比右旋氧氟沙星对双股小牛胸腺DNA的连接更加有效。这两个异构体在亲和吸附性上的区别大概相差五倍,这比其他已知的异构体的差异要大[19]。右旋氧氟沙星在存在和缺乏DNA情况下的圆二色谱与左旋氧氟沙星的最大不同在于对应异构体的亲和吸附性上。LDr的结果表明,氧氟沙星的两个对应异构体在分子平面和DNA螺旋轴之间的角度及约束几何参数是相似的,在亲和吸附性上的区别可能不是由氧氟沙星在它的束缚位点上的几何排列的原因造成的[20]。因此,亲和吸附性上的区别不能直接体现它们在抗药性上的区别[21],只有在对映体形态水平上研究手性污染物的分离、分析、环境变化等问题,才能阐明其在环境中的行为和效应,准确评价其对人类健康和生态系统的风险性。在手性水平上研究食品污染物问题,已经逐渐成为国际前沿领域[22-23]。
4 结论
4.1 紫外扫描图谱证明四种抗原均合成成功,OFLA-BSA、OFL-D-BSA、OFL-A-OVA 和 OFL-D-OVA的偶联比分别为19.67、3.03、1.93和0.99。
4.2 消旋氧氟沙星的间接竞争ELISA法的线性检测范围为 16.35~444.10ng/mL,IC50为 5.42ng/mL,最低检测限为6.23ng/mL。
4.3 消旋氧氟沙星抗体具有较高的特异性,对左旋氧氟沙星和右旋氧氟沙星的识别并非对等,对左旋的识别能力大于右旋,左旋氧氟沙星对抗体的产生起主要作用。
[1]张智超,李朝阳,张玲,等.环境样品中手性农药对映体浓度测定方法研究进展[J].农药科学与管理,2004,2(2):4-7.
[2]Franco EJ,Hofstetter H,Hofstetter O,et al.A comparative evaluation of random and site-specific immobilization techniques for the preparation of antibody-based chiral stationary phases[J].Journal of Separation Science,2006,29(10):1458-1469.
[3]Morrissey I,Hoshino K,Sato K,et al.Mechanism of differential activities of ofloxacin enantiomers[J].Antimicrobial Agents and Chemotherapy,1996,40(8):1775-1784.
[4]沈关心,周汝麟.现代免疫学实验技术[M].武汉:湖北科学技术出版社,1998:16-26.
[5]朱国念,杨挺,吴银良.抗克百威多克隆抗体的研制[J].中国农业科学,2002,35(8):1025-1029.
[6]陈新建,陈梅英,赵会杰.免疫学技术在植物科学中的应用[M].北京:中国农业大学出版社,1998:45.
[7]李俊锁,邱月明,王超.兽药残留分析[M].上海:上海科学技术出版社,2002.
[8]李俊锁,钱传范.兽药残留免疫分析及其进展[J].中国兽医学报,1998,18(4):411-415.
[9]Duan J,Yuan Z.Development of an indirect competitive ELISA for ciprofloxacin residues in food animal edible tissues[J].Journal of Agricultural Food Chemistry,2001,49(3):1087-1089.
[10]Holtzapple CK,Buckley SA,Stanker LH.Developmant of antibodies against the fluoroquionolone sarafloxacin and molecular modeling studies of cross- reactive compounds[J].Food and Agricultural Immunology,1997,9(1):13-26.
[11]谢忠良,李文,何计国.氯羟吡啶人工抗原合成和鉴定[J].食品科学,2009,30(1):229-231.
[12]Blaine EH,Fanelli GM,Irvin JD,et al.Enantiomers of indacrinone:a new approach to producing an isouricemic diuretic[J].Clinical and Experimental Hypertension,1982,4(1-2):161-176.
[13]Kamiya Y,Andoh T,Furuya R,et al.Comparison of the effects of convulsant and depressant barbiturate stereoisomers on AMPA- type glutamate receptors[J].Anesthesiology,1999,90(6):1704-1713.
[14]Ekatodramis G,Borgeat A.The enantiomers:revolution or evolution[J].Current Topic in Medicinal Chemistry,2001,1(3):205-206.
[15]Higaki K,Nakano M.Stereoselective disposition of S-8666,a novel uricosuric antihypertensive diuretic,and its N -monodemethylated metabolite in a perfused rat liver preparation.Effect of protein binding on the kinetics of S-8666[J].Drug Metabolism Disposition,1992,20(3):350-355.
[16]Eichelbaum M.Enantiomers:implications and complications in developmental pharmacology[J].Developmental Pharmacology and Therapeutics,1992,18(3-4):131-134.
[17]Szabelski P,Warzocha TP,Pańczyk T.Thermal desorption of chiral molecules from a nanostructured chiral surface:Insights from computer simulations[J].Thermochimica Acta,2010,497(1-2):77-84.
[18]Hwangbo HJ,Yun BH,Cha JS,et al.Enantioselective binding of S-and R-ofloxacin to various synthetic polynucleotides[J].European JournalofPharmaceuticalSciences,2003(18):197-203.
[19]Ranieri DI,Hofstetter H,Hofstetter O.Computational structural analysis of an anti-L-amino acid antibody and inversion of its stereoselectivity[J].Journal of Separation Science,2009,32(10):1686-1695.
[20]Lee EJ,Yeo JA,Jung K,et al.Enantioselective binding of ofloxacin to B form DNA[J].Archives of Biochemistry and Biophysics,2001,395(1):21-24.
[21]Anklam E,Gadani F,Heinze P,et al.Analytical methods for detection and determination of genetically modified organisms in agricultural crops and plant- derived food products[J].European Food Research and Technology,2002,214(1):23-26.
[22]Hofstetter H,Hofstetter O.Antibodies as tailor-made chiral selectors:an interdisciplinary approach to enantiomer separation and detection[J].Chinese Journal of Chromatography,2005,23(5):508-519.
Study on monoclonal antibodies preparation and
chiral recognition characteristics against racemic ofloxacin
WANG Wei-hua,LEI Hong-tao*,SUN Yuan-ming*,WANG Li-ying,WANG Bao-ling
(College of Food Science,South China Agricultural University/Key Laboratory of Food Quality and Safety of Guangdong Province,Guangzhou 510642,China)
Active ester method and direct EDC method were used to synthesize two kinds of coating antigens(OFL-A-OVA and OFL-D-OVA)and two kinds of immunity antigens(OFL-A-BSA and OFL-D-BSA).The objective of experiment was to product artificial antigen and polyclonal antibodies against racemic ofloxacin(OFL),then by which balb/c mice were immunized and acquired polyclonal antibodies.Meanwhile,racemic ofloxacin residual immunity examination method was established.The results indicated that four artificial antigens synthesized successfully proved by ultraviolet scanning.Happen to carrier protein ratios of OFL-A-BSA,OFL-D-BSA,OFL-A-OVA and OFL-D-OVA were 19.67,3.03,1.93 and 0.99,respectively.Detection scope of racemic ofloxacin with indirect competitive ELISA was 16.35~444.10ng/mL,and IC50value was 5.42ng/mL,and detection limit was 6.23ng/mL.The cross reaction rates between racemic ofloxacin antibody and enrofloxacin,ciprofloxacin,or gatifloxacin were low,which indicated racemic ofloxacin had high specificity.Meanwhile,the abilities were not on balance with greater recognition for L-ofloxacin than D-ofloxacin.L-Ofloxacin played a major role for production of antibody which had high affinity and specificity.
ofloxacin;artificial antigen;polyclonal antibodies;cross reaction rate;chiral recognition
Q939.91
A
1002-0306(2011)09-0198-05
2010-06-21 *通讯联系人
王伟华(1977-),女,博士研究生,讲师,研究方向:食品质量安全。
国家自然科学基金(20877029,30700663);广东省科技项目(cgzhzd0808,2009B040500002,2009A01010004)。

