硅胶固定的褐藻渣对重金属Cu2+吸附特征研究
杨沛珊, 于艳卿, 李超峰, 邹晓兰, 王新亭, 朱校斌
(1.中国科学院 海洋研究所, 山东 青岛266071; 2.中国科学院 研究生院, 北京 100049)
硅胶固定的褐藻渣对重金属Cu2+吸附特征研究
杨沛珊1,2, 于艳卿1,2, 李超峰1,2, 邹晓兰1,2, 王新亭1, 朱校斌1
(1.中国科学院 海洋研究所, 山东 青岛266071; 2.中国科学院 研究生院, 北京 100049)
褐藻渣是褐藻工业产生的固体废弃物, 直接排放到环境中容易破坏水体生态平衡。本研究用硅胶固定的褐藻渣吸附重金属Cu2+, 并对其吸附特征进行了检测。结果表明, 吸附pH、Cu2+初始浓度以及吸附时间对吸附过程均有很大的影响。该吸附材料对初始浓度在2.0 mmol/L以下的Cu2+溶液吸附率可达 85%, 25℃时最大吸附容量在 0.7~0.8 mmol/g之间; 其吸附等温线符合 Langmuir、Dubimim-Radushkevich方程, 基本符合Freundlich方程; 吸附动力学过程符合伪二级动力学模型, 说明吸附限速步骤是化学吸附过程; 实验结果表明硅胶固定的褐藻渣可以用于吸附 Cu2+, 其成本低廉, 选择性好。
生物吸附; 褐藻渣; 固定化; Cu2+
早在20世纪50年代, 纪明侯等[1-2]进行的一系列研究奠定了我国褐藻工业的基础。此后以海带为主要原料的褐藻工业蓬勃发展, 在沿海地区形成了生产褐藻胶、甘露醇、碘等产品的工业体系, 其主要产品褐藻酸钠的产量稳居世界第一。但在工业生产中, 按干物质计, 海带的利用率仅为 30%~50%左右,50%以上的海带成分作为固体废弃物——褐藻渣排入环境中[3]。这种废弃物如果投入海中, 会造成大片水域富营养化, 破坏水体生态平衡; 集中堆放则会形成藻渣滩或藻渣山, 既污染周围水体, 又占用土地资源。因而褐藻渣的资源化是控制以至消除污染,改善环境, 节约资源的根本途径, 已成为一个受关注的课题[3]。
国际上针对褐藻渣再利用的研究鲜见报道。但国内几名学者提出了值得借鉴的研究思路: 1.将褐藻渣添加入动物饲料或制成膳食纤维[4]。褐藻渣干物质中粗蛋白约占20%, 粗纤维约50%[5], 有可能成为食品原料或动物饲料成分; 2.海带渣糖化技术。冯大伟等[6]的研究表明, 海带渣总糖含量为52.6%, 可采取稀硫酸预处理后纤维素酶酶解产糖, 以作为能源生物利用; 3.利用褐藻渣处理工业废水中的重金属离子。邓莉萍[7]利用褐藻渣对水体中多种重金属离子进行生物吸附研究, 表明褐藻渣是一种高效、廉价的生物吸附材料, 可以用其对污水中的重金属离子进行吸附。
工业污水中的重金属离子有在生物体内富集的特性, 直接排放将严重威胁人类赖以生存的地表水和地下水安全。生物吸附对处理此类大体积、低浓度重金属废水具有明显优势[8]。褐藻渣的主要成分是纤维素和蛋白质, 表面所含官能团丰富, 用它作为生物吸附剂具有吸附量大, 选择性强, 效率高, 原材料成本低等优点。但直接将褐藻渣投入水体回收成本过高, 若不予回收藻渣会在水体中腐化, 造成二次污染。上述矛盾可通过将吸附材料固定化的方法解决。目前, 尚未见国内外有固定化褐藻渣的研究报道。本研究探索了使用硅胶固定化处理褐藻渣的方法, 成功制成均一的球状吸附材料。硅胶固定的褐藻渣吸附材料有以下优点: 1.小球状的吸附材料易于回收, 可作为填料装入柱、塔之中, 利于与生产实际衔接; 2.硅胶小球具有一定机械强度, 且内部结构多孔,比表面积大, 有利于金属离子与吸附剂充分接触;3.褐藻渣表面丰富的多聚复合体提供了大量可与金属离子结合的官能团; 4.原料成本低廉, 易于获得。因此这种以废治废的吸附方法在处理重金属污染方面有广阔的应用前景。本文探讨了硅胶固定的褐藻渣对重金属Cu2+的吸附特征, 从吸附影响因子、吸附热力学及吸附动力学方面进行分析。
1 材料与方法
1.1 褐藻渣的来源及预处理
实验所用的工业废弃物褐藻渣由胶南明月海藻有限公司提供, 经测定其含水率约为 85%, pH约为10。将褐藻渣用去离子水反复漂洗去盐, 压滤出的渣饼在 80℃下烘干至恒重, 粉碎机粉碎后过筛, 得到的藻渣粉末置于干燥器内备用。
1.2 褐藻渣-硅胶复合吸附材料的制备
1.2.1 反应机理
本实验采用自制硅胶小球固定褐藻渣, 即将褐藻渣粉末包埋在硅胶小球中。制备硅胶的反应方程式如下:
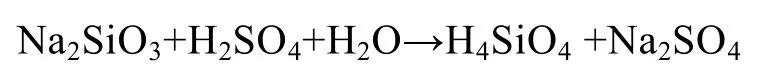
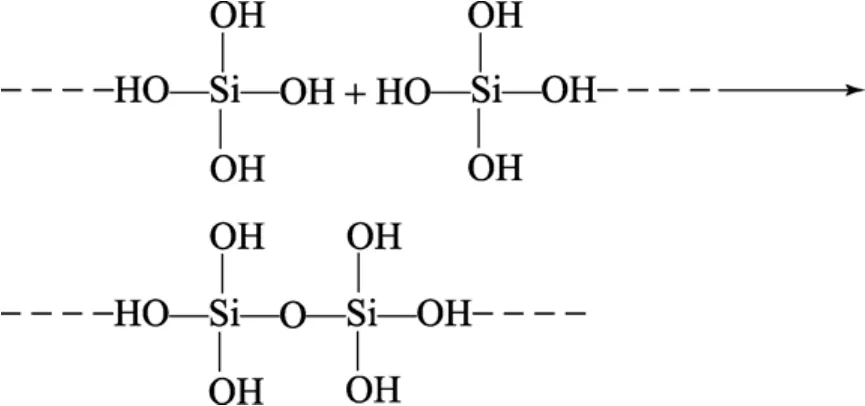
硫酸和水玻璃反应生成硅酸, 硅酸不稳定, 分子间通过缩合作用形成多聚硅酸, 以至硅溶胶。硅溶胶经胶凝成硅胶[9]。
1.2.2 制备方法
配制质量分数为 25%的 Na2SiO3溶液(可认为此溶液是模数为 1的水玻璃), 用碱式滴定管将Na2SiO3溶液滴入浓度为 30%的稀硫酸中, 充分搅拌并使用电极监测pH, 待溶液pH达到7.0时, 结束滴定。按1 : 10的质量比将褐藻渣与Na2SiO3溶液均匀混合, 50℃水浴内恒温老化24 h, 得到混有褐藻渣的硅胶块。将硅胶塑成均一的球形, 用蒸馏水多次洗涤。当在洗出液中滴入1mol/L BaCl2溶液,无白色沉淀出现后, 再加洗 10余次, 此时可认为洗出液的电导与蒸馏水的电导在相同数量级内。将洗好的硅胶在85℃下干燥24 h, 得到直径3~4 mm的球形吸附材料。
1.3 Cu2+溶液的配制
Cu2+储备液(100 mmol/L)采用溶解优级纯CuSO4·5H2O的方法制得。其他浓度Cu2+溶液通过稀释储备液配制。
1.4 实验方法
1.4.1 pH对吸附的影响
配制1.0 mmol/L的Cu2+溶液50 mL, 加入0.15 g吸附材料, 调整pH分别为2.0, 3.0, 4.0, 5.0, 6.0, 恒温摇床内振荡使体系达到平衡。将吸附材料用纱网滤除, 取剩余的滤液5 mL用优级纯 HNO3酸化后, 原子吸收法测剩余Cu2+的浓度。吸附前后 2次测得的 Cu2+量的差值为硅酸固定褐藻渣吸附Cu2+的量, 计算如下:

其中qt为时间t时吸附材料对 Cu2+的单位吸附量(mmol/g);c0为溶液初始Cu2+浓度(mmol/L);ct为时间t时溶液中的Cu2+浓度(mmol/L);V为溶液体积(L);W为加入吸附材料的质量(g)。
实验同时设一系列不加吸附材料的对照组实验,以消除氢氧化物沉淀、反应器壁吸附等因素的影响。为保持pH恒定, 实验过程中每隔1 h调pH 1次。
1.4.2 Cu2+初始浓度对吸附的影响
分别制取1.0~4.0 mmol/L的Cu2+溶液7组(经测定其浓度分别为 1.03、1.40、1.93、2.13、2.80、3.14、3.83 mmol/L, 见图2)各100 mL于250 mL锥形瓶中,用0.1 mol/L的HNO3和NaOH调节溶液的pH值至5.0。分别称取7份0.3 g硅胶固定的褐藻渣同时加入配制好的 Cu2+溶液中, 恒温水浴摇床内在 25℃、60 r/min下进行振荡吸附实验, 吸附24 h后, 用移液枪移取上层溶液5 mL放到稀HNO3浸泡过的小塑料瓶内, 用 HNO3酸化后原子吸收测量溶液中的 Cu2+含量。Cu2+的吸附量由吸附前后的 Cu2+浓度差值确定,计算方法同pH的测定。
1.4.3 Cu2+吸附时间对吸附的影响
分别制取 1.0、2.0、4.0 mmol/L的 Cu2+溶液 3组, 每种Cu2+溶液各取200 mL于1 000mL锥形瓶中,用0.1mol/L的HNO3和NaOH溶液调节pH值至5.0。分别称取3份质量为0.6 g硅胶固定的褐藻渣。同时加入配制好的 Cu2+溶液中, 恒温水浴摇床内在60 r/min下进行振荡吸附实验。在吸附时间分别为0、5、25、50、75、100、150、200、300、400、600、900、1500 min时, 用移液枪移取上层溶液5mL至稀HNO3浸泡过的小塑料瓶内, 用 HNO3酸化后原子吸收测量溶液中的Cu2+含量, 计算方法同pH的测定。
1.4.4 温度对吸附的影响
配制 3组浓度均为 1.0 mmol/L的 Cu2+溶液各50 mL, 分别置于15、25、35 ℃水浴中达到恒温。调节pH值为5.0, 并各加入0.15g硅胶固定的褐藻渣,在60 r/min下进行吸附实验。24 h后测量Cu2+溶液的浓度以确定吸附量, 计算方法同pH的测定。
1.4.5 吸附热力学
吸附热力学分析采用1.4.2中实验所得数据。
1.4.6 吸附动力学
吸附动力学分析采用1.4.3中实验所得数据。
2 结果与讨论
2.1 pH值对吸附效果的影响
由于溶液 pH值对吸附剂表面的质子化程度和重金属离子的水化学性质两方面都有影响, 不管生物吸附材料是否经过固定化处理, pH对重金属离子吸附效果的影响都十分显著。如图1所示, pH为2,吸附体系达到平衡时Cu2+去除率仅为38%, 当pH在2~4之间吸附材料对Cu2+的吸附量随着pH的增加有显著增加的趋势; 在pH为4时, 体系已达到相对稳定的最大值, 去除率大于90%。褐藻渣的主要成分为粗纤维(50%)和粗蛋白(20%), 这些组成中可与 Cu2+相结合的主要官能基团有羧基、磷酰基、羟基、硫酸脂基、氨基和酰胺基等, 其中氮、氧、磷、硫作为配位原子可与金属离子配位络合[10]。表面络合机理认为, pH较低时, 褐藻渣表面基团易因质子化而显正电, 由于斥力作用 Cu2+难以靠近络合位点, 致使吸附量减少。pH值越低, 质子化现象越明显, 吸附材料对 Cu2+的单位吸附量就越小。随着 pH的升高,质子化的官能团被暴露出来, 吸附剂表面带负电,有利于金属离子的接近并吸附在材料表面[11-12]。上述现象也可以用离子交换机理进行解释[13]。Cu2+进行离子交换必须在吸附位点上发生复分解反应与活性基团结合, 当溶液 pH变低, H3O+浓度增加, 使复分解反应向 H3O+与活性基团结合的方向进行, 即H3O+与Cu2+产生竞争, 不利于Cu2+吸附。
空白实验数据显示在各个 pH下 Cu2+均有一定的损失, pH为6时损失增加。这可能是由于反应容器对 Cu2+的吸附损失和较高 pH下 Cu2+水解作用共同产生的。如果pH进一步增大, 产生的Cu(OH)2沉淀沉积在吸附材料表面, 很可能造成空隙阻塞, 吸附活性位点无法良好接触Cu2+离子, 影响吸附。由于从已有数据来看, pH为5时褐藻渣对几种常见有害重金属的吸附情况最佳[7], 因此重点考察pH为5时硅胶固定的褐藻渣吸附材料吸附 Cu2+的性质, 下文涉及的吸附实验初始pH均在5.0±0.1的范围内。
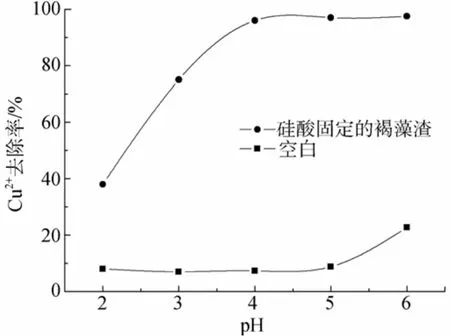
图1 不同pH下硅胶固定的褐藻渣对重金属Cu2+的吸附Fig. 1 Adsorption of Cu2+by silica-gel-immobilized brown algae residue at different pHs
2.2 Cu2+初始浓度的影响
溶液的化学状态是决定生物吸附效率的重要因素, 除pH外, 金属离子的浓度也是溶液化学状态的重要方面。图 2是 Cu2+起始浓度对吸附率及吸附材料单位质量吸附量的关系曲线。
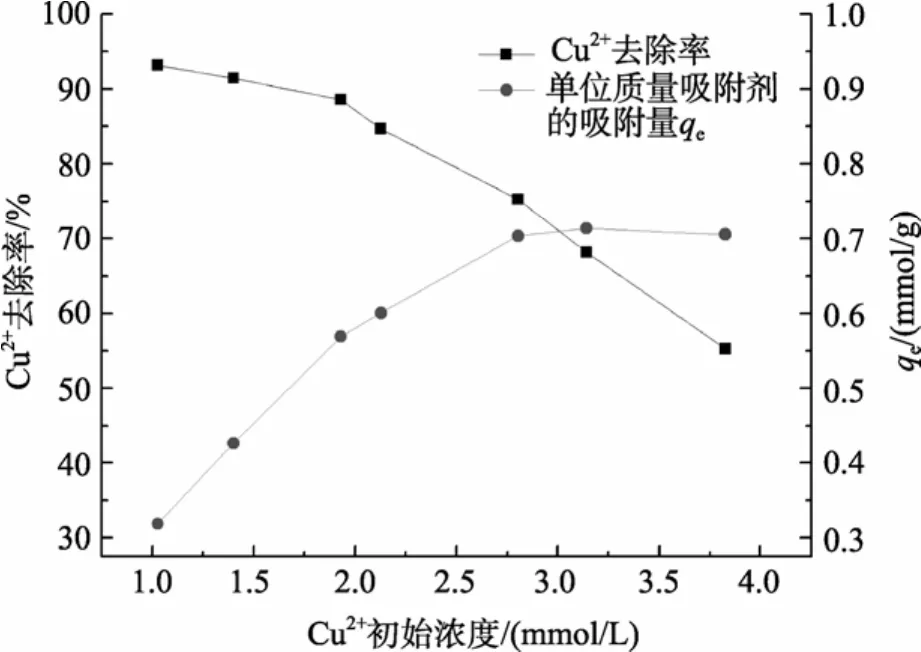
图2 不同初始浓度对平衡时Cu2+去除率及吸附剂单位质量吸附量的影响Fig. 2 Variation of Cu2+removal efficiency and equilibrium biosorption capacity at different initial concentrations of Cu2+
由图2可见, Cu2+初始浓度在1~2 mmol/L时去除率可达 85%, 随着 Cu2+初始浓度升高, 在添加吸附剂的量不变的情况下, 去除率逐渐降低。这一现象可认为与吸附位点的量有关[15]。另外, 吸附剂的吸附效率随着 Cu2+浓度的增加而增加。当初始浓度大于3 mmol/L时, 可认为吸附接近饱和, 每克吸附剂的吸附量稳定在0.7 mmol左右。假设有离子吸附反应:
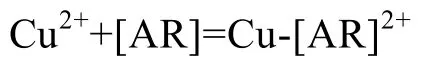
其中[AR]表示固定化褐藻渣, 则有反应平衡常数K。当在其他条件不变的情况下, 溶液中Cu2+浓度增加并不改变反应平衡常数K的大小, 所以有利于吸附反应向右进行, 吸附量增加。
2.3 Cu2+的吸附平衡时间
图3显示了25℃下, Cu2+初始浓度为1.0、2.0、4.0 mmol/L时, 吸附百分率随时间的变化。在反应开始阶段的前 75 min内, 吸附反应保持快速进行, 随后 Cu2+浓度下降缓慢, 吸附 3 h后趋于平衡。改变Cu2+初始浓度, 吸附行为基本相同。这种反应趋势是由于吸附材料内部发达的孔隙使反应初期 Cu2+在小球内扩散的时间可忽略不计, Cu2+得以迅速与大量活性吸附位点接触, 因此反应从一开始就快速进行,并且迅速接近平衡。接近吸附平衡时, 固液两相中Cu2+间的斥力使 Cu2+占据剩余吸附位点变得困难,吸附速度降低[14]。褐藻渣-硅酸复合吸附材料在短时间内接近吸附平衡的特点有利于在实际应用中提高效率。
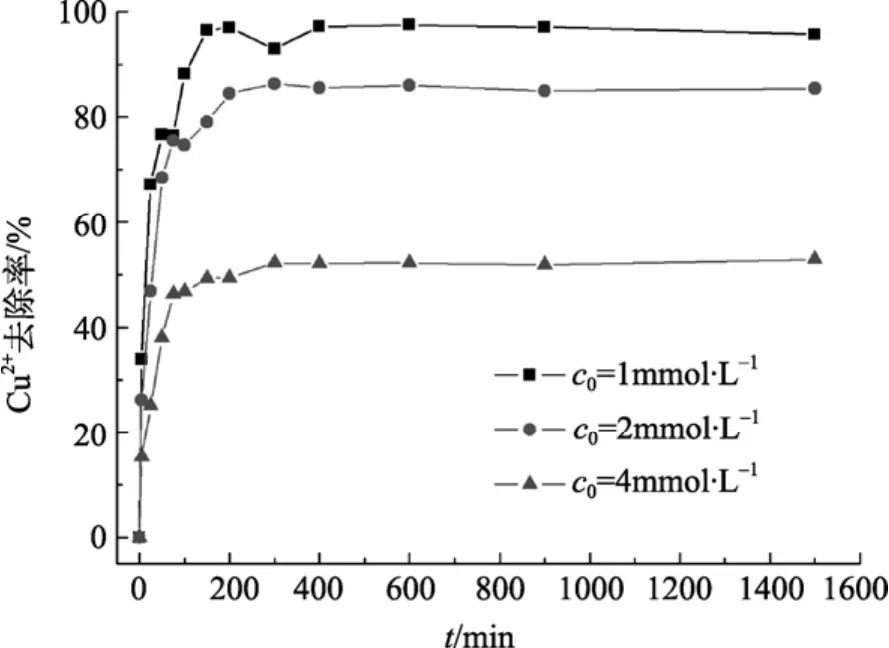
图3 不同初始浓度下重金属Cu2+去除率随时间的变化Fig. 3 Kinetics of Cu2+removal efficiency at different initial concentrations of Cu2+
2.4 温度对吸附的影响
硅胶固定的褐藻渣对 Cu2+的吸附率随温度的变化曲线如图4所示。随着温度变化, 吸附量变化不大,在 15~35℃范围内吸附反应受温度影响较小。在实验范围内, 吸附剂的吸附率均随温度的升高小幅增大, 说明在该吸附过程可能为吸热反应。其中, 15~25℃区间内Cu2+去除率增加幅度大于25~35℃区间的去除率增加幅度, 这可能是由于温度升高导致吸附剂对Cu2+的解吸作用增强。
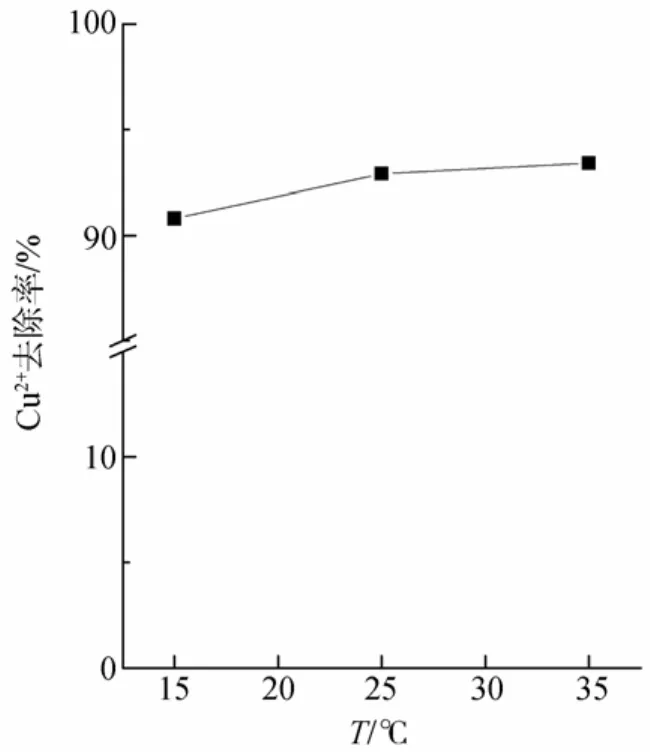
图4 不同温度下Cu2+去除率的变化Fig. 4 Variation of Cu2+removal efficiency at different temperatures
2.5 吸附热力学
2.5.1 吸附平衡模型
用于拟合实验数据的吸附模型有 3种: Langmuir、Freundlich 和 Dubimim-Radushkevich。
2.5.1.1 Langmuir吸附等温式
Langmuir吸附等温式是基于假设吸附发生在吸附剂表面特定均一的吸附位点的基础上提出的, 它常常被用来描述吸附体系中金属离子吸附量与溶液中金属离子平衡浓度之间的关系。其表达式[16]为:

式中qe为平衡时的单位吸附量(mmol/g),qm为单层吸附的单位吸附容量(mmol/g),ce为平衡时溶液中Cu2+的浓度(mmol/L),KL是Langmuir常数(L/mmol), 其大小与生物吸附自由能有关, 反映了吸附质与吸附剂之间的结合力[17]。方程(2)可转化为线性方程的形式:
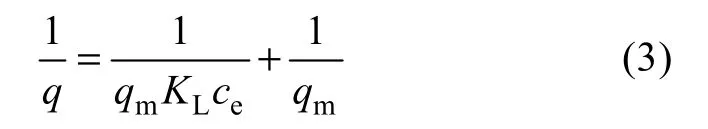
Freundlich吸附等温式:
Freundlich吸附等温式是基于吸附质在多相表面上的吸附建立的经验吸附平衡模式:

其中,KF为Freundlich常数, 与吸附量有关;n为Freundlich指数, 与吸附强度有关。方程(2)可转化为线性方程的形式[18]:
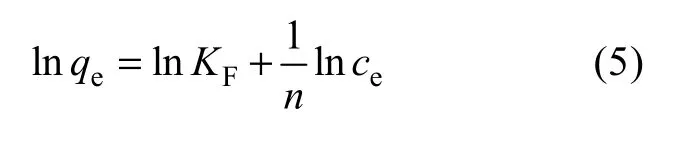
2.5.1.2 Dubimim-Radushkevich等温式
Dubimim和Radushkevich发现生物吸附特征曲线与吸附剂的多孔结构有关, 依据特性曲线的形状特点, 提出孔分布呈Gaussin分布的假设, 导出公式带入吸附势ε的表达式, 得到 Dubimim-Radushkevich(D-R)等温式。表达形式如下:
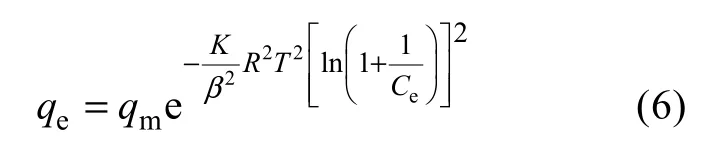
其中,β为亲和系数,K是与孔结构有关的常数。上式可化为线性表达式:
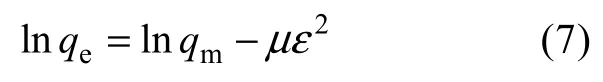
2.5.2 拟合结果
实验数据用Langmuir、Freundlich和Dubimim-Radushkevich等温线方程分别进行线性拟合(使用(3)、(5)、(7)式)和非线性拟合(使用(2)、(4)、(6)式)得到回归方程的参数结果见表1。
可见线性拟合和非线性拟合所得的各项参数基本一致。其中, 非线性拟合的曲线见图5。
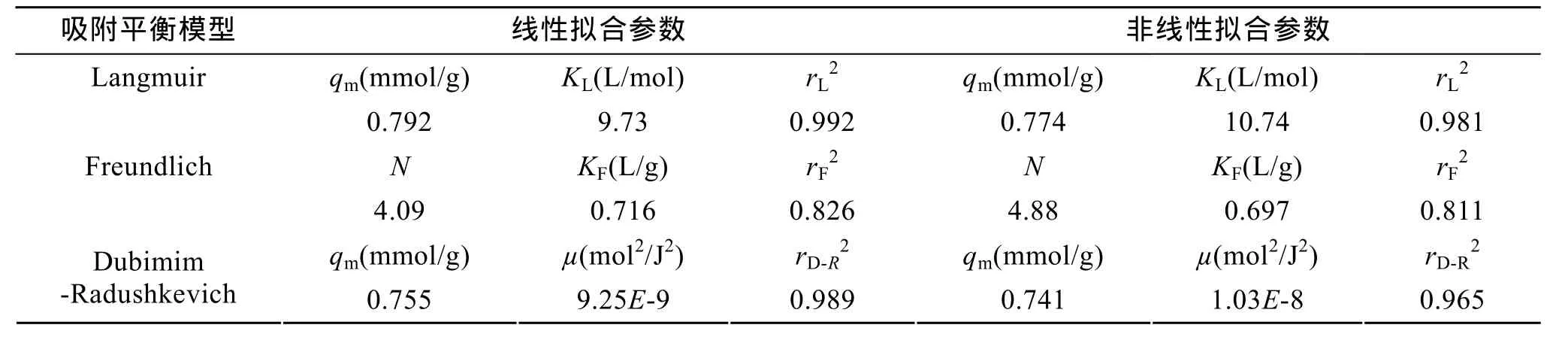
表1 硅胶固定的褐藻渣对重金属离子Cu2+的吸附热力学参数Tab. 1 Langmuir, Freundlich, and Dubimim-Radushkevich sorption constants of Cu2+by silica-gel-immobilized brown algae residue
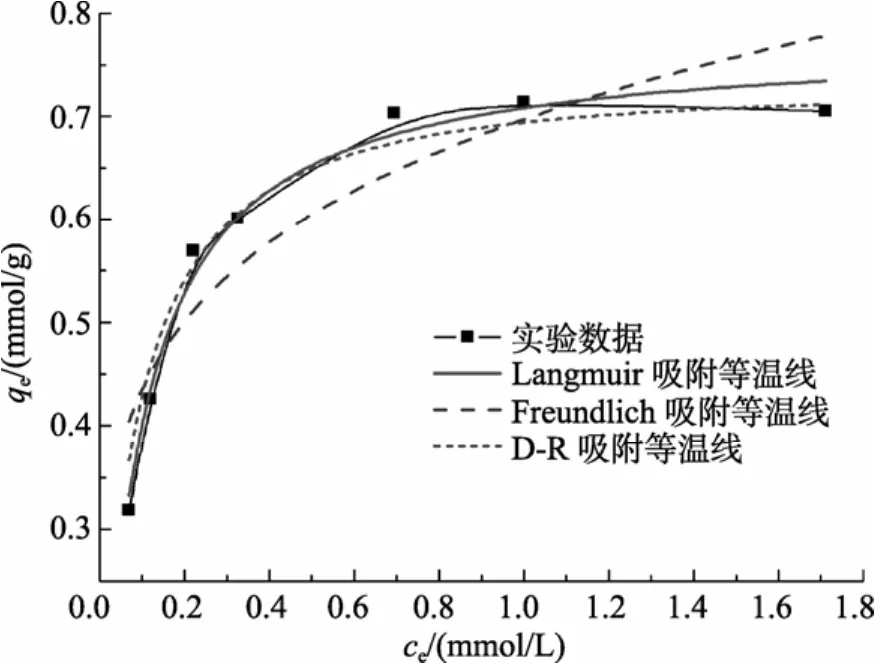
图5 硅胶固定的褐藻渣对重金属Cu2+的吸附等温线Fig. 5 Adsorption isotherms of Cu2+by silica-gel-immobilized brown algae residue
由线性相关系数r2可以看出, 试验结果用Langmuir方程模拟的效果较好, 其次是D-R方程,而用 Freundlich方程模拟的结果较差。其中, Langmuir吸附等温线的方差为0.992和0.981, 可以认为吸附符合Langmuir模式的基本假设: 吸附质呈单分子层形式附着在吸附剂表面[19]。同时也表明吸附材料表面均一性良好, 故能对 Cu2+的吸附呈单分子层形式。
Langmuir吸附等温式的平衡参数RL是描述吸附过程是否有利的分离因子,RL(无量纲常量)计算式如下:
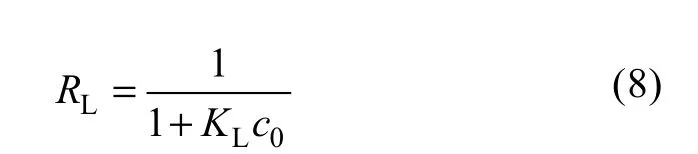
RL值可用来预测吸附剂与吸附质之间的结合力。RL若处于0~1之间, 表明吸附性能良好, 若大于1, 则对吸附不利[19,20], 其值等于0和1时, 分别为不可逆反应和线性吸附的情况[21]。RL值越接近0, 显示Cu2+吸附后不易脱附。由线性拟合的Langmuir等温式计算出的KL代入式(8), 得RL的值由图6表示。当溶液初始浓度在1.0~4.0 mmol/L范围内,RL值均小于0.1, 且浓度越高,RL值越小。这说明了吸附材料对Cu2+的吸附性能很好, 且溶液初始浓度较高时对吸附更有利。
Freundlich等温式的特征参数一般能表明吸附的难易程度。0.1<1/n<1.0时容易吸附, 而且1/n的值越大, 吸附性能越好[19]。由表1中n的数据值可算出1/n=0.244, 介于 0.1~1.0之间, 吸附材料对 Cu2+的吸附性能较好。
Dubimim-Radushkevich等温线的相关系数列于表1中, 其最大吸附量qm和Langmuir等温线推算出的最大吸附量相近, 在0.7~0.8 mmol/g之间。硅胶固定的褐藻渣最大吸附量小于海带等褐藻的吸附量[22],但大于绝大多数其他种类的生物吸附材料, 如菌体[15, 23]、植物体[24, 25]等等。
从数值上看, 硅酸固定的褐藻渣单位质量对Cu2+的吸附量小于未经固定的褐藻渣吸附量 4.20 mmol/g[7], 但硅酸固定的褐藻渣中褐藻渣的实际质量只占总质量的十分之一左右, 与使用纯褐藻渣吸附 Cu2+得出的数据没有可比性, 因此不能得出固定化过程会降低褐藻渣吸附能力的结论。另外, 硅胶表面的硅羟基也能与 Cu2+离子结合起到一定的吸附作用, 硅胶固定的褐藻渣中的两种主要成分对吸附均有贡献。
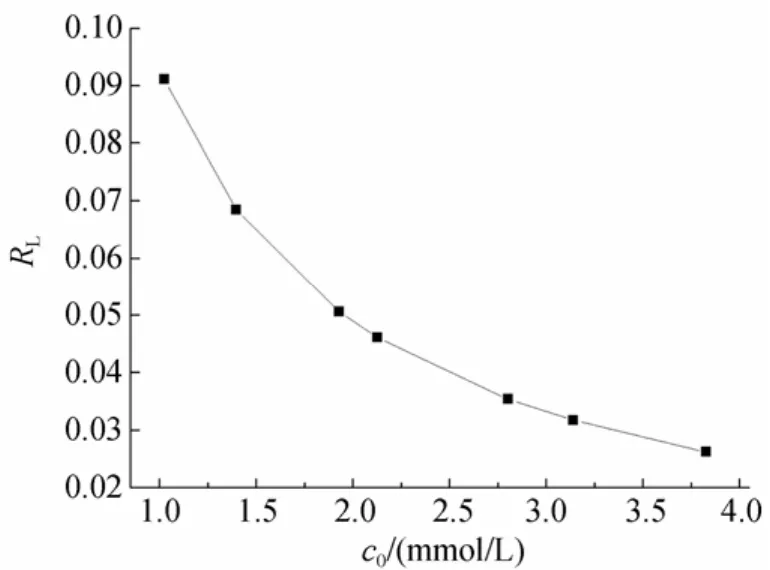
图6 RL随初始浓度的变化曲线Fig. 6 Variation of RLat different initial concentrations of Cu2+
2.6 吸附动力学
吸附过程的动力学研究主要用来描述吸附剂吸附溶质的速率。通常用伪一级和伪二级动力学方程对试验数据进行模拟, 来分析金属离子浓度随吸附时间的变化关系[26,27]。
伪一级动力学方程表示如下:
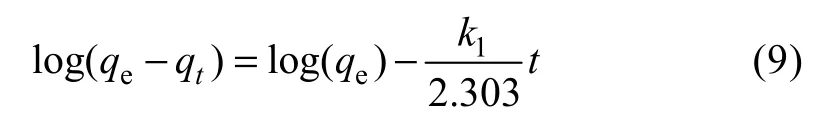
式中,k1为伪一级反应速率常数(min−1)。按式(9)对初始浓度分别为1、2、4mmol/L的Cu2+的吸附速率实验数据进行线性拟合, 以 log(qe−qt)对t作图(图7), 由图 7的斜率和截距计算得k1的数据(表 2), 线性相关系数为R2在0.884~0.929之间, 线性相关性不十分理想。
伪二级模型是建立在假设检测离子浓度等于细胞表面的离子浓度基础上的。伪二级动力学方程表示如下:
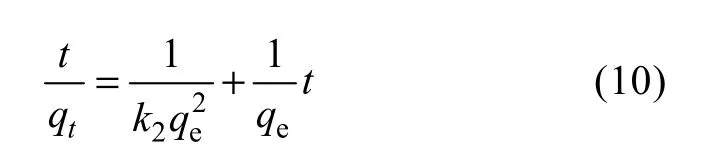
式中,k2为伪二级反应速率常数(min−1)。按式(10)对Cu2+的吸附速率实验数据进行线性拟合, 以t/qt对t作图8, 由图8的斜率和截距计算得k2的数据(见表2), 线性相关系数为R2均在0.999以上, 线性相关性很好, 这表明硅胶固定的褐藻渣对 Cu2+的吸附动力学过程可用伪二级动力学模式描述。根据伪二级动力学方程建立的机理, 可推测在符合此方程的吸附时间内质量扩散对吸附速率的影响可以忽略, 限速步骤是化学吸附过程。该过程可能与吸附剂及金属离子之间电子共享或电子交换的共价力有关[15]。
与伪一级动力学方程相比, 伪二级动力学方程能更好地描述吸附材料对 Cu2+的吸附过程, 由伪二级动力学方程推测出的平衡吸附量q2nd与实测平衡吸附量qe十分接近(见表2), 因此二级动力学参数可以用于平衡吸附量、去除率等的计算。初始吸附速率和速率常数等有助于反应器的设计。
3 结论
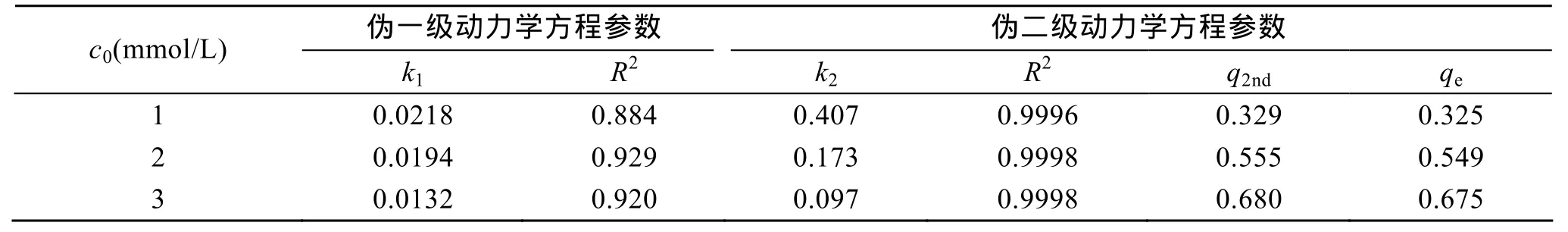
表2 硅胶固定的褐藻渣对重金属离子Cu2+的吸附动力学参数Tab. 2 Pseudo first-order and Pseudo second-order adsorption constants of Cu2+by silica-gel-immobilized brown algae residue
褐藻渣材料易得, 成本低廉, 硅胶固定化的褐藻渣球状吸附材料对 Cu2+有较强的吸附能力, 并且兼有易于回收、比表面积大、机械强度增强等特点。
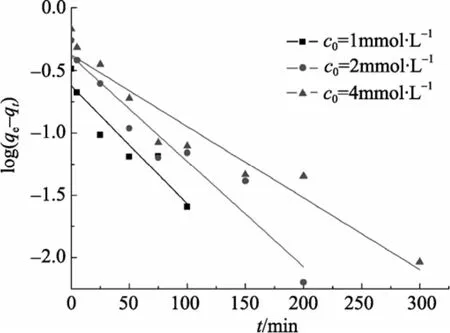
图7 伪一级动力学线性关系图Fig. 7 Linearized pseudo-first order kinetics at different initial concentrations of Cu2+
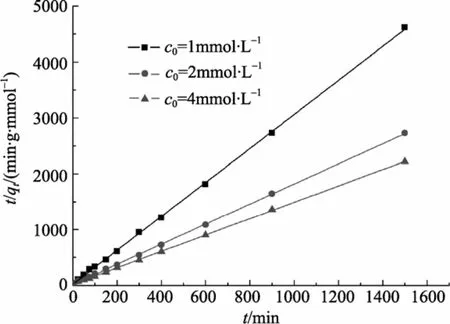
图8 伪二级动力学线性关系图Fig. 8 Linearized pseudo-second order kinetics at different initial concentrations of Cu2+
使用硅胶固定的褐藻渣对重金属 Cu2+的吸附特征实验表明pH值、Cu2+初始浓度以及吸附时间对吸附过程均有很大的影响。25℃时, 实验最佳pH为5,吸附3 h对初始浓度在2.0 mmol/L以下的铜溶液吸附率可达85%, 其中前75 min为快速反应阶段。其吸附等温线符合Langmuir、Dubimim- Radushkevich方程, 基本符合Freundlich方程。在25℃、pH为5.0的条件下, 吸附材料对 Cu2+的最大吸附容量在0.7~0.8 mmol/g之间。吸附动力学过程符合伪二级动力学模型, 说明吸附时间内质量扩散对吸附速率的影响可以忽略, 限速步骤是化学吸附过程。
实验结果表明, 硅胶固定的褐藻渣可以作为吸附 Cu2+的生物吸附材料二次利用, 达到以废治废的目的。此材料在吸附回收水体中的低浓度重金属离子方面有广阔的开发潜力。
[1] 科学通报编辑部. 褐藻胶试制成功[J]. 科学通报, 1953, 7: 98.
[2] 纪明侯, 史升耀. 海带褐藻胶提取条件的研究[J]. 海洋科学集刊, 1962, 1: 188-195.
[3] 甘纯玑, 彭时尧, 施木田, 等. 海带工业废弃物综合利用现状和展望[J]. 环境科学进展, 1999, 7(1):50-53.
[4] 王寿昆, 李建生, 林树根, 等. 海带废渣水平对罗非鱼饲料蛋白质和氨基酸消化率的影响[J]. 福建农业大学学报, 1997, 26(4): 465-469.
[5] 甘纯玑, 施木田, 彭时尧, 等. 海藻工业废料的组成及其利用价值[J]. 天然产物研究与开发, 1994, 6(2): 88-91.
[6] 冯大伟. 利用两种大型海藻制备生物能源的探索研究[D]. 青岛: 中国科学院海洋研究所, 2009: 87-89.
[7] 邓莉萍. 藻体对水环境中N、P及重金属Cu2+、Pb2+、Cd2+、Cr2+的吸附特征研究[D]. 青岛: 中国科学院海洋研究所, 2008: 102.
[8] R. Herrero, B. Cordero, P. Lodeiro, et al. Interactions of cadmium(II) and protons with dead biomass of marine algae Fucus sp.[J]. Marine Chemistry, 2006, 99:106-116.
[9] 张松涛. 大孔径硅胶的制备研究[J]. 上海化工, 1994,19(5): 13-17.
[10] 刘瑞霞, 汤鸿霄, 劳伟雄. 重金属的生物吸附机理及吸附平衡模式研究[J]. 化学进展, 2002, 14(2): 87-92.
[11] Dönmez G C, Aksu Z, Öztürk A, et al. A comparative study on heavy metal biosorption characteristics of some algae[J]. Process Biochemistry, 1999, 34(9):885-892.
[12] Aksu Z. Equilibrium and kinetic modeling of cadmium(II) biosorption by C. vulgaris in a batch system:effect of temperature[J]. Separation and Purification Technology, 2001, 21(3): 285-294.
[13] Liping Deng, Xiaobin Zhu, Xinting Wang, et al. Biosorption of copper(II) from aqueous solutions by green alga Cladophora fascicularis[J]. Biodegradation, 2007,18: 393-402.
[14] Vijayaraghavan K, Mao J, Yun Y S. Biosorption of methylene blue fromaqueous solution using free and polysulfone-immobilized Corynebacterium glutamicum:Batch and column studies[J]. Bioresource Technology,2008, 99: 2 864-2 871.
[15] 陈灿, 王建龙. 酿酒酵母吸附Zn2+、Pb2+、Ag+、Cu2+的动力学特性研究[J]. 环境科学学报, 2007, 27(4):544-553.
[16] Akar T, Kaynak Z, Ulusoy S, et al. Enhanced biosorption of nickel(II) ions by silica-gel-immobilized wastebiomass: Biosorption characteristics in batch and dynamic flow mode[J]. Journal of Hazardous Materials,2009, 163: 1 134-1 141.
[17] Holan Z R, Volesky B, Prasetyo I. Biosorption of cadmium by biomass of marine algae[J]. Biotechnology and Bioengineering, 1993, 41: 819-825.
[18] 苏峰, 罗胜联, 曾光明, 等. 海带对镉的吸附动力学与热力学研究[J]. 环境工程学报, 2009, 3(5):857-860.
[19] Erenturk S, Malkoc E. Removal of lead(II) by adsorption onto Viscum album L.Effect of temperature and equilibrium isotherm analyses[J]. Applied Surface Science, 2007, 253: 4 727-4 733.
[20] Han R P, Zhang J H, Zhou W H, et al. Equilibrium biosorption isotherm for lead ion on chaff[J]. Journal of Hazardous Materials, 2005, B125: 266-271.
[21] Al-Rub F A A, El-Naas M H, Benyahia F, et al. Biosorption of nickel on blank alginate beads, free and immobilized algal cells[J]. Process Biochemistry, 2004,39: 1 767-1 773.
[22] Fourest E, Volesky B. Alginate properties and heavy metal biosorption by marine algae [J]. Applied Biochemistry and Biotechnology, 1997, 67(1): 33-44.
[23] Beolchini F, Pagnanelli F, Toro L, Veglio F. Ionic strength effect on copper biosorption by Sphaerotilus natans: Equilibrium study and dynamicmodelling inmembrane reactor[J]. Water Research, 2006, 40:144-152.
[24] Handan Ucuna, Ozkan Aksakalb, Ergun Yildiz. Copper(II) and zinc(II) biosorption on Pinus sylvestris L[J].Journal of Hazardous Materials, 2009, 161: 1 040-1 045.
[25] Ofomaja A E, Naidoo E B, Modise S J. Dynamic studies and pseudo-second order modeling of copper(II)biosorption onto pine cone powder[J]. Desalination,2010, 251: 112-122.
[26] Yahaya Y A, Don M M, Bhatia S. Biosorption of copper(II) onto immobilized cells of Pycnoporus sanguineus from aqueous solution: Equilibrium and kinetic studies[J]. Journal of Hazardous Materials, 2009, 161:189-195.
[27] Miretzky P, Saralegui A, Cirelli A F. Simultaneous heavy metal removal mechanism by dead macrophytes[J]. Chemosphere, 2006, 62(2): 247-254.
Received: Mar., 18, 2010
Key words:biosorption; algal residues; immobilization; copper.
Abstract:Algal residues, solid wastes in brown algae industrial production, can destroy ecological balance if they are discharged directly into natural waters. We investigated the biosorption characteristics of Cu2+by silica-gel-immobilized algal residues. The experimental data show that pH, initial Cu2+concentrations, and contact time have significant impact on biosorption process. The removal of Cu2+could reach about 85% when initial Cu2+concentration was below 2mmol/L, and the maximum adsorption capacities was around 0.7~0.8mmol/g at 25 °C.We also fit our equilibrium data with Langmuir, Freundlich or Dubinin–Radushkevich isotherm models. Kinetic features of Cu2+biosorption were modeled by pseudo first-order and pseudo second-order equations. The results indicate that the silica-gel-immobilized algal residue is low-cost, selective, easily regenerated, and of improved mechanical strength, and can be used for remove heavy metals from wastewater.
(本文编辑:康亦兼)
Biosorption of Cu2+by silica-gel-immobilized brown algae residue
YANG Pei-shan1,2, YU Yan-qing1,2, LI Chao-feng1,2, ZOU Xiao-lan1,2, WANG Xin-ting1, ZHU Xiao-bin1
(1. Institute of Oceanology, the Chinese Academy of Sciences, Qingdao 266071, China; 2. Graduate School of the Chinese Academy of Sciences, Beijing 100049, China)
X799
A
1000-3096(2011)02-0044-08
2010-03-18;
2010-06-01
国家863计划项目(2006AA06Z362)
杨沛珊(1984-), 女, 山东青岛人, 中国科学院海洋研究所硕士研究生, 主要从事环境友好化学研究, E-mail: yangpeishan@ms.qdio.ac.cn,电话: 0532-82898710; 朱校斌, 通信作者, 电话: 0532-82898710, E-mail:xbzhu@qdio.ac.cn

