LAMP(环介导等温扩增)的原理及在寄生虫检测上的应用*
史亚东,赵子方,朱 丹,张龙现,宁长申,菅复春
LAMP(环介导等温扩增)的原理及在寄生虫检测上的应用*
史亚东,赵子方,朱 丹,张龙现,宁长申,菅复春
2000年,Notomi等[1]建立了一种快速、简单、灵敏、特异并且低成本的核酸扩增方法——环介导等温扩增法(LAMP),这种新颖的核酸扩增方法具有许多优势[2-4]:(1)扩增效率极高,60min内扩增产物可达到靶基因的109~1010倍;(2)操作简单,只需在65℃左右的恒温条件下将反应物混合即可,不需要复杂的温度变化过程;(3)灵敏性高,扩增模板只需10拷贝或更少;(4)特异性高,设计4条引物识别靶基因上6个不同区域;(5)结果判定简单,可以通过反应副产物直接肉眼观察,也可以通过浊度仪实时监控,无需电泳。LAMP方法的这些优势,使其短时间内在病毒、微生物、寄生虫等检测上广泛应用。以下就LAMP方法的原理及在寄生虫检测上的应用,简述如下。
1 LAMP原理[1,5]
1.1 引物 LAMP方法需要根据靶基因设计两对特殊引物,分别是内引物FIP和BIP、外引物F3和B3。它们特异识别靶基因的6个不同区域:3′端的F3c、F2c、F1c和5′端的B1、B2、B3。FIP由F2(与F2c互补)和F1c构成;BIP由B2(与B2c互补)和B1c构成,如图1。
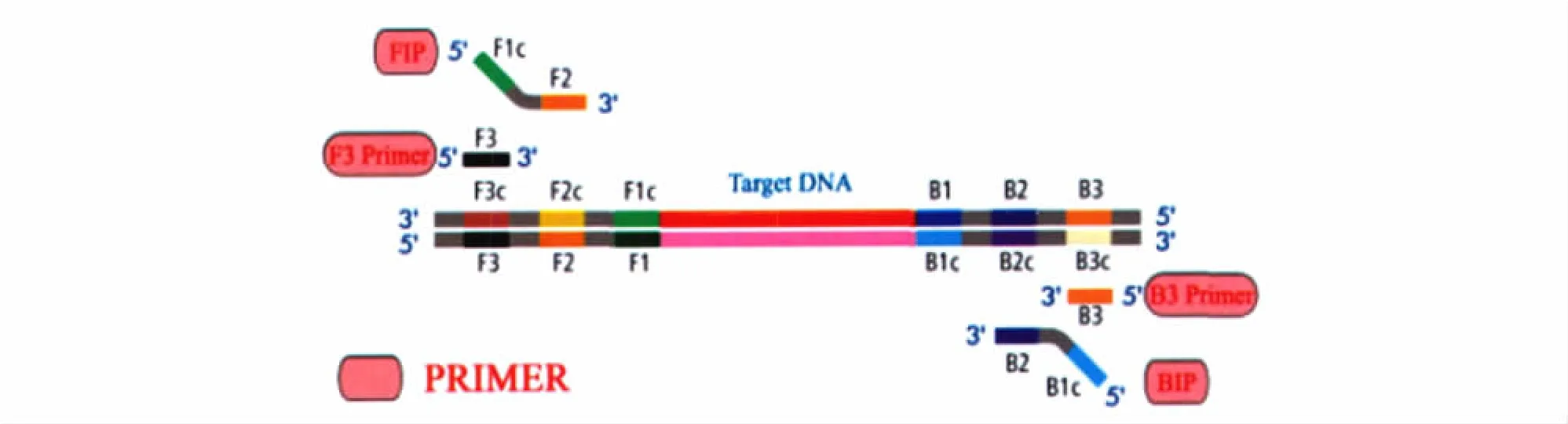
图1 LAMP的引物组成及对应区域
LAMP方法的引物设计较为复杂,但有专门软件可以设计LAMP引物,这使LAMP方法变的很易操作,Eiken GENOME SITE网站(http://primerexplorer.jp/e/)专门开发了 LAMP引物设计软件,研究者可以通过该软件获得精准的LAMP引物。
1.2 循环过程 在65℃左右时,DNA双链处于解链和聚合的动态平衡中,一个LAMP引物可以和靶基因链的一端互补结合,然后开始利用DNA聚合酶通过链置换作用合成DNA,置换并释放出一条单链DNA,这不像PCR方法那样需要通过热变性来得到单链DNA。下面就从FIP释放单链DNA开始说明LAMP的扩增机制。
通过链置换作用,DNA聚合酶从FIP上F2的3'端开始合成一条和靶基因链互补的DNA链。接着,F3和F3c区域互补结合,在靶基因链通过DNA聚合酶合成DNA,并置换出FIP结合的互补链。F3依照靶基因链合成一个互补链,这样就形成了一个双链DNA。F3引物合成新DNA链并把原来的DNA链置换出,这样FIP结合的互补链就被释放。然后,因为F1c区域和F1区域互补,被释放的单链DNA就在其5'端形成一个茎环结构。上面形成的单链DNA作为一个模板用于BIP启动DNA合成,也用于后来的B3引物通过链置换进行DNA合成。BIP与在上面形成的DNA链结合,从BIP的3'端开始合成互补DNA链。通过这个过程,DNA由环状结构恢复成线性结构。B3引物在BIP的外侧通过DNA聚合酶的活动从3'端开始进行复性过程,BIP合成的DNA在B3引物合成DNA之前被置换释放出来。经过上面的过程就产生了双链DNA。而BIP结合的互补链被置换后在两端各自形成环茎结构,类似于哑铃结构,如图2。

图2 哑铃结构
哑铃结构是LAMP循环的起始结构,它以自身为模板,由3’末端F1启动合成;与此同时,FIP结合于哑铃状结构的F2c上启动合成。随后,在哑铃结构中新合成的3’末端B1c与B1互补形成茎环结构,并以B1引物自身为模板启动合成,并释放出刚刚FIP引导合成的互补链。如此往复,形成新的茎环结构又引导合成互补链。最终形成许多长短不一的DNA链,但都是靶基因的整数倍。如图3。
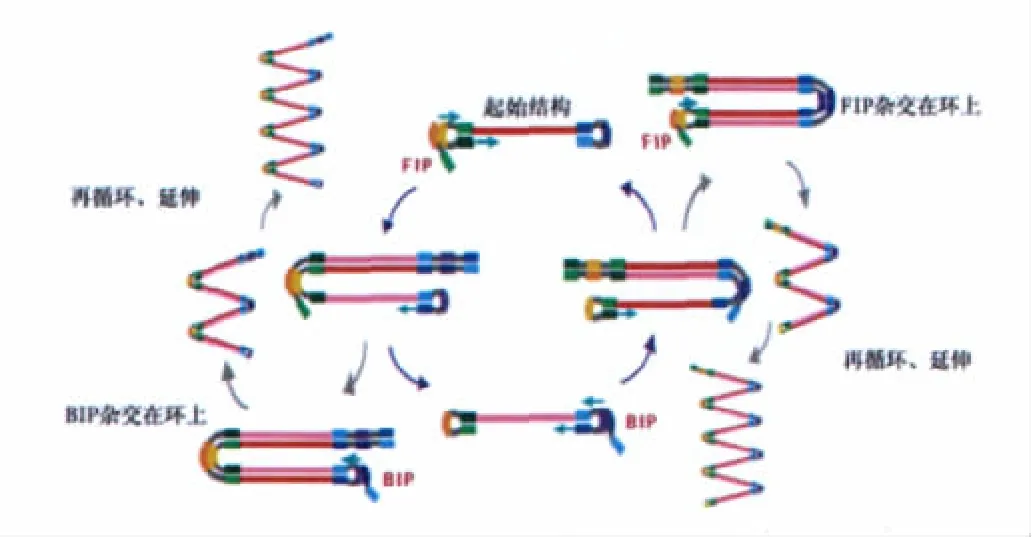
图3 LAMP循环过程
1.3 产物分析 LAMP方法扩增产物的检测可通过以下4种方式进行:(1)LAMP扩增副产物焦磷酸镁为白色沉淀,可肉眼观察,如果有扩增产物,可以看到白色沉淀;反之,则没有;(2)SYBR Green I检测,在反应液中加入SYBR Green I,可在紫外灯或日光下通过肉眼进行扩增结果判定。如果含有扩增产物,反应混合物变绿;反之,则保持SYBR Green I的橙色不变;(3)副产物焦磷酸镁的浊度检测,这种检测方式具有极高的特异性,使用浊度仪可以判断扩增发生与否,也可进行实时监控;(4)琼脂糖电泳检测,LAMP扩增产物为靶基因的整数倍,扩增产物经琼脂糖电泳后形成特征性梯状条带。
2 LAMP方法在寄生虫检测上的应用
近年来,LAMP方法在寄生虫检测上的应用得到了快速发展,表1列出了一些学者用LAMP方法检测寄生虫的一些内容。
2.1 原虫
2.1.1 锥虫 Thekisoe等[2]用不同方法检测实验感染猪的伊氏锥虫,结果表明LAMP方法同样具有较好的特异性和敏感性。Thekisoe等[6]后来又建立了种属特异性锥虫病的LAMP检测技术,用于检测布氏冈比亚锥虫、刚果锥虫、克氏锥虫和伊氏锥虫,可以检测锥虫DNA的最低限度是1fg,在锥虫病的田间和实验室诊断中具有很好前景。
2.1.2 隐孢子虫 隐孢子虫病是一种重要的人兽共患病,据报道[31]会导致艾滋病等免疫缺陷或抑制病人的因严重腹泻而死亡。Karanis等[8]等利用LAMP技术进行了动物隐孢子虫的检测研究,根据微小隐孢子虫60-kDa糖蛋白(gp60)基因设计引物,并以蒸馏水、正常牛血、布氏锥虫、牛巴贝斯虫等作为对照,验证LAMP方法的特异性,结果只有微小隐孢子虫电泳出现梯状条带。其研究还进行了敏感性实验,证明LAMP方法至少可以检测到一个卵囊。所建立的方法可以快速对动物粪便和环境样品判断是否有隐孢子虫,方便调查隐孢子虫病的流行情况。
2.1.3 弓形虫 人的先天性弓形虫病在胎儿或婴儿可出现发育畸形、智力障碍、脑炎甚至死亡等临床症状。Sotiriadou等[11]建立了检测水中弓形虫的LAMP方法。根据B1和TgOWP基因建立的方法检测极限为0.1个速殖体的DNA,与巢式PCR同时检测26个含有已知数目卵囊的水样,LAMP的检出率为100%,而巢式PCR为53.8%;又用自然水样来比较LAMP、PCR和免疫荧光试验3种检测方法,结果LAMP方法弓形虫检出率明显高于另外两种方法。
2.1.4 泰勒虫 Thekisoe等[14]利用小泰勒虫的PIM和p150基因建立LAMP方法,分别设计引物,每组靶基因引物包括6个引物,可以识别靶基因上的8个不同区域,这样可以高特异地检出小泰勒虫。每个引物组的检出限度是1fg,相当于小泰勒虫PIM或p150基因的1个拷贝。利用PIM和p150设计的LAMP引物组可以从不同国家的家畜和水牛隔离群中扩增出小泰勒虫。
2.1.5 巴贝斯虫 Iseki等[17]设计了针对牛巴贝斯虫和双芽巴贝斯虫棒状体联合蛋白-1基因(rhoptry-associated protein-1genes)的两套 LAMP引物,进行扩增试验,两条引物完成了各自的扩增,并且通过后来的酶切片段不同加以区分,建立了同时检测牛巴贝斯虫和双芽巴贝斯虫的多重LAMP方法。此法检测牛巴贝斯虫和双芽巴贝斯虫的敏感性比常规PCR分别高出103和105倍。
2.1.6 疟原虫 疟疾是世界六大热带病和我国五大寄生虫病之一,人体的疟原虫有4种:间日疟原虫、恶性疟原虫、三日疟原虫和卵形疟原虫。Han等[20]用根据人疟原虫18SrDNA建立LAMP方法可以检测人体的4种疟原虫,检测三日疟原虫、卵形疟原虫的极限为10拷贝,而对于恶性疟原虫和间日疟原虫的检测极限为100拷贝。与显微镜检相比其显示了较高的敏感性和特异性;与巢式PCR相比其检出率相符,但出结果时间更短。

表1 近年来LAMP方法在寄生虫检测中的一些应用
2.1.7 孢子虫 杨秋林等[24]根据卡氏肺孢子虫线粒体核糖体大亚基(mtrRNA)基因设计引物利用LAMP方法检测该虫。以结核杆菌、弓形虫、大鼠白细胞等为对照,将卡氏肺孢子虫DNA 10倍稀释后同时进行LAMP和PCR,比较两者的敏感性。结果卡氏肺孢子虫检测为阳性,对照组均为阴性。卡氏肺孢子虫LAMP产物经电泳后呈特征性梯状条带,扩增产物经Tail限制性内切酶酶切鉴定正确,对照组也均无扩增产物。LAMP可检测到虫体DNA的最低浓度是1Pg/μL,为PCR的10倍。
2.1.8 贾第虫 卢潍媛等[26]根据蓝氏贾第鞭毛虫rRNA序列设计4条特异引物建立了检测该虫的LAMP方法。以隐孢子虫卵囊、疟原虫为对照,并将纯水作为阴性对照,结果蓝氏贾第鞭毛虫检测为阳性;对照组均为阴性。且与LAMP产物琼脂糖凝胶电泳分析结果一致。
2.2 吸虫 Cai等[28]利用华支睾吸虫组织蛋白酶B3基因建立LAMP的方法能够敏感、快速的检测鱼是否感染华支睾吸虫,而且实验中的肝片吸虫、日本血吸虫等对照没有发生交叉反应,试验中LAMP检测华支睾吸虫的敏感性为常规PCR的100倍。该方法为检测鱼的华支睾吸虫提供了一个快速、敏感的工具,这为预防人的华支睾吸虫病提供了有效的手段。
2.3 绦虫 Nkouawa等[29]根据绦虫组织蛋白酶样半胱氨酸肽酶(CLP)和细胞色素C氧化酶亚基1(Cox1)基因设计LAMP引物,建立的检测绦虫的LAMP方法。其中根据Cox1基因建立的LAMP方法可以区分3个种,而根据CLP基因建立的LAMP可以区分有钩绦虫和无钩绦虫或亚洲带绦虫,通过限制性酶消化LAMP产物又可区分无钩绦虫和亚洲带绦虫。
2.4 线虫 郑洋妹等[30]根据简单异尖线虫ITS保守区域序列设计引物建立了快速鉴定该虫的LAMP方法。优化后对10倍比稀释的简单异尖线虫ITS序列重组质粒进行灵敏性试验;用典型异尖线虫、对盲囊线虫、针蛔线虫作为对照进行特异性试验;并将7份简单异尖线虫样品进行验证试验。结果检测简单异尖线虫的灵敏度达到10拷贝/μL,且对照均无交叉反应,7份简单异尖线虫样品检验为阳性。所建立的LAMP方法灵敏性高、特异性强,是鉴定简单异尖线虫的有效手段。
3 展 望
LAMP作为一种新颖的核酸扩增方法,在短短10年内,以其显著优势被研究者们广泛应用于分子检测,其发展前景非常广阔。虽然它的引物设计过程繁复,但是引物设计可以由相关研究单位和试剂公司来完成,对于操作人员来说是极为简单,只需要把处理好的样本和LAMP相关试剂一起放入65℃恒温水浴中,1h左右就能通过肉眼报告结果。这点作为临床检测具有很大意义,可开发成LAMP检测试剂盒,便于广大基层医疗卫生单位检验人员使用。总之,随着LAMP技术的不断完善和改进,相信LAMP方法将在寄生虫病的分子诊断及检测中发挥更大的作用。
[1]Notomi T,Okayama H,Masubuchi H,et al.Loop-mediated isothermal amplification of DNA[J].Nucleic Acids Research,2000,28(12):63.
[2]Thekisoe OM,Inoue N,Kuboki N,et al.Evaluation of loopmediated isothermal amplification(LAMP),PCR and parasitological tests for detection ofTrypanosomaevansiin experimentally infected pigs[J].Veterinary Parasitology,2005,130(3-4):327-330.
[3]Soliman H,EI-Matbouli M.Reverse transcription loop-mediated isothermal amplification(RT-LAMP)for rapid detection of viral hemorrhagic septicaemia virus(VHS)[J].Veterinary Microbiology,2006,114(3-4):205-213.
[4]潘树德,刘宝山,刘金铃,等.环介导等温扩增技术及其在病原检测中的应用[J].动物医学进展,2009,30(2):74-77.
[5]Nagamine K,Hase T,Notomi T.Accelerated reaction by loopmediated isothermal amplification using loop primers[J].Molecular and Cellular Probes,2002,16(3):223-229.
[6]Thekisoe OM,Kuboki N,Nambota A,et al.Species-specific loop-mediated isothermal amplification(LAMP)for diagnosis of trypanosomosis[J].Acta Tropica,2007,102(3):182-189.
[7]Njiru ZK,Mikosza AS,Matovu E,et al.African trypanosomiasis:Sensitive and rapid detection of the sub-genusTrypanozoonby loop-mediated isothermal amplification(LAMP)of parasite DNA[J].International Journal for Parasitology,2008,38(5):589-599.
[8]Karais P,Thekisoe O,Kioiptsi K,et al.Development and preliminary evaluation of a loop-mediated isothermal amplification procedure for sensitive detection ofCryptosporidiumoocysts in fecal and water samples[J].Applied and Environmental Microbiology,2007,73(17):5660-5662.
[9]Bakheit MA,Torra D,Plaomino LA,et a1.Sensitive and specific detection ofCryptosporidiumspecies in PCR-negative samples by loop-mediated isothermal DNA amplification and confirmation of generated LAMP products by sequencing[J].Veterinary Parasitology,2008,158(1-2):11-22.
[10]袁忠英,沈玉娟,曹建平,等.环介导等温扩增技术检测牛源隐孢子虫的研究[J].国际医学寄生虫病杂志,2009,36(3):144-146.
[11]Sotiriadou I,Karanis P.Evaluation of loop-mediated isothermal amplification for detection ofToxoplasmagondiiin water samples and comparative findings by polymerase chain reaction and immunofluorescence test(IFT)[J].Diagnostic Microbiology and Infectious Disease,2008,62(4):357-365.
[12]Alhassan A,Thekisoe OM,Yokoyama N,et al.Development of loop-mediated isothermal amplification(LAMP)method for diagnosis of equine piroplasmosis[J].Veterinary Parasitology,2007,143(2):155-160.
[13]Liu Z,Hou J,Bakheit MA,et al.Development of loop-mediated isothermal amplification(LAMP)assay for rapid diagnosis of ovine theileriosis in China[J].Parasitology Research,2008,103(6):1407-1412.
[14]Thekisoe OMT,ambritch NE,Nakao R,et al.Loop-mediated isothermal amplification(LAMP)assays for detection ofTheileriaparvainfections targeting the PIM and p150genes[J].International Journal for Parasitology,2010,40(1):55-61.
[15]王中光,张守发,曹世诺,等.牛瑟氏泰勒虫环介导等温扩增检测方法的建立[J].中国预防兽医学报,2010,32(2):108-111.
[16]Ikadai H,Tanaka H,Shibahara N,et al.Molecular evidence of infections withBabesiagibsoniparasites in Japan and evaluation of the diagnostic potential of a loop-mediated isothermal amplification method[J].Journal of Clinical Microbiology,2004,42(6):2465-2469.
[17]Iseki H,Alhassan A,Ohta N,et al.Development of a multiplex loop-mediated isothermal amplification(mLAMP)method for the simultaneous detection of bovineBabesiaparasites[J].Journal of Microbiological Methods,2007,71(3):281-287.
[18]Guan G,Chauvin A,Luo J,et a1.The development and evaluation of a loop-mediated isothermal amplification(LAMP)method for detection ofBabesiaspp.infective to sheep and goats in China[J].Experimental Parasitology,2008,120(1):39-44.
[19]He L,Zhou YQ,Oosthuizen M C,et al.Loop-mediated isothermal amplification(LAMP)detection ofBabesiaorientalisin water buffalo(Bubalusbabalis,Linnaeus,1758)in China.VeterinaryParasitology,2009,165(1-2):36-40.
[20]Han ET,Watanabe R,Sattabongkot J,et al.Detection of four Plasmodium species by genus-and species-specific loop-mediated isothermal amplification for clinical diagnosis[J].Journal of Clinical Microbiology,2007,45(8):2521-2528.
[21]Aonuma H,Suzuki M,Iseki H,et al.Rapid identification ofPlasmodium-carrying mosquitoes using loop-mediated isothermal amplification[J].Biochemical and Biophysical Research Communications,2008,376(4):671-676.
[22]El-Matbouli M,Soliman H.Development of a rapid assay for the diagnosis ofMyxoboluscerebralisin fish and oligochaetes using loop-mediated isothermal amplification[J].Journal of Fish Diseases,2005,28(9):549-557.
[23]El-Matbouli M,Soliman H.Rapid diagnosis ofTetracapsuloidesbryosalmonae,the causative agent of Proliferative kidney disease(PKD)in salmonid fish by a novel DNA amplificaiton method,loop-mediated isothermal amplification(LAMP)[J].Parasitology Research,2005,96(4):277-284.
[24]杨秋林,张如胜,伍和平,等.环介导等温扩增技术检测卡氏肺孢子虫的研究[J].中华微生物学和免疫学杂志,2008,28(6):565-567.
[25]金超,贾立军,曹世诺,等.牛新孢子虫病LAMP检测方法的建立[J].中国兽医科学,2009,39(12):1084-1088.
[26]卢潍媛,袁忠英,沈玉娟,等.环介导等温扩增技术检测蓝氏贾第鞭毛虫[J].国际医学寄生虫病杂志,2010,37(3):145-147.
[27]Xu J,Rong R,Zhang HQ,et al.Sensitive and rapid detection ofSchistosomajaponicumDNA by loop-mediated isothermal amplification(LAMP)[J].International Journal for Parasitology,2010,40(3):327-331.
[28]Cai XQ,Xu MJ,Wang YH,et al.Sensitive and rapid detection ofClonorchissinensisinfection in fish by loop-mediated isothermal amplification(LAMP)[J].Parasitology Research,2010,106(6):1379-1383.
[29]Nkouawa A,Sako Y,Nakao M,et a1.Loop-mediated isothermal amplification method for differentiation and rapid detection ofTaeniaspecies[J].Journal of Clinical Microbiology,2009,47(1):168-174.
[30]郑洋妹,陈信忠,龚艳清,等.简单异尖线虫环介导等温扩增(LAMP)鉴定方法的建立和应用[J].国际医学寄生虫病杂志,2010,37(3):141-144.
[31]Xiao L,Fayer R,Ryan U,et al.Cryptosporidiumtaxonomy:recent advances and implications for public health[J].Clinical Microbiology Reviews,2004,17(1):72-97.
R181.2
A
1002-2694(2011)10-0935-05
*河南省科技厅重点科技攻关项目(92102110138)资助
菅复春,Email:jfchun2008@yahoo.com.cn
河南农业大学牧医工程学院,郑州 450002
2011-03-16;
2011-06-02

