复方米诺地尔酊微生物限度检查方法学的验证
李辽闽 曾庆莉
(1 湖北省襄阳市妇幼保健院,湖北 襄阳 441000;2 湖北省黄石市食品药品监督检验所,湖北 黄石 435000)
复方米诺地尔酊为淡黄色至棕褐色的澄清液体。主要成分为生姜、辣椒、米诺地尔等。对斑秃、脂溢性脱发、病后脱发、老年性脱发均有效。因其具有较强的抑菌作用,采用常规实验方法难以除去其抑菌成分,我们采用薄膜过滤法[1],按中国药典2005年版二部相关规定[2]进行试验,结果表明,该方法省时、易操作,适用于复方米诺地尔酊微生物限度检查。
1 仪器、试药和菌种
1.1 生物安全柜、隔水式恒温培养箱(30~35℃)、生化培养箱(23~28℃)、电热干燥箱(160~250℃)、立式灭菌器、电子天平、薄膜过滤器、集菌仪、超净台。
1.2 营养琼脂、改良马丁氏液体培养基、改良马丁氏琼脂培养基、胆盐乳糖培养基、营养肉汤、甘露醇氯化钠琼脂培养基、溴化十六烷三甲胺琼脂培养基,均由北京陆桥技术有限公司生产。
1.3 稀释剂:氯化钠-蛋白胨缓冲液,由北京陆桥技术有限公司生产。
1.4 菌种:大肠埃希菌[CMCC(B)44102]、金黄色葡萄球菌[CMCC(B)26003]、铜绿假单胞菌[CMCC(B)10104]、枯草芽孢杆菌[CMCC(B)63501]、白色念珠菌[CMCC(F)98001]、黑曲霉[CMCC(F)98003]由中国药品生物制品检定所提供;所有菌种均为第四代。
1.5 样品:复方米诺地尔酊(批号:100305、100510、100916,100ml/瓶)襄阳市妇幼保健院制剂室。
2 方法与结果
2.1 细菌数、霉菌和酵母菌数测定方法验证试验
2.1.1 菌液的制备
接种大肠埃希菌、金黄色葡萄球菌、枯草芽孢杆菌的新鲜培养物至营养肉汤培养基中,35℃培养18~24h,各取1mL,分别加9mL的0.9%无菌氯化钠溶液,10倍稀释至10-5~10-7,活菌数约为50~100cfu/mL,做活菌计数备用。
接种白色念珠菌的新鲜培养物至改良马丁氏液体培养基中,25℃培养18~24h,取1mL,加9mL的0.9%无菌氯化钠溶液,10倍稀释至10-5~10-7,活菌数约为50~100cfu/mL,做活菌计数备用。
接种黑曲霉的新鲜培养物至改良马丁氏琼脂斜面培养基中,25℃培养一周,加5mL的0.9%无菌氯化钠溶液,洗下霉菌孢子,吸出菌液,用标准比浊管比浊。取1mL,加9mL的0.9%无菌氯化钠溶液,10倍稀释至10-4,活菌数约为50~100cfu/mL,做活菌计数备用。
2.1.2 供试液的制备
吸取样品10mL至有无菌玻璃珠的250mL三角烧瓶中,加90mL无菌的稀释液,混匀,使成1∶10的供试液。取上述供试液10mL(相当于样品1g),加入100mL无菌稀释液中,混匀,过滤,接着用400的稀释剂冲洗,消除抑菌成分后,取出滤膜,菌面朝上,贴于规定的琼脂平板上培养。
2.1.3 回收率测定
①试验组:分别取1∶10的供试液10mL(相当于样品1g),加入100mL无菌稀释液中,混匀,过滤,接着用400mL的稀释剂冲洗,预留100mL稀释剂各加入大肠埃希菌、金黄色葡萄球菌、枯草芽孢杆菌、白色念珠菌、黑曲霉菌各1mL(50~100cfu/mL),按薄膜过滤法过滤,取出滤膜,菌面朝上,贴于规定的琼脂平板上,置规定温度培养24~72h,逐日观察结果。②菌液组:除不加供试液外,其余操作同试验组。③供试品对照组:除不加菌悬液外,其余操作同试验组。④稀释剂对照组:用稀释剂取代供试液,其余操作同试验组。
2.1.4 结果
验证试验至少进行三次独立的平行试验,并分别计算各试验菌每次试验的回收率。(所得回收率均不低于70%)。
结论:采用薄膜过滤法检验复方米诺地尔酊,该试验对5种菌种的回收率均高于70%,该验证试验通过。结果见表1。

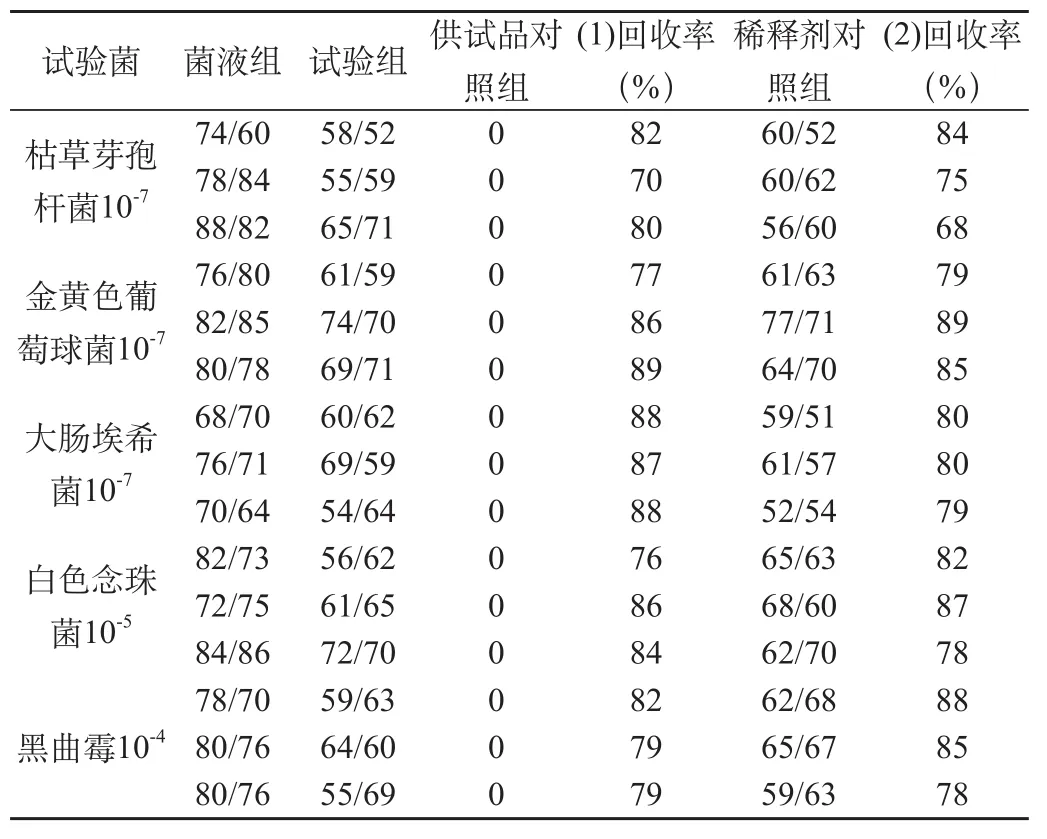
表1 菌落计数方法验证结果(cfu)
2.2 金黄色葡萄球菌检查方法验证试验
2.2.1 试验组
取1∶10的供试液10mL(相当于样品1g),加入100mL无菌稀释液中,混匀,过滤,接着用400mL的稀释剂冲洗,预留100mL稀释剂,加入金黄色葡萄球1mL(50~100cfu/mL),按薄膜过滤法过滤,取出滤膜,菌面朝上,贴于甘露醇氯化钠琼脂培养基中35℃培养24h。
2.2.2 阴性菌对照组
取1∶10的供试液10mL(相当于样品1g),加入100mL无菌稀释液中,混匀,过滤,接着用400mL的稀释剂冲洗,预留100mL稀释剂,加大肠埃希菌1mL(50~100cfu/mL),按薄膜过滤法过滤,取出滤膜,菌面朝上,贴于甘露醇氯化钠琼脂培养基中35℃培养24h。
2.2.3 阳性对照组
除不加供试液外,其余操作同试验组。
2.2.4 阴性对照组
用稀释液取代供试液,不加菌液,其余操作同试验组。
结果:阴性菌对照组未检出阴性对照菌;试验组检出金黄色葡萄球;阳性对照组检出金黄色葡萄球;阴性对照组无菌生长。结论:根据验证试验结果,表明供试品可采用薄膜过滤法检验金黄色葡萄球。
2.3 铜绿假单胞菌检查方法验证试验
2.3.1 试验组
取1∶10的供试液10mL(相当于样品1g),加入100mL无菌稀释液中,混匀,过滤,接着用400mL的稀释剂冲洗,预留100mL稀释剂,加铜绿假单胞菌1ml(50~100cfu/mL),按薄膜过滤法过滤,取出滤膜,菌面朝上,贴于溴化十六烷三甲胺琼脂培养基中35℃培养24h。
2.3.2 阴性菌对照组
取1∶10的供试液10mL(相当于样品1g),加入100mL无菌稀释液中,混匀,过滤,接着用400mL的稀释剂冲洗,预留100mL稀释剂,加大肠埃希菌1mL(50~100cfu/mL),按薄膜过滤法过滤,取出滤膜,菌面朝上,贴于溴化十六烷三甲胺琼脂培养基中35℃培养24h。
2.3.3 阳性对照组
除不加供试液外,其余操作同试验组。
2.3.4 阴性对照组
用稀释液取代供试液,不加菌液,其余操作同试验组。
结果:阴性菌对照组未检出阴性对照菌;试验组检出铜绿假单胞菌;阳性对照组检出铜绿假单胞菌;阴性对照组无菌生长。结论:根据验证试验结果,表明供试品可采用薄膜过滤法检验铜绿假单胞菌。
3 讨 论
经过试验观察,说明用薄膜过滤法处理过的供试液适合各种试验菌的生长;供试品对照组无菌生长说明供试品中无影响试验的杂菌;菌液组各种菌生长良好,说明该方法的实验环境适合参加试验的各种菌的生长;阴性对照组无菌生长,说明稀释剂、培养基及试验操作过程符合无菌操作的标准。试验结果表明,采用薄膜过滤法能有效去除复方米诺地尔酊的抑菌成分,对试验菌的生长无影响,该方法适合复方米诺地尔酊的微生物限度检查。
[1] 马绪荣,苏德模.药品微生物学检验手册[M].北京:科学出版社,2000:60.
[2] 国家药典委员会.中国药典.2005.二部[S].北京:化学工业出版社,2005:附录XI J.

