金银花抗流感病毒活性成分峰的化合物归属研究
宋 健, 张会敏, 郭承军, 石俊英*
(1.山东中医药大学,山东济南 250355;2.山东省中医药研究院,山东济南 250014)
近年来,流感病毒大规模流行给人类带来极大的恐慌,很大程度上影响了人类正常生活,迫切需要加大力度研究开发新型的抗流感药物。金银花具有明确的抗流感病毒作用[1-4]。课题组曾应用体内外代谢成分指纹图谱的方法找到了金银花抗流感病毒的主要效应指纹峰[5-7],本实验将对效应指纹峰利用制备型高效液相色谱仪,快速制得高纯度的单峰提取物,再应用 HPLC-MS-MS联用技术,得到各成分峰的一级质谱图及二级质谱图,经图谱解析,并参考有关的文献资料对色谱峰进行了成分归属研究,为进一步确证金银花抗流感病毒的有效成分组成奠定了实验基础。
1 实验材料与仪器
AGILENT 1100 LC高效液相色谱仪(Agilent公司,USA);Venusil XBP-Cl8(4.6 mm × 250 mm,5 μm)色谱柱;AGILENT 1100S(Agilent公司,USA,1361A PrePump VWD);pegasil ODS制备型色谱柱(20 mm ×150 mm,10 μm);AGILENT 1100 LC-MSDTrap-VL型高效液相色谱质谱联用仪(Agilent公司,USA),ZORBAX-RRHT C18(2.1 mm ×30 mm,1.8 μm)超高效色谱柱等。乙腈(色谱纯,TEDIA);甲醇(色谱纯,TEDIA),其他所用试剂为分析纯。金银花样品:产自山东平邑,经山东中医药大学石俊英教授鉴定为忍冬科植物忍冬Lonicera japonicaThunb.的干燥花蕾。
2 方法与结果
2.1 供试样品的制备 金银花的50%乙醇提取物[3]既含有极性化合物,又含有非极性化合物,所含成分复杂多样,用HPLC-DAD检测可得到分离度良好的指纹图谱,但应用同样的色谱条件进行HPLC-MSD联用分析,供试液中存在的大量无紫外吸收成分会构成强的背景吸收,对质谱结构解析形成干扰,因此需要对样品进行必要的除杂处理。我们利用制备型液相色谱仪制备了与金银花药材指纹图谱1号、2号、4号、7号、8号色谱峰相对应的高纯度提取物,作为液质联用分析的供试样品。
2.2 HPLC-MSD 联用分析
2.2.1 液相色谱-质谱联用系统条件 液相色谱条件 ZORBAX-RRHT C18(2.1 mm ×30 mm,1.8 μm)超高效色谱柱,0→4→6 min流动相梯度为乙腈-0.1%乙酸水溶液10∶90→90∶10→10∶90;体积流量0.4 mL/min;柱温30 ℃;进样量5 μL。质谱条件见表1。

表1 MS关键参数设置Tab.1 The key parameters of MS
2.2.2 质谱检测 分别精密吸取各样品溶液5 μL,注入HPLC-MS联用仪,依法测定各色谱峰相关质谱。将各样品峰UV扫描图、MS图、MS2图、相关数据进行汇总分析。
2.3 图谱解析与成分鉴定
2.3.1 1号峰的UV扫描曲线与绿原酸极为相似,-MS检出353[M-H]-,+MS 检出 355[M+H]+,表明此成分相对分子质量为354,与绿原酸一致。推断此成分应为单咖啡酰奎尼酸类。-MS2(353)显示是以m/z191.0为基峰,参照 Clifford等[4]对绿原酸类化合物MSn质谱裂解规律的研究结果,推断此化合物为5-咖啡酰奎尼酸(5-CQA),其主要离子峰的归属见表2。推断主要碎片离子裂解方式如图1。
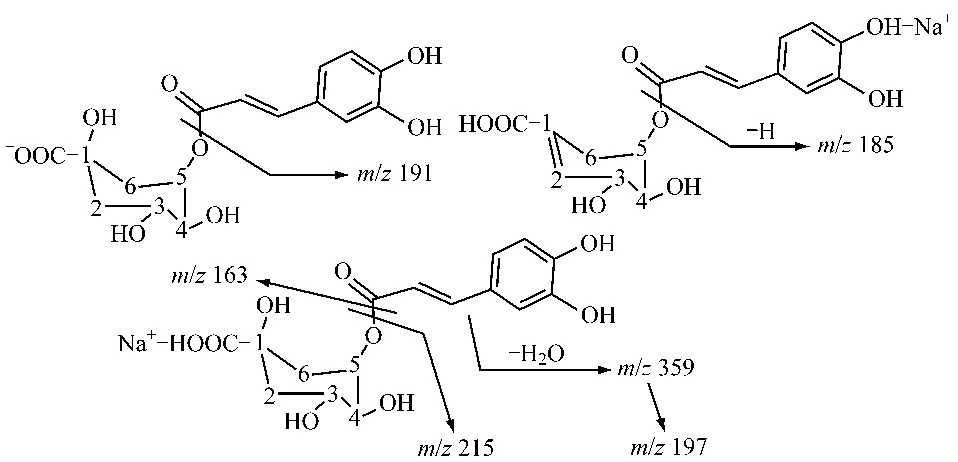
图1 5-CQA主要碎片离子裂解方式Fig.1 Major fragmentation ions of 5-CQA
2.3.2 2号峰UV扫描曲线与绿原酸及1号峰基本一致,-MS检出 353[M-H]-,+MS 检出 355[M+H]+,表明此成分为单咖啡酰奎尼酸类。-MS2(353)碎片离子显示 173、179、191、135 由高到低的分布。参照Clifford等[8]对绿原酸类化合物MSn质谱裂解规律的研究结果,推断此化合物为4-咖啡酰奎尼酸(4-CQA),其主要离子峰的归属见表2。推断主要碎片离子裂解方式如图2。
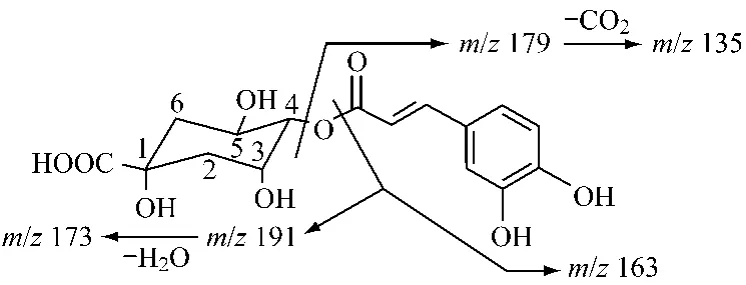
图2 4-CQA主要碎片离子裂解方式Fig.2 Major fragmentation ions of 4-CQA
2.3.3 4号峰本为绿原酸对照峰,但应用超高效色谱柱进行质谱分析时发现原来在普通HPLC的色谱柱上的1个色谱峰却分成了2个色谱峰。HPLC的DAD检测器检出的4号色谱峰5个时间点的UV扫描曲线也显示,此峰的峰纯度较低,除绿原酸UV吸收曲线外,尚显示另一差异较大的UV吸收曲线,曲线的形态显示本品有共轭双键存在,但200nm~250nm之间没有与苯环类似的精细结构存在,基本可排除存在苯环的可能。排除咖啡酰奎尼酸和黄酮类化合物,可能为环烯醚萜类。文献[9]已报道应用HPLC-ESI/MS2方法确定4种环烯醚苷类化合物,总结了环烯醚苷类化合物在ESI/MS2质谱中的裂解特点:①[M+Na]+峰丰度比[M+H]+要大,②优先从糖苷键处断裂,可见丰度较高[M+H-162]+或[M+Na-162]+碎片离子,③苷元易再次通过RDA 裂解产生碎片[M+H-162-70]+或[M+Na-162-70]+。此化合物的质谱基本符合上述特点,将金银花中已知的环烯醚萜苷类化合物与相关的文献[10]进行对照,根据化合物的相对分子质量(388),通过分析分子离子MS2裂解得到碎片离子,初步推定此成分应为环烯醚萜苷类化合物7-epi-vogeloside或vogeloside。其主要离子峰归属见表2。推断主要碎片离子裂解方式如图3。

图3 Vogeloside主要碎片离子裂解方式Fig.3 Major fragmentation ions of Vogeloside
2.3.4 7号峰的UV扫描曲线与绿原酸也很相似,-MS检出367[M-H]-,+MS 检出369[M+H]+,391[M+Na]+,表明此成分相对分子质量为368。其-MS2(367)检出高丰度的m/z161碎片离子[QMEH-CO2]-(QME 为奎尼酸甲酯缩写,下同),+MS2(369)检出高丰度的m/z163碎片离子[caffeoyl]+,推断此成分为咖啡酰奎尼酸甲酯,已报道的金银花单咖啡酰奎尼酸甲酯以3位、5位连接为主。文献报道[8]及本实验的研究表明3-CQA,5-CQA 的 ESI/-MS2裂解有一定的规律可循:5-CQA一般只检出191[quinic-H]-碎片离子,caffeoyloxy 有关的碎片离子如 179[caffeoyloxy]-,135[caffeoyloxy-CO2]-等极少,3-CQA 能检出丰度第二的 179[caffeoyloxy]-的碎片离子。这些规律表明5位连接的咖啡酸奎尼酸在ESI-源裂解过程中苷键的断裂优先发生在咖啡酸一侧,咖啡酰基以自由基的形式离去,不能检出。将这些特点与本成分的质谱图对照,-MS2(367)检出了一定丰度的 135[caffeoyloxy-CO2]-,+MS2(369)更是检出了最高丰度的163[caffeoyl]+。根据上述分析,推断此成分应为 3-O-咖啡酰奎尼酸甲酯(3-OCQME),其主要离子峰归属见表2。推断主要碎片离子的裂解方式如图4。
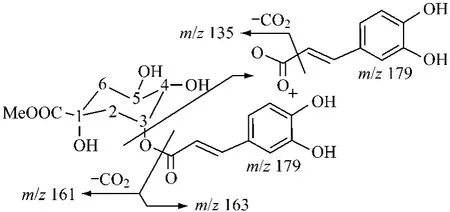
图4 3-O-CQME主要碎片离子的裂解方式Fig.4 Major fragmentation ions of 3-O-CQME
2.3.5 8号峰的UV扫描曲线显示与4号峰确证的化合物vogeloside极为相似。-MS基峰为403、807,+MS显示基峰为427,可推算其相对分子质量为404。+MS[M+Na]+丰度甚高,成为基准峰,与环烯醚萜苷类质谱特点一致。在已知的金银花所含的环烯醚萜苷类化合物中具有此相对分子质量只有secoxyloganin。分子离子的裂解碎片离子也充分的支持了这一点。因此,推断此峰为成分Secoxyloganin,其主要离子峰的归属见表2。推断主要碎片离子的裂解方式如图5。

表2 主要离子峰的归属Tab.2 The ownership of the major ions

图5 Secoxyloganin主要碎片离子的裂解方式Fig.5 Major fragmentation ions of Secoxyloganin
3 小结与讨论
3.1 通过上述HPLC-ESI/MS联用技术,对金银花指纹图谱中与抗流感病毒活性密切相关的几个色谱峰的成分归属进行了研究。结果表明本方法先进、简便,易于操作,较传统的通过分离纯化、1HNMR、13C-NMR、IR、X-ray、MS 等多重光谱数据分析进行结构鉴定大大节约了时间与物力。
3.2 通过对UV扫描曲线及ESI/MS及MS2检测得到的一级及二级质谱数据进行分析,并参考已有文献[11-13],对质谱进行了图谱解析,确定了 1 号、2号、4号、7号、8号色谱峰成分归属,质谱中各主要离子峰的来源、裂解方式均得到了科学合理的解释,因此认为各色谱峰的成分归属结果是准确可靠的。图谱解析结果表明:1号峰为5-咖啡酰奎尼酸、2号峰为4-咖啡酰奎尼酸、7号峰为3-咖啡酰奎尼酸甲酯、8号峰为Secoxyloganin应为环烯醚萜苷类化合物 vogeloside 或其构象异构体7-epi-vogeloside(有可能是其中的1个成分,也可能是2个成分的混合物,空间构型的鉴定,还有待进一步NMR的数据支持,为叙述方便统称为vogeloside),加上已知的绿原酸、咖啡酸,通过本研究,金银花指纹图谱中与抗流感病毒活性有关的效应指纹峰,其成分归属均得到了确认。
3.3 综上所述,金银花药材中,与抗流感病毒密切相关的几个主要成分已确认,除已知的绿原酸、咖啡酸外,还有绿原酸的同分异构体4-咖啡酰奎尼酸、5-咖啡酰奎尼酸,及3-咖啡酰奎尼酸甲酯、Secoxyloganin、Vogeloside。涉及到4个咖啡酰奎尼酸类化合物、2个环烯醚萜苷类化合物及咖啡酸。这些成分结构的确认,为金银花抗病毒物质基础的阐明提供了坚实的实验基础,为下一步进行成分药理试验提供了实验依据与数据支持。
[1]潘曌曌,王雪峰,闫丽娟,等.金银花提取物体处抗甲型流感病毒FM1株的研究[J].中国中医药信息杂志,2007,14(6):37-39.
[2]何显忠,兰荣德.金银花的药理作用与临床应用[J].时珍国医国药,2004,14(12):865-867.
[3]胡克杰,王跃红,王 栋.金银花中氯原酸在体外抗病毒作用的实验研究[J].中医药信息,2010,27(3)27-28.
[4]胡克杰,孙考祥,王瑗璐,等.绿原酸体外抗病毒作用研究[J].哈尔滨医科大学学报,2001,35(6):430-432.
[5]郭承军,石俊英.金银花抗小鼠流感作用的谱效关系研究[J].中药药理与临床,2009,25(4):50-52.
[6]石俊英,郭承军.金银花体外抗流感病毒有效部位研究[J].山东中医药大学学报,2010,34(2):178-180.
[7]郭承军,石俊英.金银花小鼠血清移行成分指纹图谱研究[J].时珍国医国药,2009,20(12):2968-2970.
[8]Clifford M N,Johnston K L,Knight S,et al.Hierarchical scheme for LC-MSnidentification of chlorogenic acids[J].J Agric Food Chem,2003,51(10):2900-2911.
[9]Suryawanshi S,Mehrotra N,Asthana RK,et al.Liquid chromatography/tandem mass spectrometric study and analysis of xanthone and secoiridoid glycoside composition of Swertia chirata,a potent antidiabetic[J].Rapid Commun Mass Spectrom,2006,20(24):3761-3768.
[10]Li Xiaoqin,Sun Xiaohong,Cai Shuang,et al.Investigation on the chemical constituents and variation of the flower buds of Lonicera species by UPLC-ESI-MS/MS and principle component analysis[J].Acta Pharm Sin,2009,44(8):895-904.
[11]陈秋竹,林瑞超,王钢力,等.金银花提取物化学成分研究[J].中药材,2010,33(6):920-922.
[12]张培芬,李 冲.白花泡桐花黄酮类化学成分研究[J].中国中药杂志,2008,33(22):2629-2632.
[13]孙燕荣,董俊兴,吴曙光.杜仲化学成分研究[J].中药材,2004,27(5):341-343.

