MK-801建立谷氨酸功能低下精神分裂症大鼠模型的研究☆
于文娟朱浩卢卫红金志兴朱丽萍
·论 著·
MK-801建立谷氨酸功能低下精神分裂症大鼠模型的研究☆
于文娟*朱浩△卢卫红*金志兴*朱丽萍*
目的 用N-甲基-D-天门冬氨酸(NMDA)非竞争性受体拮抗剂地卓西平马来酸盐(MK801)建立具有类精神分裂症症状的大鼠模型。方法 24只SD大鼠随机分为MK801组、生理盐水组和正常对照组,每组各8只。MK801组的大鼠每天腹膜腔内注射0.5 mg/kg(给药体积为10 mL/kg)MK801共6 d以建立精神分裂症模型,生理盐水组给予等体积生理盐水。用自发活动、强迫游泳试验、逃避性抑制(inhibitory avoidance,IA)试验以及海马神经生长因子表达评价该模型。结果 MK801组、生理盐水组和对照组的大鼠10min自发活动总路程分别为(3127±381)cm、(935±196)cm、(1060±243)cm,游泳不动时间分别为(147±18)s、(58± 10)s、(52±10)s。3组的自发活动和游泳不动时间差异均有统计学意义 (F=149.7,P<0.01;F=122.6,P<0.01),MK801组的自发活动较另两个组均增加(P<0.01),而游泳不动时间延长(P<0.01)。3组的24 h IA的记忆潜伏期也有明显差异(F=5.2,P<0.05),MK801组的记忆潜伏期[(26±10)s]较生理盐水组[(47±16)s]和对照组[(46±14)s]均缩短(P<0.05)。而且,MK801组海马神经生长因子表达明显下调。结论 连续给予高剂量MK801诱导的大鼠谷氨酸功能低下模型不仅具有类精神分裂症症状,而且还存在神经生物学改变,可作为模拟精神分裂症的模型。
MK801 精神分裂症 大鼠模型 神经生长因子
精神分裂症(schizophrenia)是一类常见的精神疾病,发病机理至今仍不清楚,因此建立合适的动物模型对研究该病具有重要意义。用N-甲基-D-天门冬氨酸(NMDA)非竞争性受体拮抗剂地卓西平马来酸盐(MK801)诱导精神分裂症模型已被广泛使用,但在建立大鼠模型时所使用的剂量以及给药持续的时间都不一致,并且评价指标单一。国内多数研究者在建立该疾病大鼠模型时,使用的剂量参照吴金华等[1]或苏允爱等[2]研究的剂量,但他们的研究对象是小鼠,而且没有检测认知功能以及生化因子变化。近来,研究发现腹膜腔内连续6 d注射高剂量MK-801(0.5 mg/kg)的大鼠扣带等脑区谷氨酸和谷氨酰胺浓度明显升高[3],这与首发精神分裂症患者脑区代谢变化相似[4]。重复注射MK-801可能诱导与精神分裂症患者更相似的脑生化改变,可能获得更好的模拟精神分裂症患者的模型。故本研究以连续给予高剂量MK801建立精神分裂症大鼠模型,并从行为学以及生化因子表达等方面评价此模型。
1 材料与方法
1.1 研究对象 清洁级成年雄性Spragus-Dawley大鼠24只,体质量200~250 g,由上海交通大学医学院动物实验科学部提供。动物生产和使用许可证号码分别为SCXK(沪)2004-0001和SYXK(沪)2003-0026。大鼠随机分为3组,即MK801组、生理盐水组(NS组)和正常对照组,每组8只。实验前在动物房饲养至少3 d,维持室温(23±1)℃,采用12 h昼夜节律(8:00~20:00)。所有实验都在9:00~17:00之间完成。整个实验过程中饮水及进食均自由。
1.2 药物及处理 地卓西平马来酸盐(dizocilpine,(+)-MK-801;美国Sigma公司),溶于生理盐水,配置成5 mg/mL的储备液。MK801组以0.5 mg/kg(给药体积为10 mL/kg)MK801腹膜腔内注射,每天1次,连续6 d;而生理盐水组以同样的方式给予等体积生理盐水;正常对照组为未经处理的正常大鼠。
1.3 行为学检测 末次给药30 min后,先行各组大鼠的自发活动检测,随后行逃避性抑制试验(inhibitory avoidance,IA),最后进行强迫游泳实验。
1.3.1 自发活动 大鼠的自发活动采用Smart-128小动物行为分析系统(西班牙Panlab公司)。各组大鼠于末次给药30 min后,将单只大鼠放入顶部内置有摄像头的观察箱(42 cm×42 cm×30 cm),对大鼠活动进行视频跟踪,自动记录大鼠活动轨迹,计算活动路程。自发活动评价的指标是:大鼠一定时间段内(如10 min)的活动总路程,即总路程变长显示自发活动增加。
1.3.2 逃避性抑制试验 给药第5 d,将大鼠背朝隔离门置入IA训练仪的明室中,当大鼠面向升降门时,把门升起,暴露暗室。当大鼠四足全部迈进暗室时即将升降门关闭,给予大鼠足部单次电击(0.4 mA,2 s),随后将大鼠取出。24 h后,检测大鼠IA记忆:将大鼠再次置入IA训练仪的明室中,记录大鼠进入暗室前在明室内停留的时间 (潜伏期)。潜伏期越长代表大鼠记忆越好。潜伏期上限为600 s,超过亦记作600 s。
1.3.3 强迫游泳试验 各组大鼠于末次给药后,单只放入水温(23±1)℃、水深30 cm、高40 cm、直径25 cm的玻璃容器中,记录大鼠5 min内累计不动的时间。不动指标为动物仅露出鼻孔保持呼吸,四肢偶尔划动以保持身体悬浮,或下沉接触水池底部超过1 s时间。每只大鼠游泳前更换温水。
1.4 神经生长因子检测 行为学测试结束后,大鼠断头取双侧海马,用RIPA(Sigma公司)裂解液提取蛋白,经BCA (Pierce公司)蛋白定量后行western blotting检测神经生长因子 (nerve growth factor,NGF)。蛋白变性后,经加样、电泳、湿转、封闭,再用 anti-NGF一抗(Santa cruz公司,1∶400)4℃孵育过夜。而后加入二抗室温孵育,ECL(Pierce公司)曝光显影。
1.5 统计学分析 采用SPSS 16.0进行分析,实验数据以均数±标准差表示。三组比较采用方差分析(ANOVA)检验,两两多重比较采用LSD。检验水准α=0.05,双侧检验。
2 结果
2.1 MK801诱导大鼠自发活动增加 末次给药30 min后,MK801组、NS组和对照组的10 min内自发活动总路程的差异有统计学意义(F=149.7,P<0.01),前者明显高于后两组(P<0.01),但NS组与对照组无差异(P﹥0.05)。见图1。
2.2 MK801降低大鼠IA的潜伏期 IA试验中,MK801组、NS组和对照组大鼠24 h记忆保持的时间(潜伏期)的差异有统计学意义(F=5.2,P<0.05),前者明显低于后两组(P<0.01),但 NS组与对照组无差异(P﹥0.05)。见图2。
2.3 MK801延长大鼠强迫游泳静止的时间
MK801组、NS组和对照组大鼠强迫游泳5 min内总不动时间的差异有统计学意义(F=122.6,P<0.01),前者明显高于后两组(P<0.05),但NS组与对照组无差异(P﹥0.05)。见图3。
2.4 MK801下调大鼠海马NGF表达 Western blotting检测显示,MK801组大鼠海马NGF表达明显下调,而NS组NGF表达无明显变化。见图4。
3 讨论
谷氨酸功能低下已经被认为在精神分裂症发病机制中具有重要作用。NMDA受体拮抗剂可使正常人产生类精神分裂症的症状,并能加剧精神分裂症患者原有症状[5]。与多巴胺能激动剂只能产生阳性症状相比,NMDA受体拮抗剂能诱导出现整个精神分裂症疾病谱,包括阴性症状以及认知缺陷[6]。单次高剂量或连续低剂量MK801(0.1 mg/kg,6 d)主要诱导大鼠脑部颞叶谷氨酸盐及谷氨酰胺浓度增加[7-9],而精神分裂症患者却是扣带、额前皮质、海马等脑区谷氨酸和谷氨酰胺浓度明显升高[4],表明单次高剂量或连续低剂量建立的模型不能很好地模拟精神分裂症。近来研究发现连续高剂量MK801诱导的大鼠脑区代谢变化与精神分裂症患者的一致[3],但连续给予高剂量MK801诱导的模型具有的症状却未评价。
本研究中通过自发活动、强迫游泳试验、IA试验等多种行为学方法评价高剂量MK801诱导的精神分裂症模型大鼠。自发活动试验是观察自然状态下实验动物的活动情况,NMDA受体拮抗剂诱导啮齿类动物活动增多被作为精神分裂症阳性症状[10];NMDA受体拮抗剂诱导动物强迫游泳不动时间延长可作为精神分裂症阴性症状的行为模型,强迫游泳不动时间延长可反映精神分裂症阴性症状[11]。IA试验是利用大鼠趋暗喜黑的天性,检测大鼠相关记忆的一种方法,24 h潜伏期缩短表明实验动物记忆保持下降。本研究结果显示,与生理盐水组和空白对照组比较,连续腹腔内注射高剂量MK801可显著增加模型组大鼠自发活动,延长强迫游泳不动时间,缩短24 h记忆保持的时间,表明该模型的大鼠行为紊乱、记忆力下降等,可很好地模拟精神分裂症患者的阳性、阴性症状以及认知障碍。
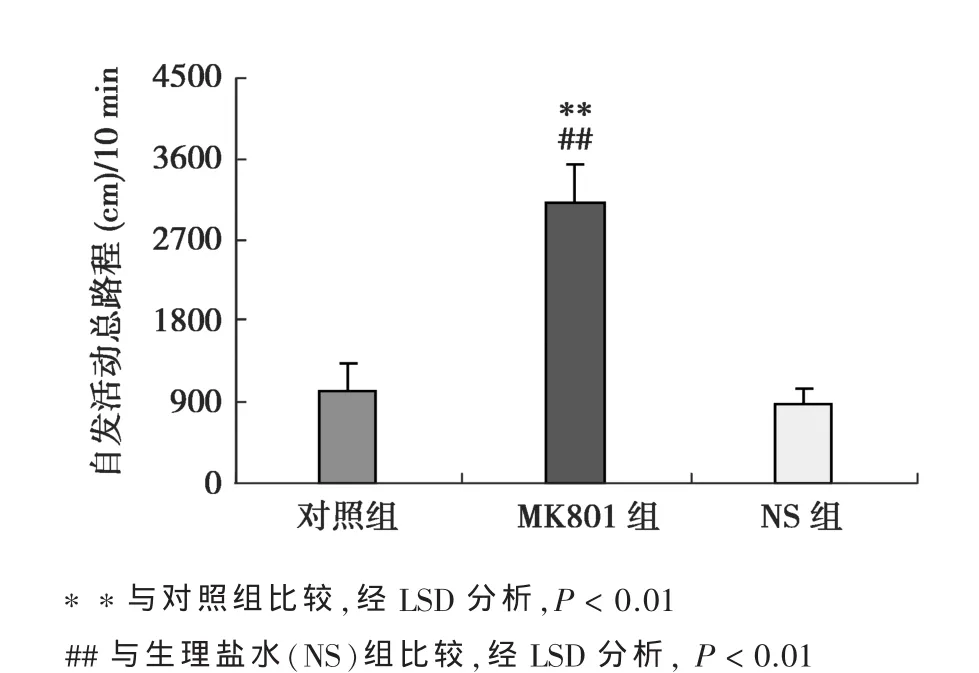
图1 各组大鼠自发活动10 min总路程的比较

图2 各组大鼠24 h记忆潜伏期的比较
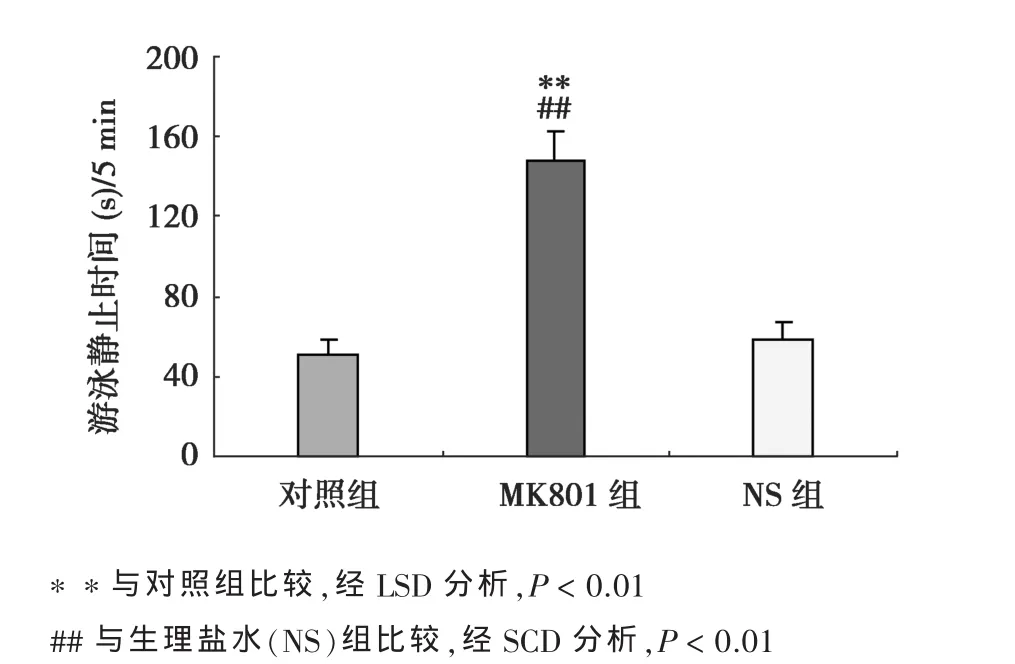
图3 各组大鼠强迫游泳试验中不动时间的比较
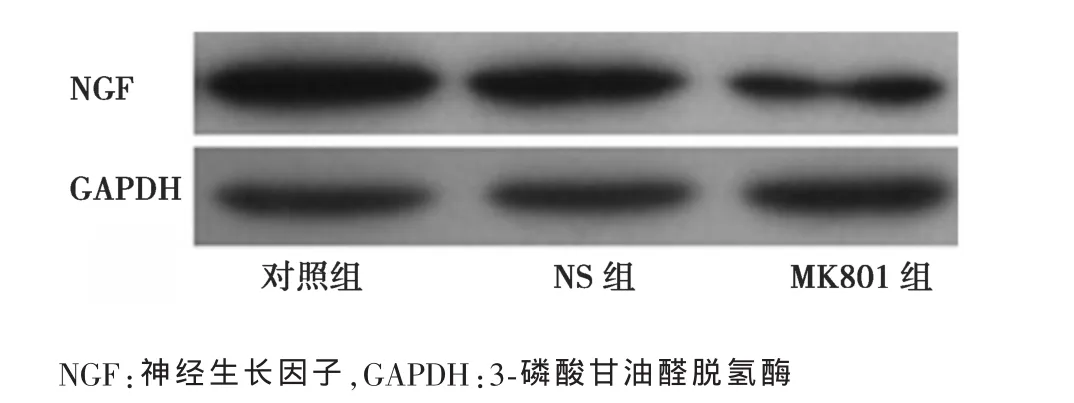
图4 Western botting检测大鼠海马NGF表达
有研究表明NMDA受体拮抗剂可致强迫游泳不动时间缩短[12],而本研究连续高剂量MK801可延长强迫游泳不动时间,表明模型大鼠模拟了精神分裂症的阴性症状。此不一致的结果可能是由于以下两种原因:给药剂量和给药时间。MK-801缩短强迫游泳不动时间具有明显的剂量关系,高剂量时才可导致不动时间缩短[12-13]。而在此剂量范围,MK-801又能诱导自主活动能力增加[13],所以不排除药物缩短强迫游泳不动时间是自主活动能力增加导致的,可能是假阳性结果。另外,以上研究都是单次给药,而本实验是连续6 d给药。另一个NMDA受体拮抗剂-PCP诱导强迫游泳不动时间延长也有时间条件:连续给药两周可增加强迫游泳不动时间,而单次或连续5 d给药却没有导致强迫游泳不动时间延长[11]。
NGF是维持神经元细胞存活、生长、发育和分化的必需营养因子。精神分裂症患者不仅血清中NGF水平改变,脑组织、脑脊液中NGF水平也发生变化。研究显示,首发未服药的精神分裂症患者血清NGF水平显著低于正常人群,而且血清NGF水平与患者阴性症状有关,而典型或非典型抗精神病药物都能使NGF血清水平升高[14]。Parikh等[14]检测精神分裂症模型大鼠血清和脑NGF水平变化也获得与人一致的结果。以上研究表明NGF与精神分裂症发病机理以及药物治疗有关。本研究显示连续给予高剂量MK801可导致大鼠海马中NGF水平明显下降,说明连续给予高剂量MK801可诱导相似于精神分裂症患者生化因子变化,同时也进一步支持该模型可更好模拟精神分裂症。
[1] 吴金华,邹洪,于军,等.用不同实验小鼠品系建立精神分裂症的动物模型[J].生理学报,2003,55(4):381-387.
[2] 苏允爱,司天梅,周东丰,等.MK-801建立谷氨酸功能低下精神分裂症小鼠模型的研究[J].中国神经精神疾病杂志,2006,32(6):558-560.
[3]Kondziella D,Brenner E,Eyjolfsson EM,et al.Glial-neuronal interactions are impaired in the schizophrenia model of repeated MK801 exposure[J].Neuropsychopharmacology,2006,31(9):1880-1887.
[4]van Elst LT,Valerius G,Büchert M,et al.Increased prefrontal and hippocampal glutamate concentration in schizophrenia: evidence from a magnetic resonance spectroscopy study[J].Biol Psychiatry,2005,58(9):724-730.
[5]Manahan-Vaughan D,von Haebler D,Winter C,et al.A single application of MK801 causes symptoms of acute psychosis,deficits in spatial memory,and impairment of synaptic plasticity in rats[J].Hippocampus,2008,18(2):125-134.
[6]Carlsson A,Waters N,Holm-Waters S,et al.Interactions between monoamines,glutamate,and GABA in Schizophrenia:new evidence[J].Annu Rev Pharmacol Toxicol,2001,41:237-260.
[7]Brenner E,Kondziella D,Haberg A,et al.Impaired glutamine metabolism in NMDA receptor hypofunction induced by MK801[J].J Neurochem,2005,94(6):1594-1603.
[8]Eyjolfsson EM,Brenner E,Kondziella D,et al.Repeated injection of MK801:an animal model of schizophrenia?[J].Neurochem Int,2006,48(6-7):541-546.
[9] 李文强,郭伟云,张红星,等.谷氨酸能低下精神分裂症模型大鼠不同脑区核因子κB表达分析[J].中国神经精神疾病杂志,2009,35(11):646-649.
[10]Gainetdinov RR,Mohn AR,Caron MG.Genetic animal models:focus on schizophrenia[J].Trends Neurosci,2001,24(9):527-533.
[11]Mouri A, Noda Y, Enomoto T, et al.Phencyclidine animal models of schizophrenia:approaches from abnormality of glutamatergic neurotransmission and neurodevelopment[J].Neurochem Int,2007,51(2-4):173-184.
[12]Molina-Hernández M, Téllez-Alcántara NP, Pérez-García J,et al.Desipramine or glutamate antagonists synergized the antidepressant-like actions of intra-nucleus accumbens infusions of minocycline in male Wistar rats[J].Prog Neuropsychopharmacol Biol Psychiatry,2008,32(7):1660-1666.
[13]Ghasemi M,Raza M,Dehpour AR.NMDA receptor antagonists augment antidepressant-like effects of lithium in the mouse forced swimming test[J].J Psychopharmacol,2010,24(4):585-594.
[14]Parikh V,Evans DR,Khan MM,et al.Nerve growth factor in never-medicated first-episode psychotic and medicated chronic schizophrenic patients: possible implications for treatment outcome[J].Schizophr Res,2003,60(2-3):117-123.
Establishment of a MK801-induced glutamate dysfunction model of schizophrenia in rats.
YU Wenjuan,ZHU Hao, LU Weihong, JIN Zhixing, ZHU Liping.Shanghai Mental Health Centre, Shanghai Jiaotong University School of Medicine,No.600 South Wanping Road,Shanghai 200025,China.Tel:021-64901737.
Objective To establish a rat glutamate dysfunction model of schizophrenia using MK801,a noncompetitive antagonist for the NMDA-type of glutamate receptors.Methods Twenty-four SD rats were randomly divided into three groups:MK801,vehicle(normal saline)and control groups.Rats in MK801 group were administrated intraperitoneally with MK801 (0.5 mg/kg, 10 mL/kg body weight) while rats in vehicle group were administered intraperitoneally with an equal volume of saline normal saline every day for 6 consecutive days.The behaviors were evaluated by locomotor activity,forced swimming test,inhibitory avoidance(IA)training and the expression of nerve growth factor(NGF) was detected in rat hippocampus.Results The locomotion in MK801 group was significantly increased[(3127±381)cm]compared with vehicle group[(935±196)cm]and control group[(1060±243)cm](F=149.7,P<0.01).In addition,the immobility time of swimming in MK801 group was also significantly increased[(147±18)s]compared with vehicle group[(58±10)s]and control group[(52±10)s](F=122.6,P<0.01).However,24-h IA memory retention latency in MK801 group[(26±10)s]was significantly decreased compared with vehicle group[(47 ±16)s]and control group[(46±14)s](F=5.2,P<0.05).The level of NGF was downregulated in MK801 group.Conclusion Repeated high dose MK801-induced glutamate dysfunction model not only mimics symptoms of schizophrenia but also induces neurobiological changes,which may serve as a model of schizophrenia.
MK801 Schizophrenia Rat modelNerve growth factor
R749.3
A
2011-05-06)
(责任编辑:曹莉萍)
☆ 上海市精神卫生中心基金(编号:09-YJ-08),上海市科学技术委员会中药现代化专项(编号:10DZ1973300)
* 上海交通大学医学院附属精神卫生中心(上海 200030)
(Email:zhulipingjsk@yahoo.com.cn)
△ 上海交通大学医学院解剖学教研室

