注射用地塞米松磷酸钠中细菌内毒素的检测
郑剑峰 王育红
沈阳绿洲制药有限责任公司(沈阳 110300) 辽宁广播电视大学(沈阳 110034)
注射用地塞米松磷酸钠中细菌内毒素的检测
郑剑峰 王育红
沈阳绿洲制药有限责任公司(沈阳 110300) 辽宁广播电视大学(沈阳 110034)
建立注射用地塞米松磷酸钠的细菌内毒素检查方法。使用两个厂家的鲎试剂和自制的3批注射用地塞米松磷酸钠样品进行干扰试验。注射用地塞米松磷酸钠浓度稀释至0.3125 mg/mL时无干扰。注射用地塞米松磷酸钠可按内毒素限值6 Eu/mg进行细菌内毒素检查。
注射用地塞米松磷酸 鲎试剂 细菌内毒素
地塞米松磷酸钠为肾上腺皮质激素类药,主要用于过敏性与自身免疫性炎症性疾病。本研究参照中国药典2005年二部有关要求及应用指导原则,进行了地塞米松磷酸钠冻干粉针细菌内毒素检查法的可行性研究。
1 仪器和试药
内毒素工作标准品(中国药品生物制品检定所,规格:180 EU/支,批号:2004-5)。鲎试剂:福州新北生化工业有限公司(标示灵敏度:0.25 EU/mL,规格:0.1mL/支,批号:04101411);湛江安度斯生物有限公司(标示灵敏度:0.25 EU/mL,规格:0.1 mL/支,批号:0411121)。细菌内毒素检查用水:湛江安度斯生物有限公司(规格:5 mL/支,批号:0409230)。注射用地塞米松磷酸钠(自制,规格:2 mg/支,批号:20080501、20080502、20080503)。
2 方法与结果
2.1 灵敏度复核
鲎试剂按中国药典2005年规定方法进行灵敏度复核试验,结果均符合规定。
2.2 细菌内毒素限值(L)的确定
USP28版、中国药典2005年版只收载地塞米松磷酸钠注射液标准,未见本品的收载。美国USP28版规定的地塞米松磷酸钠注射液限度为:31.3 EU/mg。地塞米松磷酸钠注射液说明书表明,临床最大可静脉推注50 mg。根据L=K/M,其中K=5 EU(Kg·h)-1,计算限度为:L=6 EU/mg,参照临床最大剂量规定本品的限度为6 EU/mg。
2.3 有效稀释浓度(MVD)的计算
公式MVD(λ=0.25)=λ/L,其中L为地塞米松磷酸钠细菌内毒素限值6 EU/mg,λ为鲎试剂标示灵敏度。取样品配成2.5 mg/mL,则MVD=6×2.5÷0.25 =60倍(即0.04 mg/mL)。
2.4 供试品干扰预试验
取供试品,加细菌内毒素检查用水,配成2.5 mg/mL,作为供试品贮备液;再用细菌内毒素检查用水稀释成系列浓度的供试样品,参照细菌内毒素检查法进行干扰预试验,结果表明本品2.5mg/mL液的1:8稀释液无干扰。结果见表1。
2.5 干扰确证试验
根据预试验结果,对以上两批鲎试剂,取供试品贮备液(2.5 mg/mL)稀释8倍(0.3125 mg/mL)进行干扰确证试验。结果表明,本品对两批鲎试剂均无干扰,0.5λs<λt<2.0λs,符合中国药典2005年版对细菌内毒素检查有效性的规定,进行细菌内毒素检查。见表2和表3。
2.6 样品细菌内毒素检查
按中国药典2005年版细菌内毒素检查法,使用两批不同厂家的鲎试剂分别对样品进行细菌内毒素检查,同时设样品阳性对照管,结果3批样品均呈阴性。结果见表4和表5。

表1 注射用地塞米松磷酸钠干扰预试验结果

表2 干扰确证试验结果(鲎试剂批号:04101411)

表3 干扰确证试验结果(鲎试剂批号:0411121)
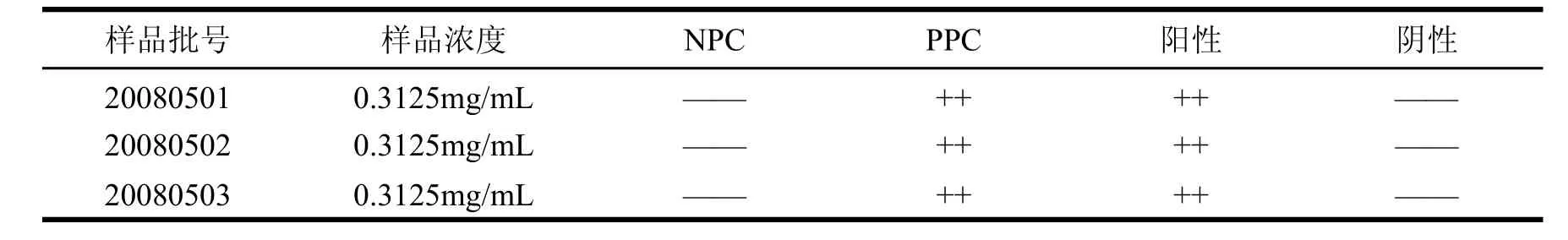
表4 细菌内毒素检查结果(鲎试剂批号:04101411)
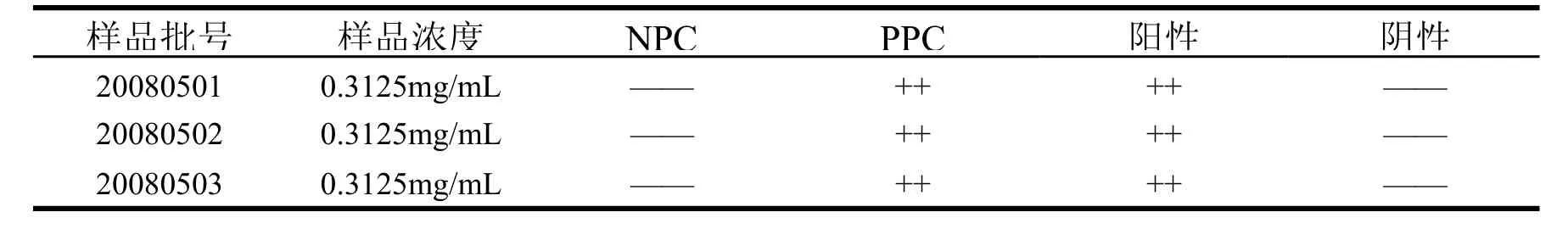
表5 细菌内毒素检查结果(鲎试剂批号:0411121)
3 结论
由干扰预试验结果可初步判断,当样品稀释至0.3125 mg/mL时与鲎试剂无干扰,且两个厂家的鲎试剂反应结果相当。正式干扰试验用0.3125 mg/mL样品浓度,且两个厂家的鲎试剂反应结果均为0.5 λs<λt<2.0 λs,确证无干扰影响,细菌内毒素限值定为6 Eu/mg。注射用地塞米松磷酸钠可适用细菌内毒素检查法,但供试品浓度应在0.3125 mg/mL或以下,鲎试剂灵敏度在0.5 Eu/mL以上均可。
[1]国家食品药品监督管理局.地塞米松磷酸钠注射液说明书.国家药品标准化学药说明书内容汇编第一册.
[2]国家药典委员会.地塞米松磷酸钠质量标准.中华人民共和国药典二部(2005).北京:化学工业出版社,2005.
[3]国家药典委员会.细菌内毒素检查法.中华人民共和国药典二部(2005).北京:化学工业出版社,2005.
齐婷婷)

