310.15 K时蛋白质模型化合物与二元醇在水溶液中的异系焓相互作用
朱 焰 庞现红 于 丽
(1泰山医学院化学与化学工程学院,山东泰安 271016;2山东大学胶体与界面化学教育部重点实验室,济南 250100)
310.15 K时蛋白质模型化合物与二元醇在水溶液中的异系焓相互作用
朱 焰1,*庞现红1于 丽2
(1泰山医学院化学与化学工程学院,山东泰安 271016;2山东大学胶体与界面化学教育部重点实验室,济南 250100)
利用2277热活性检测仪的流动量热系统测量蛋白质模型化合物(甘氨酸、丙基酸、N,N-二甲基甲酰胺(DMF)和N,N-二甲基乙酰胺(DMA))与二元醇(1,3-丁二醇和2,3-丁二醇)的混合过程焓变以及各自的稀释焓;依据McMillan-Mayer理论对实验数据进行分析,获得310.15 K时水溶液中蛋白质模型化合物与二元醇异构体分子的异系焓相互作用系数(hxy,hxxy,hxyy).结果表明,hxy值均为正值,此过程吸热效应占主导作用,并且hxy(DMA)> hxy(丙氨酸)>hxy(甘氨酸)>hxy(DMF)和hxy(2,3-丁二醇)>hxy(1,3-丁二醇).根据结果讨论了溶质-溶质相互作用和溶质-溶剂相互作用情况,阐明了二元醇官能团相对位置的变化对hxy值的影响,发现DMF或DMA与二元醇之间有较强的氢键作用,由于DMF分子共振结构有较好的可极化性,DMF与二元醇的氢键作用被进一步加强.
氨基酸;N,N-二甲基甲酰胺;N,N-二甲基乙酰胺;二元醇;溶质-溶质相互作用
二元醇是一类特殊的有机化合物,它可以增强球状蛋白的热稳定性,也可以通过其它方式来降低变性程度,虽然在生物有机体细胞和细胞外都未被发现,但它们在药品和化妆品行业中已有广泛的应用.当它们被作为一种医药品和化妆品的媒介被引入生物体中时,它们就影响了细胞中物质的成分,其作用已经在二元醇和生物细胞的大量研究中被证实[1-4],所以,探索二元醇与蛋白质在水溶液中的作用本质是非常有意义的.由于蛋白质的结构非常复杂,很难直接以蛋白质为研究对象来研究它在水溶液中与二元醇作用的本质.因此,必须从研究简单的蛋白质模型化合物入手来探索二元醇对蛋白质结构的影响.氨基酸是重要的生物活性物质,是组成蛋白质的基本结构单位.N,N-二甲基甲酰胺(DMF)和N,N-二甲基乙酰胺(DMA)是用途极广的化工原料,由于DMF和DMA似肽结构和—CH3的存在常被认为是模拟多肽和蛋白质分子内部环境的模型化合物[5-8].所以,以氨基酸、肽、酰胺及其衍生物作为蛋白质模型分子来探讨复杂溶液中两性离子与共溶剂及共溶质的相互作用的溶液热力学是很有意义的[9-15].
为深入了解蛋白质和多肽链在复杂溶液中的物理化学现象,在我们的前期工作[16-18]中,主要偏重于研究298.15 K时蛋白质模型化合物在水溶液及混合水溶液(乙二醇、丙三醇、丙二醇等)中的热力学性质,其它温度的相关研究少见报道.为了进一步完善蛋白质模型分子体系溶液热力学性质的研究,本文在前期研究的基础上进一步选取新的研究体系和温度,测量蛋白质模型化合物(甘氨酸、丙氨酸(全文均为L-丙氨酸)、DMF和DMA)与二元醇(1,3-丁二醇和2,3-丁二醇)在水溶液中的混合焓和稀释焓,并根据McMillan-Mayer理论[20]计算出水溶液中蛋白质模型化合物与二元醇相互作用的各级异系焓相互作用系数,来探讨溶质-溶质分子间相互作用的机制.由于310.15 K接近人体的平常温度,对该温度下的蛋白质模型化合物热力学性质的探索,可以为生物化学和医药化学的研究提供更多的信息.
1 实验部分
1.1 试剂与仪器
氨基酸(生化级,中国医药(集团)上海化学试剂公司(进口分装))置于真空硅胶干燥箱内48 h后使用.DMF、DMA、1,3-丁二醇和2,3-丁二醇(分析纯,中国医药(集团)上海化学试剂公司)经减压精馏精制后使用.2277精密热活性检测仪(瑞典AB公司,测量精度(300 μW量程)为±0.2%,恒温精度为±0.0002 K),LKB-2132微蠕动泵,Mettler AE 200型电子天平(误差为±0.0001 g).水为新制备的二次重蒸水.
1.2 实验方法
混合过程的焓变、稀释焓用2277精密热活性检测仪的流动混合系统测定.实验温度为310.15 K.不同质量摩尔浓度的溶液用称量法配制,所配溶液均在12 h内使用.当量热计恒温水浴和检测系统达到热平衡后,用溶剂水设定基线并进行电标定.设备具体使用和测量方法已在前期工作[16-18]中详细阐述.
1.3 数据处理
根据McMillan-Mayer理论[19],利用测量得到的混合焓和稀释焓计算出各级异系焓相互作用系数.在恒定温度和压强下,含两种不同溶质x和y的三元水溶液过量焓HE(mx,my)可以表示为质量摩尔浓度的维里展开形式[20]:
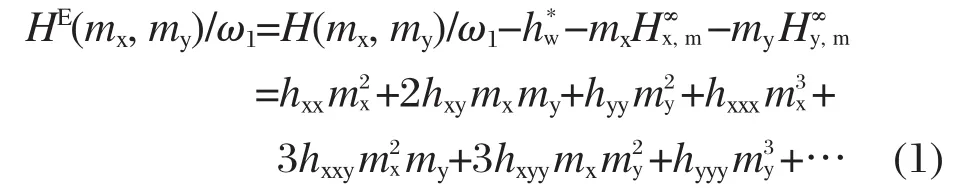
式中HE(mx,my)/ω1表示由质量摩尔浓度为mx的溶质x,质量摩尔浓度为my的溶质y所组成的溶液在水(质量为ω1)中的过量焓;H(mx,my)表示1 kg溶剂水的总焓;为纯水的绝对焓;和分别为溶质x和y的极限偏摩尔焓;hxx,hyy,hxy和hxxx,hxxy,hxyy, hyyy分别为焓对和焓叁作用系数.
以每kg溶剂水计的溶质(x或y)的稀释焓ΔHdil(J·kg-1)可按下式计算:

式中P为溶质的稀释热功率,mx,i为稀释前溶液的质量摩尔浓度,fA为溶液的流速,fB为溶剂水的流速, Mx为溶质x的摩尔质量.
稀释后溶液的质量摩尔浓度mx为
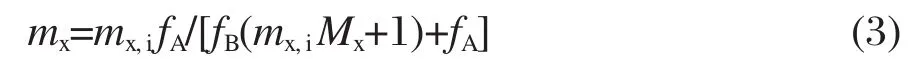
以每kg溶剂水计的溶质x的溶液和溶质y的溶液的混合过程焓变ΔHmix(J·kg-1)按下式计算:
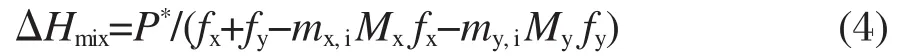
式中P*为混合过程热功率,fx和fy分别为溶质x和溶质y的流速,mx,i,my,i分别为这两种溶液混合前的质量摩尔浓度,Mx,My分别为溶质x,y的摩尔质量.
定义一个辅助函数ΔH*

由方程(1-5)可得:
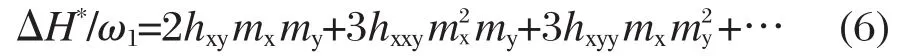
将多组不同的mx和my值的实验结果带入上式进行计算,就可以得到焓对和焓叁相互作用系数.
2 结果与讨论
由实验获得的蛋白质模型化合物与二元醇在水溶液中混合过程焓变ΔHmix/ω1,各自稀释焓ΔHdil(x), ΔHdil(y)以及计算所得的不同浓度时的ΔH*/ω1的值都列于表1.并将数据按式(6)进行多元线性回归分析,得到异系焓作用系数(hxy,hxxy,hxyy),相关系数R(均在0.99以上)和标准偏差(SD)列于表2.

表1 310.15 K时蛋白质模型化合物水溶液与二元醇水溶液的稀释焓及混合过程的焓变Table 1 Enthalpies of dilution and mixing of aqueous solutions of protein model compounds and diol aqueous solutions at 310.15 K

表2 蛋白质模型化合物与二元醇分子的各级异系焓相互作用系数Table 2 Heterotactic enthalpic interaction coefficients between model compounds of protein and diols in aqueous solutions at 310.15 K
异系焓作用系数(hxy,hxxy,hxyy)是溶液中溶剂化的溶质分子靠近时相互作用产生热效应的量度.当两种水合分子从溶质与溶剂作用几乎可以忽略不计的远距离到溶质与溶质以及水之间有作用的距离相互靠近时,焓对作用系数的物理意义就与热力学特性的变化有关[21].因为很难解释更高的异系焓作用系数,本文仅讨论焓对作用系数hxy.
在酰胺类分子中,那些氮原子上的氢未被取代的或一个氢被取代的化合物,它们都有NH基团,都可能通过形成氢键(NH…OC)参与分子间的连接.水溶液中DMF或DMA与二元醇相互作用过程中, DMF和DMA的氮原子没有能力形成氢键,因为氮原子上的氢都被烷基所取代,根据热力学特性的研究[16,22],假定它们有图1所示的共振结构.
DMF和DMA的负电荷位于该分子的氧原子上,通过这些氧负离子上的非共轭电子对,易暴露的原子很容易溶剂化,另一头的正电荷藏于该分子内部,在DMF和DMA上由于两个甲基基团的供电子作用使得这种共振结构更加稳定[23].
焓相互作用系数描绘了溶液中焓作用的特性,并且成为衡量两种溶剂化的溶质作用方式的工具,其大小取决于溶质分子和溶剂水的相互作用,因此,整个作用反映在三个过程中:(1)溶剂化的蛋白质模型化合物分子的部分去溶剂化(吸热过程,对hxy值的正贡献);(2)溶剂化的二元醇分子的部分去溶剂化(吸热过程,对hxy值的正贡献);(3)蛋白质模型化合物与二元醇分子之间的直接作用.
溶剂化的DMF和DMA分子被认为已经高度极化,正电荷被两个甲基环绕.DMF和DMA分子性质与阳离子或正电中心有关联[21].由于分子结构的差异,甘氨酸和丙氨酸不会出现DMF和DMA那样的高度极化的分子结构.因此,过程(3)主要包含4种作用方式:(a)蛋白质模型化合物的氧负离子与二元醇分子羟基之间的氢键作用,由于DMF或DMA的共振结构存在,这一作用被氮原子加强了[24-25](见图2)(放热过程,对hxy值有负贡献);(b)氨基酸的离子头部与二元醇分子羟基之间的亲水-亲水相互作用(放热过程,对hxy值有负贡献);(c)蛋白质模型化合物非极性基团和二元醇羟基之间的疏水-亲水作用(吸热过程,对hxy值有正贡献);(d)蛋白质模型化合物非极性基团与二元醇分子的非极性基团之间的疏水-疏水作用(吸热过程,对hxy值有正贡献).

图1 DMF和DMA分子共振结构式Fig.1 Resonance structures of DMF and DMA
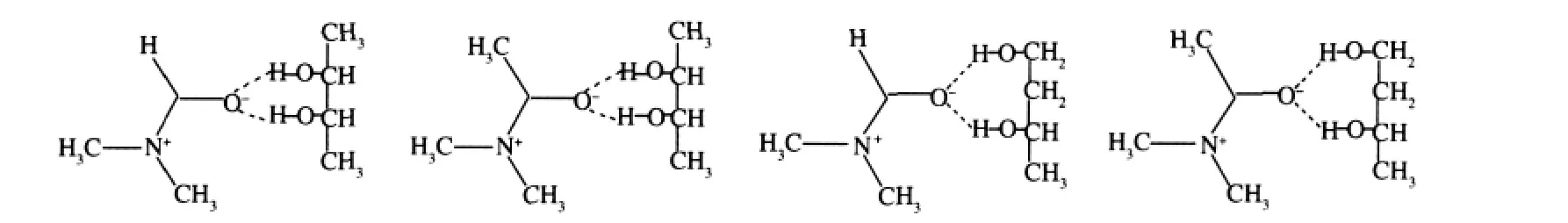
图2 DMF或DMA的共振结构与二元醇分子的氢键相互作用Fig.2 Hydrogen bond interactions of resonance structures of DMF or DMA with diols molecules

图3 蛋白质模型化合物的结构式Fig.3 Structures of model compounds of proteins
hxy的符号和数值是以上去溶剂化作用和溶质分子间直接作用过程达到竞争平衡的结果,蛋白质模型化合物与二元醇之间的直接作用是最主要的作用,并且在整个作用过程中发挥着重要的角色.正如表2中所看到的,它们之间的hxy值是正的,这表明蛋白质模型化合物与二元醇之间的作用吸热效应占主导地位,hxy值的差异主要取决于所研究分子的结构的差异.
蛋白质模型化合物与同一种二元醇的相互作用过程中,其hxy值的大小差异主要取决于蛋白质模型化合物的分子结构.甘氨酸是最简单的氨基酸,没有疏水的烷基侧链,而丙氨酸是非极性侧链氨基酸的代表,二者相比,丙氨酸比甘氨酸多了一个疏水的甲基结构的烷基侧链,丙氨酸的作用力(c)和(d)都比甘氨酸的大,所以hxy(丙氨酸)>hxy(甘氨酸).
关于DMF和DMA两分子,从图1可以看出DMF比DMA分子的羰基C原子上少了一个甲基,所以hxy(DMA)>hxy(DMF),这个实验结果可以由以下两方面来解释.一方面,从分子结构来看,DMF的羰基碳原子的一端是一个氢原子,单独来看是一个醛基,而DMA不是,相互作用时DMA分子的位阻效应就稍大一些;DMF的偶极矩是12.74×10-30C·m, DMA偶极矩是12.64×10-30C·m;由此推断DMF可极化性大于DMA,所以,对于作用力(a),DMF的比DMA的更强烈.另一方面,由于DMA分子比DMF分子羰基C原子上多了一个甲基,所以,对于作用力(b)和(c),DMA的要比DMF的活跃.
甘氨酸和丙氨酸与DMF和DMA分子虽然都是蛋白质模型化合物,但结构差别比较大.表2中数据表明,甘氨酸和丙氨酸的hxy值大于DMF,小于DMA.从它们的结构对比来看(见图3),甘氨酸和DMF都没有烷基侧链,丙氨酸和DMA的烷基侧链都是甲基,但是DMF和DMA氮原子上都含有两个甲基,这就说明DMF和DMA比甘氨酸和丙氨酸疏水性基团多,DMF和DMA的hxy值理论上应该比甘氨酸和丙氨酸大,特别是DMA应该大得更多,但是却出现了hxy(DMA)>hxy(丙氨酸)>hxy(甘氨酸)> hxy(DMF)的大小顺序.从这个结果来看就进一步证实了上段所说的DMF和DMA与二元醇有较强氢键存在,氢键的作用对hxy值是负贡献,造成DMF的hxy值最小,甚至比甘氨酸的hxy值还要小;DMA氢键的存在使得比自己疏水基团少得多的丙氨酸的hxy值略大.
二元醇与蛋白质模型化合物之间的hxy系数的差异主要取决于二元醇分子之间结构差异.1,3-丁二醇和2,3-丁二醇不同之处在于两个羟基的相对位置不一样,二者与蛋白质模型化合物相互作用时,实验结果均表现为hxy(2,3-丁二醇)>hxy(1,3-丁二醇).这主要有以下两方面原因:首先,两个羟基相对位置的不一样导致了疏水基团的不一样,归因于2,3-丁二醇有两个裸露在外的甲基,而1,3-丁二醇只有1个,这样对于(b)和(c)作用力,2,3-丁二醇的作用就比1,3-丁二醇的激烈;其次,2,3-丁二醇的两个羟基相邻,在极性溶剂中,很容易以分子内氢键的形式形成五元环结构,这样就削弱了亲水-亲水相互作用,减少了分子间氢键的形成.
3 结 论
利用2277热活性检测仪获得了蛋白质模型化合物与二元醇分子间的异系焓相互作用系数.结果表明,hxy值均为正值,表明此过程吸热效应占主导作用,并且它们大小顺序分别为hxy(DMA)>hxy(丙氨酸)>hxy(甘氨酸)>hxy(DMF)和hxy(2,3-丁二醇)>hxy(1,3-丁二醇).根据hxy值的差异,讨论了溶质-溶质相互作用和溶质-溶剂相互作用的情况,阐明了二元醇官能团相对位置的变化对hxy值的影响,发现DMF或DMA与二元醇之间有较强的氢键作用,由于DMF分子共振结构有较好的可极化性,DMF与二元醇氢键作用被进一步加强.这一作用对稳定蛋白质的构象有非常重要的作用.
1 Back,J.F.;Oakenfull,D.;Simith,M.B.Biochemistry,1979,19: 5191
2 Bartlomiej,P.;Henryk,P.J.Solution Chem.,1997,26:621
3 Fujita,Y.;Iwasa,Y.;Noda,Y.B.Chem.Soc.Jpn.,1982,55:1896
4 Fujita,F.;Noda,Y.B.Chem.Soc.Jpn.,1984,57:1891
5 Liu,M.;Sun,D.Z.;Lin,R.S.;Qu,X.K.;Wang,X.J.Chem.Eng. Data,2007,52:783
6 Hedwig,G.R.;Lilley,T.H.;Linsdell,H.J.Chem.Soc.Faraday Trans.,1991,87:2975
7 Thenappan,T.;Sankar,U.J.Mol.Struct.,2006,126:38
8 Liu,M.;Zhu,L.Y.;Li,B.;Zhao,Q.;Sun,D.Z.;Lin,R.S.Acta Phys.-Chim.Sin.,2008,24:1316 [刘 敏,朱兰英,李 斌,赵 强,孙得志,林瑞森.物理化学学报,2008,24:1316]
9 Liu,H.J.;Lin,R.S.;Zhang,H.L.Thermochim.Acta,2004, 412:7
10 Shao,S.;Hu,X.G.;Lin,R.S.Acta Chim.Sin.,2000,58:1240 [邵 爽,胡新根,林瑞森.化学学报,2000,58:1240]
11 Liu,H.J.;Lin,R.S.;Zhang,H.L.J.Chem.Eng.Data,2004,49: 416
12 Yu,L.;Yuan,S.L.;Hu,X.G.;Lin,R.S.Chem.Eng.Sci.,2006, 61:794
13 Liu,H.J.;Chen,Y.;Zhang,H.L.;Lin,R.S.J.Chem.Eng.Data, 2007,52:609
14 Shao,S.;Hu,X.G.;Lin,R.S.Acta Phys.-Chim.Sin.,2001,17: 645 [邵 爽,胡新根,林瑞森.物理化学学报,2001,17:645]
15 Liu,C.L.;Ma,L.;Lin,R.S.Acta Chim.Sin.,2009,67:2875 [刘春丽,马 林,林瑞森.化学学报,2009,67:2875]
16 Zhu,Y.;Pang,X.H.;Cheng,X.L.;Yu,L.;Cao,X.Q.Chem.J. Chin.Univ.,2004,25:2312 [朱 焰,庞现红,程学礼,于 丽,曹晓群.高等学校化学学报,2004,25:2312]
17 Zhu,Y.;Pang,X.H.;Yu,L.J.Chem.Eng.Data,2009,54:1910
18 Yu,L.;Zhu,Y.;Pang,X.H.J.Chem.Eng.Data,2006,51:1110
19 McMillan,W.G.;Mayer,J.E.J.Chem.Phys.,1945,13:276
20 Franks,F.;Pedley,M.;Reid,D.S.J.Chem.Soc.Faraday Trans.I, 1976,72:359
21 Castronuovo,G.;Dario,R.P.;Della,V.C.Thermochim.Acta, 1992,206:43
22 Ren,X.L.;Lin,R.S.;Hu,X.G.;Ni,Y.M.Acta Chim.Sin.,1999, 57:875 [任小玲,林瑞森,胡新根,倪亚明.化学学报,1999,57: 875]
23 Venkatesu,P.;Prabhakara,M.V.;Prasad,D.H.;Kumar,Y.V. Thermochim.Acta,1999,342:73
24 Petersen,R.C.J.Phys.Chem.,1960,64:184
25 Ren,X.L.;Lin,R.S.;Ni,Y.M.Chemistry Online,1999,5:36 [任小玲,林瑞森,倪亚明.化学通报,1999,5:36]
March 12,2010;Revised:April 22,2010;Published on Web:June 24,2010.
Heterotactic Enthalpy of the Interaction between Protein Model Compounds and Diols in Aqueous Solutions at 310.15 K
ZHU Yan1,*PANG Xian-Hong1YU Li2
(1Department of Chemistry and Chemical Engineering,Taishan Medical University,Taian 271016,Shandong Province,P.R.China;2Key Laboratory of Colloid and Interface Chemistry,Ministry of Education,Shandong University,Jinan 250100,P.R.China)
The enthalpies of mixing for model protein compounds(glycine,alanine,N,N-dimethyl formamide(DMF) and N,N-dimethyl acetamide(DMA))with diols(1,3-butanediol and 2,3-butanediol)and their respective enthalpies of dilution in aqueous solutions at 310.15 K were determined by flow microcalorimetric measurements.Heterotactic enthalpic interaction coefficients(hxy,hxxy,hxyy)were obtained by analyzing these experimental results according to McMillan-Mayer theory.The results indicated that the hxyvalues were all positive with a dominant endothermic effect and the coefficients decreased according to the order of hxy(DMA)>hxy(Ala)>hxy(Gly)>hxy(DMF)and hxy(2,3-butanediol)> hxy(1,3-butanediol).Based on these results,we discussed solute-solute and solute-solvent interactions with regards to the influence of the relative position of the diol functional groups on the value of hxy.We found that the hydrogen bonds between DMF or DMA and the diols were strong,and because of the good polarizability of DMF′s resonance structure,hydrogen bonds between DMF and the diols were further strengthened.
Amino acid;DMF;DMA;Diol;Solute-solute interaction
[Article] www.whxb.pku.edu.cn
*Corresponding author.Email:2004zy428@163.com;Tel:+86-538-6234228.
The project was supported by the Doctoral Fund of the Ministry of Education of China(New Teachers Fund)(070422047)and Natural Scientific Foundation of Shandong Province,China(Z2007B03).
教育部博士点基金(新教师基金)(070422047)和山东省自然科学基金(Z2007B03)资助项目
O642

