时间分辨拉曼光谱研究一氧化氮与肌红蛋白的结合过程
李 涛 吕 荣 于安池
(中国人民大学化学系,北京 100872)
时间分辨拉曼光谱研究一氧化氮与肌红蛋白的结合过程
李 涛 吕 荣 于安池*
(中国人民大学化学系,北京 100872)
纳秒瞬态拉曼光谱技术是研究分子结构变化超快动态过程的重要实验手段之一.而肌红蛋白(Mb)与小分子配体的结合过程一直是人们研究的焦点.本文旨在利用纳秒瞬态拉曼光谱技术研究小分子配体NO与肌红蛋白结合的动力学过程.通过考察MbNO光解后产物脱氧肌红蛋白(DeoxyMb)与反应物MbNO的ν4特征振动峰的强度比值随激光激发功率的变化,阐述了利用纳秒瞬态拉曼光谱技术研究MbNO体系中NO与DeoxyMb结合过程的可行性.利用纳秒瞬态拉曼光谱技术,获得了与皮秒时间分辨拉曼和皮秒时间分辨吸收相一致的结合动力学实验结果.为研究其它复杂体系的超快结合动力学过程提供了一种新的思路.
纳秒瞬态拉曼;皮秒时间分辨拉曼;皮秒时间分辨吸收;肌红蛋白;一氧化氮;结合过程
肌红蛋白(myoglobin,Mb)是一种广泛存在于脊椎动物肌肉细胞中的血红素蛋白,主要生理功能是为生命有机体储存和运输氧气[1].除此之外,肌红蛋白还通过可逆地与一氧化碳和一氧化氮等小分子配体结合与释放来调控其他血红素蛋白的生理功能[2,3].因此,肌红蛋白又被称为“生物学中的氢原子”[4],一直被科学家们作为一个模型体系来研究蛋白质的结构与功能关系[5-7].
虽然一氧化碳、一氧化氮和氧气分子都可以与肌红蛋白结合,但它们的结合动力学行为有着很大的差异[8-23].在短脉冲激光作用下,配体以很快的速度解离(>1013s-1),解离后的一氧化氮在两三百皮秒内便可完全与肌红蛋白孪生结合(结合幅度>95%)[8-17].一氧化碳则相反,不但孪生结合速度非常慢(微秒量级),而且结合幅度也非常小(<5%)[8-21];氧气的结合情况更为复杂,既有非常快的孪生结合过程(约为6 ps),又有比较慢的孪生结合过程(约为30 ns)[12,21-23].对引起三种配体结合行为的差异,人们的认识也不尽相同[7,10,11,24-28].一直以来人们认为自旋选择定律是造成三种配体结合行为差异的内在本质[24-26,28].在非结合态,血红素铁原子的自旋态为S=2,而结合态中, MbCO的自旋态为S=0,MbNO的自旋态为S=1/2, MbO2的自旋态为S=0.结合过程中,不同的自旋态中间体可以参与反应从而引起它们结合行为的差异.但最近强磁场条件下的结合动力学实验结果表明,强磁场对配体的结合动力学行为没有明显影响[29].此外,Ionascu等[10]同样提出了“Harpoon”模型和“Doming”模型来解释三种配体结合行为的差异.因此,肌红蛋白与三种小分子配体(O2、NO、CO)结合过程差异的内在原因仍不清楚,仍需更多的实验来揭示.
时间分辨拉曼光谱已被广泛地应用于探测反应中间体的结构变化信息和反应历程[30,31].对于肌红蛋白体系而言,目前人们主要利用皮秒时间分辨拉曼光谱技术研究肌红蛋白的结构变化信息[30,32,33],利用皮秒时间分辨拉曼光谱技术研究小分子配体与蛋白结合的动力学过程鲜有报道.此外,纳秒瞬态拉曼光谱同样可以用于跟踪观测快反应中间体的反应过程[34-36].与时间分辨拉曼光谱技术相比,纳秒瞬态拉曼光谱技术主要是利用一束激光中单脉冲内分子被多次激发的时间间隔来观测样品在该时间量级的瞬态过程,即激光的脉冲前沿激发样品引起化学反应,激光的脉冲后沿探测化学反应的进行.与皮秒时间分辨拉曼光谱技术相比,纳秒瞬态拉曼光谱技术的优势在于可以利用高能量的激光对样品进行激发及探测,并且有很高的光谱分辨率.缺点是由于是多光子激发过程,相对于单光子激发的时间分辨拉曼光谱技术,数据处理较为复杂.但由于纳秒激光系统相对于皮秒激光系统容易操作,因此同样具有广泛的应用前景.目前,纳秒瞬态拉曼光谱技术对肌红蛋白体系的研究工作主要集中在针对五配位的脱氧肌红蛋白(DeoxyMb)激发态性质的研究[34-36],而对于其应用于小分子配体结合过程中的研究还未见文献报道.
本文将利用纳秒瞬态拉曼光谱和皮秒时间分辨拉曼光谱技术对一氧化氮与肌红蛋白结合的动力学过程进行研究,并与时间分辨吸收实验结果进行比较,为人们认识小分子配体(NO)与肌红蛋白的相互作用增加部分实验依据.
1 实验部分
马心肌红蛋白购于美国Sigma公司,纯度≥90%,-20℃密封保存.其它试剂均为AR级国产试剂.取适量Mb,加入800 μL浓度为0.1 mol·L-1,pH为7.2的K2HPO4-KH2PO4缓冲溶液中,室温超声1-2 min,待其完全溶解后,离心处理,将上清液转移至厚度为2 mm的石英池中,密封,抽真空,充氩气,重复3-5次,除去溶解在溶液中的氧气.随后加入10 μL浓度约为 1 mol·L-1经过同样除氧操作的Na2S2O4溶液,充分反应,将Mb还原成DeoxyMb.最后加入5 μL浓度约为1 mol·L-1经过同样除氧操作的NaNO2溶液,充分反应,制得MbNO样品溶液.
纳秒瞬态拉曼实验光源由Nd:YAG激光和光学参量振荡器(Spectra-Physics)产生,波长为435 nm,脉冲宽度为7 ns,重复频率为10 Hz.拉曼信号采用背向收集方式,信号由三联-三光栅单色仪(TriVista-555)进行分光,ICCD(PI-Max:1024 18mm-Gen III)采集.激光的功率通过两个格兰棱镜调节.样品处激光聚焦半径大小((59±3)μm)由半径已知的针孔(40 μm)测定.
皮秒时间分辨拉曼和吸收实验装置是利用飞秒激光系统(Spectra-Physics)搭建的,由振荡器、千赫兹放大器和其光学参量放大器组成.皮秒时间分辨拉曼实验中,泵浦光和探测光的波长分别为540和407 nm,脉冲宽度分别约为150 fs和4 ps,样品处功率分别为1 mW和90 μW.其中探测光407 nm是由波长为814 nm、脉冲宽度为150 fs的激光先经过倍频得到407 nm波长的光,然后再由单色仪分光获得.拉曼信号采用背向收集,经单色仪分光,由CCD (Spec-10:400BR/LN)采集.所得拉曼光谱分辨率约为10 cm-1,峰值精确度约为2 cm-1.皮秒时间分辨吸收实验中,泵浦光和探测光的波长分别为540和414 nm,脉冲宽度分别约为150 fs和4 ps,样品处功率分别为0.75 mW和30 μW.信号由光电二极管接收,经锁相放大器处理.两种实验的延时器均放于泵浦光光路上.实验过程中样品由自制磁子搅拌器搅拌,以保证激光聚焦区域样品始终保持新鲜.
实验中的所有MbNO样品浓度均约为50 μmol·L-1.实验前后通过检验样品的吸收光谱检验样品的稳定性.
2 实验结果
图1(a-g)为MbNO在不同激光功率密度下获得的纳秒瞬态拉曼光谱,图1h为MbNO光解产物DeoxyMb的拉曼光谱.图中获得的DeoxyMb的稳态拉曼光谱与文献报道结果[32]完全一致.在MbNO各激光功率密度下的瞬态拉曼光谱中,我们既检测到了六配位MbNO的特征拉曼振动ν4(1377 cm-1)又检测到了五配位光解产物DeoxyMb的特征拉曼振动ν4(1358 cm-1),且随着照射激光功率密度的增大光解产物DeoxyMb所占比例明显增加.
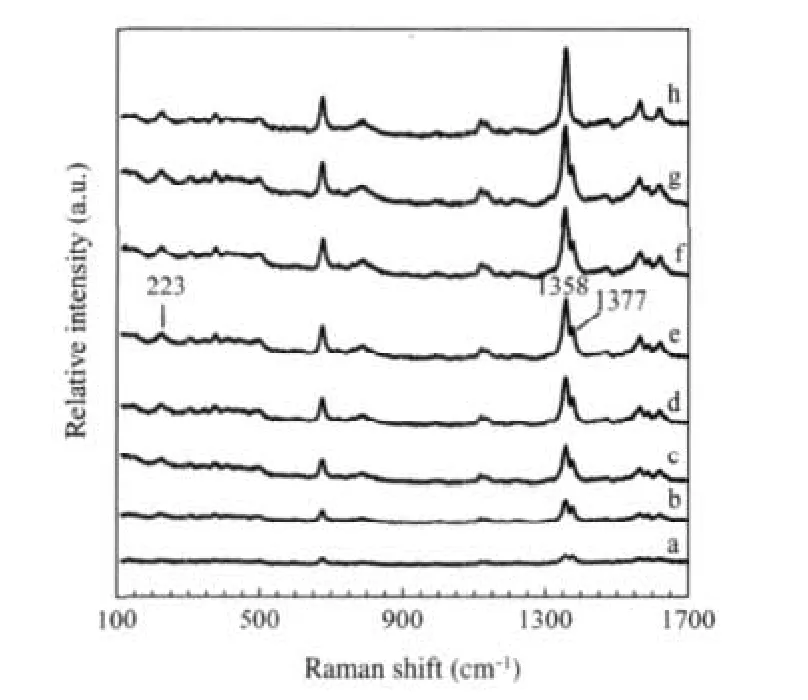
图1 不同激光功率密度(F)下MbNO的纳秒瞬态拉曼光谱图(a-g)和DeoxyMb的拉曼光谱图(h)Fig.1 Nanosecond transient Raman spectra of MbNO at different laser fluxes(F)(a-g)and Raman spectrum of DeoxyMb(h)10-8F/(W·cm-2):(a)0.38,(b)0.76,(c)1.14,(d)1.52,(e)1.90, (f)2.28,(g)2.66
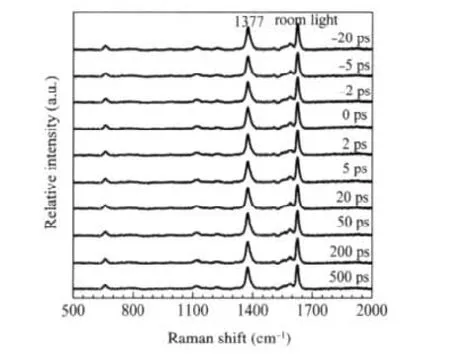
图2 不同时间延迟下MbNO的皮秒时间分辨拉曼光谱图Fig.2 Picosecond time-resolved Raman spectra of MbNO at different time delayspump photolysis wavelength:540 nm, Raman probe wavelength:407 nm
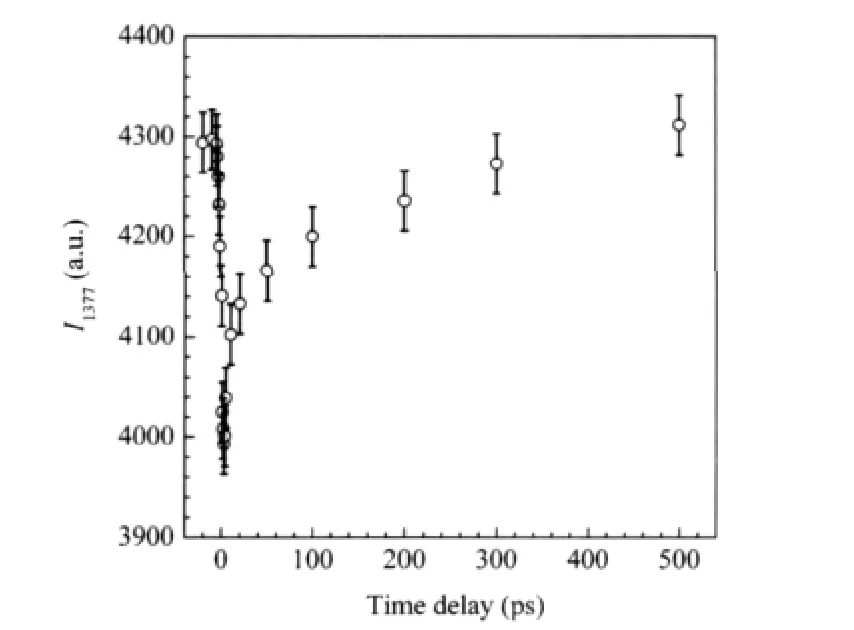
图3 利用1377 cm-1振动峰强度(I)表示MbNO体系中DeoxyMb和NO结合的动力学曲线Fig.3 Rebinding kinetics between DeoxyMb and NO in MbNO by monitoring the peak intensity(I)at 1377 cm-1The adding error bars come from several measurements.
图2为MbNO在不同时间延迟下的皮秒时间分辨拉曼光谱.由于受激光光解产率(实验条件下最大光解产率约为10%)的限制,我们在各时间分辨拉曼光谱中并没有明显检测到光解产物DeoxyMb的特征光谱.但是通过分析反应物MbNO在不同延迟下的拉曼光谱,我们发现随着时间延迟的改变,反应物MbNO的特征振动峰(ν4,1377 cm-1)强度有着明显的改变,如图3所示.
图4为利用时间分辨吸收实验获得的DeoxyMb与NO结合的动力学曲线,其中N(t)表示t时刻光解产物的剩余百分数,空心圆圈为实验数据点,实线为三指数衰减函数拟合曲线,拟合获得的所有参数(见表1)与文献报道结果[8,10,12,13,15-17,21]吻合较好.
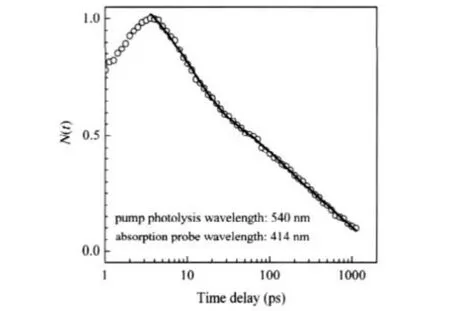
图4 利用皮秒时间分辨吸收测得MbNO中DeoxyMb与NO结合的动力学曲线Fig.4 Rebinding kinetics curves between DeoxyMb and NO in MbNO measured by picosecond timeresolved absorptionThe circles are experimental data,the solid line is the fitting result with three-exponential decay function.N(t)is the survival fraction of DeoxyMb at time t.In the figure,all the data have been normalized to 1 at 3 ps.

表1 三指数衰减函数模拟参数Table 1 Fitting parameters with three-exponential decay function
3 数据分析及讨论
纳秒瞬态拉曼光谱技术是一个多光子激发的过程,即一个脉冲中的光子数远大于聚焦区域中样品的分子数.本实验中,我们所用激光的脉冲宽度为7 ns.由于MbNO光解后DeoxyMb与NO的孪生结合速度很快,在几百个皮秒内结合幅度就达到95%以上,因此在图1所有瞬态拉曼光谱中,我们既探测到了光解后五配位产物DeoxyMb的特征振动峰(1358 cm-1),又探测到了反应物MbNO的特征振动峰(1377 cm-1),这充分说明了在一个激光脉冲中同一MbNO分子被激发了很多次.利用公式(1)[35]可以计算单位时间内同一MbNO分子被激发的次数,即MbNO的激发速率(k),

其中F为入射激光的功率密度(W·cm-2),x为样品MbNO的吸收效率,σ为MbNO分子在激光激发波长处的吸收截面(cm2),Ephoton为入射激光单个光子的能量(J·photon-1).并进而由公式(2)计算出MbNO分子相邻两次激发的时间间隔.

实验条件下,σ435nm(MbNO)=8.15×10-17cm2,Ephotoh(435 nm)=4.57×10-19J·photon-1,x=0.71,由此可以计算出不同入射激光功率密度下MbNO分子相邻两次激发的时间间隔,见表2.
表2结果表明,随着激光功率密度的增大, MbNO分子相邻两次激发的时间间隔变小.这表明激光功率密度越大,与单个MbNO分子相互作用的光子数越多,同一个MbNO分子被激发的次数也就越多,即同一MbNO分子相邻两次激发的时间间隔就越短.由于MbNO光解后生成的五配位产物DeoxyMb很快会与解离的NO分子发生孪生结合,因此激发时间间隔越短,产物DeoxyMb的量相对于反应物MbNO的比例就越高.产物DeoxyMb与反应物MbNO量的比例大小可以利用图1中1358与1377 cm-1振动峰的强度比值表示.若将1358与1377 cm-1振动峰的强度比值对相应激发时间间隔作图,可得图5.由于相邻两次激发的时间间隔可以近似看成样品被一次激发和一次探测,因此相邻两次激发的时间间隔等同于时间分辨拉曼光谱技术中泵浦与探测之间的时间延迟,所以图5中的曲线与图4中的曲线呈现出很大的相似性.

表2 不同入射激光功率密度(F)下单个MbNO分子相邻两次激发的时间间隔(t)Table 2 Excitation time intervals(t)of a single MbNO at different laser fluxes(F)
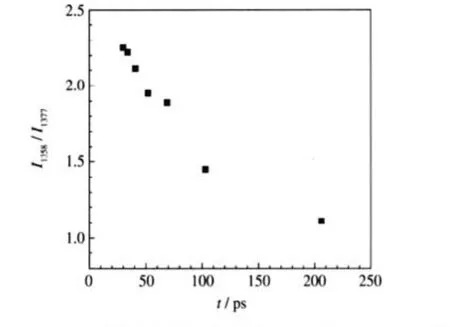
图5 MbNO纳秒瞬态拉曼光谱中1358与1377 cm-1的峰强度比与激发时间间隔的关系Fig.5 Relationship between the peak intensity ratio of 1358 and 1377 cm-1in the nanosecond transient Raman spectrum of MbNO and the excitation time interval
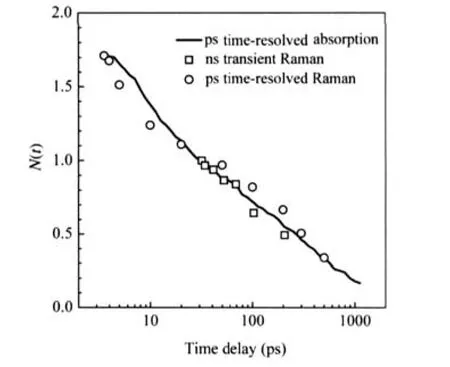
图6 纳秒瞬态拉曼、皮秒时间分辨拉曼和皮秒时间分辨吸收实验结果对比Fig.6 Comparison results on nanosecond transient Raman,picosecond time-resolved Raman,and picosecond time-resolved absorptionIn the figure,all the data have been normalized to 1 at 30 ps.
综上,我们利用皮秒时间分辨拉曼(图3)、皮秒时间分辨吸收(图4)和纳秒瞬态拉曼(图5)三种实验手段分别测得了MbNO体系中DeoxyMb与NO结合的动力学行为.其中图3为通过检测反应物MbNO的变化来表征,图4为通过检测产物DeoxyMb的变化来表征,而图5为通过检测不同激光功率密度下产物DeoxyMb与反应物MbNO的相对比值的改变来表征.虽然三种实验手段测定方法不同,但它们测定的同为MbNO分子光解后DeoxyMb与NO结合的动力学过程.若将图3、图4和图5作一对比,应该获得相同的实验结果.图6为三种实验结果的对比图,图中的所有数据都归一于30 ps处.通过对比可以发现三种实验技术给出了非常相近的结合动力学曲线,这说明我们同样可以利用较为简单的纳秒瞬态拉曼光谱技术,通过改变激光照射于样品的强度来研究MbNO体系中光解后DeoxyMb与NO结合的动力学过程.该实验的有效性同样为研究其它化学或生物中复杂体系的结合动力学过程提供了一种新思路.
4 结 论
通过改变激光功率获得MbNO分子在不同激光功率下的瞬态拉曼光谱.通过分析光解产物DeoxyMb和反应物MbNO的ν4特征振动峰强度比值与照射于样品的激光功率即单个分子激发时间间隔的关系,获得了与传统时间分辨吸收和时间分辨拉曼光谱实验相一致的DeoxyMb与NO的结合动力学行为.实验结果表明利用较为简单的纳秒瞬态拉曼光谱技术同样可以研究MbNO体系中DeoxyMb与NO超快结合过程.该实验的成功为人们研究其它化学或生物中复杂体系的超快结合动力学过程提供了一种新思路.
1 Theorell,H.BioChem.Z,1934,268:73
2 Frauenfelder,H.;McMahon,B.H.;Austin,R.H.;Chu,K.;Groves, J.T.Proc.Natl.Acad.Sci.U.S.A.,2001,98:2370
3 Wittenberg,J.B.;Wittenberg,B.A.J.Exp.Biol.,2003,206:2011
4 Frauenfelder,H.;McMahon,B.H.;Fenimore,P.W.Proc.Natl. Acad.Sci.U.S.A.,2003,100:8615
5 Parak,F.G.;Nienhaus,G.U.ChemPhysChem,2002,3:249
6 Springer,B.A.;Sligar,S.G.;Olson,J.S.;Phillips,G.N.Chem. Rev.,1994,94:699
7 Olson,J.S.;Phillips Jr.,G.N.J.Biol.Chem.,1996,271:17593
8 Petrich,J.W.;Lambry,J.C.;Kuczera,K.;Karplus,M.;Poyart,C.; Martin,J.L.Biochemistry,1991,30:3975
9 Ikeda-Saito,M.;Dou,Y.;Yonetani,T.;Olson,J.S.;Li,T.;Regan, R.;Gibson,Q.H.J.Biol.Chem.,1993,268:6855
10 Ionascu,D.;Gruia,F.;Ye,X.;Yu,A.C.;Rosca,F.;Beck,C.; Demidov,A.;Olson,J.S.;Champion,P.M.J.Am.Chem.Soc., 2005,127:16921
11 Meuwly,M.;Becker,O.M.;Stote,R.;Karplus,M.Biophys. Chem.,2002,98:183
12 Ye,X.;Demidov,A.;Champion,P.M.J.Am.Chem.Soc.,2002, 124:5914
13 Ye,X.;Yu,A.C.;Champion,P.M.J.Am.Chem.Soc.,2006,128: 1444
14 Carver,T.E.;Rohlfs,R.J.;Olson,J.S.;Gibson,Q.H.;Blackmore, R.S.;Springer,B.A.;Sligar,S.G.J.Biol.Chem.,1990,265:2007
15 Kholodenko,Y.;Gooding,E.A.;Dou,Y.;Ikeda-Saito,M.; Hochstrasser,R.M.Biochemistry,1999,38:5918
16 Kim,S.;Lim,M.J.Phys.Chem.B,2004,108:20366
17 Shreve,A.P.;Franzen,S.;Simpson,M.C.;Dyer,R.B.J.Phys. Chem.B,1999,103:7969
18 Tian,W.D.;Sage,J.T.;Srajer,V.;Champion,P.M.Phys.Rev. Lett.,1992,68:408
19 Austin,R.H.;Beeson,K.W.;Eisenstein,L.;Frauenfelder,H.; Gunsalus,I.C.Biochemistry,1975,14:5355
20 Schotte,F.;Lim,M.;Jackson,T.A.;Smirnov,A.V.;Soman,J.; Olson,J.S.;Phillips Jr.,G.N.;Wulff,M.;Anfinrud,P.A.Science, 2003,300:1944
21 Walda,K.N.;Liu,X.Y.;Sharma,V.S.;Magde,D.Biochemistry, 1994,33:2198
22 Yu,A.C.;Ye,X.;Ionascu,D.;Cao,W.X.;Champion,P.M.Rev. Sci.Instrum.,2005,76:114301
23 Wang,Y.;Baskin,J.S.;Xia,T.;Zewail,A.H.Proc.Natl.Acad. Sci.U.S.A.,2004,101:18000
24 Franzen,S.Proc.Natl.Acad.Sci.U.S.A.,2002,99:16754
25 Harvey,J.N.Faraday Discuss.,2004,127:165
26 Alden,R.G.;Ondrias,M.R.J.Phys.Chem.,1990,94:85
27 Agmon,N.;Hopfield,J.J.J.Chem.Phys.,1983,79:2042
28 Strickland,N.;Harvey,J.N.J.Phys.Chem.B,2007,111:841
29 Zhang,Z.Y.;Benabbas,A.;Ye,X.;Yu,A.C.;Champion,P.M. J.Phys.Chem.B,2009,113:10923
30 Uchida,T.;Kitagawa,T.Acc.Chem.Res.,2005,38:662
31 Schoonover,J.R.;Strouse,G.F.Chem.Rev.,1998,98:1335
32 Mizutani,Y.;Kitagawa,T.Chem.Rec.,2001,1:258
33 Cianetti,S.;Negrerie,M.;Vos,M.H.;Martin,J.L.;Kruglik,S.G. J.Am.Chem.Soc.,2004,126:13932
34 Li,P.;Sage,J.T.;Champion,P.M.J.Chem.Phys.,1992,97: 3214
35 Loparo,J.J.;Cheatum,C.M.;Ondrias,M.R.;Simpson,M.C. Chem.Phys.,2003,286:353
36 Simpson,M.C.;Peterson,E.S.;Shannon,C.F.;Eads,D.D.; Friedman,J.M.;Cheatum,C.M.;Ondrias,M.R.J.Am.Chem. Soc.,1997,119:5110
September 14,2009;Revised:October 27,2009;Published on Web:November 25,2009.
Recombination Process between Myoglobin and NO Studied by Time-Resolved Raman Spectroscopy
LI Tao LÜ Rong YU An-Chi*
(Department of Chemistry,Renmin University of China,Beijing 100872,P.R.China)
Nanosecond transient Raman spectroscopy is a widely used technique to investigate ultrafast structural dynamics in molecules.We studied the rebinding kinetics between deoxymyoglobin(DeoxyMb)and NO using nanosecond transient Raman spectroscopy.By monitoring the ratio between the intensity of the ν4vibrational mode in thephotoproduct(DeoxyMb)andinthereactant(MbNO)atdifferentincidentlaserfluxes,weobtainedtherecombination kinetics between DeoxyMb and NO in MbNO.For comparison,the kinetics of NO rebinding to DeoxyMb in MbNO was also studied using picosecond time-resolved Raman and absorption experiments.The kinetics results obtained with nanosecond transient Raman were consistent with those obtained by picosecond time-resolved Raman and absorption experiments.
Nanosecond transient Raman;Picosecond time-resolved Raman;Picosecond time-resolved absorption;Myoglobin;NO;Recombination
O643
*Corresponding author.Email:a.yu@chem.ruc.edu.cn;Tel:+86-10-62514601.
The project was supported by the National Natural Science Foundation of China(20603047,20733001).
国家自然科学基金(20603047,20733001)资助项目

