催化剂对乳液模板法制备碳材料形貌的影响
甘礼华 刘明贤 陈龙武 胡 军 刘洪来,*
(1同济大学化学系,上海 200092; 2华东理工大学化学系,结构可控先进功能材料及其制备教育部重点实验室,上海 200237)
催化剂对乳液模板法制备碳材料形貌的影响
甘礼华1,*刘明贤1,2陈龙武1胡 军2刘洪来2,*
(1同济大学化学系,上海 200092;2华东理工大学化学系,结构可控先进功能材料及其制备教育部重点实验室,上海 200237)
以液体石蜡为油相,间苯二酚和甲醛的水溶液为水相,吐温80和司班80为乳化剂,获得油/水(O/W)型乳状液.将该乳状液聚合、碳化去除模板后制得了碳材料,研究了不同催化剂对所得碳材料形貌的影响.结果表明:选择NaOH为催化剂时,制得的碳材料是一种具有孔壁和孔洞的多孔碳泡沫,典型样品的孔径约为1-2 μm;当氨水为催化剂时,所得碳材料是由微球或者相互缠绕的蠕虫状粒子组成的块体材料,这些微球或粒子的直径主要集中在1-2 μm,与NaOH为催化剂时所得碳泡沫的孔径尺寸相当.研究发现,氨水的加入使得乳液体系发生了相转化,由原来的O/W型乳液逐渐转变为W/O型高内相乳液.从分子间氢键出发,应用内聚能理论探讨了催化剂导致的乳液相变以及不同形貌碳材料的形成过程.
乳状液; 催化剂; 碳材料; 形貌; 相变; 氢键
乳液是一种分散体系,它由水相、油相以及乳化剂组成[1-2].根据稳定性的不同,乳液可以分为微乳液和普通乳状液.微乳液是热力学稳定的分散体系,将形成微乳液的各个组分按照适当比例混合可自发形成透明或半透明的、低粘度和各同向性的体系.乳状液在热力学上处于不稳定状态,它的形成一般需要外加能量如搅拌等.乳液聚合是一类发生在乳液中的聚合反应,一般由水、单体、乳化剂和催化剂组成.乳液聚合体系粘度低、易散热,它具有较快的反应速率,而且所需设备工艺简单,操作方便灵活,这些特点使得乳液聚合技术在合成橡胶、树脂涂料、粘合剂、絮凝剂等实际工业生产中具有非常广阔的应用前景.近年来,乳液或乳液聚合方法在制备多孔材料、微球材料以及各种无机纳米材料等方面吸引了众多科研工作者的广泛兴趣[3-5].例如甘礼华等[6-8]通过乳液法制备了多孔的SiO2和TiO2/SiO2气凝胶微球材料.Menner等[9]通过高内相乳液(HIPE)聚合的方法获得了开孔的聚合物材料;在前期的工作中,我们选择间苯二酚+甲醛(R+F)的水溶液为水相,液体石蜡为油相,司班80-吐温80为乳化剂,通过乳液聚合法制备了多孔的碳泡沫材料[10].在随后的研究过程中我们发现,不同的催化剂对该乳液体系的结构以及所得样品的形貌有着重要的影响.本文选择NaOH和氨水两种催化剂,在司班80-吐温80/液体石蜡/R-F-水体系中,通过乳液聚合法制备了具有不同形貌的碳材料,同时探讨了催化剂对乳液结构的影响以及在碳材料形成过程中的作用机制.
1 实验部分
1.1 试剂与仪器
甲醛溶液(38%,w,下同)、间苯二酚、氢氧化钠、司班80、吐温80、液体石蜡,皆为分析纯试剂,中国医药(集团)上海化学试剂有限公司生产;氨水(28%),分析纯试剂,太仓市直塘化工厂生产;JSM-6700F型扫描电子显微镜(SEM),日本电子株式会社(JEOL)生产.
1.2 碳材料的制备
质量比为3∶2的司班80与吐温80混合剂作为乳化剂,液体石蜡为油相,物质的量比为1∶2的间苯二酚和甲醛(R+F)溶于蒸馏水中作为水相.在强力机械搅拌条件下,将2.0 g乳化剂和10.0 g液体石蜡的混合液滴加到28.0 g水相中(R+F在水相中的质量分数可以变化),反应体系处于40℃的恒温水浴中.滴加结束后,继续搅拌40 min后得O/W乳状液.在体系中加入NaOH或NH3·H2O作为催化剂后,R、F开始聚合,体系逐渐固化.分别以稀盐酸和蒸馏水洗涤聚合产物并干燥,然后在N2气氛中,将其置于管式炉中升温加热到1000℃以制备碳材料.
2 结果与讨论
2.1 NaOH为催化剂时碳材料的形貌
司班80-吐温80/液体石蜡/R-F-水体系参照稀释法确定为O/W型乳液.在该体系中,每一个油相液滴就相当于一个微小的胶囊.催化剂NaOH的加入使水相中的R、F迅速聚合得到酚醛树脂聚合体.另一方面,液体石蜡微胶囊均匀地分布在酚醛树脂聚合体内,经过高温碳化去除后留下孔洞,因此,所得样品是一种具有孔洞和孔壁的碳泡沫材料[10].图1是以NaOH为催化剂,乳液水相中R+F质量分数不同时所得样品的SEM照片.由图1可知,在制备过程中,R、F作为碳源,其在乳液水相中的含量对所得碳泡沫的微观结构有较大的影响.当水相中R+F的质量分数为0.357时,碳泡沫的孔结构较差(图1(A)).在这些样品中,既存在几十微米的大孔,也同时存在几个微米的小孔.此外,所得碳泡沫的孔壁中也充满了小孔.这是由于低浓度的R+F在乳液中的聚合仅仅为碳泡沫提供了基本的连接骨架,而难以为碳泡沫提供完整的孔壁和韧带,从而造成所得的碳泡沫的骨架结构比较松散.当水相中R+F的质量分数增加到0.486时,所得碳泡沫的孔结构较好,样品的孔洞大都集中在1-2 μm,分布较为均匀,如图1(B-C)所示.此外,水相中R+F的质量分数增加至0.850时,制得的碳泡沫的孔结构较差,而且孔洞较少.这是由于水相中R+F的含量过高,严重地影响到乳液的稳定性所造成的;当水相中不含R和F时,可以获得比较稳定的O/W型乳状液;当R+F的质量分数增加至0.850时,乳液的稳定性明显降低,停止搅拌后,体系发生分层现象.
2.2 氨水为催化剂时碳材料的形貌

图1 NaOH为催化剂时水相中不同(R+F)质量分数制得的碳泡沫的SEM照片Fig.1 SEM images of carbon foams prepared by using NaOH as the catalyst with different mass fractions of an aqueous R+Fw(R+F):(A)0.357,(B)0.486,(C)0.714,(D)0.850;R:resorcinol;F:formaldehyde

图2 氨水为催化剂时水相中不同(R+F)质量分数制得的碳材料样品的SEM照片Fig.2 SEM images of carbon materials prepared by using ammonia as the catalyst with different mass fractions of an aqueous R+Fw(R+F):(A,B)0.714,(C)0.357,(D)0.298
图2是以氨水为催化剂时制得的碳材料的SEM照片.由图2可知,所得样品与以NaOH为催化剂时所得的多孔碳泡沫材料相比,两者在微观形貌上有着明显的区别.当以NaOH为催化剂时,制得的是具有孔壁和孔洞的多孔碳泡沫;当以氨水为催化剂时,所得样品是由球状的粒子(或微球)组成的块状材料(图2(A)),其孔隙存在于微球之间.样品中的微球并不是完全独立的,而是相互连接在一起(图2(B)),这些微球的直径大部分集中在1-2 μm之间,与NaOH为催化剂时制得的碳材料中孔径的尺寸基本一致.此外,所得碳材料中粒子的形状与水相中R+F的质量分数有关:当R+F的质量分数较高时,所得碳材料中的粒子是球形的;当R+F的质量分数降低至0.357时,碳材料中的粒子为近似球状(图2(C));而当进一步降低R+F的质量分数至0.298时,样品由尺寸大小与微球类似,形状上为高度缠绕的蠕虫状的粒子组成,如图2(D)所示.
对比图1和图2可以发现,不同的催化剂对所得碳材料的微观形貌有着显著的影响.当以NaOH为催化剂时,制得的样品是具有孔壁和孔洞的碳泡沫材料,对应于O/W型乳液聚合得到的结果.采用氨水为催化剂时,所得样品由球状或者蠕虫状粒子组成,因此,氨水的加入使乳液体系的结构发生了改变.在该体系中,加入催化剂后,通过相稀释法或者电导法来确定其结构类型变得十分困难,这是因为加入催化剂之后,R和F开始聚合,这既增加了体系的不稳定性,也使得体系快速聚合.不过,体系结构的变化可以通过观察所得样品的微观形貌来加以推测.既然氨水加入到乳液中以后,体系不再保持O/ W结构,那么,在该体系中可能存在以下两种情形: (1)O/W乳液的结构由于氨水的加入而被完全破坏; (2)O/W乳液反相形成W/O型乳液.然而,如果乳液结构受到完全破坏,在既没有任何造孔剂,也没有溶胶-凝胶过程等情况下,仅仅通过R、F之间的聚合难以获得含孔的碳材料,而且所得样品中也不可能存在球状或者蠕虫状的粒子.因此,该乳液中只存在第二种可能性,即氨水的加入使得体系发生了相变.另一方面,图2样品中粒子直径与图1样品中孔洞尺寸的一致性也表明,氨水导致乳液体系的结构发生了重构.由于乳液体系中水相的质量分数为0.70,将其换算成体积分数时超过了0.80,因此,乳液反相后由于水相成为了乳液内相而获得了HIPE[11](Lissant首次将HIPE定义为内相体积分数占0.70或以上的乳液[12]).在HIPE中,乳液内相所占的体积非常高,因此,其内相并不是像传统乳液中内相那样,被分散相分散成彼此分离的“微滴”,而是形成互相连接的“微滴”(见图3).
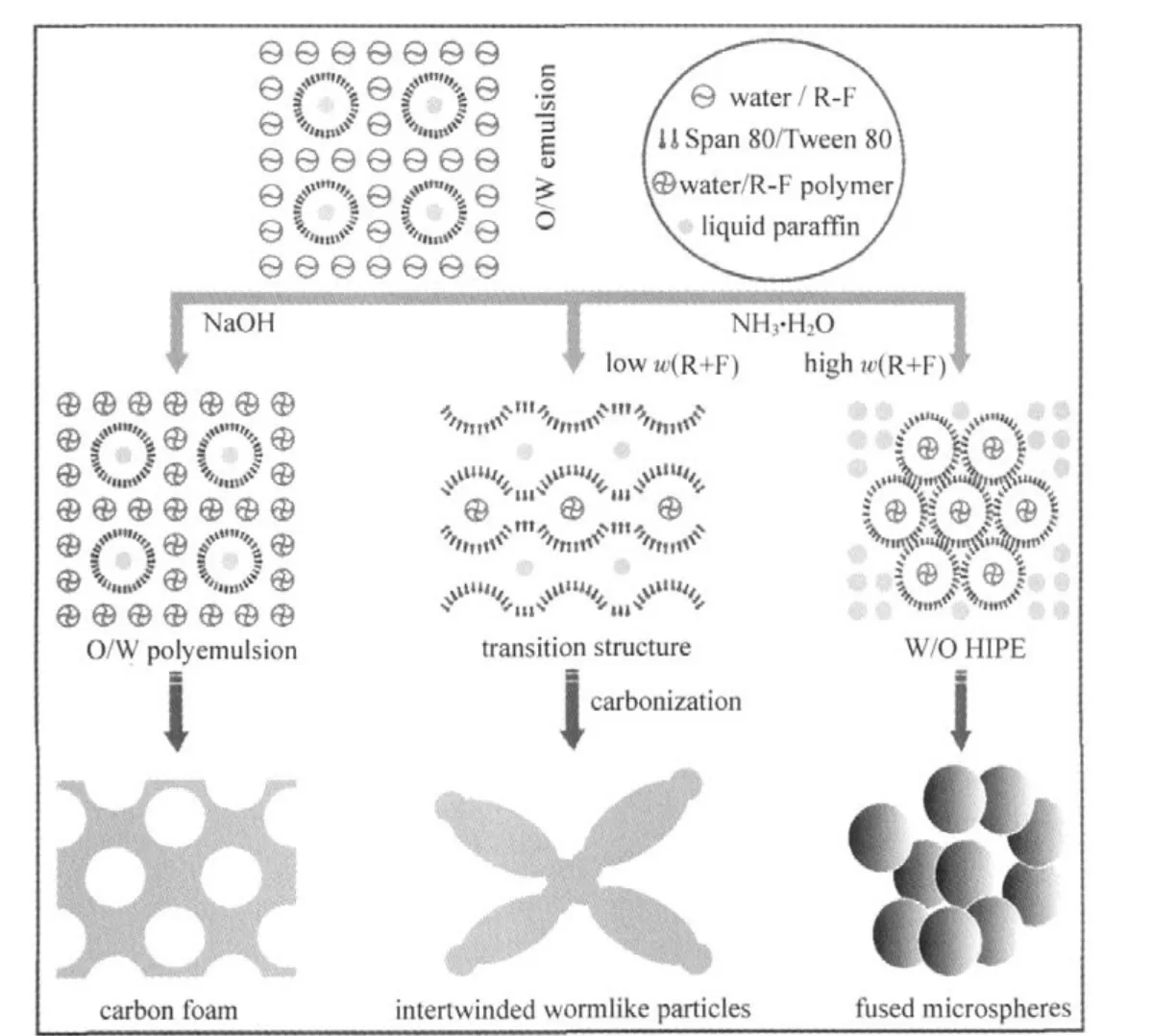
图3 NaOH和氨水为催化剂时乳液模板法合成碳材料过程示意图Fig.3 Schematic formation of carbon materials synthesized via emulsion templating method by using NaOH or ammonia as the catalystHIPE:high internal phase emulsion
通过普通乳液聚合法制备聚合物或碳材料时,如制得的是多孔材料,则该材料为具有孔洞和孔壁的块体材料;若制得的是微球材料,那么,这些微球是相互分离的,沉积于容器底部而形成粉体材料[7].本文通过HIPE制得的碳材料中,微球是互相连接的,这与通过HIPE制得的多孔材料中,其孔洞是开孔的而不是闭孔的结果相一致 :HIPE聚合制备多孔材料时形成孔洞的“咽喉”,而本文得到互相连接的微球.然而,与图2(B)相比,图2(D)中样品在形貌上存在较大的差异.该样品由高度缠绕的蠕虫状粒子组成,这些粒子的形貌与乳液中的过渡结构(类似于微乳液的双连续相结构)特征类似[13],而不同于W/O以及O/W型乳液的结构特征,因此,它应该对应于乳液中的过渡结构聚合而得的结果.以上分析结果表明,在乳液体系中,NaOH为催化剂时,O/W乳液结构保持不变,所得样品为多孔的碳泡沫材料;氨水为催化剂时,乳液体系发生了相变,其中在R+F的质量分数较低时,乳液存在一个过渡结构.R和F在乳液中经原位聚合、干燥和碳化后获得由蠕虫状或者微球状粒子组成的碳材料,如图3所示.
2.3 催化剂对乳液结构和碳材料形貌影响的机理分析
为什么在加入氨水后,O/W乳液体系会发生反相或者说重构呢?我们推测认为,这可能与氨水能够形成氢键有关.在有关乳液结构理论中,内聚能理论是一个有关乳液结构的理论,它首先由Winsor提出,以内聚能(R)描述由乳化剂、油、水所构成体系中,各种分子之间相互作用的强弱,从而预测各种结构的分子有序组合体的形成、转换和稳定性理论的表示式.内聚能理论从分子间相互作用出发,提出如下公式[14-16]:

式中,Aco、Acw、Aoo、Aii、Aww、Ahh分别为界面层单位面积上乳化剂的疏水基与油分子、乳化剂亲水基与水分子、油分子之间、乳化剂疏水之间、水分子之间、乳化剂亲水基之间的内聚能[17].
在方程(1)中存在以下三种情况:R<1(O/W型乳液),R=1(双连续相结构),R>1(W/O型乳液).由于该方程中的各个内聚能参数一般不易获得,Beerbower等[18]运用Winsor的内聚能理论,结合Hildebrand稳定性参数以及Hansen的氢键理论,得到内聚能理论的一般表达式:

式中,HLB为乳化剂的亲水亲油平衡值;σ为溶解度参数,包括分散性贡献(σd),极性贡献(σp)和氢键贡献(σh)三个部分[19];dH和dL为乳液中亲水和亲油部分的密度,L和H代表乳化剂亲油部分和亲水部分.根据内聚能理论,R值受乳化剂HLB值、水相/油相体积比等参数影响[20-23],例如,一个O/W乳状液的油相体积分数逐渐增加时,可以发生反相;一些非离子型表面活性剂稳定的O/W型乳状液在相转变温度下会发现相变[23].然而,在本文所选的乳液体系中,仅仅通过改变催化剂就发生相变还是令人非常意外的.这是因为乳化剂的HLB值、油相/水相的比例等条件都没有改变.此外,对比图1(C)和图2 (B)可知,水相中R+F质量分数相同时,不同催化剂所制得的碳材料也不同,这说明R+F浓度的变化也不是引起乳液相变的原因.
在乳液体系中加入NaOH或者氨水,一方面由于pH的变化使得体系中Acw-Ahh增加,但另一方面,由于加入的碱是电解质,可以降低Acw-Ahh[17,24].因此,碱的加入引起乳液体系的何种变化取决于上述两种因素影响大小的比较.由于NaOH是强碱,氨水是弱碱,碱的改变可能会影响到体系pH值以及由体系聚合引起的温度的稍许变化.不过,在实验过程中发现,即使大幅度改变NaOH或氨水的用量(如控制这两种碱的用量使反应体系的pH值相同),所得样品在各自的形貌上并没有发生明显的改变.这表明碱性的强弱或者pH值的变化也不是引起乳液反相的原因.
氨水具有形成氢键的能力,将氨水加入乳液中时,它可以与司班80和吐温80的亲水头基中的羟基(图4)形成氢键.此外,氨水与油/水界面上的水分子、R、F均可以形成氢键.这些氢键的形成使得乳液体系本身的亲水基团在界面上的氢键贡献(σh)H降低,或者说降低了界面层中水相和乳化剂之间的内聚能Acw,因此,氢键的形成使得方程(1)或(2)中的内聚能比R值逐渐增加,从而引起乳液结构的变化.这一结果与乳液体系中由于无机盐电解质的加入导致界面层表面活性剂和水之间的内聚能Acw的降低,从而引起体系的相变的结果类似[25].随着水相中R+ F的浓度逐渐增加,氨水与之形成的氢键的能力增加,进一步降低了参数(σh)H或者Acw.当R+F浓度增加到0.357时,R值进一步增大,导致体系发生相变.在相变过程中,体系经聚合、碳化后得到具有不同形貌的碳材料.然而,由于NaOH不具备形成氢键的能力,也就没有引起体系中(σh)H参数的变化,因此,以它为催化剂,经乳液聚合后得到多孔的碳泡沫材料.

图4 司班80和吐温80分子结构示意图Fig.4 Schematic molecular structures of Span 80(a) and Tween 80(b)

图5 以二甲胺为催化剂制得的碳材料样品的SEM图Fig.5 SEM image of carbon materials prepared by using dimethylamine as the catalyst
基于以上分析,我们推测,在本文所选乳液中,由于氢键的形成使得体系发生相变.为了验证这一推测,在实验过程中选择同样具备形成氢键能力的二甲胺溶液为催化剂制备碳材料,所制得的典型样品的SEM照片如图5所示.由图5可知,制得的碳材料也是由粒径为1-2 μm且互相连接的球形粒子组成,这与氨水为催化剂时所得样品的微观形貌是一致的,这一结果初步证实了氢键的形成使得乳液体系发生相变的推测.
3 结 论
以液体石蜡为油相,吐温80和司班80为乳化剂,R+F的水溶液作为水相,获得O/W型乳状液.以NaOH为催化剂,将所得O/W型乳状液聚合后制得了具有孔壁和孔洞、孔直径在1-2 μm的多孔碳泡沫材料.氨水为催化剂时,乳液体系发生了相变,原来的O/W型乳液逐渐转变成W/O型HIPE.所得碳材料由粒径集中在1-2 μm的微球状或者蠕虫状粒子组成.从分子间氢键出发,应用内聚能理论探讨了不同催化剂时乳液的相变机理以及不同形貌碳材料的形成过程.这一结果为乳状液的结构控制以及通过乳液模板法制备具有不同形貌的碳材料提供了一种简单方法.
1 Nagarajan,R.;Ruckenstein,E.Langmuir,2000,16:6400
2 Wang,F.;Xu,G.;Zhang,Z.;Xin,X.Eur.J.Inorg.Chem.,2006, (1):109
3 Tai,H.;Sergienko,A.;Silverstein,M.S.Polymer,2001,42:4473
4 Mock,E.B.;De Bruyn,H.;Hawkett,B.S.;Gilbert,R.G.;Zukoski, C.F.Langmuir,2006,22:4037
5 Lu,X.;Tang,J.;Fan,Y.B.;Hu,J.;Liu,H.L.Acta Phys.-Chim. Sin.,2009,25:178 [路 霞,唐 静,范玉冰,胡 军,刘洪来.物理化学学报,2009,25:178]
6 Liu,M.X.;Gan,L.H.;Pan,Y.C.;Xu,Z.J.;Hao,Z.X.;Chen,L. W.Colloid Surf.A,2008,317:490
7 Pan,Y.C.;Gan,L.H.;Xu,Z.J.;Hao,Z.X.;Chen,L.W.Acta Phys.-Chim.Sin.,2005,21:1363 [庞颖聪,甘礼华,徐子颉,郝志显,陈龙武.物理化学学报,2005,21:1363]
8 Gan,L.H.;Liu,M.X.;Pan,Y.C.;Xu,Z.J.;Hao,Z.X.;Chen,L. W.Chin.J.Inorg.Chem.,2006,22:1740 [甘礼华,刘明贤,庞颖聪,徐子颉,郝志显,陈龙武.无机化学学报,2006,22: 1740]
9 Menner,A.;Powell,R.;Bismarck,A.Macromolecules,2006,39: 2034
10 Liu,M.X.;Gan,L.H.;Zhao,F.Q.;Xu,H.X.;Fan,X.Z.;Tian,C.; Wang,X.;Xu,Z.J.;Hao,Z.X.;Chen,L.W.Carbon,2007,45: 2710
11 Liu,M.X.;Gan,L.H.;Xu,Z.J.;Chen,L.W.;Hu,J.;Liu,H.L. Chem.Lett.,2010,39:274
12 Lissant,K.J.J.Colloid Interf.Sci.,1966,22:462
13 Liu,E.H.;Callaghan,P.T.;McGrath,K.M.Langmuir,2003,19: 7249
14 Winsor,P.A.Trans.Faraday Soc.,1948,44:376
15 Beerbower,A.;Hill,M.W.McCutcheon′s detergents and emulsifiers.Ridgewood:Annual.Allured Publ.Co.,1971:223
16 Bourrel,M.;Chambu,C.Soc.Pet.Eng.J.,1983,23:327
17 Guo,R.;Li,G.Z.;Liu,M.X.Comm.Chem.Ind.,1994:32 [郭 荣,李干佐,刘木辛.日用化学工业,1994:32]
18 Beerbower,A.;Hill,M.W.Am.Cosmet.Perfum.,1972,87:85
19 Hansen,C.M.J.Paint.Technol.,1967,39:505
20 Dimitrova,T.D.;Leal-Calderon,F.Langmuir,1999,15:8813
21 El-Aasser,M.S.;Lack,C.D.;Vanderhoff,J.W.;Fowkes,F.M. Colloid Surf.,1988,29:103
22 Morales,D.;Gutiérrez,J.M.;García-Celma,M.J.;Solans,Y.C. Langmuir,2003,19:7196
23 Liang,W.P.The foundation of emulsion science and technology. Beijing:Science Press,2001:55-62 [梁文平.乳状液科学与技术基础.北京:科学出版社,2001:55-62]
24 Qutubuddin,S.;Miller,C.A.;Fort Jr.,T.J.Colloid Interf.Sci., 1984,101:46
25 Pecaock,J.M.;Matijevic′,E.J.Colloid Interf.Sci.,1980,77:548
April 28,2010;June 4,2010;Published on Web:July 22,2010.
Effect of Catalysts on the Morphologies of Carbon Materials Synthesized by an Emulsion Templating Method
GAN Li-Hua1,*LIU Ming-Xian1,2CHEN Long-Wu1HU Jun2LIU Hong-Lai2,*
(1Department of Chemistry,Tongji University,Shanghai200092,P.R.China;2Key Laboratory for Advanced Materials, Department of Chemistry,East China University of Science and Technology,Shanghai 200237,P.R.China)
An oil in water(O/W)emulsion with a resorcinol and formaldehyde(R+F)water solution as the external phase and liquid paraffin as the internal phase together with Span 80/Tween 80 as emulsifiers was obtained.Carbon materials were prepared by polymerization of the emulsion,followed by carbonization for template removal.The effect of catalysts on the morphologies of the carbon materials was investigated.The results indicate that the resultant representative carbons are a type of porous carbon foam and possess pore walls and pores of 1-2 μm in size when NaOH is used as a catalyst.However,monolithic carbon materials consisting of microspheres or intertwinded wormlike particles were prepared using ammonia as an alternative catalyst.The diameters of these microspheres or particles were mainly around 1-2 μm and these dimensions are similar to the pore sizes of the carbon foams.We find that ammonia causes the initial O/W emulsion system to experience a phase inversion toward a W/O high internal phase emulsion.A mechanism involving intermolecular H-bond interactions and cohesive energy theory is proposed to explain the catalyst-induced phase inversion phenomenon as well as the formation of carbon materials with different morphologies.
Emulsion;Catalyst;Carbon material;Morphology;Phase inversion;H-bond
O648
*Corresponding authors.GAN Li-Hua,Email:ganlh@tongji.edu.cn;Tel:+86-21-65982654-8430.LIU Hong-Lai,Email:hlliu@ecust.edu.cn; Tel:+86-21-64252921.
The project was supported by the National Natural Science Foundation of China(20973127,20776045,20736002),Shanghai Nanotechnology Promotion Center,China(0952nm00800),National High Technology Research and Development Program of China(2008AA062302),China Postdoctoral Science Foundation(20090460647)and Shanghai Postdoctoral Scientific Program,China(10R21412100).
国家自然科学基金(20973127,20776045,20736002)、上海市科委纳米专项基金(0952nm00800)、国家高技术研究发展计划(863)项目(2008AA062302)、中国博士后科学基金(20090460647)和上海市博士后科研资助计划(10R21412100)资助

