动态浸滤及几种静态预测法对云浮硫铁矿酸化特征及产酸潜力的比较*
李锦文 陈 南 吴惠明 罗定贵 陈永亨**
(1 广州大学环境科学与工程学院;2 广州大学化学与化工学院,广州 510006)
动态浸滤及几种静态预测法对云浮硫铁矿酸化特征及产酸潜力的比较*
李锦文1陈 南1吴惠明2罗定贵1陈永亨1**
(1 广州大学环境科学与工程学院;2 广州大学化学与化工学院,广州 510006)
用几种静态预测方法研究了来自云浮硫铁矿矿石的产酸潜力,并结合动态浸滤试验方法对比了新旧矿石的氧化过程及产酸的动力学特征.静态预测结果表明:该矿矿石的净中和酸潜力 NNP<-20、中和酸能力与产酸潜力比 NP/AP<1∶1、静产酸量 NAG>10、NAG-pH<4,是强产酸矿.连续 25周的动态浸滤试验研究表明:受碳酸盐控制,新矿浸滤液的 pH值在 7.46—6.45呈缓慢下降的趋势,25周内减小了近 1个 pH单位;旧矿已经产酸,浸滤液初期 pH<4,10周内迅速下降到 pH<3,体系氧化性及硫化物的氧化速率远远高于新矿,金属的释放大大增加.
静态预测,动态浸滤,矿石,酸性排放.
矿山酸性废水(ARD)主要来源于金属矿体矿石中的硫化矿.这些硫化矿物在空气、水和微生物的共同作用下,发生溶蚀、氧化、水解等一系列物理化学反应,形成含大量重金属离子的黄棕色酸性废水.这些酸性水的 pH值一般为 2—4,每升废水中金属离子的含量从几十到几百毫克,对矿区周围生态环境构成了严重的威胁.大量的废矿石、尾矿的处置及酸性水的处理是矿产业面临的最大挑战.
近年来ARD问题引起了我国学者的关注,并开展了一些相关研究工作.束文圣等[1]用静态法研究了广东乐昌铅锌矿尾矿的产酸潜力及不同剖面酸度与重金属分布的关系.徐小春[2]研究了矿山尾矿和废石产生酸性排水的可能性及其差异,以及矿山固体废弃物中重金属元素的赋存形式.秦燕[3]对铜矿采矿废石进行了 42天的淋溶实验,研究了淋溶液 pH值对金属析出的影响.胡宏伟[4]用动态法研究了乐昌铅锌矿尾矿酸化及金属释放的特征.
本文结合静态 ABA酸碱计算法、静产酸量NAG、NAG-pH及硫酸滴定法与连续的动态浸滤实验方法对云浮硫铁矿新旧矿石的产酸潜力与酸化特征进行了研究与比较,对矿石产酸的控制因素进行了讨论.
1 实验方法
样品取自云浮硫铁矿采矿场.样 1为 2008年新开采出的硫铁矿,样 2是 2003年采集的硫铁矿.
1.1 静态试验[5,6]
ABA酸碱计算法 将矿样制成 200目粉末,取少量用水调成糊状,测定 pH值.硫酸钡重量法测定矿石中的总硫,产酸潜力 AP(kgCaCO3·t-1)=S总% ×31.25.加入已知过量的标准盐酸溶液到 200目准确称取的矿样中,加热近沸,冷却后用标准氢氧化钠溶液返滴定剩余的盐酸,通过化学计量关系计算被消耗的盐酸量,即可得到中和酸能力NP.净中和酸潜力 NNP(kgCaCO3·t-1)=NP-AP.产酸潜力评价[7—9]:NNP>20或 NP/AP>3∶1时,为不产酸矿石;NNP<-20或 NP/AP<1∶11,为产酸矿石,中间为产酸不确定.
静产酸量 NAG法 将 100mL 30%的 H2O2加入到 5.00g的矿样中,充分搅拌使氧化反应完全,冷却后测定溶液的 pH值,得到NAG-pH.然后用氢氧化钠标准溶液滴定至 pH7.0,通过化学计量关系计算产生的硫酸量,即可得到NAG.
硫酸直接滴定法[10]重量法测定总硫量,通过下式计算:产酸能力 APP=S% ×30.6,将 100ml水加到 10g矿样中,搅拌均匀后用 1.0mol·l-1的硫酸标准溶液直接滴定到 pH3.5为终点.根据消耗的硫酸标准溶液计算出酸消耗能力 AC值.产酸潜力评价:APP>AC时,为产酸矿;APP 本研究采用文献[9,11]的方法,将 1kg矿石破碎成 1cm3,装入直径 20cm的布氏漏斗中,暴露于实验室条件下 (25℃±5℃),7d为一周期,每周用 500ml水浸泡 1h达到溶解平衡,连续不断收集并分析滤液成分. 采用 3种不同的静态方法研究实验矿样的产酸能力,其结果见表1. 表1 静态法实验结果Table 1 The result based on ABA 由表1可知,两个样的 NNP均小于 -20,NP/AP<1∶1,具有产酸潜力 .样 1的 NP较高,说明含较高的中和酸的成分,且主要为碳酸盐 .而样 2 NP为 5,已经基本不含中和酸的成分.硫酸滴定法的结果也与ABA的结果一致,且NAG结果表明两个样均为高产酸矿样.研究的矿样为高产酸矿.其中新矿样为高NP的产酸矿,初始 pH=6.92表明较高的NP对酸化具有抑制的作用.据样 2的 NP与AC值分析可知,矿样经长时间的暴露已经部分氧化,初始 pH=4.96表明该样已经开始产酸. 图1是实验矿样浸出液 pH值随时间的变化曲线.图1表明,08年新采的硫铁矿样在实验室条件下充分暴露的 25周期间,其浸出液的 pH值在前 10周大于 7并保持中性形成一个平台,11周后且呈缓慢震荡下降的趋势.在此阶段 pH值下降了 1个单位,从 7.46降到 6.45.而 03年的旧样,初期浸出液 pH<4,呈酸性,且前 10周浸出液 pH值随时间迅速下降,11周后 pH值小于 3,并趋于平稳. 图1 浸出液 pH值随时间的变化Fig.1 pHvstime for sample 结合静态研究的结果分析,样 1是含高NP的高产酸潜力矿,当充分暴露于环境时,NP对矿石硫化物氧化产生的酸释放具有很强的缓冲作用.由于中和酸的成分主要是碳酸盐,与酸结合形成了缓冲体系,因此在前 10周浸出液呈中性并形成一个平台.随着 NP的消耗,pH值缓慢下降,在 25周内pH值下降了 1个单位.当 NP消耗到一定程度或完全时,浸出液将开始显示酸性 .与前人研究[12]的NP/AP=0.13、NP=75的样本比较,该硫铁矿样 35周排放液 pH<4,而本研究的硫铁矿样 NP/AP=0.15、NP=115,估计本矿样 40周左右将产生酸性排放.本试验在继续运行中,以确定产酸的时间. 而样 2已经部分风化,所含 NP极低.矿石接触空气与水分不断氧化生成硫酸,由于缺乏中和酸成分的缓冲作用,使浸出液的酸强度不断加大,导致 pH迅速下降,10周内变化接近 1个 pH单位.当酸度增大到一定程度又构成强酸性环境的缓冲体系,pH值随时间的变化形成平台. 前人探讨过对矿石产酸起决定作用的是碳酸盐而不是金属硫化物[2],本研究的结果表明,在风化的不同阶段决定矿石产酸的因素不同.含高NP的产酸矿,前期 NP大小对矿石产酸与否起决定作用,而当NP消耗后,硫化物的氧化对矿石的产酸起决定作用. 图2 -浓度与时间的关系Fig.2 -vst ime for sample 图4为 pH值与电极电位的关系,酸性条件下,体系氧化性增强,且酸性越强体系氧化性越强.而在中性条件下,还原性较强,电极电位为负值.因此硫化矿石排出液显酸后形成较强的氧化环境,将加速硫化物的氧化.结果进一步表明,受 pH值的影响,矿石在氧化过程中硫化物的氧化速率是非线性[12]变化的,在矿石的氧化过程中,pH值随时间的变化也是非线性的. 图4 pH值与氧化还原电位的关系Fig.4 Oxidation-reduction potentialvspH for sample 排水电导率随 pH值的变化表明,pH值减小将提高矿石中固相物的溶出.在中性环境下,电导率 <500μS·cm-1,受 pH值的影响较小.而在酸性环境下,电导率 >1.5mS·cm-1,且受 pH值的影响极大,pH值微小的降低会大大增加排水电导率.从结果可以推测,当矿石产生酸性排放后,排水的盐分含量大量增加,重金属离子也将随之释放到环境中,且酸性越强,重金属的溶出越高,因此金属产酸矿对环境具有潜在性重金属污染风险. 图5 pH值与电导率的关系Fig.5 pHvsconductivity for sample 研究表明,新开采的云浮硫铁矿矿石是含高中和酸成分即高 NP的高产酸矿,NNP<-20,NP/AP<1∶1,NAG>10,NAG-pH<4,NP=115.由于中和酸的成分形成了缓冲体系,矿石在实验室暴露的 25周内其浸出液表现为中性,pH值维持在 6—7,在此期间矿石产酸受碳酸盐控制.而已经部分氧化的矿石基本不含 NP,且具很高产酸潜力,其浸出液初期 pH值为 3—4,10周以后下降到 PH 3以下并逐渐趋于稳定,此阶段矿石产酸受硫化物氧化控制.硫化矿石在氧化产酸过程中,S2-的氧化速率是非线性变化的.在中性条件下,氧化还原电位呈负值,S2-氧化产酸的速率较慢.在酸性条件下,体系氧化性较强,S2-氧化产酸的速率加快.pH值与电导率呈负相关,中性时固相溶出物的释放较小,排水的盐分较低.酸化将促进固相物质的溶出,随酸化的加剧可能导致金属离子大量释放到环境中. [1] 束文圣,张志权,蓝崇钰,广东乐昌铅锌尾矿的酸化潜力 [J].环境科学,2001,22(3)∶113—117 [2] 徐小春,陈芳,王军等,铜陵矿山酸性排水及固体废弃物中的重金属元素 [J].岩石矿物学杂志,2005,24(6)∶591—596 [3] 秦燕,徐小春,谢巧勤等,铜矿采矿废石重金属环境污染的淋溶实验研究 [J].地球学报,2008,29(2)∶247—252 [4] 胡宏伟,束文圣,蓝崇钰等,乐昌铅锌尾矿的酸化及重金属淋溶实验研究 [J].环境科学与技术,1999(3)∶1—3 [5] Lawrence R W,Marchant P B,Acid Rock Drainage PredictionManual[M].NorthVancouver,1991 [6] 李锦文,吴惠明,陈永亨,矿山酸性排水静态预测与评价 [J].广州大学学报 (自然科学版)2008,7(4)∶60—63 [7] SchaferW illiam M,Use of theNetAcid Generation pH Test forAssessingRisk ofAcid Generation[C].Proc.of Fifth InternationalConference on Acid Rock Drainage,Canada,2000,613—618 [8] PriceW A,Guidelines and RecommendedMethods for the Prediction ofMetalLeaching and Acid Rock Drainage atMinesites in British Columbia[C].Canada,2000 [9] Miller S,Robertson A,Donahue T,AdvancesAcid Drainage Prediction Using the NetAcid Generation(NAG)Test[C].Proc.of the Forth International Conference on Acid Rock Drainage,Vancouver,1997,410—422 [10] Bruynesteyn A,Hackl R P,Evaluation ofAcid Production Potential ofMiningWasteMaterials[J].M inerals and Environment,1982 4(1) ∶5—8 [11] Morin KA,HuttN M,LessonsLearned from Long-Term and Large-Batch Humidity Cells[C].Proc.of Fifth International Conference on Acid Rock Drainage,Canada,2000,661—664 [12] LiMichael G,Neutralization Potential versusObservedMineralDissolution in Humidity Cell Tests forLouvicourt Tailings[C].Proc.of the Forth International Conference on Acid Rock Drainage,Vancouver,1997,149—164 STUDY ON AC I D GENERATI ON POTENTIAL AND PROCESS USING KINETIC FLOOD LEACHING AND STATIC M ETHODS FOR YUNFU PYRITE L I Jin-wen1CHEN N an1WU Hui-m ing2LUO D ing-gui1CHEN Yong-heng1 Acid rock drainage(ARD)causes seriouswater pollution.ARD prediction using static methods and acid generation process using kinetic flood leaching in humid cellwere studied in thispaper for Yunfu pyrite.Static prediction results show that Yunfu pyrite with NNP<-20,NP/AP<1∶1,NAG>10,NAG-pH<4 is a strong acid producer. Kinetic flood leaching test for 25 weeks shows that the drainage from pr imary sample is neutral and pH gently falls within pH 7.46—6.45 under the control of carbonate.The pH of drainage from secondarysample is less than 4 and falls to<3 after 10 weekswith lots ofmetals releasing.The rate of sulfide oxidation for secondary sample ismuch faster than primary sample. static prediction,kinetic flood leaching,acid rock drainage. 2009年5月9日收稿. *国家自然科学基金委-广东省人民政府联合基金项目 (U0633001). **通讯联系人,Tel:13342883886,E-mail:chenyong_heng@163.com1.2 动态浸滤试验:
2 结果与讨论
2.1 产酸潜力
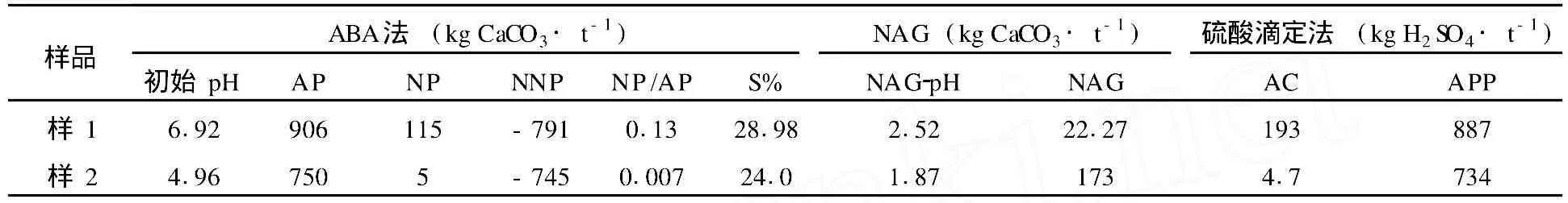
2.2 浸出液 pH值随时间的变化特征
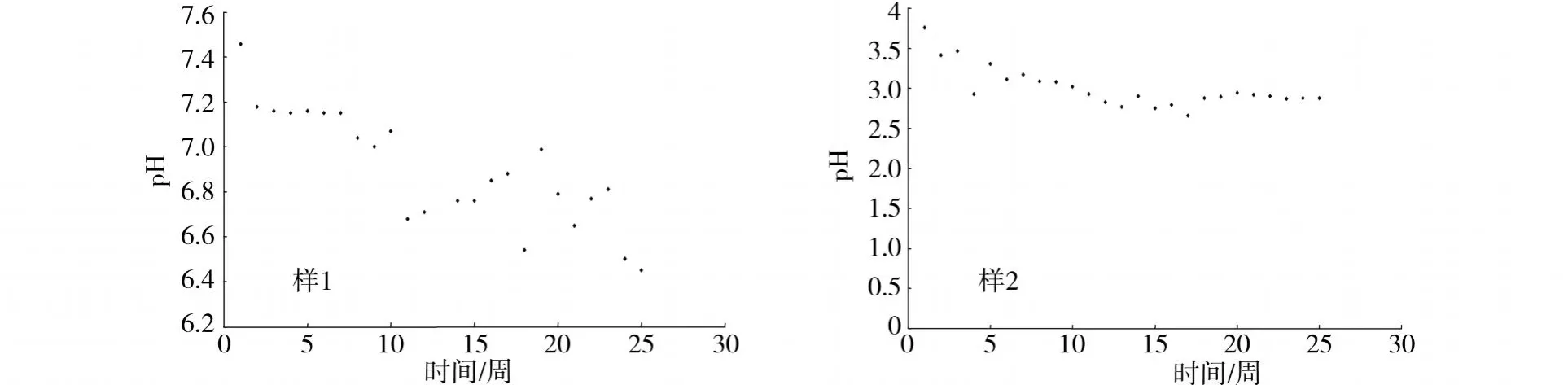
2.3 硫化矿石的氧化特征

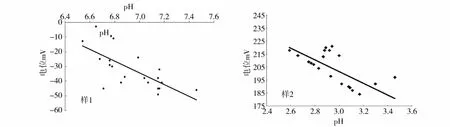
2.4 pH值对固相物溶出的影响
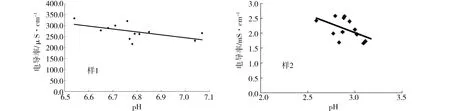
3 结论
(1 College of Environmental Science and Engineering,Guangzhou University;2 College of Chemistry and Chemical Engineering,Guangzhou University,Guangzhou,510006,China)

