化学镀法制备纳米Ni-B包覆Al复合粉末
程志鹏,徐继明,朱玉兰,李 栋,杨 毅,李凤生
(1江苏省低维材料化学重点建设实验室(淮阴师范学院),江苏淮安223300; 2南京理工大学国家特种超细粉体工程技术研究中心,南京210094)
化学镀法制备纳米Ni-B包覆Al复合粉末
程志鹏1,徐继明1,朱玉兰1,李 栋1,杨 毅2,李凤生2
(1江苏省低维材料化学重点建设实验室(淮阴师范学院),江苏淮安223300; 2南京理工大学国家特种超细粉体工程技术研究中心,南京210094)
以硼氢化钾(KBH4)为还原剂,采用化学镀法制备了纳米Ni-B包覆Al复合粉末,研究了镀液组分及工艺对包覆效果的影响,获得了制备复合粉末的优化条件。采用SEM,XRD,ICP和BET对复合粉末的表面形貌、物相结构、元素组成和比表面积进行了表征分析。结果表明:纳米Ni-B在Al表面包覆连续、均匀,且纳米Ni-B呈非晶态,粒径80~100 nm,化学组成约为Ni72B28,纳米Ni-B/Al复合粉末比表面积达到了26.21m2·g-1。
化学镀;铝粉;包覆;纳米复合粉末
Abstract:Ni-B/Al nanocomposites were preparedviaelectroless plating by using KBH4as a reducing agent.The bath components and processing parameters were investigated in order to obtain the optimized condition.The surface morphology,crystal phase,chemical composition and specific surface area of the as-prepared nanocomposites were characterized by SEM,XRD,inductively coupled plasma (ICP)atomic emission spectrometry and Brumauer-Emmett-Teller(BET)specific surface area.The results show that a continuous layer of 80-100 nm amorphous Ni72B28is covered on the surfaces of Al particles,and BET data of the as-prepared nanocomposites are up to 26.21m2·g-1.
Key words:electroless plating;aluminum particle;coating;nanocomposite
以铝粉为芯核的复合粉末在有机化工催化剂、导电填料和固体火箭等领域具有广泛的应用前景[1]。如镀铜铝粉可作为有机化工的优良催化剂[2];镀银铝粉因具有优异的导电性而被作为导电填料广泛应用于电子、通讯、印刷、航空航天等领域[3];镀镍铝粉,相比单一Al粉而言,具有更高的熔点,可以提高Al粉高温下的抗烧结性能,从而阻止Al粉的桥接和团聚[4]。目前,Al核复合粉末的制备主要靠电镀法完成,该法成本高、效率低,因此研究制备Al核复合粉末新的工艺具有极其重要的意义。随着化学镀工艺的不断完善,近年来其镀覆材料的范围已不再局限于传统的块状大尺寸材料,而是延伸到粉末等小尺寸材料[5]。近年来,在科研人员的努力下,通过对镀覆工艺的探索和优化已成功地在炭纤维[6]、氮化硅[7]、碳化硅[8]、氧化锆[9]等粉体表面得到了均匀的金属镀层。
但迄今为止,已报道的在化学镀液添加的粉体均限于不溶或难溶的稳定的惰性粉体,对Al粉表面化学镀工艺的研究还鲜有报道。与传统的添加惰性粉体的化学镀工艺相比,Al粉施镀的困难在于Al粉的表面活性很大、电位很负。而且Al属两性金属,在酸性和碱性条件下都不稳定,因此Al粉在镀液条件下迅速发生溶解的倾向很大,并易于造成镀液不稳定。与其他粉末材料相比,其镀覆难度较大。
考虑到Al核复合粉末具有广泛的应用前景,而其传统的电镀法制备工艺又存在诸多缺点和不足,本工作采用化学镀法制备纳米Ni-B包覆Al复合粉末,研究镀液组成及工艺条件对镀覆效果的影响,并对产物进行详细的表征。
1 实验
1.1 试样与试剂
铝粉为鞍山鞍钢实业超细粉有限公司产品,平均粒度为 5μm,纯度 99%(质量分数)。NiCl2·6H2O (国药集团化学试剂有限公司)、KBH4(国药集团化学试剂有限公司)、乙二胺(上海凌峰化学试剂有限公司)、NaOH(南京化学试剂有限公司)均为分析纯。实验用水为去离子水。
1.2 实验步骤
在一定质量浓度NiCl2溶液中加入适量络合剂乙二胺;然后在剧烈搅拌条件下将预先超声分散的Al粉悬浊液与上述溶液混合;用NaOH溶液调节体系的p H值,并将混合溶液升温至指定温度后,向体系中匀速滴加一定质量浓度的 KBH4溶液,反应约30 min后,将得到的黑色粉末离心、洗涤、干燥,获得最终产物。
1.3 表征
包覆前后Al粉的形貌变化由L EO 1530VP型扫描电子显微镜(SEM)观察;复合粉末的物相组成由Bruker D8型X射线粉末衍射仪(XRD)分析获得;复合粉末的比表面积采用BC SA3100Plus型比表面仪(BET)测试得到;Ni-B合金中Ni与B元素的相对含量由PE Optima-2000DV型等离子体原子发射光谱仪(Inductively Coupled Plasma atomic emission spectrometry,ICP)测定。
2 结果与讨论
2.1 实验原理
KBH4是一种强还原剂,可以将多种金属离子还原成单质。可是 KBH4在水溶液中不稳定,易分解而放出 H2,但它在碱性环境中稳定性增加,所以镀覆过程选择在碱性溶液中进行。KBH4在还原Ni2+过程中,自身也会分解生成B,反应方程式可分别由式(1), (2)所示:
Ni与B结合形成非晶合金,总的方程式可由式(3)所示:

另外考虑到此化学镀液显碱性,则Al粉在镀液中也存在副反应发生,如式(4)所示:
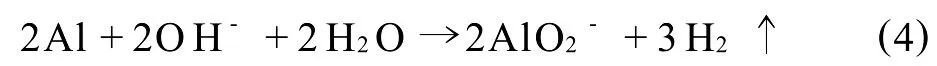
在化学镀过程中,Ni2+和 KBH4吸附在具有催化活性的Al粉表面,KBH4催化脱氢后释放的游离电子将Ni2+还原为Ni原子,并自身分解出B原子,Ni原子和B原子在Al粉表面结合,并不断生长,从而在Al粉表面包覆上Ni-B层。碱性镀液中Al粉的析氢反应(式(4))产生的 H2会降低Ni-B层和Al粉的结合力,从而影响镀层质量。通过控制镀液组分以及工艺可以有效抑制其发生。
2.2 镀液组分及工艺的研究
通过单因素实验及分析,在恒定Al质量浓度为8 g/L的前提下,对NiCl2质量浓度、KBH4质量浓度、乙二胺体积分数、镀液温度及镀液p H值等五种因素进行四水平正交实验,设计L16(45)正交实验,以质量变化和包覆质量的综合结果为实验指标,得出最优的镀液成分及工艺,结果如表1所示。

表1 化学镀组分与工艺条件Table 1 Components and processing parameters
2.2.1 镀液组分的影响
化学镀液主要由主盐、络合剂与还原剂等组成。主盐即NiCl2,当其质量浓度较低时,镀覆速率较慢,反应时间延长。提高NiCl2的质量浓度,正向反应的驱动力较大,反应速率较快,相应地反应时间缩短。但[Ni2+]增加到一定值后镀速无明显变化,本实验中NiCl2的合适用量为32~36g/L。
乙二胺作为络合剂,其作用是使Ni2+与它生成稳定的络合物[Ni(H2NCH2CH2N H2)3]2+,防止生成Ni(OH)2沉淀,拓宽镀液p H值工作范围,稳定镀液。另外,乙二胺体积分数对化学镀过程也存在较大的影响。从动力学角度看,当乙二胺体积分数较低时,它能有效地吸附在Al粉表面,提供较高的反应激活能和提高 KBH4的利用率,有利于缩短反应时间、提高反应速率;另一方面,增加乙二胺的体积分数,也会使它与NiCl2的摩尔比增加,Ni2+将以稳定的络合物形式存在,金属Ni的析出难度随之增加,镀覆速率也随之下降。综合考虑,其用量控制为45~60mL/L。
KBH4被用作还原剂,当其浓度较低时,还原能力较小,镀覆速率缓慢;随浓度增大,镀覆速率增大,达到最佳值时,包覆层质量好;当浓度进一步提高,还原能力进一步加强,但镀液稳定性下降,且Ni-B还原出来的速率较快易于单独成核。本实验中控制其浓度为8~12g/L。
2.2.2 镀液温度的影响
因为施镀过程是吸热反应,温度是影响反应速率的重要参数。温度较低时,Ni2+的活动能力差,且还原剂的还原能力弱,因此反应速率缓慢;随着温度升高,镀液中的离子扩散速度增加,使得Al粉表面离子交换频率增加,相应地完成化学镀所需要的时间减少,反应速率提高。但过快的反应速率易使得Ni-B在沉积过程中自身成核,从而脱落Al粉的表面,导致镀层的质量下降。为了得到合适的镀覆速率和较好的镀层质量,镀液温度控制在35~40℃。
2.2.3 镀液p H值的影响
KBH4在酸性与中性介质中会迅速分解,随着p H的提高,其稳定性明显增强。实验发现,p H维持在10~14的范围内,镀液的稳定性较好。另外由于化学镀过程中,OH-参与了反应,p H值增加,即相应增加了OH-的浓度,促进反应向正方向进行,使Ni2+的还原速率加快。p H值除影响还原速率外,对镀层质量也有较大的影响。p H<10时,Ni-B沉积速率小,甚至不能沉积Ni-B;p H>12时,反应瞬间即可完成,高的反应速率使得Ni-B镀层杂乱、无序,且Al粉的腐蚀比较严重;而当p H值为10~11时,Ni-B的沉积速率比较理想,且能有效防止Al粉的腐蚀,得到的Ni-B镀层比较均匀、致密。
2.3 XRD表征
对按上述优化工艺制备出的复合粉末进行XRD分析,结果见图1。曲线(a)为原料 Al粉的 XRD图谱;曲线(b)为制备的纳米Ni-B/Al复合粉末的 XRD图谱,发现复合粉末的衍射峰与原料Al粉相似,所不同的仅仅是基线稍有杂乱,可以说明Ni-B为非晶态。为了进一步确定Ni-B非晶的结构,利用5mol/L HCl溶液溶解掉芯核Al核,对剩余产物作XRD分析,发现XRD图谱在2θ≈45°出现了Ni系非晶态特征衍射峰(曲线(c)),这进一步证实了纳米Ni-B的非晶结构。
2.4 SEM表征
图2(a)为原料Al粉的 SEM照片,可以看到Al粉颗粒为球形,表面较光滑且吸附有少量纳米Al粉颗粒;图2(b),(c)反映了在其他条件相同时,温度和p H值对纳米Ni-B镀层的影响。其中图2(b)为p H= 10.0,温度60℃时制备出的复合粉末SEM照片,可以看出,纳米Ni-B杂乱地包覆在Al粉的四周,包覆效果较差。这主要是因为镀液温度较高时,导致纳米Ni-B颗粒生长的速率较快,影响了纳米Ni-B颗粒在Al粉表面的有序沉积;图2(c)为p H=13.0,温度40℃时制备得到的复合粉末SEM照片,可以看出,Al的球形形貌被明显破坏,且形成的纳米Ni-B颗粒很多散落在Al粉的四周。这主要是因为在较高的p H值下,溶液中碱性较强,从而Al粉的腐蚀较明显;另外大量 H2从Al表面逸出,也影响了纳米Ni-B颗粒的沉积。图2(d)为按优化工艺制备的复合粉末SEM照片,可见Al粉表面包覆较致密的纳米Ni-B层,且基本没有观察到散落的纳米Ni-B颗粒;图2(e)为图2(d)上选中矩形区域的局部SEM图,可清晰观察到纳米Ni-B在Al粉表面形成了较均匀的包覆层;图2(f)为复合粉末经5mol/L HCl腐蚀后剩余产物的SEM照片,可见纯纳米Ni-B粒径大小均匀,约为80~100nm,且经 ICP测定其组成约为Ni72B28。
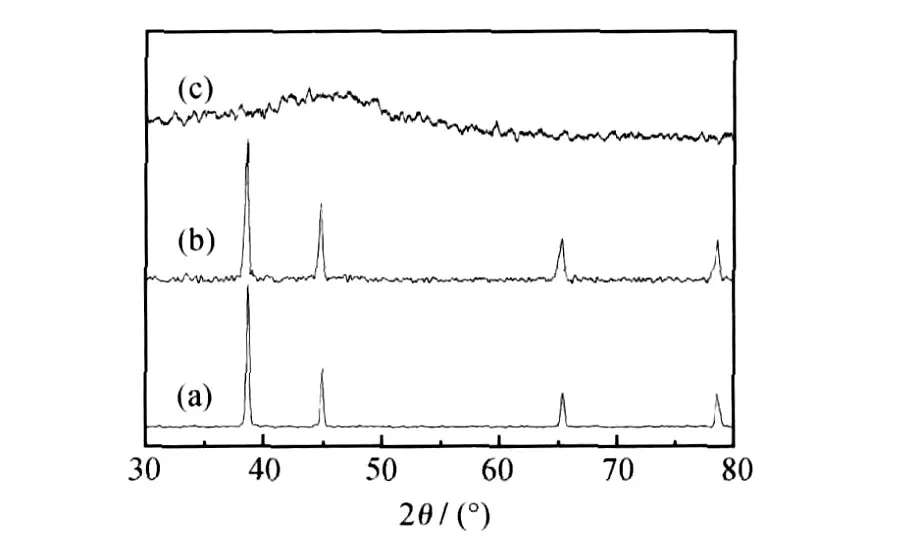
图1 原料Al粉(a),纳米Ni-B/Al复合粉末(b)及纳米Ni-B(c)的X射线衍射图谱Fig.1 XRD patterns of raw Al(a),Ni-B/Al nanocomposites(b)and nano Ni-B(c)
2.5 BET测定
通过测定包覆前后Al粉比表面积的变化可间接反映Al粉表面的结构变化。另外,考虑到纳米Ni-B/ Al复合粉末在有机化工催化领域有着广泛的应用前景,而催化活性与比表面积存在密切的关系,比表面积往往是衡量催化活性的重要指标之一,比表面积大的粉体能表现出更强的催化能力。因此以氮气吸附法对原料Al粉、纳米Ni-B/Al复合粉末及纯Ni-B颗粒进行比表面积测试,测试结果如表2所示。
通过表 2得知,原料 Al粉的比表面积为0.89m2·g-1,纯Ni-B颗粒的比表面积为18.68m2· g-1,而纳米 Ni-B/Al复合粉末的比表面积达到了26.21m2·g-1。这一方面表明经过包覆处理后的Al粉表面结构已经发生明显变化,另外可以发现纳米Ni-B/Al复合粉末比单一纳米Ni-B具有更大的比表面积。这主要是因为单一纳米Ni-B具有较大的表面能,极易团聚,而纳米Ni-B包覆Al复合粉末在很大程度上提高了纳米Ni-B的分散性,从而提高了比表面积。
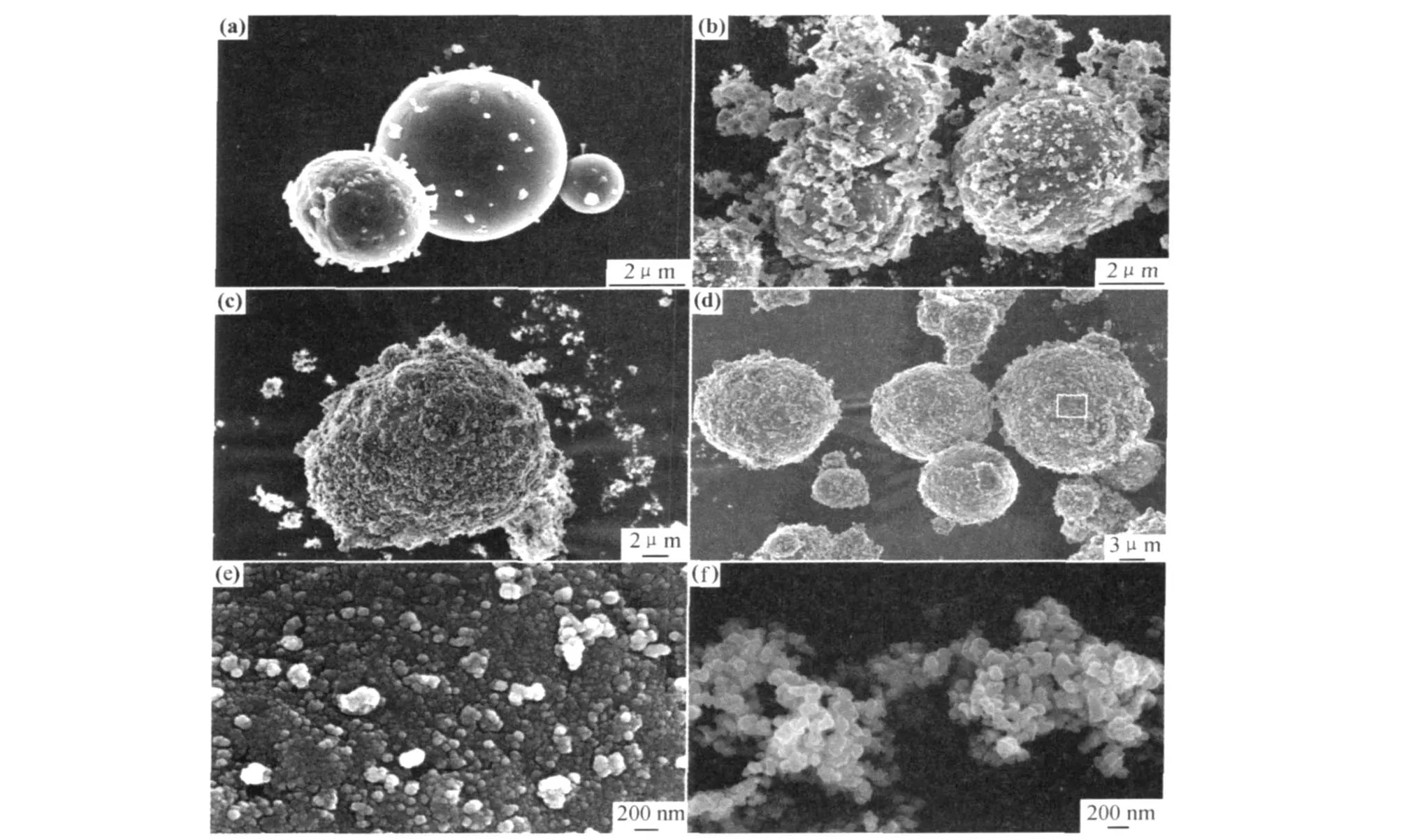
图2 原料Al粉(a),pH=10.0,60℃(b),pH=13.0,40℃(c)和优化工艺(d)制备的纳米Ni-B/Al复合粉末SEM照片;(e)图2(d)中选中区域的局部放大照片;(f)Ni-B颗粒Fig.2 SEM images of raw Al(a)and the product prepared at different conditions:(b)p H=10.0,60℃;(c)p H=13.0,40℃; (d)optimized condition;(e)SEM image of the boxed region of the sample in fig.2(d);(f)nano Ni-B

表2 样品的比表面积Table 2 The surface area of the samples of Al,Ni-B and Ni-B/Al
3 结论
(1)采用化学镀法在微米Al粉表面包覆致密的纳米Ni-B层,得到Al粉为核,Ni-B为壳的纳米Ni-B/ Al复合粉末。
(2)优化后的镀液配方及工艺如下:NiCl232~36g/L;乙二胺 45~60mL/L;KBH48~12g/L;镀液温度35~40℃;镀液p H值10~11。
(3)纳米Ni-B在Al表面连续、均匀包覆,且纳米Ni-B呈非晶态,粒径约为80~100nm,化学组成约为Ni72B28,纳米Ni-B/Al复合粉末比表面积达到26.21m2·g-1。
[1]程志鹏,杨毅,刘小娣,等.置换法制备核壳结构Cu/Al复合粉末[J].化学学报,2007,65(1):81-85.
[2]KANUNGO M,CHAKRAVARTY V,MISHRA K G,et al.Influence of perchloric acid on the kinetics of immersion plating of copper onto aluminum[J].Hydrometallurgy,2001,61:1-11.
[3]常仕英.镀银铝粉的制备技术与性能研究[D].昆明:昆明理工大学硕士学位论文,2006.
[4]BABU K V A,VASSILIEV V A,SVIRIDOV V V.Propellant formulation factors and metal agglomeration in combustion of aluminized solid rocket propellant[J].Combust Sci Tech,2001, 163:261-289.
[5]OH I H,LEE J Y,HAN J K,et al.Microstructural characterization of Al2O3-Ni composites prepared by electroless deposition [J].Surf Coat Technol,2005,192:39-42.
[6]矫海霞,谢广文,崔作林.纳米螺旋碳纤维表面化学镀Ni-Co-B涂层研究[J].材料工程,2007,(4):47-49.
[7]翟华嶂,戴金辉,李建保,等.纳米镍包覆氮化硅粉体的制备和磁性能研究[J].材料工程,2008,(10):204-207.
[8]王海龙,张锐,卢红霞,等.两种Cu包裹SiC复合粉体工艺的研究[J].中国陶瓷工业,2005,12(4):18-21.
[9]徐惠,王毅,翟钧,等.Ni-P包覆纳米氧化锆复合粉体的制备及性能研究[J].兰州大学学报,2005,41(3):63-66.
Synthesis of Ni-B/Al Nanocomposites by Electroless Plating
CHENG Zhi-peng1,XU Ji-ming1,ZHU Yu-lan1, LI Dong1,YANG Yi2,LI Feng-sheng2
(1 Jiangsu Key Laboratory for Chemistry of Low-Dimensional Materials, Huaiyin Normal University,Huaian 223300,Jiangsu,China; 2 National Special Superfine Powder Engineering Research Center,Nanjing University of Science&Technology, Nanjing 210094,China)
TB331
A
1001-4381(2010)01-0019-04
国家自然科学基金资助项目(50876046)
2009-02-20;
2009-11-26
程志鹏(1982—),男,博士,研究方向为微纳米核壳复合粉末的制备及应用,联系地址:江苏省淮安市淮阴师范学院化学化工学院低维材料重点建设实验室(223300),E-mail:nano301@126.com

